斑點叉尾鲖源海豚鏈球菌Srr蛋白海藻酸鈉-殼聚糖口服疫苗的制備及其免疫效果研究
王興麗 汪開毓 王二龍 王 濤 楊 倩 陳德芳 耿 毅
(1. 四川農業大學動物醫學院, 成都 611130; 2. 四川農業大學動物科技學院, 成都 611130)
海豚鏈球菌(Streptococcus iniae, 曾用名Streptococcus shiloi), 隸屬于鏈球菌科(Streptococcaceae),鏈球菌屬(Streptococcus)。自1976年Pier和Madin[1]從亞馬遜河河豚皮膚中初次分離出海豚鏈球菌后,該菌便在北美洲、中東、亞太地區以及歐洲蔓延開來, 主要感染淡水和海水魚[2—5]。曾經的海豚鏈球菌被認為對斑點叉尾鲙不敏感, 但是最近幾年,海豚鏈球菌從斑點叉尾鲙上頻頻被分離出來, 且在中國多地出現暴發性流行, 對斑點叉尾鲙的健康養殖存在一定的威脅[6]。研究表明, 海豚鏈球菌可引起斑點叉尾鲙異常游動, 體色變深, 鰭條出血, 腹部膨大; 剖解可見內臟腫大、充血, 積滿腹水, 腸炎等[7]。
海豚鏈球菌絲氨酸富集蛋白(Srr)是鏈球菌中一種重要的蛋白(GenBank登錄號: CP005941.1, 對應蛋白登錄號AGM97982.1), 具有一個3618 bp的開放閱讀框, 預計編碼蛋白125 kD, 且在C-端的第251—405個氨基酸殘基之間含有一個碳端細菌纖維蛋白原結合黏附素超家族(SdeG_C_C_supperfamily)的保守結構域[8]。研究表明, Srr可能通過調控一些重要因子來影響細菌致病過程中的黏附、定殖以及在宿主體內存活等活動, 從而使細菌達到在宿主體內生存、繁殖和致病的目的[9,10]。由此可見Srr相關蛋白在鏈球菌對宿主的感染中起著相當重要的作用, 但目前關于海豚鏈球菌Srr蛋白疫苗的研究相對較少, 其作用機制有待進一步研究。
目前世界多數漁用疫苗是通過注射進行免疫,該方式不僅存在工作量大, 且易對魚體造成應激等缺點; 相對于注射免疫, 口服免疫不僅操作方便, 且對魚體應激反應小, 成為魚類免疫最有前景的免疫方式之一, 而口服疫苗預防海豚鏈球菌病的研究還鮮有報道。本實驗采用海藻酸鈉和殼聚糖2種天然高分子聚合物作為海豚鏈球菌Srr蛋白的包被載體, 對微球制備后的包封率、載藥率以及包被蛋白的抗原性進行了檢測, 并通過微球拌飼投喂方式免疫斑點叉尾鲙, 利用免疫后的血清對其免疫指標進行測定, 最后通過相對保護率的測定綜合判斷該疫苗有望成為斑點叉尾鲙預防海豚鏈球菌病的候選疫苗, 且為海豚鏈球菌口服疫苗的研制及應用提供基礎。
1 材料與方法
1.1 實驗材料
斑點叉尾鲙源海豚鏈球菌(DGX07, 登錄號:FJ951434)由四川農業大學魚病研究中心分離保存。海豚鏈球菌Srr蛋白由四川農業大學魚病研究中心進行生物信息學分析、克隆表達、純化并保存(70 kD左右)。海藻酸鈉、殼聚糖購自上海生物工程有限公司, 食品級液體石蠟、Span-80、氯化鈣和乙酸鈉等均購自成都科龍試劑廠。健康斑點叉尾鲙購自四川成都某斑點叉尾鲙養殖基地, 體重(50±5) g。HRP goat anti-rabbit IgG購自百奇生物科技有限公司; 兔抗斑點叉尾鲙IgM血清由本實驗室提供; 可溶型單組分TMB底物溶液購自北京天根生化科技有限公司; 總蛋白檢測試劑盒、溶菌酶檢測試劑盒、總超氧化物歧化酶檢測試劑盒均購自南京建成科技有限公司。
1.2 海藻酸鈉-殼聚糖-海豚鏈球菌Srr蛋白微球疫苗以及空微球的制備
1.5 %濃度海藻酸鈉溶液與2 mg/mL的Srr蛋白(空微球的制備是將Srr蛋白替換為PBS)充分混合,將混合溶液按4鯰6緩慢滴加到食品級液體石蠟(含乳化劑Span-80和硬脂酸鎂)中, 1800 r/min攪拌, 待充分乳化后, 將8%濃度(M/V)CaCl2溶液加入乳化好的海藻酸鈉蛋白中鈣化形成微球, 8000 r/min離心5min收集沉淀, 用0.01 mol/L的乙酸鈉(pH=4.0)洗滌液清洗3次, 再與0.8%濃度的殼聚糖(pH=5的乙酸鈉配制)1800 r/min混勻10min, 8000 r/min離心5min收集沉淀, 同上洗滌3次后相同緩沖液重懸, 加入等體積的2%的甘露醇攪拌均勻, 凍干保存。
1.3 微球粒徑、包封率、載藥率以及抗原性檢測
微球粒徑參考陽磊等[11]的實驗方法計算微球粒徑。
包封率及載藥率將收集到的一定量的微球重懸, 取3 mL微球懸液離心, 將得到的微球加入到適量PBS溶液中超聲破碎, 充分溶解。再將溶液10000 r/min離心10min, 將所收集的上清液用Bradford法檢測蛋白濃度, 按照公式計算包封效率和載藥率:
包封效率(%)=(實際微球中的蛋白質量/理論微球中蛋白質量)×100%
載藥率(%)=(實際微球中的蛋白質量/最后測得總質量)×100%
抗原性取一部分上清液利用兔抗組氨酸標簽抗體(1鯰200稀釋)和兔抗海豚鏈球菌抗體進行Western-Blot, 室驗操作參考Jiang等[12]的方法。
1.4 分組及免疫
實驗前隨機剖檢5尾斑點叉尾鲙檢查其健康情況, 隨后將健康斑點叉尾鲙240尾隨機分為4組, 具體分組見表 1, 以下各組簡稱為Srr組、Srr微球組、空微球組以及對照組。各組實驗前均馴養14d, 馴養后的魚能每日進料情況良好。14d后, 將制備的微球疫苗定量與粉碎后的飼料粉末混合后再成型、干燥, 按照魚體重的2%進行投喂, 各組均連續投喂14d。
1.5 樣品采集與處理
免疫后第1—8周每周定時在每組隨機選取5尾通過靜脈采血0.2 mL, 血液室溫靜置2h后移入4℃冰箱過夜, 次日4000 r/min離心10min, 收集上清,-20℃保存。于免疫后第4周每組隨機選取15尾斑點叉尾鲙進行S. iniae攻毒, 攻毒后24h和48h每組隨機選取6尾魚分別取其頭腎和脾臟, 液氮研磨提取總RNA反轉錄cDNA后于-80℃保存備用。
1.6 間接ELISA檢測血清抗體效價
方法參照任燕等[13]的方法通過間接ELISA法檢測血清抗體效價。
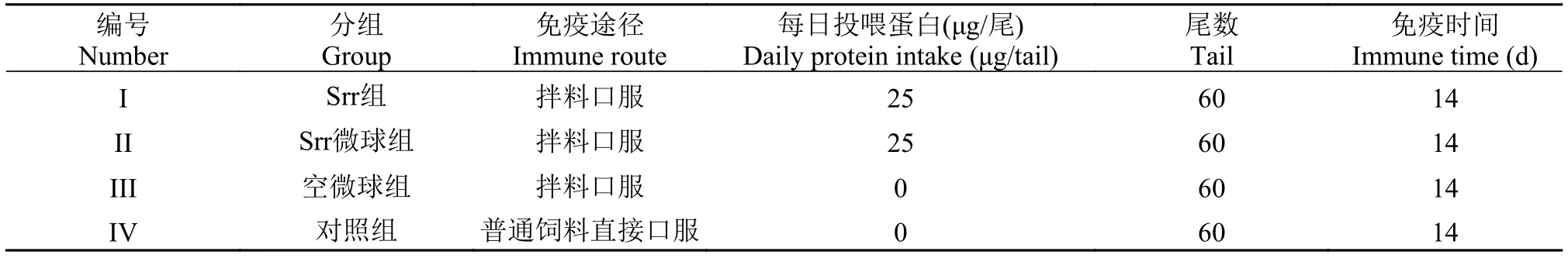
表 1 免疫程序Tab. 1 Immunization program
1.7 非特異性指標的檢測與分析
血清總蛋白、T-SOD以及溶菌酶的測定參照南京建成生物有限公司的試劑盒說明書進行, 并按說明書公式進行計算, 所得結果利用SPSS18.0 軟件包進行統計分析, 比較各實驗組與對照組的顯著性差異, 其中P>0.05 為差異不顯著, 0.01<P<0.05為差異顯著,P<0.0l為差異極顯著。
1.8 實時熒光定量PCR分析
參照Yang等[14]的引物設計合成斑點叉尾鲙EF-1α、IFN-γ、TNF-α、CD4L-2、MHC-IIβ的引物, 以EF-1α因子為內參基因, 采用熒光定量PCR測定斑點叉尾鲙IFN-γ、TNF-α、CD4L-2、MHCIIβ的表達影響。參照ABI公司SYBR@Green PCR Supermix染料說明書配置PCR反應體系進行反應,反應后進行PCR產物溶解曲線分析, 鑒定擴增產物。
實驗中的每個樣品有3個重復(n=3), 結果取其循環閾值(Ct)的平均值, 利用公式RQ=2-ΔΔCt計算斑點叉尾鲙頭腎和脾臟中IFN-γ、TNF-α、CD4L和MHC-Ⅱ基因的相對表達量。其中ΔCt=目的基因平均Ct值-內參基因平均Ct值, ΔΔCt=實驗組ΔCt-對照組ΔCt。所得結果利用SPSS18.0 軟件包進行統計分析, 所有實驗數據用Mean±SD表示, 各不同組織ΔCt值釆用獨立樣本t檢驗。P>0.05為差異不顯著, 0.01<P<0.05 為差異顯著,P<0.0l為差異極顯著。
1.9 攻毒實驗及相對保護率的測定
在免疫后第4周, 利用S.iniae(6×107cfu/mL)[7]對各組斑點叉尾鲙進行攻毒, 每組隨機選取20尾,腹腔注射0.2 mL/尾, 記錄攻毒后14d內各組魚的發病及死亡情況, 另取瀕死魚的肝、腎進行接菌培養,確定病原菌種類。并計算相對保護率(Relative Percent Survival, RPS), 按下列公式計算:
RPS(%)=[(對照組死亡率-免疫組死亡率)/對照組死亡率]×100%
2 結果
2.1 微球疫苗包封率、載藥率以及抗原性檢測
利用顯微鏡對制備微球進行觀察, 制得的微球形態呈圓形或橢圓形(圖1), 粒徑較為均-[(4.26±1.13) μm]。通過超聲破碎后測得Srr蛋白微球疫苗的包封率為92.38%, 載藥率為19.41%。Westernblot結果表明Srr蛋白微球與兔抗海豚鏈球菌抗體/兔抗組氨酸標簽抗體均能結合, 在70 kD大小處有明顯的條帶, 表明微球中的蛋白具有較好的抗原性。
2.2 血清抗體水平
本實驗采用了間接ELISA方法測定了Srr組、Srr微球組、空微球組以及對照組免疫后第1—8周的抗體消長規律(圖2)。實驗結果可見, 實驗組可在第2周檢測到抗體效價, 但是檢測值較低, 隨后開始增加, Srr組和Srr微球組均在第4周時實驗組均達到峰值, 分別為0.85和0.99。從第5周開始實驗組出現下降峰, 而對照組始終無特異性檢出。雖然空微球組也有抗體效價的檢出, 但是其持續時間較短。

圖1 微球的形態以及Western-blot結果Fig. 1 The shape of alginate microparticles and result of Western-blotting analysis
2.3 血清總蛋白檢測結果
如圖3所示, 在免疫后的前3周, Srr組和Srr微球組血清總蛋白含量均極顯著升高(P<0.01), 而空微球組和對照組均無明顯差異。在實驗的第4周, 所有實驗組血清總蛋白含量極顯著(P<0.01)或顯著(P<0.05)高于對照組, 其中Srr微球組血清總蛋白含量最高。第5周后出現所有實驗組均有所下降, 且均在第6周以后達到穩定狀態。在整個實驗期間,Srr微球組血清蛋白含量一直高于其他組。
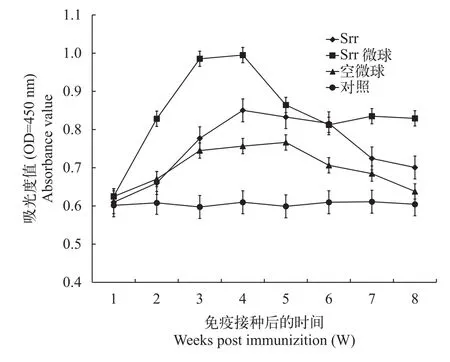
圖2 斑點叉尾鲙血清中的抗體水平Fig. 2 The antibody level in the serum of Ictalurus punctatus
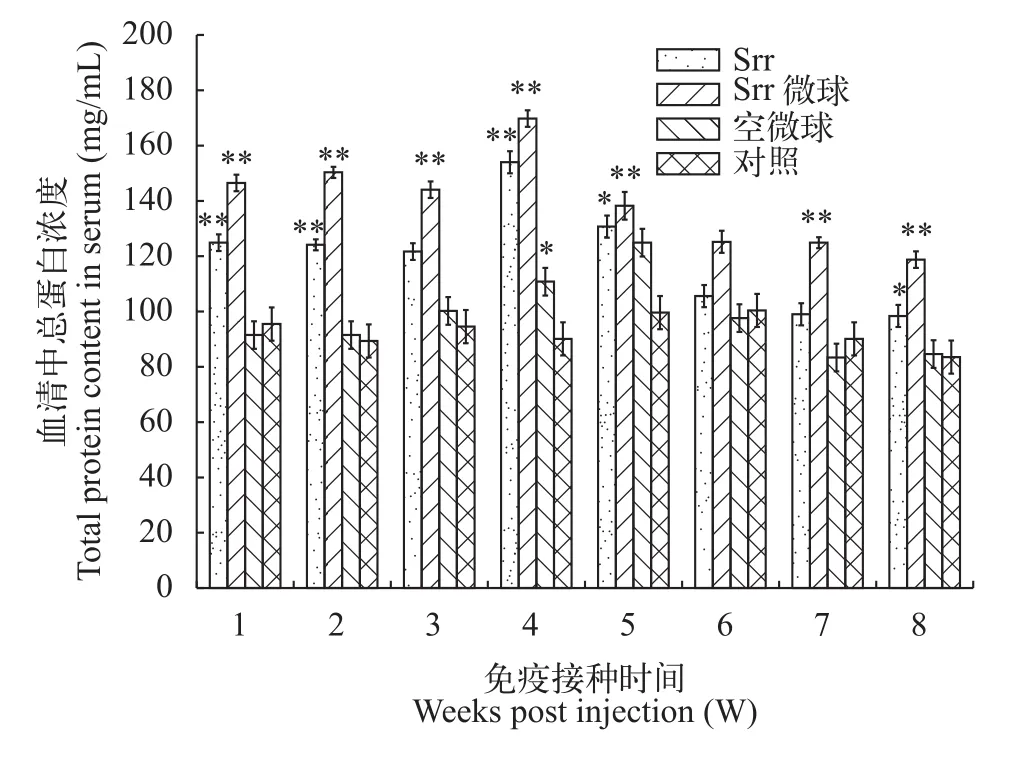
圖3 斑點叉尾鲙血清總蛋白含量變化Fig. 3 Changes of total protein content in serum of Ictalurus punctatus
2.4 血清T-SOD活力檢測結果
如圖4所示, 免疫后各實驗組T-SOD活力均呈上升趨勢, 在第3、4周時Srr組和Srr微球組的酶活力均極顯著高于對照組(P<0.01), 且Srr微球組在第3周出現峰值, Srr組在第4周出現峰值。峰值后各實驗組均出現下降峰, 但在第5周后便基本維持穩定。空微球組僅在第5周與對照組差異顯著(P<0.05)。
2.5 血清溶菌酶活力檢測結果
如圖5所示, Srr微球組血清溶菌酶活力從免疫后第1—8周均極顯著(P<0.01)高于對照組, 且在第2周達到峰值。Srr組在第4周達到峰值, 除了第2周,其余實驗期間均顯著或極顯著高于對照組。空微球包被組在第6、7、8周顯著(P<0.05)或極顯著(P<0.01)高于對照組, 但在整個實驗期間皆低于Srr組和Srr微球組。在整個實驗期間, 對照組血清溶菌酶活力相對穩定在105—120 U/mL。
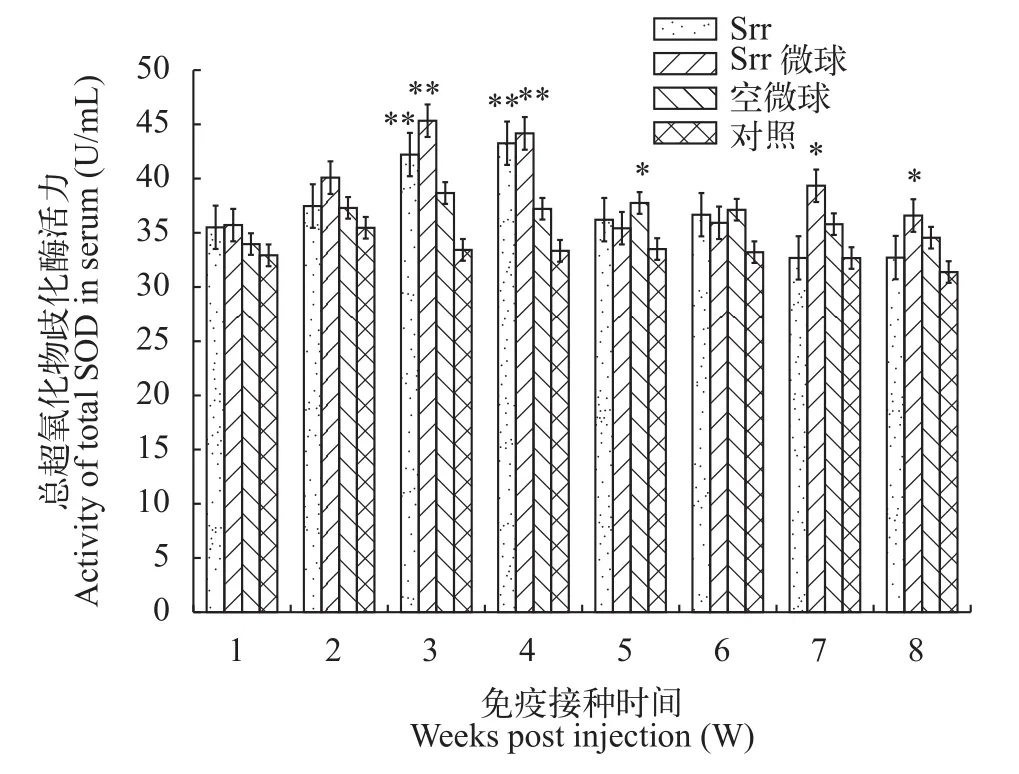
圖4 斑點叉尾鲙血清總超氧化物歧化酶活力變化Fig. 4 Changes of T-SOD activity in serum of Ictalurus punctatus
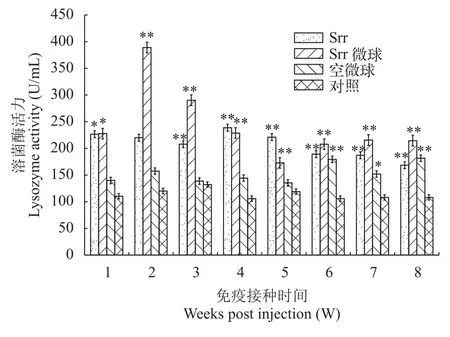
圖5 斑點叉尾鲙血清溶菌酶活力變化Fig. 5 Changes of lysozyme activity in serum of Ictalurus punctatus
2.6 微球疫苗對斑點叉尾鲖頭腎和脾臟免疫相關基因表達的影響
海豚鏈球菌攻毒后24h(圖6A), Srr微球組的的IFN-γ基因表現出極大的上調, 顯著(P<0.05)高于對照組, 而Srr組和空微球組雖也有上調, 但與對照組不存在顯著性關系(P>0.05); Srr微球組的TNF-α基因的表達量顯著(P<0.05)或者極顯著(P<0.01)的高于其他實驗組; 所有實驗組的CD4L-2基因和MHC-Ⅱβ基因的表達量不存在顯著性關系(P>0.05), 但是均略高于對照組有上調趨勢。攻毒后48h的脾臟(圖6B), Srr組和Srr微球組IFN-γ基因的表達量均顯著(P<0.05)高于空微球組和對照組;TNF-α的表達均較低, 但是Srr組和Srr微球組均顯著(P<0.05)或極顯著(P<0.01)高于空微球組和對照組; Srr微球組CD4L-2基因的表達顯著(P<0.05)高于空微球組和對照組; Srr微球組MHC-Ⅱβ基因極顯著(P<0.01)高于Srr組、空微球組以及對照組, Srr組與空微球組和對照組之間存在顯著差異(P<0.05)。
海豚鏈球菌攻毒后24h的頭腎(圖6C), Srr微球組的IFN-γ、CD4L-2和MHC-Ⅱβ基因表達量皆顯著(P<0.05)高于對照組,TNF-α基因表達量極顯著(P<0.05)高于其他實驗組,CD4L-2基因的表達量顯著(P<0.05)高于空微球和對照組,MHC-Ⅱβ的表達量顯著(P<0.05)高于空微球組。攻毒后48h的頭腎(圖6D), 斑點叉尾鲙頭腎中IFN-γ、TNF-α和MHC-Ⅱβ基因的表達在Srr微球組極顯著(P<0.01)高于空微球組和對照組,CD4L-2的表達顯著高于空微球組和對照組,IFN-γ的表達與Srr組存在顯著(P<0.05)差異,TNF-α的表達與Srr組存在極顯著(P<0.01)差異,MHC-Ⅱβ基因的表達顯著(P<0.05)高于Srr組。

圖6 海豚鏈球菌攻毒后24h/48h斑點叉尾鲙脾臟/頭腎中免疫相關基因相對表達量Fig. 6 Relative expression level of immune genes in spleen /kidney of vaccinated I. punctatus at 24h/48h post-challenge by S. iniae
2.7 微球疫苗對斑點叉尾鲖的保護效果
斑點叉尾鲙實驗前隨機剖解檢測, 均為正常健康斑點叉尾鲙。免疫后第4周進行攻毒, 對瀕死的斑點叉尾鲙接菌檢測, 確定致病菌為海豚鏈球菌;海豚鏈球菌攻毒14d后, Srr組和Srr微球組分別獲得抗海豚鏈球菌相對免疫保護率為35%和60%, 而空微球組和對照組在攻毒后14d內全部死亡(圖7)。
3 討論
海藻酸鈉是一種聚陰離子多聚物, 殼聚糖是一種聚陽離子聚合物, 兩者接觸后發生靜電反應, 可在海藻酸鈉表面形成一層聚電解質膜, 從而緊密包裹蛋白, 使微球的穩定性和載藥量都得到顯著提高[15]。本實驗以海藻酸鈉和殼聚糖兩種天然高分子聚合物為載體包被海豚鏈球菌Srr蛋白, 利用乳化法制備海藻酸鈉-殼聚糖-海豚鏈球Srr蛋白微球口服疫苗, 獲得了較高的包封率和載藥率; 通過Western-blot對微球釋放蛋白的抗原性進行檢測, 結果表現出較好的抗原性, 由此可見該制備方法較為溫和, 可以保證包裹抗原的完整性。
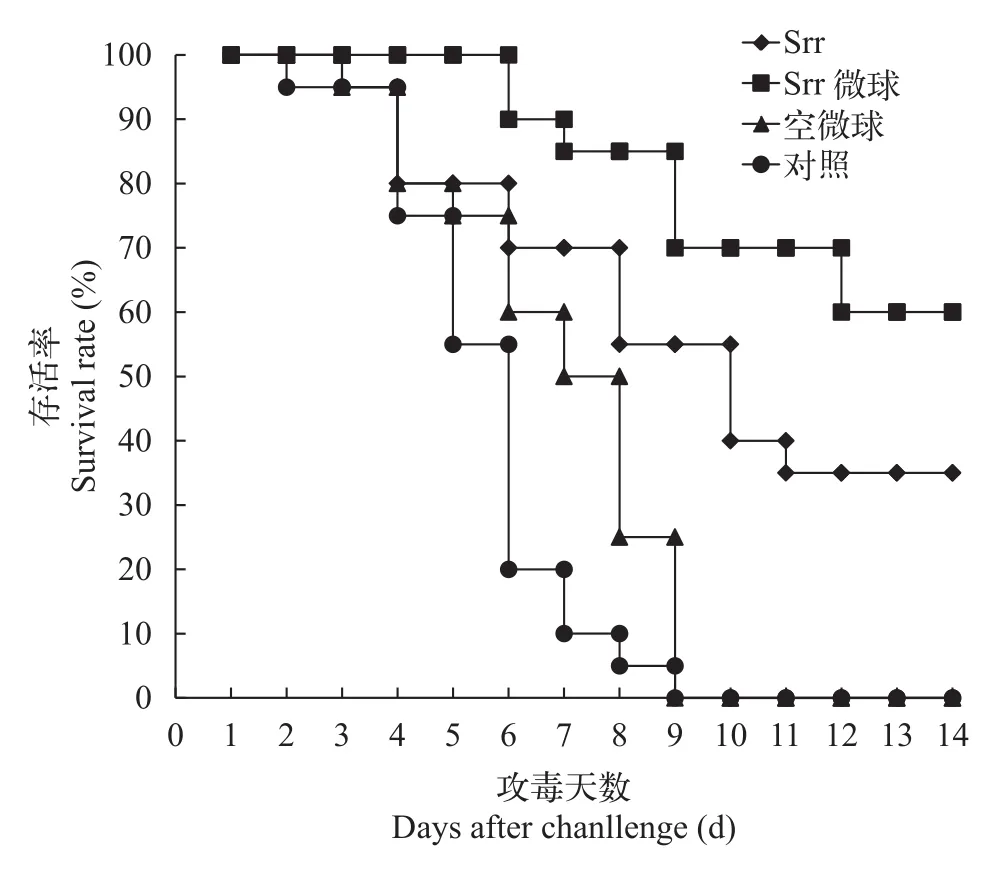
圖7 攻毒后的存活率Fig. 7 Survival rate after chanllenge
酶聯免疫吸附實驗(ELISA)自1971年被Engvall和Perlmann創建以來, 該方法以操作簡單, 檢測樣本量大, 敏感度較高以及特異性較強等優點逐步成為血清抗體效價檢測的重要方法[16]。本實驗通過間接ELISA檢測了斑點叉尾鲙在免疫后的血清抗體水平。Srr組和Srr微球組在實驗中均能檢測到特異性抗體, 且峰值均出現在了第4周, 分別為0.85和0.99, 由此說明微球疫苗Srr組和Srr微球組均能刺激機體產生免疫應答; 空微球雖然也能檢測到特異性抗體, 但是抗體效價相對較低, 推測可能是殼聚糖和海藻酸鈉本身可作為免疫增強劑的原因[17,18]; 而對照組始終沒有檢測出特異性抗體。最后通過攻毒實驗測定了各實驗組的相對保護率,Srr組和Srr微球組分別為35%和60%, 由此可見Srr蛋白對機體具有一定的保護效果, 且Srr微球組的保護效率遠遠高于Srr直接拌飼投喂組, 推測是海藻酸鈉-殼聚糖的包裹作用通過酸堿反應控制藥物的釋放速度, 減少了Srr蛋白在機體胃腸酸堿環境中的損失, 使蛋白更有效地被腸道吸收發揮作用。
非特異性免疫在作為低等脊椎動物的魚類疫系統中起著重要的作用。血清總蛋白的成分和含量與魚體的健康狀況緊密相連[19]。本實驗對斑點叉尾鲙免疫包被的口服微球疫苗后, 實驗組血清總蛋白含量均顯著升高, 且Srr組和Srr微球組在第4周達到最高值, 說明Srr蛋白對機體增強免疫能力具有一定的積極意義。超氧化物歧化酶(SOD)是一種廣泛存在于機體內的重要抗氧化酶, 對平衡機體氧化作用和抗氧化作用中必不可少, 且在清除O2-自由基, 增強機體防御能力中起到了重要的作用[20]。實驗結果表明, SOD的活力與機體免疫水平具有緊密的關系, Srr微球組免疫后SOD活力逐步增強, 并在第3周和第4周極顯著高于對照組, 隨后出現下降,魚體免疫力相應有所下降。由此推測疫苗免疫斑點叉尾鲙后能夠刺激魚體識別抗原, 促使SOD分泌, 維持機體氧化物和抗氧化物的平衡, 達到保護魚體的目的。溶菌酶(LSZ)是魚類抵御外來病原感染的重要非特異性免疫防御因子之一, 主要存在魚類的黏液、血清以及巨噬細胞中, 能夠病原微生物,保護魚體[21]。在本實驗中, 免疫后各實驗組的溶菌酶活性均有提高, 且在整個實驗期間, Srr微球組的溶菌酶活性一直顯著(P<0.05)或者極顯著(P<0.01)的高于對照組。由此可推測溶菌酶的高活性能夠提高魚體抵御病原微生物的能力。
本實驗利用Real-time RCP方法探究了Srr蛋白疫苗對斑點叉尾鲙免疫相關基因表達的影響。TNF-α、IFN-γ、MHC-Ⅱβ和CD4L-2基因在機體脾臟和頭腎的表達情況是疫苗效果評價中的重要指標。本實驗中Srr微球組免疫攻毒后的脾臟和頭腎中TNF-α、IFN-γ、CD4L-2和MHC-Ⅱβ因子的表達均明顯高于Srr組、空微球組以及對照組, 由此可推測Srr蛋白刺激了TNF-α因子調節趨化因子的產生,對中性粒細胞和巨噬細胞進行誘導, 并遷移到病原菌入侵部位發揮免疫功能[22,23], 同時,IFN-γ因子的上調可能刺激了機體巨噬細胞對病原微生物的殺傷能力, 從而起到增強機體免疫應答的作用[24], 推測Srr包被疫苗在增強魚體抵抗病原能力以及增強機體免疫力起到了一定的作用。研究表明, 不僅海藻酸鈉和殼聚糖能發生靜電反應, 其微球進入體內后外膜殼聚糖上游離的氨基能與黏膜上皮細胞上帶負電的糖蛋白或細胞間緊密結合部分固有的負電荷也能發生靜電作用, 從而打開了上皮細胞之間緊密連接, 促進了藥物的吸收[25—27], 且釋放的藥物可通過跨細胞途徑或者細胞旁路途徑穿過上皮細胞, 提高免疫效果[28]。本實驗結果表明Srr蛋白對斑點叉尾鲙海豚鏈球菌病具有一定的防御作用, 同時Srr組和Srr微球組的免疫效果差異不僅體現了海藻酸鈉-殼聚糖對蛋白藥物的保護作用, 也體現了這兩種高分子載體對蛋白藥物的促進吸收作用。
[1]Pier G B, Madin S H.Streptococcus iniaesp. nov., a beta-hemolyticStreptococcusisolated from an Amazon Freshwater Dolphin,Inia geoffrensis[J].International Journal of Systematic Bacteriology, 1976, 26(4): 545—553
[2]Agnew W, Barnes A C.Streptococcus iniae: An aquatic pathogen of global veterinary significance and a challenging candidate for reliable vaccination [J].Veterinary Microbiology, 2007, 122(1-2): 1—15
[3]Cheng S, Hu Y H, Jiao X D,et al. Identification and immunoprotective analysis of aStreptococcus iniaesubunit vaccine candidate [J].Vaccine, 2010, 28(14): 2636—2641
[4]Elaamri F. First report ofStreptococcus iniaein red porgy(Pagrus pagrus,L.) [J].Journal of Fish Diseases, 2010,33(11): 901—905
[5]Prettogiordano L G, Scarpassa J A, Barbosa A R,et al.Streptococcus iniae: an unusual important pathogen fish in Brazil [J].Journal of Aquaculture Research & Development, 2015, 6(9): 363
[6]Yu X L, Chen M, Li C,et al. Channel catfishIctalurus punctatusoutbreak infected by bacteriumStreptococcus iniae[J].Journal of Dalian Fisheries University, 2008,23(3): 185—191 [余曉麗, 陳明, 李超, 等. 斑點叉尾鲙暴發性海豚鏈球菌病的研究. 大連海洋大學學報, 2008,23(3): 185—191]
[7]Chen D F, Wang K Y, Geng Y,et al.Streptococcus iniaeisolated from channel catfish (Ictalurus punctatus) in China [J].The Israeli Journal of Aquaculture. Bamidgeh,2011, 63(1): 63—70
[8]Fischetti V A, Pancholi V, Schneewind O. Conservation of a hexapeptide sequence in the anchor region of surface proteins from Gram-positive cocci [J].Molecular Microbiology, 1990, 4(9): 1603—1605
[9]Seifert K N, Adderson E E, Whiting A A,et al. A unique serine-rich repeat protein (Srr-2) and novel surface antigen (epsilon) associated with a virulent lineage of serotype IIIStreptococcus agalactiae[J].Microbiology, 2006,152(4): 1029—1040
[10]Zhou M, Zhang H, Zhu F,et al. Canonical SecA associates with an accessory secretory protein complex involved in biogenesis of a streptococcal serine-rich repeat glycoprotein [J].Journal of Bacteriology, 2011, 193(23):6560—6566
[11]Yang L, Wang K Y, Zhou Y,et al. The characteristics and immune efficacy of an oral microspheres vaccine ofYersinia ruckeri[J].Acta Hydrobiologica Sinica, 2015,39(6): 1142—1149 [陽磊, 汪開毓, 周燕, 等. 魯氏耶爾森氏菌口服微球疫苗特性分析及免疫效果研究. 水生生物學報, 2015, 39(6): 1142—1149]
[12]Jiang J, Zheng Z, Wang K,et al. Adjuvant immune enhancement of subunit vaccine encoding pSCPI ofStreptococcus iniaein channel catfish (Ictalurus punctatus) [J].International Journal of Molecular Sciences, 2015,16(12): 28001
[13]Ren Y, Zhang X J, Tao J F,et al. Preparation and immune effect of chitosan-alginate microcapsules containingVibrio harveyiantigen OmpK in orange-spotted groupers [J].Chinese Journal of Biologicals, 2015, 28(2):110—114 [任燕, 張小江, 陶家發, 等. 殼聚糖-海藻酸鹽復合微囊疫苗的制備及其對斜帶石斑魚的口服免疫效果. 中國生物制品學雜志, 2015, 28(2): 110—114]
[14]Yang Q, Pan Y L, Wang K Y,et al. OmpN, outer membrane proteins ofEdwardsiella ictaluriare potential vaccine candidates for channel catfish (Ictalurus punctatus)[J].Molecular Immunology, 2016, 78: 1—8
[15]Morteza H, Kafshgari M, Khorram,et al. Reinforcement of chitosan nanoparticles obtained by an ionic cross-linking process [J].Iranian Polymer Journal, 2011, 20(5):445—456
[16]Li W M. Development and application of enzyme linked immuno sorbent assay technology [J].Journal of Hubei Vocational-Technical College, 2003, 6(4): 65—69 [李文敏. 酶聯免疫吸附反應的技術進展及應用. 湖北職業技術學院學報, 2003, 6(4): 65—69]
[17]Tan X D, Li Y, Zhang H Y,et al. Effects of sodium alginate on the immune response and the disease resistance ability of Chinese mitten crabEriocheir sinensis[J].Feed Industry, 2008, 29(6): 24—27 [譚夕東, 李義, 張紅英,等. 海藻酸鈉對中華絨螯蟹免疫功能及抗病力的影響.飼料工業, 2008, 29(6): 24—27]
[18]Xiao Y Y, Xia Y T, Liu T F,et al. Effects of chitosan on growth performance and immunity of juvenile Russian sturgeon (Acipenser gueldenstardti) [J].Acta Hydrobiologica Sinica, 2017, 41(1): 114—120 [肖艷翼, 夏永濤, 劉騰飛, 等. 殼聚糖對俄羅斯鱘幼魚生長性能及免疫功能的影響. 水生生物學報, 2017, 41(1): 114—120]
[19]Wu X J, Wang K Y, Yang L,et al. The immune effect of an oral microspheres vaccine againstEdwardsiella ictalurion channel catfish (Ictalurus punctatus) [J].Journal of Fisheries of China, 2016, 40(3): 404—413 [吳學婧, 汪開毓, 陽磊, 等. 鲙愛德華菌口服疫苗對斑點鲙的免疫效果. 水產學報, 2016, 40(3): 404—413]
[20]Chun-Xiang A I, Chen L Q, Gao L J,et al. Effect of vitamin C on SOD, ALP and ACP activities of Chinese mitten-handed crab,Eriocheir sinensis[J].Journal of Oceanography in Taiwan Strait, 2002, 21(4): 431—438
[21]Yang X L. Advance on fish immunology research [J].Journal of Fisheries of China, 1989, 13(3): 271—284 [楊先樂. 魚類免疫學研究的進展. 水產學報, 1989, 13(3):271—284]
[22]Park K C, Osborne J A, Tsoi S C,et al. Expressed sequence tags analysis of Atlantic halibut (Hippoglossus hippoglossus) liver, kidney and spleen tissues following vaccination againstVibrio anguillarumandAeromonas salmonicida[J].Fish & Shellfish Immunology, 2005,18(5): 393—415
[23]Wei Y C, Pan T S, Chang M X,et al. Cloning and expression of Toll-like receptors 1 and 2 from a teleost fish, the orange-spotted grouperEpinephelus coioides[J].Veterinary Immunology & Immunopathology, 2011, 141(3—4):173
[24]Milevmilovanovic I, Long S, Wilson M,et al. Identification and expression analysis of interferon gamma genes in channel catfish [J].Immunogenetics, 2006, 58(1): 70—80
[25]Sonia T A, Rekha M R, Sharma C P. Bioadhesive hydrophobic chitosan microparticles for oral delivery of insulin:In vitro characterization and in vivo uptake studies [J].Journal of Applied Polymer Science, 2011, 119(5): 2902—2910
[26]Sonaje K, Lin K J, Wang J J,et al. Self-assembled phsensitive nanoparticles: a platform for oral delivery of protein drugs [J].Advanced Functional Materials, 2010,20(21): 3695—3700
[27]Sarmento B, Ribeiro A, Veiga F,et al. Alginate/chitosan nanoparticles are effective for oral insulin delivery [J].Pharmaceutical Research, 2007, 24(12): 2198—2206
[28]Wang C, Wang L W, Shi X Y,et al. Advances in applications of chitosan-sodium alginate microsphere to drug carriers for microparticulated systems [J].Progress in Modern Biomedicine, 2014, 14(16): 3174—3176 [汪程,汪令偉, 史曉宇, 等. 海藻酸鈉殼聚糖微球作為藥物載體的研究進展. 現代生物醫學進展, 2014, 14(16): 3174—3176]

