重癥慢性活動性EB病毒感染2例
劉穎強, 胡曉紅, 柳亞男, 李中原, 王 宇, 李喬俊, 李巖梅
兒童慢性活動性EB病毒感染以長期或間歇發熱、淋巴結腫大、肝/脾腫大為突出表現,癥狀持續存在或退而復現,臨床表現復雜、多樣,易漏診、誤診,延遲治療導致多器官、多系統損傷,甚至死亡[1]。本研究報告2016年我科收治的2例慢性活動性EB病毒感染患兒的臨床資料,以期提高基層醫師對兒童慢性活動性EB病毒感染臨床多樣性和隱匿性的認識。
1 臨床資料
病例1,11歲女童,因“反復發熱伴咽痛1年,加重2周”入我院。1年前首次出現發熱、咽痛,自服“感冒藥”及“抗生素”無效,外周血異型淋巴細胞0.09,血沉 43 mm/h,擬診傳染性單核細胞增多癥,予“阿昔洛韋”足量、足療程治療,體溫逐漸降至37.3~37.6 ℃,18 d后停藥出院。2個月后類似癥狀反復發作,伴有頸部淋巴結腫痛,服“中藥”可暫時緩解。本次入院前2周再次發熱,伴咽痛,血清抗EB病毒衣殼抗原(VCA)-IgM陰性、VCA-IgG>7 500 U/mL、抗EB病毒核抗原(NA)-IgG>1 500 U/mL以及抗早期抗原(EA)-IgG>6 000 U/mL均陽性,EB病毒-DNA定量5.70×106拷貝/mL。擬診“慢性EB病毒感染”收入院。追問病史3年前跑步后突發胸痛,當地醫院查心臟超聲提示主動脈根部增寬,自身抗體及抗鏈球菌溶血素等相關檢查多次陰性,除外風濕免疫相關疾病后未予治療;患兒平素體健,生長發育如同齡兒。否認心肌炎、川崎病病史,發病以來無明顯乏力、呼吸困難、無皮疹、盜汗及關節痛;體重無明顯改變。
入院后檢查:T38.2?℃,耳后及下頜可觸及綠豆大小淋巴結數個,質中,輕度觸痛,邊界清楚。胸骨左緣第3、4肋間可聞及3/6級嘆氣樣雜音;雙側呼吸音對稱清晰,脾稍大。多次血涂片見異型淋巴細胞,波動于0.02~0.18;EB病毒-DNA定量(+);腦脊液抗EB病毒-VCA-IgM(+)、EB病毒-DNA定量(+)(見表1);血液及腦脊液寡克隆區帶(+)。骨髓涂片見異型淋巴細胞,未見嗜血細胞。胸部CT:右上肺條索樣改變,右肺水平裂胸膜增厚。心臟彩超:主動脈根部增寬加重,最寬處41 mm,左心擴大。腹部超聲:腎動脈起始段狹窄;脾稍大。頭顱MRI提示右顳葉側腦室周圍異常信號。
依據患兒病例特點: ①反復發熱、咽痛、淋巴結腫大,持續超過3個月;②先后出現大動脈炎及心臟擴大、間質性肺炎、腦炎等多臟器受損;③血中抗EB病毒抗體異常增高及DNA定量陽性,腦脊液抗EB病毒抗體及DNA定量(+);④除外自身免疫性疾病、EB病毒相關嗜血綜合征以及其他感染性疾病,慢性活動性EB病毒感染診斷明確[2-3],先后給予更昔洛韋、丙種球蛋白、甲潑尼龍治療,患兒體溫逐漸降至正常。9周后患兒出現右側顳部發作性刺痛及左側面、軀干和肢體游走性麻木;伴頭暈、惡心、嘔吐;復查血液及腦脊液EB病毒-DNA定量(+)(見表1);血液及腦脊液寡克隆區帶(+);頭顱MRI顯示右顳葉側腦室周圍異常信號,較前范圍略增大;腦電圖提示右側頂、枕、后顳反復發放不規則慢波;右前中顳散在非同步不規則慢波。胸部CT提示雙肺感染并出現胸腔積液;患兒病情進展并出現肺炎、腦炎及心、腎動脈改變,符合重癥EB病毒感染[2,4],轉至專科醫院準備造血干細胞移植[2]。移植準備治療過程中患兒血液EB病毒-DNA定量持續>103拷貝/mL,后因感染、多臟器功能衰竭死亡。
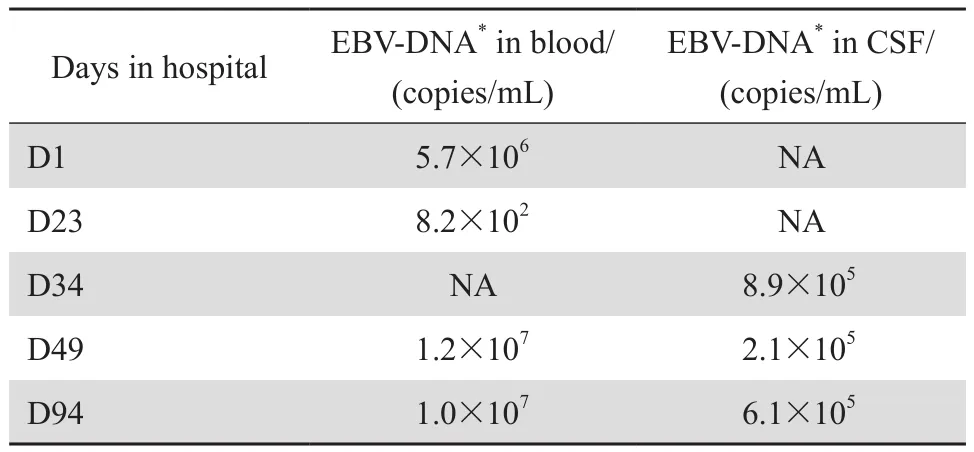
表1 病例1 治療期間外周血和腦脊液EB病毒-DNA定量Table 1 On-treatment EBV-DNA quantification in peripheral blood and cerebrospinal fluid samples of patient 1
病例2,6歲女童,因“間歇發熱、淋巴結腫大3周”入院。病初當地診斷“急性化膿性扁桃體炎”,靜脈滴注“阿奇霉素”、“頭孢唑林”未見效。入院后檢查:T40.2 ℃,神清語利,雙側耳后、頸部及腋窩均可及多個腫大淋巴結,無紅腫,質中,活動度可,不融合,與周圍組織無粘連。最大者3.0 cm×4.0 cm;觸痛明顯。雙肺呼吸音粗,未聞及干濕性啰音。血涂片異型淋巴細胞 0.06;EB病毒-IgG陽性,EB病毒-DNA定量:9.3×104拷貝/mL; PPD、肥達試驗、血培養未見異常;胸部CT提示肺部及縱隔多發淋巴結腫大,肺部多發小結節,肺泡灌洗液提示:EB病毒-DNA定量1.1×106拷貝/mL;腹部超聲提示:脾腫大。擬診EB病毒感染,予更昔洛韋治療4周,體溫正常,淋巴結消退出院。出院1個月后再次出現反復發熱、淋巴結腫痛,多次復查血液EB病毒DNA定量陽性(見表2);腦脊液EB病毒抗體陽性;胸部CT提示雙肺多發結節影,較前增多;縱隔內及雙側腋窩多發增大淋巴結;骨髓涂片見異型淋巴細胞;給予甲潑尼龍沖擊治療后體溫逐步正常,頸部淋巴結縮小。停藥后再次出現發熱伴淋巴結腫痛,予更昔洛韋及甲潑尼龍、丙種球蛋白治療無效,外周血三系出現進行性減低(表3)。診斷慢性活動性EB病毒感染,轉至專科行骨髓移植,過程順利,移植后合并感染死亡。
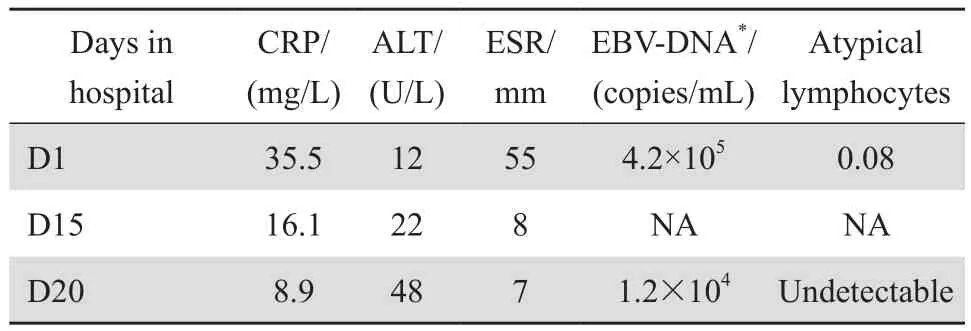
表2 病例2 住院期間血液檢驗結果Table 2 In-hospital blood tests for patient 2

表3 病例2 血常規Table 3 Routine blood tests of patient 2
2 討論
EB病毒是一種嗜B淋巴細胞的人類皰疹病毒,主要通過唾液、飛沫傳播,咽部上皮細胞復制。EB病毒感染在人類無處不在,以兒童和青少年常見[5],我國3~5歲兒童EB病毒抗體陽性率高達80.7%[4]。兒童最常見的EB病毒感染為急性感染,表現為發熱、咽峽炎、淋巴結腫大“三聯征”為特點的傳染性單核細胞增多癥,預后良好,極少患兒病情遷延,反復發作,轉變為慢性活動性EB病毒感染[2-3,6]。部分患者可發展為 EB病毒相關性噬血性淋巴組織增生(EB病毒-HLH),致死率高達30%~40%[7-8]。
本組2例患者分別是11歲和6歲女孩,平素體健,表現為反復發熱,肝/脾、淋巴結腫大,抗生素治療無效,伴有肺、心、腦并發癥;外周血EB病毒抗體和EB病毒-DNA定量持續增高,故符合慢性活動性EB病毒感染診斷[2,9]。更昔洛韋抗病毒以及丙種球蛋白、糖皮質激素聯合治療初期可以緩解,但仍反復發作且逐漸加重,符合重癥慢性活動性EB病毒感染。見表4[2-4,10]。

表4 重癥慢性活動性EB病毒感染的診斷標準Table 4 Diagnostic criteria of severe chronic active EB virus infection
病例1入院前1年內反復出現發熱、咽峽炎和淋巴結腫大等EB病毒感染相關表現,血清EB病毒-DNA定量持續波動在5×106~8.22×102拷貝 / mL,給予更昔洛韋、大劑量丙種球蛋白和激素治療效果不佳,病毒持續復制,直至出現腦、肺并發癥,移植前化療過程中,因多臟器受損和嚴重感染死亡。追問病史得知,患兒出現EB病毒感染典型表現前2年,因運動后胸痛,且主動脈進行性增寬、左心擴大及腎動脈增寬,除外風濕免疫相關疾病,未治療。患兒血液、腦脊液中EB病毒-DNA定量持續升高,基于文獻復習[9,11],推測其3年前的主動脈異常系EB病毒感染引起,而EB病毒感染持續活動可能是造成主動脈、腎動脈異常和心臟增大的原因,未能早期進行病毒檢查導致延誤診斷及治療。實踐中,慢性活動性EB病毒感染患者合并嚴重心血管損害并不少見。Muneuchi等[11]報道了20年內追蹤的15例慢性活動性EB病毒感染患者的心血管系統損害的發生率達60%,而且心血管并發癥是慢性活動性EB病毒感染患者致死的重要危險因素。提醒廣大兒科醫師,對發現大動脈損害的患兒一定要完善EB病毒病原相關檢查,明確病因,避免誤診和漏診。同時,對慢性活動性EB病毒感染患者選擇心臟彩超、CT血管重建等影像學檢查早期發現心血管系統并發癥,有助于改善預后。
病例2無咳嗽、咯痰等肺部感染表現;胸部CT提示肺結節,支氣管鏡檢并肺泡灌洗液提示EB病毒肺炎;及時診斷慢性活動性EB病毒感染,給予更昔洛韋、丙種球蛋白和糖皮質激素治療后,癥狀緩解,肺結節減少。與EB病毒感染相關的肺結節少見描述,臨床醫師關注不夠。文獻報道12歲日本男孩,CT發現肺上多個小圓形結節(7個,4~8 mm )。咽部扁桃體活檢提示EB病毒編碼小RNA陽性細胞,淋巴瘤相關檢查陰性,診斷為非典型傳染性單核細胞增多癥,給予相應治療后肺結節大小和數目減少[12]。肺結節發病機制是咽部持續增殖的EB病毒不能有效清除,直接入血液循環播散到肺組織,引起肺部損害,并以肺間質改變為主[13]。本例患兒雖無明顯咳嗽、咯痰,但肺泡灌洗液提示抗EB病毒-VCA-IgG及EB病毒-DNA均為陽性。提醒廣大基層兒科醫師,頭頸部非典型淋巴增生一定要鑒別診斷,提示EB病毒感染時注意肺部并發癥[14]。肺部發現結節時也要注意EB病毒感染可能,尤其是慢性活動性EB病毒感染。
結合這2例患兒的不良預后,提醒我們,盡可能提高意識,早期診斷[3]。臨床癥狀不典型時,病毒學實驗室檢查對早期診斷有重要意義。目前EB病毒血清學特異性抗體檢測主要包括抗EB病毒VCA-IgM 、IgG、抗NA-IgG以及抗EA-IgG。抗VCA-IgM 為EB 病毒新近感染的標志性抗體,產生于感染4~7 d,3~4周后滴度可逐漸降低直至消失,再次感染時,抗VCA-IgM 不出現升高[9,15]。抗EA-IgG出現在感染的急性期,部分潛伏感染病毒重新激活,抗EA-IgG 可呈現陽性結果[16],正如這2個患兒的情況。抗VCA-IgG 、抗NA-IgG則對既往感染的意義較大[17]。EB病毒特異性抗體譜可以因宿主體液免疫應答的個體差異有所變化。本組例1診斷時EA-IgG抗體陰性,但EB病毒-NDA定量明顯升高[9-11],可能與機體對EB病毒特異性免疫應答存在某些缺陷有關。由于慢性活動性EB病毒感染發病與病毒復制有關,EB病毒-DNA定量作為EB病毒感染的分子生物學標記,可以反映體內的病毒復制水平[18]。本2例患兒,病情反復發作、逐漸加重,雖抗VCA-IgM 出現陰性結果,但外周血EB病毒-DNA定量持續增高與病情進展相符合。提醒兒科醫師,對病程長、癥狀反復、病情重的患兒監測血漿中EB病毒-DNA定量有助于評估治療效果及預后轉歸[19]。
慢性活動性EB病毒感染治療困難,成為重癥醫學新的關注熱點。更昔洛韋、丙種球蛋白治療,嚴重病例加用激素[18,20],療效并不確切,治療有效也多為暫時緩解,目前認為異基因造血干細胞移植是慢性活動性EB病毒感染最終的治愈方法[21-22]。本組病例1出現EB病毒感染典型癥狀前,已出現大動脈受損,但未能及時診斷,延誤治療時機,在準備移植過程中因逐漸出現多臟器功能衰竭死亡;病例2及時進行造血干細胞移植,取得滿意效果,出院后因合并巨細胞病毒感染、輪狀病毒腸炎死亡。因此,慢性活動性EB病毒感染預后并不樂觀,早期發現和早期診斷有非常重要的臨床意義。
[1]KIMURA H, HOSHINO Y, KANEGANE H, et al. Clinical and virologic characteristics of chronic active Epstein-Barr virus infection[J]. Blood,2001,98(2):280-286.
[2]胡亞美,江載芳,申昆玲,等. 諸福棠實用兒科學[M]. 8版.北京:人民衛生出版社,2015:916-919.
[3]郭子雄,鐘敏泉,翟瓊香,等. 小兒嗜血細胞綜合癥并多臟器功能不全臨床特征研究[J]. 中華臨床醫師雜志(電子版),2011,5(8):2374-2377.
[4]KIMURA H, MORISHIMA T, KANEGANE H,et al.Prognostic factors for chronic active Epstein-Barr virus infection[J]. J Infect Dis,2003,187(4):527-533.
[5]COHEN JI. Epstein-Barr virus infection[J]. N Engl J Med,2000,343(7):481-492.
[6]胡榮盛,徐亞麗,俞曉春,等. 血漿 EB 病毒 DNA 載量檢測在兒童EB 病毒感染中的應用價值[J]. 中華醫院感染學雜志,2014,24(11):2855.
[7]IMASHUKU S. Treatment of Epstein-Barr virus-related hemophagocytic lymphohistiocytosis (EBV-HLH);update 2010[J]. J Pediatr Hematol Oncol,2011,33(1):35-39.
[8]陸曉茜,高舉. 慢性活動性 EBV 感染診治進展[J]. 中國小兒血液與腫瘤雜志,2013,18(5):198-200,213.
[9]段紅梅,姚瑤,謝正德,等. 91例EB病毒相關疾病兒童血漿EB病毒DNA的檢測[J]. 中國當代兒科雜志,2009,11(11):897-900.
[10]中華醫學會兒科學分會感染學組,全國兒童EB病毒感染協作組. 兒童主要非腫瘤性EB病毒感染相關疾病的診斷和治療原則建議 [J]. 中華兒科雜志,2016,54(8):563-568.
[11]MUNEUCHI J,OHGA S,ISHIMURA M, et al.Cardiovascular complications associated with chronic active Epstein-Barr virus infection[J]. Pediatr Cardiol, 2009,30(3):274-281.
[12]SHINOZUKA J,AWAGUNI H,TANAKA S, et al.Spontaneous regression of pulmonary nodules presenting as Epstein-Barr virus-related atypical infectious mononucleosis [J].J Pediatr Hematol Oncol,2016,38(5):e162-e165.
[13]BODE SF,LEHMBERG K,MAUL-PAVICIC A,et al. Recent advances inthe diagnosis and treatment of hemophagocytiec lymphohistiocytosis[J]. Arthritis Res Ther,2012,14(3):213.
[14]AUERBACH A,AGUILERA NS. Epstein-Barr virus (EBV)-associated lymphoid lesions of the head and neck[J]. Semin Diagn Pathol,2015,32(1):12-22.
[15]KIMURA H,ITO Y,SUZUKI R,et al. Measuring Epstein-Barr virus (EBV)load:the significance and application for each EBV . associated disease[J]. Rev Med Virol, 2008,18(5):305-319.
[16]馬展,張泓. 兒童 EB 病毒感染的實驗室診斷[J]. 中華檢驗醫學雜志,2015,38(4):223.
[17]AHN JS,REW SY,SHIN MG,et al. Clinical significance of clonality and Epstein-Barrvirus infection in adult patients with hemophagocytic lymphohistiocytosis [J]. Am J Hematol ,2010,85(9):719-722.
[18]VOULOUMANOU EK, RAFAILIDIS PI, FALAGAS ME. Current diagnosis and management of infectious mononucleosis[J]. Curr Opin Hematol,2012,19(1):14-20.
[19]YAMASHITA N,KIMURA H,MORISHIMA T. Virological aspects of Epstein-Barr virus infections[J]. Acta Med Okayama,2005,59(6):239-246.
[20]MAAKAROUN NR, MOANNA A, JACOB JT, et al. Viral infections associated with haemophagocytic syndrome[J]. Rev Med Virol, 2010,20(2):93-105.
[21]SABURI M, OGATA M, SATOU T, et al. Successful cord blood stem cell transplantation for an adult case of chronic active epstein-barr virus infection[J]. Intern Med,2016,55(23):3499-3504.
[22]MATSUI S, TAKEDA Y, ISSHIKI Y, et al. Chronic active Epstein-Barr virus infection with marked pericardial effusion successfully treated with allogeneic peripheral blood stem cell transplantation[J]. Rinsho Ketsueki,2016,57(5):624-629.

