深圳南澳海域半葉馬尾藻的金屬元素富集特性分析*
劉莉萍,楊舒珊,金 剛
(深圳職業技術學院 應用化學與生物技術學院,廣東 深圳 518055)
半葉馬尾藻(Sargassum hemiphyllum)隸屬褐藻門(Phaeophyta)、馬尾藻科(Sargassaceae)、馬尾藻屬、反曲葉亞屬,在我國東海和南海沿岸均比較常見[1].大部分馬尾藻不直接食用,但可廣泛用于飼料、藻膠和醫藥行業.馬尾藻中含有豐富的礦物質和維生素,是某些礦物質和維生素的重要來源[2].半葉馬尾藻中富含海藻多糖,海藻多糖具有抗腫瘤、抗病毒、抗輻射、抗氧化、免疫調節等作用[3-7].此外,半葉馬尾藻也能從周圍水環境中富集濃度很低的營養鹽和重金屬元素[8-10],所吸附的重金屬元素能被酸很好地解吸[11-12],是一類很有潛力的生物吸附材料.因而研究利用馬尾藻作為生物吸附材料,用于生態環境污染的治理和修復,對實現某些地區資源與環境的可持續發展,不僅具有理論意義,而且具有潛在的應用價值.本研究通過對深圳近岸海水域半葉馬尾藻和海水中的金屬元素含量進行分析,探究金屬元素在生態系統內的遷移和轉化規律,有助于研究生物富集作用,為半葉馬尾藻的環保作用提供基礎數據.
1 實驗部分
1.1 材料與試劑
2016年3月至5月在深圳南澳月亮灣采集半葉馬尾藻及海水.
As,Pb,Cu,Cd,Zn,Fe,Mn,Se,Ni,Cr,K,Ca,Na,Mg 單標準溶液(濃度為 1000μg·mL-1,廣東分析測試中心科力技術開發公司),使用時用1%硝酸溶液將其逐級稀釋成標準溶液使用液.
濃硝酸、高氯酸均為優級純;其余試劑為分析純;實驗室用水為超純水.
硝酸-高氯酸混合酸(4+1):量取40 mL濃硝酸和10 mL高氯酸,依次加入燒杯中,混勻.
硝酸溶液(1%):量取1 mL濃硝酸,稀釋至100 mL,混勻.
氫氧化鈉溶液(100g/L):稱取10 g氫氧化鈉,用水溶解,稀釋至100mL,置于聚乙烯塑料瓶中保存.
1.2 儀器與設備
7500型電感耦合等離子體質譜儀(ICP-MS)美國Agilent公司;BSA224S電子分析天平(感量0.1mg) 德國賽多利斯公司;Cascada超純水系統 美國PALL公司;LG-04搖擺式高速中藥粉碎機(200g) 新昌縣德科機械有限公司.
1.3 馬尾藻試樣制備
馬尾藻試樣經淡水沖洗干凈,除去表面的泥沙和附生物,再用去離子水洗滌3次,置于陽光下曬干,除去表面水分,放入 100℃烘箱烘干至恒重,粉碎,過40目篩,保存于干燥器中備用.
1.4 試樣消化處理
1)海水試樣消化:準確吸取10 mL海水試樣于錐形瓶中,加入硝酸-高氯酸混合液25 mL,在可調式電爐上消解.若消化液無澄清透明,再補加少量硝酸-高氯酸混合液,消解至消化液呈澄清透明.繼續加熱趕酸至近干,加入5 mL去離子水,再次加熱除去多余的混合酸,待趕酸至3 mL時,冷卻至室溫,將消化液移入50 mL容量瓶中,用水定容,搖勻備用.同時做試劑空白試驗.
2)馬尾藻試樣消化:準確稱取試樣 1g(精確至0.1mg)于錐形瓶中,加入硝酸-高氯酸混合液25 mL,在可調式電爐上消解.若消化液呈棕黑色,再加少量混合酸,消解至冒白煙,消化液呈無色透明或略帶黃色.加入20 mL水趕酸2次,每次趕酸至殘留消化液2 mL,冷卻后將消化液移入50 mL容量瓶中,用水定容,混勻備用.同時做試劑空白試驗.
1.5 試樣測定
1)海水試樣測定:用原始消化液直接測定As,Pb,Cu,Cd,Zn,Fe,Mn,Se,Ni,Cr;原始消化液逐級稀釋 500倍后,用于測定 K,Na,Ca;原始消化液逐級稀釋1000倍后,用于測定Mg.
2)馬尾藻試樣測定:用原始消化液直接測定Pb,Cu,Cd,Zn,Fe,Se,Ni,Cr;吸取原始消化液1 mL于10 mL比色管中,定容,供測定Mn,K,Na;吸取1 mL原始消化液于50 mL比色管中,定容,供As,Ca的測定;吸取2.5 mL原始消化液于50 mL比色管中,定容,供Mg的測定.
1.6 標準工作溶液配制
用 1%硝酸溶液逐級稀釋離子標準儲備液(1000 μg·mL-1)成標準工作溶液.
As,Pb,Cu,Cd,Zn,Mn,Se,Ni,Cr工作液濃度為 0,4,10,20,30,40ng·mL-1.
Fe,K,Na,Ca,Mg工作液濃度為 0,0.2,0.5,1.0,1.5,2.0 μg·mL-1.1.7 ICP-MS工作所條件
利用多元素溶液對ICP-MS儀器測定時的工作條件進行優化,結果見表1.

表1 ICP-MS儀器工作參數
2 結果與討論
2.1 標準曲線繪制
按優化的工作條件進行測定,以測量的響應值(Y)為縱坐標,相應濃度(X)為橫坐標,繪制標準曲線,標準曲線線性關系良好,相關系數r均在0.997以上,結果見表2.
2.2 方法的準確性與精密度
按優化的工作條件進行加標回收實驗,平行測定5次,結果見表3.
由表3數據可知,14種金屬元素測定方法回收率在97.3%~105.7%,RSD小于6.7%,方法準確、可靠.
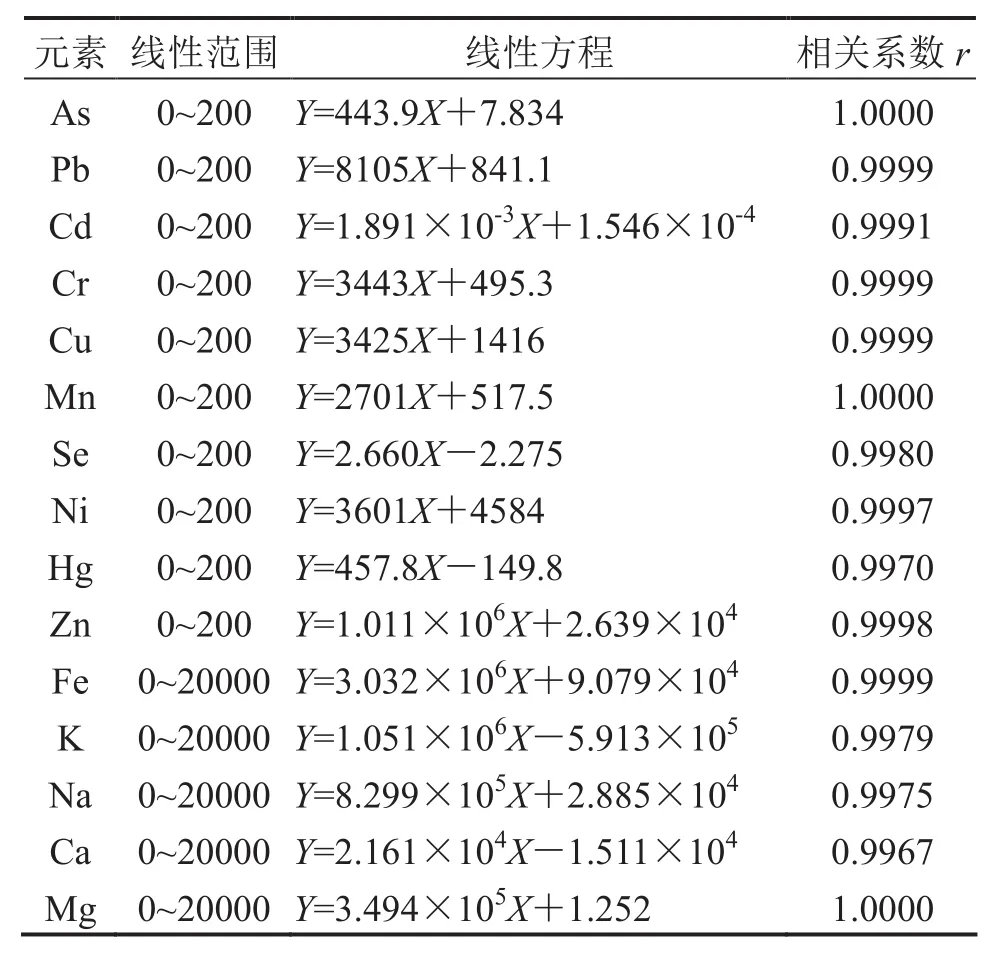
表2 標準曲線線性范圍(ng·mL-1)
2.3 金屬含量測定
半葉馬尾藻及其采集海域水體(海水)中金屬元素含量測定結果見表4.
由表4數據可知,在半葉馬尾藻中,金屬元素含量存在差異性.即使是同種金屬,在不同時期的半葉馬尾藻中,金屬元素含量也不同.在海水中含量最多的金屬是Na,其次是Mg,Ca,K.
半葉馬尾藻中金屬含量由大到小排序是K,Ca,Na,Mg,與海水中金屬元素含量順序相同.雖然各批次富集金屬元素含量存在差異,但是均呈上升趨勢,原因可能是:從3月到4月,陽光不斷地增強,半葉馬尾藻不斷生長,光合作用也在加強,需要不停地從海水中吸取各種金屬元素,參與到自身的生長代謝循環活動,導致體內在的金屬元素含量不斷的增加.
2.4 半葉馬尾藻對金屬元素的富集能力
根據半葉馬尾藻及其采集海域水體(海水)中金屬元素含量計算富集系數,結果見表5.
由表5數據可見,半葉馬尾藻中每種金屬元素含量均大于其海水中金屬元素含量,金屬元素的富集系數在0.75與85500之間,其中,富集能力最強的是半葉馬尾藻對 As的富集,富集能力較弱的是Se,富集能力最小的是半葉馬尾藻對Mg的富集.半葉馬尾藻對As,Cd,Fe的富集能力要遠遠大于對Zn,Pb的富集能力.實驗結果為區域運用藻類治理污水,水資源保護提供有用的數據支撐.
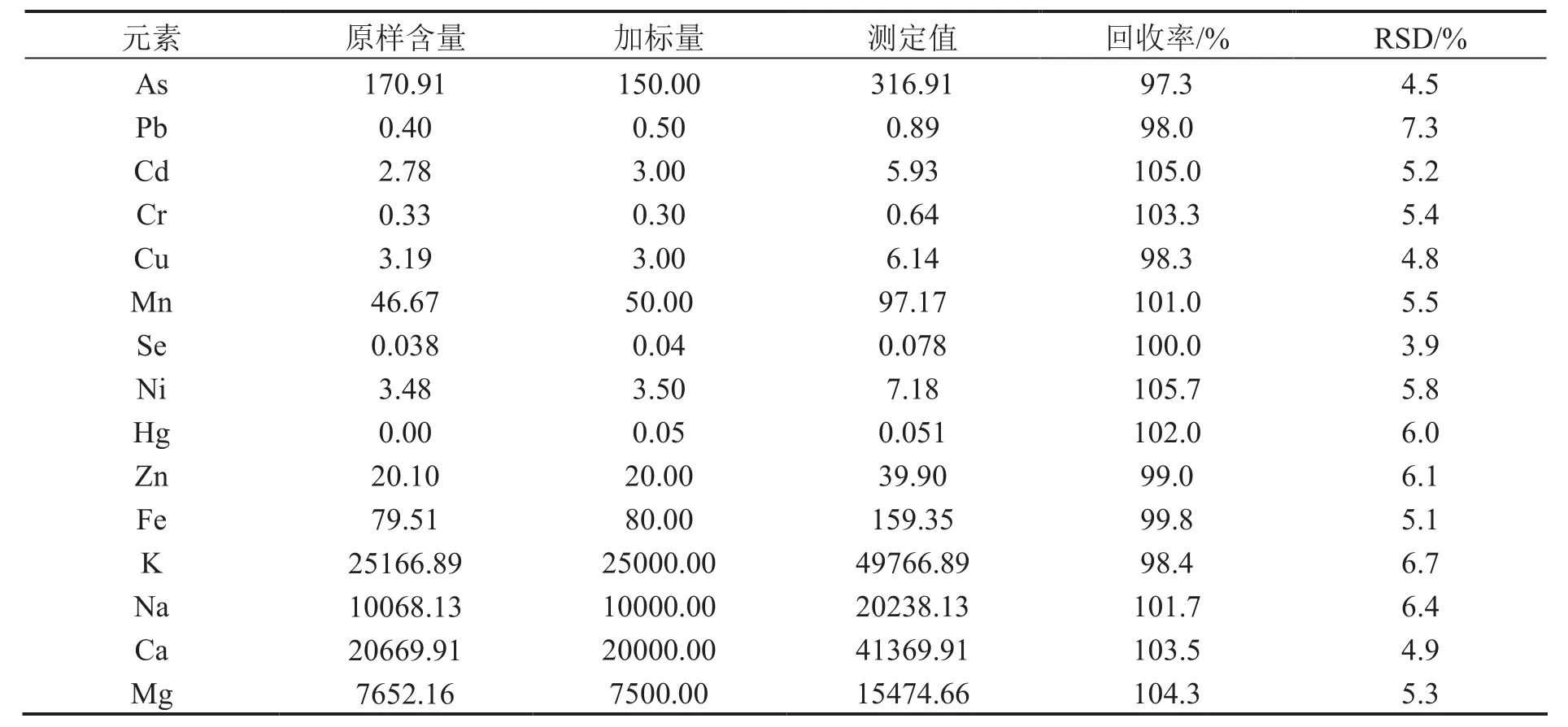
表3 回收率和精密度(mg/kg干質量,n=5)

表4 半葉馬尾藻和海水中金屬元素含量(mg/kg 干質量,n=2)
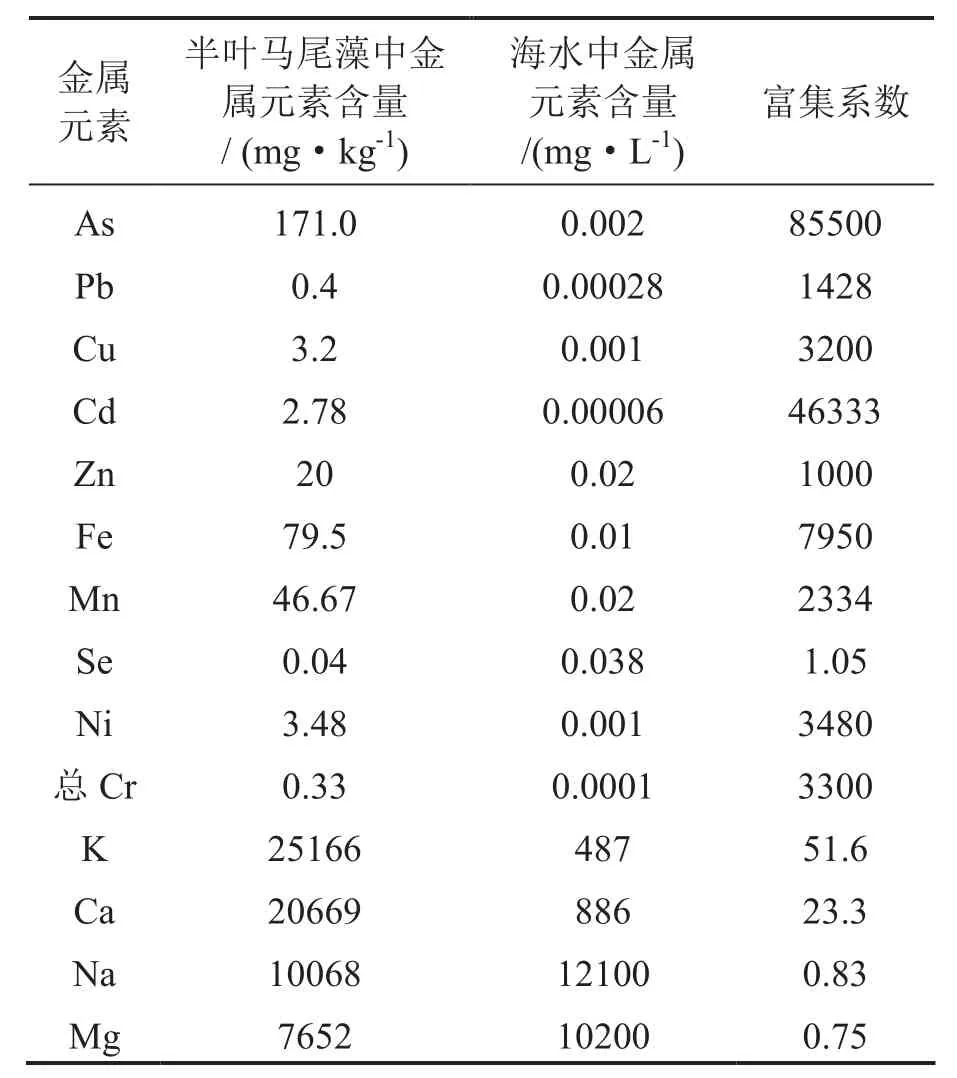
表5 半葉馬尾藻對金屬元素的富集系數
[1] 蔣福康,李慶欣,林堅士.大亞灣的馬尾藻資源研究[J].熱帶海洋,1996(1):85-902.
[2] 李來好,楊賢慶,吳燕燕,等.馬尾藻的營養成分分析和營養學評價[J].青島海洋大學學報,1997,27(3):319-325.
[3] 王新梅,閆美艷.海藻多糖生物活性研究進展[J].齊魯藥事,2009,28(4):228.
[4] 劉洪麗,胡庭俊,何穎,等.馬尾藻多糖分離提取及抗氧化活性初步觀察[J].江蘇農業科學,2009(6):337-339.
[5] 羅先群,王新廣,楊振斌.馬尾藻的營養成分測定及多糖的提取[J].化學與生物工程,2007,24(4):64-66.
[6] 王士長,陳靜,潘健存,等.馬尾藻多糖的提取及其免疫活性[J].食品科學,2006,27(9):257-260.
[7] 孫立春,張朝燕,孫國偉,等.馬尾藻茶飲料的制備及其抗氧化活性研究[J].湖北農業科學,2013,52(1):162-163.
[8] 鄧莉萍,蘇營營,蘇華,等.大型海藻吸附水體中重金屬離子的機理及影響因素[J].海洋科學,2008,32(8):90-96.
[9] 王夔.生物無機化學[M].北京:清華大學出版社,1988:200-203.
[10] 劉加飛,謝恩義,孫省利,等.湛江近岸馬尾藻中重金屬元素含量及富集分析[J].海洋開發與管理,2012(11):71-75.
[11] Ofer R, Yerachmiel A, Shmuely.Marine macroalgae as biosorbents for cadmium and nickle in water[J].Water Environment Research, 2003,75(3):246-253.
[12] Volesky B, Weber J, Park J M.Continuous-flow metal biosorption in a regenerable Sargassum column[J].Water Environment Research, 2003,37(2):297-306.

