TAC1和PRLR基因在綿羊不同繁殖狀態下的表達模式分析
李曉雨,賀小云,劉秋月,王翔宇,郭曉飛,夏 青,胡文萍,張效生,張金龍,儲明星*,狄 冉*
(1. 中國農業科學院北京畜牧獸醫研究所,農業部動物遺傳育種與繁殖重點實驗室,北京 100193;2. 天津市畜牧獸醫研究所,天津 300381)
在綿羊繁殖周期中,催乳素(Prolactin, PRL)與促性腺激素(Gonadotropins, Gn)釋放模式之間呈負相關關系:夏季即非繁殖季節血漿中PRL濃度升高而促性腺激素分泌減弱,綿羊表現為休情[1-4];秋冬季節綿羊血漿中PRL濃度降低而促性腺激素分泌增加,表現出發情特征。與秋冬繁殖季節相比,非繁殖季節綿羊垂體中催乳素細胞(Lactotropes)和濾泡星狀細胞(Folliculostellate cells, FSC)體積增大,且兩種細胞之間的縫隙連接增多,暗示這種催乳素細胞和FSC形態學季節性變化與PRL的分泌相關[5]。多項研究表明,在受光周期調控的動物中,促性腺激素細胞(Gonadotropes)和催乳素細胞之間的相互作用以及FSC的調節作用均響應于不同光照周期條件下松果體分泌的褪黑激素(Melatonin, Mel)信號。Mel首先作用于垂體結節部(Pars tuberalis, PT),然后通過PT神經肽信號以光周期依賴方式傳遞到遠側部(Pars distalis, PD)區域,并刺激PRL的分泌[6]。綿羊PT組織存在可促進PRL分泌的速激肽前體1(Tachykinin precursor 1, TAC1)[7-9],且TAC1作為綿羊PT中將Mel信號傳遞至PD部位的神經肽信號,有強烈的光周期性,TAC1基因可編碼速激肽物質P(Tachykinins substance P,SP)和神經激肽A (Neurokinin A,NKA),其中SP在肽鏈內切酶的作用下轉化為有活性的SP1-7與NKA共同調節PRL的分泌[10]。
也有研究表明,在短光照條件下,夜間Mel長時間持續存在作用于PT組織中MEL敏感細胞,通過旁分泌抑制了PD區域PRL的分泌,PRL與促性腺細胞上的催乳素受體(Prolactin receptor,PRLR)結合減弱,減少了對促性腺細胞的抑制及對FSC的下調作用;同時,PRL分泌減少也抑制了下丘腦多巴胺(Dopamine, DA)網絡的活化,由于DA能夠抑制PRL分泌以及GnRH神經元活性,因此此時GnRH神經元的去抑制作用促進了GnRH釋放,啟動了繁殖季節的到來;GnRH分泌的增加也通過促性腺細胞旁分泌作用于催乳素細胞,這可能增加了兩種細胞的相互作用以調控促性腺細胞響應于性腺反饋的信號。而長光照下,夜間Mel的短暫持續分泌不能抑制催乳素的分泌,PRL分泌突然增加,通過催乳素受體活化了DA神經元,導致GnRH分泌減少,通過FSC、催乳素細胞和DA調控網絡活動的增強完全抑制了促性腺細胞,從而使動物表現休情特征[11]。綜上,催乳素主要通過作用于垂體促性腺細胞和下丘腦神經元上的PRLR引起后續一系列生理變化[12-13]。
然而,PRL在動物季節性繁殖和繁殖時期轉換中的詳細調控機制尚不清楚,本研究針對PRL調控通路中的2個重要基因TAC1和PRLR在不同光照條件和不同繁殖時期綿羊垂體等組織中進行表達譜研究,并且分析由短光照變為長光照后2個基因的表達變化模式,為進一步揭示PRL在動物季節性繁殖和繁殖時期轉換中的作用機制奠定基礎。
1 材料與方法
1.1 動物材料
隨機選取2~3周歲健康、經產的空懷蘇尼特母羊和小尾寒羊母羊,飼養于天津市畜牧獸醫研究所試驗羊場。所有羊只的飼養管理方式、飼料配方和環境一致。每天飼喂2次,時間分別為05:30和15:30,每天給每只羊提供2.4 kg全混合日糧(2 kg干草與0.4 kg精料)供其自由采食,羊舍內提供舔磚補充微量元素,自由飲水。
1.1.1 蘇尼特羊 表達譜試驗:蘇尼特羊在人工控光條件下短光照(光照時長8 h,SP)第21天和長光照(光照時長16 h,LP)第49天(每個光照處理條件各3只)處死并分別采集下丘腦、垂體、松果體、大腦、小腦、卵巢、子宮體、輸卵管、腎、腎上腺等組織樣品,采集到的組織樣品經液氮速凍后-80 ℃保存。
短光照轉為長光照的表達模式試驗:蘇尼特羊在天津市畜牧獸醫研究所試驗羊場摘除卵巢并埋植雌激素處理(OVX+E2),短光照42 d后轉為長光照,并根據文獻報道[14-17]與本課題組預試驗結果,分別在短光照第21天(SP21D),長光照第3天(LP3D)、15天(LP15D)、21天(LP21D)、42天(LP42D)、49天(LP49D)上述每個時間點屠宰3只羊并采集上述組織,組織樣品經液氮速凍后-80 ℃保存。
1.1.2 小尾寒羊 用孕酮陰道栓(CIDR)對6只小尾寒羊進行處理,12 d后撤栓,撤栓之后第45小時為卵泡期,撤栓第10天為黃體期,在兩個時期分別屠宰3只后,采取相應組織樣品,樣品經液氮速凍后-80 ℃保存。
1.2 RNA提取
用Trizol和RNAprep pure動物組織總RNA提取試劑盒(天根生化科技北京有限公司)提取上述組織總RNA,提取過程中用RNase-free DNaseⅠ去除基因組DNA。利用NANODROP 2000檢測總RNA濃度和純度,OD值(A260 nm/A280 nm)為1.8~2.1,并用1%的瓊脂糖凝膠對RNA進行電泳檢測,無明顯降解,置于-80 ℃冷凍備用。
1.3 cDNA合成(RT-PCR)
使用PrimeScriptTM RT Reagent Kit反轉錄試劑盒(TaKaRa, Japan),按照說明書操作合成cDNA第一鏈。反轉錄產物稀釋后,用持家基因β-actin進行PCR檢測,可成功擴增。
1.4 定量引物設計
根據NCBI公布的綿羊TAC1 mRNA序列(NM_001082596.1)以及PRLRmRNA序列(GenBank:Y10578.1),并結合本課題組RNA-seq序列結果設計引物。引物信息如表1所示,由生工生物工程(上海)股份有限公司合成。
表1 熒光定量引物信息
Table 1 The information of primer sequences for qPCR
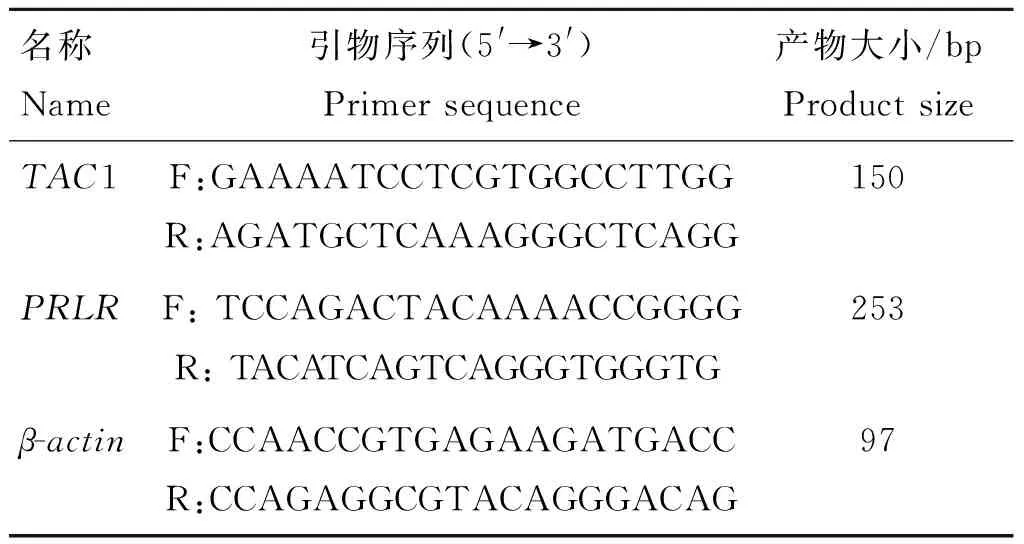
名稱Name引物序列(5'→3')Primersequence產物大小/bpProductsizeTAC1F:GAAAATCCTCGTGGCCTTGGR:AGATGCTCAAAGGGCTCAGG150PRLRF:TCCAGACTACAAAACCGGGGR:TACATCAGTCAGGGTGGGTG253β-actinF:CCAACCGTGAGAAGATGACCR:CCAGAGGCGTACAGGGACAG97
1.5 熒光定量PCR
使用Roche Light Cycler 480Ⅱ熒光定量PCR儀和SYBR?Premix Ex TaqTMⅡ(TaKaRa, Japan)試劑盒對2個基因進行熒光檢測,每個試驗樣品3個技術重復,β-actin作為內參基因,設置陰性對照(模板為H2O)。熒光定量PCR擴增體系:2×SYBR premix Ex Taq 10 μL,上下游引物各0.8 μL,RNase free H2O 6.4 μL,cDNA模板2 μL,反應體系總體積為20 μL。PCR程序:95 ℃ 預變性5 s;95 ℃ 5 s,60 ℃ 30 s,40個循環。反應結束后進行熔解曲線分析。
1.6 統計分析
采用2-ΔΔCT法計算目的基因相對表達量,數據差異顯著性用SPSS 20進行統計學分析,組間比較用單因素方差分析(One-way ANOVA),用最小顯著差異法(Least significant difference, LSD)進行多重比較,P<0.05表示差異顯著,P<0.01表示差異極顯著。所有試驗數據均用“平均值±標準誤(Mean±SE)”表示。
2 結 果
2.1 TAC1基因在不同光照條件下蘇尼特羊和不同繁殖時期小尾寒羊的組織表達譜
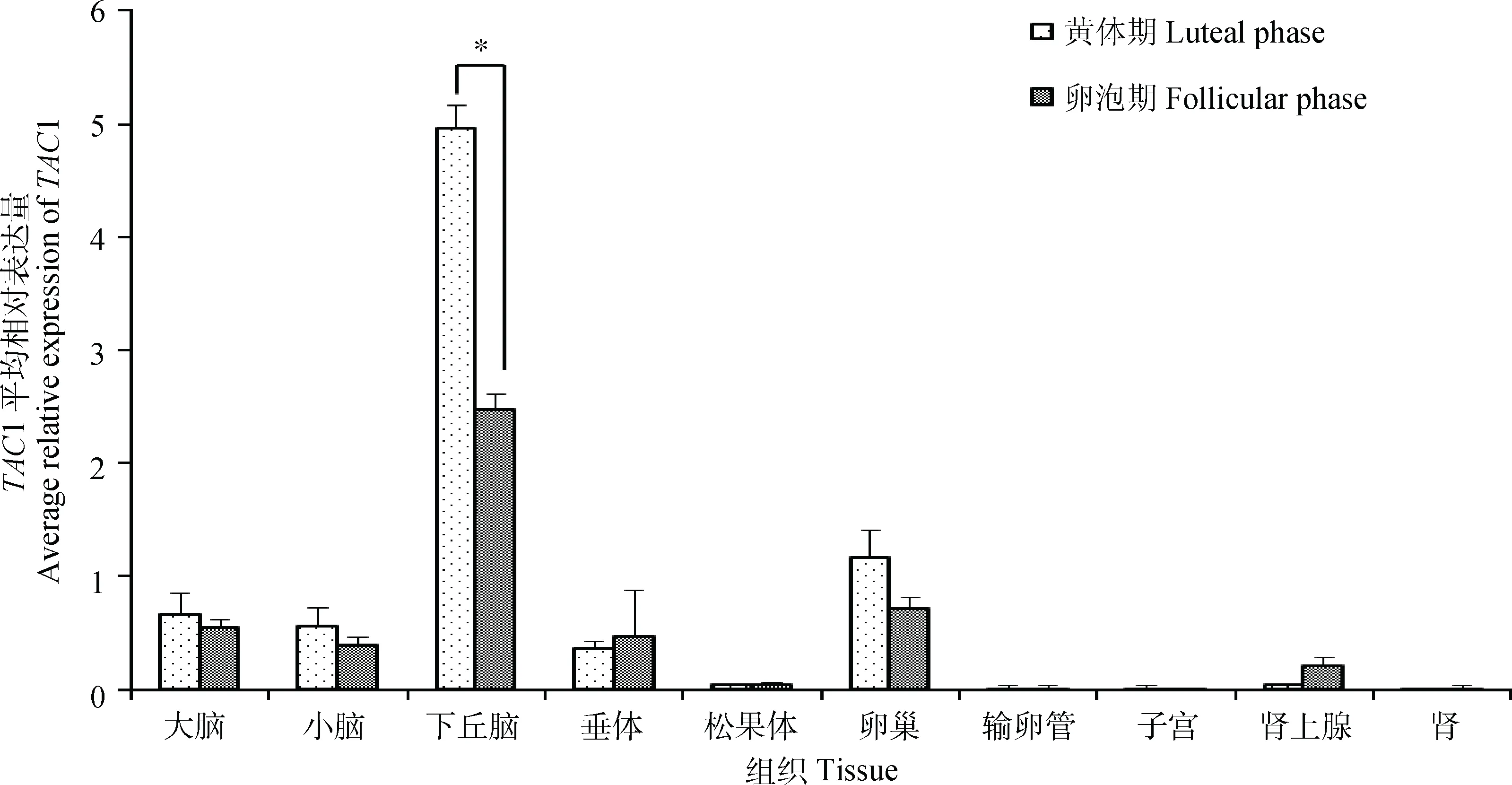
TAC1基因在長短光照條件下蘇尼特羊組織中的表達情況總結如圖1,該基因在蘇尼特羊下丘腦等10種組織中均有表達,其中下丘腦中的表達量明顯高于其他組織,在性腺軸中的表達量相對較高。各組織在不同光照條件下的表達趨勢基本一致,均為長光照條件下表達量高;其中長光照條件下蘇尼特羊垂體和輸卵管中TAC1的表達量顯著高于短光照(P<0.05)。
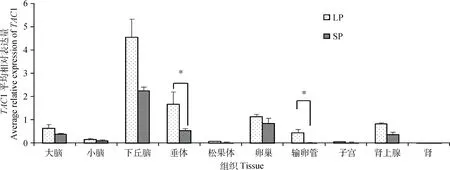
黃體期和卵泡期小尾寒羊組織表達譜結果如圖2所示,TAC1基因在小尾寒羊大腦等10種組織中均有表達,其中下丘腦中的表達量明顯高于其他組織,在性腺軸中的表達量相對較高,且黃體期小尾寒羊大多數組織(腎上腺、垂體除外)中表達量均高于卵泡期,與TAC1在長短光照條件下蘇尼特羊各組織的表達差異類似。
LP. 長光照;SP. 短光照。柱形上方“*”表示該基因在長光照與短光照蘇尼特羊該組織中表達量差異顯著(P<0.05)。圖4同LP. Long photoperiod; SP. Short photoperiod. The “*” on the columns indicate the significant difference (P<0.05) at the expression level of gene between the long photoperiod and the short photoperiod in tissues of Sunite sheep. The same as Figure 4圖1 不同光照條件下蘇尼特羊TAC1組織表達譜Fig.1 Tissue expression of TAC1 in Sunite sheep under different photoperiods
柱形上方“*”表示該基因在黃體期與卵泡期小尾寒羊該組織中表達量差異顯著(P<0.05)。圖5同The “*” on the column indicate the significant difference (P<0.05) at the expression level of gene between the luteal phase and follicular phase in tissues of STH sheep. The same as Figure 5圖2 不同繁殖時期小尾寒羊TAC1組織表達譜Fig.2 Tissue expression of TAC1 in Small Tail Han sheep at different reproductive stages
2.2 短光照轉變為長光照后蘇尼特羊垂體中TAC1基因的表達變化模式
為了闡明TAC1基因在長光照后的表達變化模式,本研究對長光照后多個時間點蘇尼特羊垂體進行TAC1基因表達分析(圖3),結果表明,短光照條件下蘇尼特羊垂體TAC1基因表達量最低,轉為長光照處理后,TAC1表達量在長光照的前42 d沒有顯著變化(P>0.05),但有緩慢上升趨勢,而在LP49D時表達量顯著升高并極顯著高于其他時間點(P<0.01)。
2.3 PRLR基因在不同光照條件下蘇尼特羊和不同繁殖時期小尾寒羊的組織表達譜
本研究檢測了長短光照條件下蘇尼特羊多個組織中PRLR基因的表達情況,結果如圖4所示。PRLR基因在各個組織中均有表達,在垂體、腎上腺中的表達量較高,其他組織中較低;其中腎上腺和垂體中的表達量明顯高于其他組織。各組織不同光照條件下的表達趨勢基本一致,均為長光照表達量高(小腦除外);其中長光照條件下下丘腦、輸卵管和腎上腺中PRLR的表達量顯著高于短光照下表達量(P<0.05)。
本研究也檢測了不同繁殖時期小尾寒羊PRLR基因的組織表達情況,結果如圖5所示。PRLR基因在小尾寒羊各組織中的表達情況與蘇尼特羊幾乎一致,在垂體、下丘腦、腎上腺、腎中表達較高,而其他組織中的表達水平較低。相對于黃體期,PRLR在卵泡期各組織(除小腦、輸卵管和子宮)中的表達量均較低,其中卵泡期卵巢中該基因的表達量顯著低于黃體期(P<0.05)。

柱形上方不同大寫字母表示差異極顯著(P<0.01),不同小寫字母表示差異顯著(P<0.05),相同字母表示差異不顯著(P>0.05)。圖6、7同Different letters above the column indicate significant differences (capital letter: P<0.01, lowercase letter: P<0.05), the same letter above the column indicate no significant difference (P>0.05). The same as Figure 6, 7圖3 短光照轉變為長光照后蘇尼特羊垂體TAC1基因的表達變化模式Fig.3 The expression pattern of TAC1 during the transition from SP to LP in pituitary of Sunite sheep
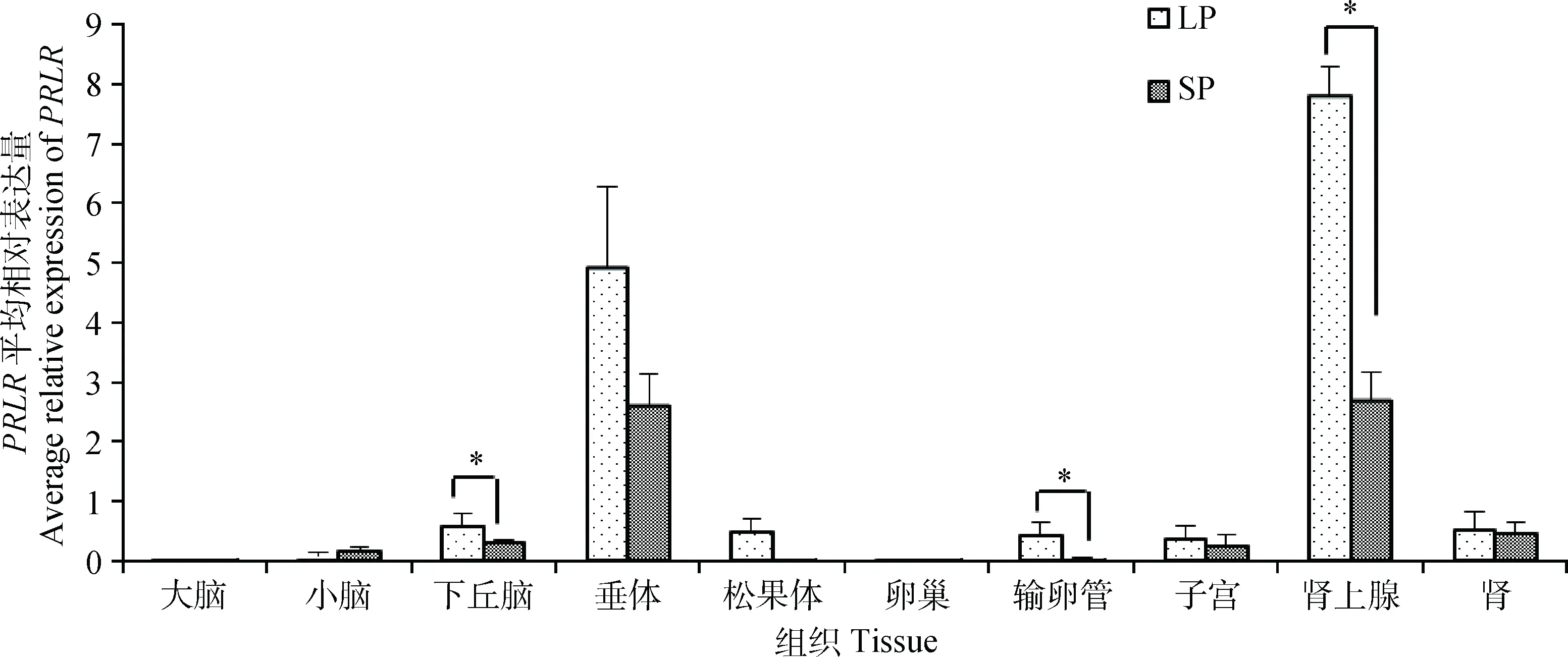
圖4 不同光照條件下蘇尼特羊PRLR組織表達譜Fig.4 Tissue expression of PRLR in Sunite sheep under different photoperiods
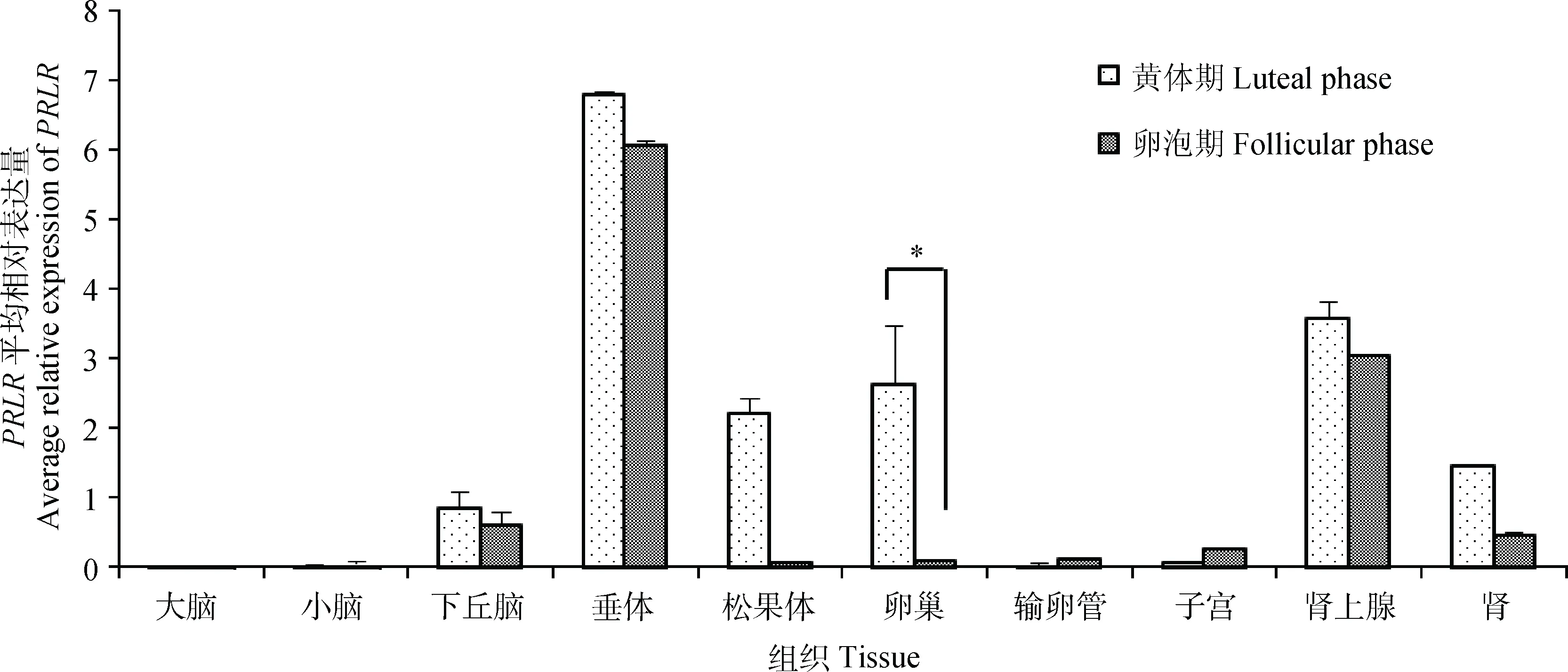
圖5 不同繁殖時期小尾寒羊PRLR組織表達譜Fig.5 Tissue expression of PRLR in STH sheep at different reproductive stages
2.4 短光照轉變為長光照后蘇尼特羊垂體和下丘腦中PRLR基因的表達變化模式
如圖6所示,由短光照轉為長光照第3天后,蘇尼特羊垂體中PRLR基因表達量顯著升高(P<0.05),至長光照21天時表達量達到峰值并顯著高于其他時間點,LP42D和LP49D時表達量有所下降,但LP42D仍顯著高于短光照時的表達量(P<0.05)。圖7表明,由短光照轉為長光照時,蘇尼特羊下丘腦中PRLR基因表達逐漸升高,且從LP15D開始其表達量顯著高于短光照(P<0.05)。
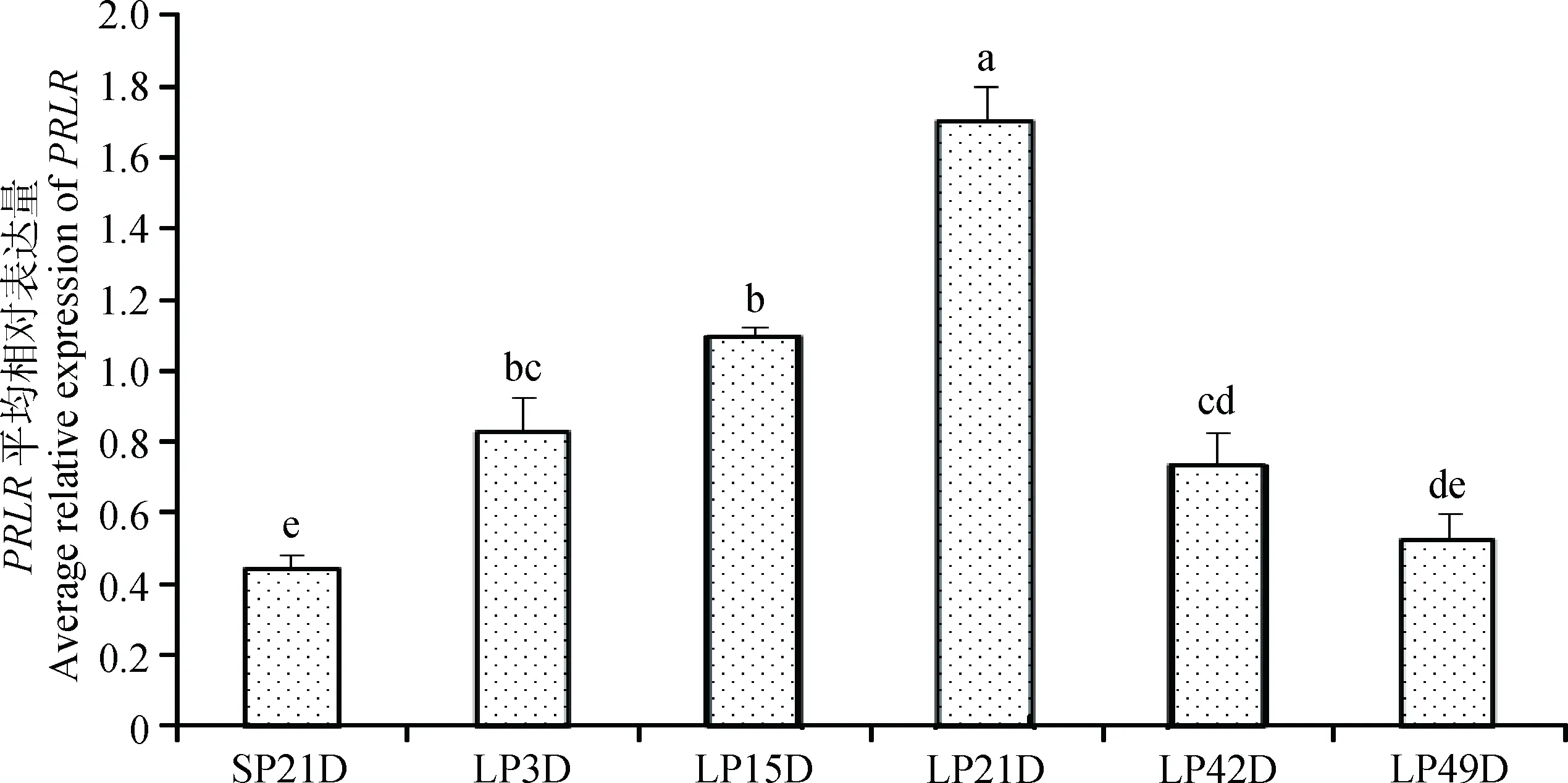
圖6 短光照轉變為長光照后蘇尼特羊垂體中PRLR基因的表達變化模式Fig.6 The expression pattern of PRLR during the transition from SP to LP in pituitary of Sunite sheep
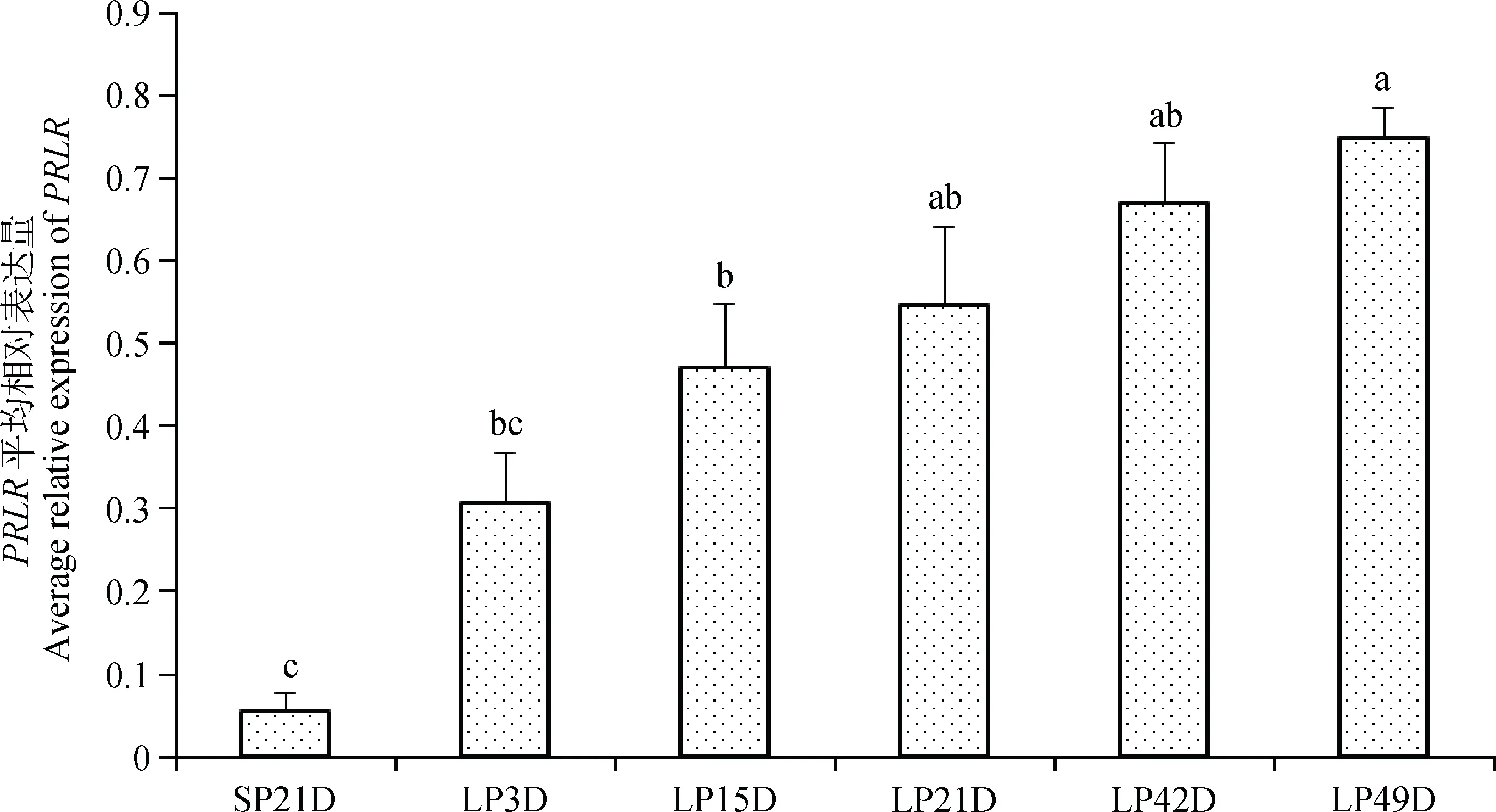
圖7 短光照轉變為長光照后蘇尼特羊下丘腦中PRLR基因的表達變化模式Fig.7 The expression pattern of PRLR during the transition from SP to LP in hypothalamus of Sunite sheep
3 討 論
3.1 TAC1基因發揮作用的主要組織及對動物繁殖的影響
本研究對TAC1基因在季節性發情綿羊品種蘇尼特羊和常年發情品種小尾寒羊大腦等10個組織中做了表達量分析。TAC1基因在兩個品種綿羊大腦等10個組織中均有表達,且組織表達特征基本一致,其在性腺軸組織和大腦中的表達量相對較高,暗示該基因在綿羊的這些組織中發揮主要作用,與繁殖性能密切相關。對人該基因的組織表達研究發現,它幾乎在所有組織中都有表達,特別是腦部組織、心、大腸、脾以及乳腺表達較高,僅在非外周神經系統支配的胎盤組織中未發現表達[18-21]。在鯉魚體內,TAC1基因主要表達于垂體、下丘腦、小腦、脊髓、鰓、心、腸、肝、肌肉和性腺組織中,在腎、血液和嗅球中沒有檢測到表達,將TAC1基因克隆于鯉魚垂體中,發現其編碼產物SP和NKA可以觸發促黃體素(Luteinizing hormone,LH)和PRL的分泌[22]。TAC1基因編碼的產物SP廣泛分布于大腦中,在下丘腦中高度表達,與Kiss1和GnRH神經元密切接觸,提示其可能與這些神經元存在相互作用[23-24],且研究顯示,雄性小鼠TAC1基因敲除后青春期明顯推遲[24],因此TAC1的表達對動物繁殖起著非常重要的作用。
本研究發現,長光照條件下蘇尼特羊各個組織中該基因的表達量均高于短光照條件下表達量,黃體期小尾寒羊各組織中表達量幾乎都高于卵泡期;這些結果表明,該基因可能在綿羊季節性繁殖和繁殖時期轉換中扮演了一定角色。研究發現,小鼠下丘腦組織中TAC1基因的表達受雌激素抑制[25],本研究結果也顯示卵泡期小尾寒羊下丘腦的TAC1基因表達量低于黃體期,暗示卵泡期綿羊下丘腦中該基因的表達可能受到高水平雌激素的調控。長短光照對比中,TAC1表達差異在垂體和輸卵管組織中達到顯著水平,暗示該基因最有可能在這2個組織中參與季節性繁殖的調控。由短光照轉為長光照處理后,蘇尼特羊垂體中TAC1基因表達量逐步上升,長光照49天時表達量達到最高值,并極顯著高于其他光照時長處理組。S. M. Dupré等[10]的研究表明,TAC1基因在綿羊PT表達受光照調節,長光照處理時表達顯著高于短光照。這些研究結果暗示TAC1是調節動物季節性繁殖的一個重要信號。
3.2 PRLR基因發揮作用的主要組織及對動物繁殖的影響
目前已經確定PRLR是細胞因子受體超家族成員之一,催乳素受體信使RNA(mRNA)先后在大鼠、綿羊和馬的垂體中得到鑒定[26-28]。本研究發現,PRLR基因在不同繁殖狀態綿羊各個組織中均有表達,在垂體和下丘腦中的表達量較高,其中垂體PRLR表達量遠高于其他各組織。這與趙強[29]通過免疫組化方法對成年小尾寒羊進行PRLR組織定位結果一致,他報道PRLR在綿羊的垂體、下丘腦、子宮和卵巢組織中均有陽性反應,且在垂體遠側端最為明顯。另外,在綿羊其他部位如腹股溝竇[30]、脂肪[31]等組織中也存在該基因的表達。吳憲紅等[32]發現,PRLR基因的mRNA在處于發情期的樂至黑山羊和藏山羊組織中廣泛表達,并且垂體中的表達量高于肝、子宮內膜和卵巢。M. Hasiec等[33]用熒光定量方法研究了休情期哺乳母羊腦部若干組織中PRLR的表達量,發現該基因在視前區(Preoptic areas)、下丘腦視上核(Supraoptic nucleus)、室旁核(Paraventricular nucleus)、脈絡叢(Choroid plexus)和垂體前葉(Anterior pituitary)均有表達。D. J. Tortonese 等[27]報道,PRLR基因在綿羊促性腺激素細胞中選擇性表達。以上研究表明綿羊PRLR基因主要在垂體和下丘腦中發揮作用。
研究表明,PRLR在動物機體不同組織中的表達存在差異并且其表達水平會隨動物的繁殖周期變化而變化。本研究發現,PRLR基因在不同繁殖時期小尾寒羊和不同光照時長處理下蘇尼特羊垂體等10個組織中均有不同程度的表達但存在差異,蘇尼特羊在短光照條件下(繁殖季節)幾乎所有組織中PRLR的表達量顯著低于長光照條件下(休情季節)表達量,暗示該基因可能參與綿羊季節性繁殖的調控;小尾寒羊PRLR在卵泡期各組織中的表達量均顯著低于黃體期,暗示該基因可能與綿羊繁殖時期轉換有關。R. A. Picazo 等[34]研究了PRLR在綿羊整個發情周期卵巢中的表達變化和細胞定位,發現在發情周期的第0、10和15天中PRLR在促性腺激素依賴性原始卵泡中的細胞定位是相似的,并且原始卵泡和初級卵泡中陽性信號最強,而在即將排卵的成熟卵泡顆粒細胞中幾乎沒有陽性信號,卵母細胞一直顯示PRLR陽性免疫染色。對雞顆粒細胞中PRLR表達的研究表明,該基因的轉錄物水平在直徑小于2 mm的卵泡基質和壁細胞中最高,隨著卵泡的成熟表達水平逐漸下降[35]。這表明,PRLR基因高表達可能對動物繁殖活動有抑制作用,或者發情和排卵可能抑制PRLR基因的表達。
在季節性繁殖的動物(如羊和馬)中,GnRH和促性腺激素的分泌受季節性變化即日照時長控制。光周期信息由松果體夜間分泌褪黑激素的模式解碼[36],腦垂體中高密度的褪黑激素受體被褪黑激素激活后可直接調控垂體內催乳素的分泌模式[37]。催乳素可能通過2種途徑調控下游因子,一種途徑是:綿羊下丘腦接收了催乳素信號后PRLR基因高表達,然后通過下丘腦-垂體-性腺軸進行繁殖信號的傳遞;另外一種途徑是垂體內局部旁分泌機制:垂體前葉接收催乳素信號后PRLR基因高表達,抑制促性腺細胞分泌LH和FSH。蘇尼特羊垂體中PRLR基因在短光照條件下表達量相對較低,轉為長光照處理后逐步上升,長光照第21天時表達量達到最高值,并極顯著高于其他光照處理組,長光照第42天和第49天時表達量有所下降,但仍高于短光照;由短光照條件下轉為長光照處理后,下丘腦中PRLR基因表達量逐步增加,且從長光照15 d后開始顯著高于短光照。S. Wood 等[38]研究表明,綿羊短光照處理的12周內其血漿催乳素水平處于穩定低水平狀態,而轉為長光照后前2周明顯升高,3周之后處于較高水平。本研究表明,催乳素受體是在長光照之后發生響應并與催乳素變化的趨勢基本一致,而且在垂體和下丘腦中顯示出不同的變化模式。
4 結 論
TAC1主要表達于性腺軸組織,PRLR基因主要在垂體和腎上腺中表達。這2個基因在不同光照條件和不同繁殖時期綿羊各組織中的表達差異暗示它們可能涉及綿羊季節性繁殖和繁殖時期轉換的調控。由短光照轉為長光照條件后PRLR基因在季節性發情綿羊的垂體和下丘腦中具有不同的響應模式,暗示存在不同的調控方式。
[1] 孫 偉, 張向楠, 左其生, 等. 湖羊催乳素受體基因外顯子10多態性及與其母性行為性狀的關聯分析[J]. 畜牧獸醫學報, 2013, 44(5): 673-680. SUN W, ZHANG X N, ZUO Q S, et al. Analysis on genetic polymorphism of exon 10 ofPRLRgene and its association with distribution type of its maternal behavior in Hu sheep[J].ActaVeterinariaetZootechnicaSinica, 2013, 44(5): 673-680. (in Chinese)
[2] 黃楊河, 王憑青, 楊 力, 等. 促性腺激素釋放激素受體(GnRHR)基因多態性及其與山羊產羔數的相關性分析[J]. 畜牧獸醫學報, 2012, 43(1): 22-28. HUANG Y H, WANG P Q, YANG L, et al. Polymorphism of gonadotropin releasing hormone receptor (GnRHR) Gene and its relationship with litter size in goats[J].ActaVeterinariaetZootechnicaSinica, 2012, 43(1): 22-28. (in Chinese)
[3] CURLEWIS J D. Seasonal prolactin secretion and its role in seasonal reproduction: a review[J].ReprodFertilDev, 1992, 4(1): 1-23.
[4] WALTON J S, MCNEILLY J R, MCNEILLY A S, et al. Changes in concentrations of follicle-stimulating hormone, luteinizing hormone, prolactin and progesterone in the plasma of ewes during the transition from anoestrus to breeding activity[J].JEndocrinol, 1977, 75(1): 127-136.
[5] CHRISTIAN H C, IMIRTZIADIS L, TORTONESE D. Ultrastructural changes in lactotrophs and folliculo-stellate cells in the ovine pituitary during the annual reproductive cycle[J].JNeuroendocrinol, 2015, 27(4): 277-284.
[6] MORGAN P J. The pars tuberalis: the missing link in the photoperiodic regulation of prolactin secretion?[J].JNeuroendocrinol, 2000, 12(4): 287-295.
[7] GRAHAM E S, WEBSTER C A, HAZLERIGG D G, et al. Evidence for the biosynthesis of a prolactin-releasing factor from the ovine pars tuberalis, which is distinct from thyrotropin-releasing hormone[J].JNeuroendocrinol, 2002, 14(12): 945-954.
[8] MORGAN P J, WEBSTER C A, MERCER J G, et al. The ovine pars tuberalis secretes a factor(s) that regulates gene expression in both lactotropic and nonlactotropic pituitary cells[J].Endocrinology, 1996, 137(9): 4018-4026.
[9] STIRLAND J A, JOHNSTON J D, CAGAMPANG F R A, et al. Photoperiodic regulation of prolactin gene expression in the Syrian hamster by a pars tuberalis-derived factor[J].JNeuroendocrinol, 2001, 13(2): 147-157.
[10] DUPRé S M, MIEDZINSKA K, DUVAL C V, et al. Identification ofEya3 andTAC1 as long-day signals in the sheep pituitary[J].CurrBiol, 2010, 20(9): 829-835.
[11] TORTONESE D J. Intrapituitary mechanisms underlying the control of fertility: key players in seasonal breeding[J].DomestAnimEndocrinol, 2016, 56 Suppl 1: S191-S203.
[12] BOLE-FEYSOT C, GOFFIN V, EDERY M, et al. Prolactin (PRL) and its receptor: actions, signal transduction pathways and phenotypes observed in PRL receptor knockout mice[J].EndocrRev, 1998, 19(3): 225-268.
[13] CLEVENGER C V, GADD S L, ZHENG J M. New mechanisms for PRLr action in breast cancer[J].TrendsEndocrinolMetab, 2009, 20(5): 223-229.
[14] DARDENTE H, WYSE C A, BIRNIE M J, et al. A molecular switch for photoperiod responsiveness in mammals[J].CurrBiol, 2010, 20(24): 2193-2198.
[15] MASUMOTO K H, UKAI-TADENUMA M, KASUKAWA T, et al. Acute induction ofEya3 by late-night light stimulation triggersTSHβ expression in photoperiodism[J].CurrBiol, 2010, 20(24): 2199-2206.
[16] WOOD S, LOUDON A. Clocks for all seasons: unwinding the roles and mechanisms of circadian and interval timers in the hypothalamus and pituitary[J].JEndocrinol, 2014, 222(2): R39-R59.
[17] TSUJINO K, NARUMI R, MASUMOTO K H, et al. Establishment ofTSHβ real-time monitoring system in mammalian photoperiodism[J].GenesCells, 2013, 18(7): 575-588.
[18] PAGE N M, BELL N J, GARDINER S M, et al. Characterization of the endokinins: human tachykinins with cardiovascular activity[J].ProcNatlAcadSciUSA, 2003, 100(10): 6245-6250.
[19] PAGE N M, WOODS R J, LOWRY P J. A regulatory role for neurokinin B in placental physiology and pre-eclampsia[J].RegulPept, 2001, 98(3): 97-104.
[20] PINTO F M, ALMEIDA T A, HERNANDEZ M, et al. mRNA expression of tachykinins and tachykinin receptors in different human tissues[J].EurJPharmacol, 2004, 494(2-3): 233-239.
[21] LI W X, DAI S X, LIU J Q, et al. Integrated analysis of Alzheimer’s disease and schizophrenia dataset revealed different expression pattern in learning and memory[J].JAlzheimersDis, 2016, 51(2): 417-425.
[22] HU G F, HE M L, KO W K W, et al. TAC1 gene products regulate pituitary hormone secretion and gene expression in prepubertal grass carp pituitary cells[J].Endocrinology, 2017, 158(6): 1776-1797.
[23] MAGUIRE C A, SONG Y B, WU M, et al. Tac1 signaling is required for sexual maturation and responsiveness of GnRH neurons to kisspeptin in the male mouse[J].Endocrinology, 2017, 158(7): 2319-2329.
[24] LASAGA M, DEBELJUK L. Tachykinins and the hypothalamo-pituitary-gonadal axis: an update[J].Peptides, 2011, 32(9): 1972-1978.
[25] NAVARRO V M, BOSCH M A, LEN S, et al. The integrated hypothalamic tachykinin-kisspeptin system as a central coordinator for reproduction[J].Endocrinology, 2015, 156(2): 627-637.
[26] CHIU S, KOOS R D, WISE P M. Detection of prolactin receptor (PRL-R) mRNA in the rat hypothalamus and pituitary gland[J].Endocrinology, 1992, 130(3): 1747-1749.
[27] TORTONESE D J, BROOKS J, INGLETON P M, et al. Detection of prolactin receptor gene expression in the sheep pituitary gland and visualization of the specific translation of the signal in gonadotrophs[J].Endocrinology, 1998, 139(12): 5215-5223.
[28] HENDERSON H L, HODSON D J, GREGORY S J, et al. Gonadotropin-releasing hormone stimulates prolactin release from lactotrophs in photoperiodic species through a gonadotropin-independent mechanism[J].BiolReprod, 2008, 78(2): 370-377.
[29] 趙 強. 綿羊PRLR,PRLH和PRLHR基因的克隆及其在下丘腦—垂體—性腺中表達的研究[D]. 蘭州: 甘肅農業大學, 2015. ZHAO Q. Molecular cloning ofPRLR,PRLHandPRLHRgene in ovine and theirs expression in the hypothalamus, pituitary, uterus and ovary[D]. Lanzhou: Gansu Agricultural University, 2015. (in Chinese)
[30] ALEXANDRE-PIRES G, MARTINS C, GALVO A M, et al. Understanding the inguinal sinus in sheep (Ovisaries)-morphology, secretion, and expression of progesterone, estrogens, and prolactin receptors[J].IntJMolSci, 2017, 18(7): 1516.
[31] PEARCE S, BUDGE H, MOSTYN A, et al. Prolactin, the prolactin receptor and uncoupling protein abundance and function in adipose tissue during development in young sheep[J].JEndocrinol, 2005, 184(2): 351-359.
[32] 吳憲紅, 龍石太, 王 永, 等. 催乳素受體基因(PRLR)在樂至黑山羊和藏山羊不同組織中的差異表達[C]//中國遺傳學會第九次全國會員代表大會暨學術研討會論文集. 哈爾濱: 中國遺傳學會, 2013. WU X H, LONG S T, WANG Y, et al. The differential expression of prolactin receptor gene (PRLR) in different tissues between the Lezhi black goat and Tibetan goat[C]//The 9th National Congress of Chinese Society of Genetics IE. Proceedings of Academic Symposium. Harbin: The Genetics Society of China, 2013. (in Chinese)
[33] HASIEC M, SZLIS M, GRSKI K, et al. Prolactin receptors mRNA expression in selected brain regions of lactating sheep[C]//Proceedings of the 4th Winter Workshop of the Society for Biology of Reproduction “Central and Local Regulations of Reproductive Processes”. Zakopane, Poland: Society for Biology of Reproduction, 2016.
[34] PICAZO R A, GARCA RUIZ J P, SANTIAGO MORENO J, et al. Cellular localization and changes in expression of prolactin receptor isoforms in sheep ovary throughout the estrous cycle[J].Reproduction, 2004, 128(5): 545-553.
[35] HU S G, DUGGAVATHI R, ZADWORNY D. Regulatory mechanisms underlying the expression of prolactin receptor in chicken granulosa cells[J].PLoSOne, 2017, 12(1): e170409.
[36] PEVET P, CHALLET E. Melatonin: both master clock output and internal time-giver in the circadian clocks network[J].JPhysiolParis, 2011, 105(4-6): 170-182.
[37] LINCOLN G A, CLARKE I J. Photoperiodically-induced cycles in the secretion of prolactin in hypothalamo-pituitary disconnected rams: evidence for translation of the melatonin signal in the pituitary gland[J].JNeuroendocrinol, 1994, 6(3): 251-260.
[38] WOOD S, CHRISTIAN H C, MIEDZINSKA K, et al. Binary switching of calendar cells in the pituitary defines the phase of the circannual cycle in mammals[J].CurrBiol, 2015, 25(20): 2651-2662.
[40] WANG L P. mRNA expression of prolactin receptor in sheep pituitary and its effect on maternal behavior[J].GenetMolRes, 2015, 14(3): 8650-8657.
[41] 曾獻存, 陳韓英, 賈 斌, 等. 中國美利奴羊PROP1和PRLR基因的表達分析[J]. 畜牧獸醫學報, 2011, 42(8): 1057-1062. ZENG X C, CHEN H Y, JIA B, et al. The expression analysis ofPROP1 andPRLRgenes in Chinese merino sheep[J].ActaVeterinariaetZootechnicaSinica, 2011, 42(8): 1057-1062. (in Chinese)

