聚鋁硅酸鹽在水處理過程中混凝焓值的測定
盧政明,刁銀軍
(金華職業技術學院 制藥與材料工程學院,浙江 金華 321007)
無機高分子混凝劑由于良好的混凝性能,在污水處理領域應用廣泛[1-3],其主要類型有聚合氯化鐵、聚合氯化鋁、聚鐵硅酸鹽及聚鋁硅酸鹽等.聚鋁硅酸鹽是近年來研制出的一種新型且性能優良的混凝劑[4],其凈水效果在一定pH值范圍內優于其他混凝劑.目前對該混凝劑的研究主要還是側重其在水處理的凈化效果方面,大多數都是通過比較濁度、色度、COD、BOD等指標的去除率來確定混凝劑的優劣性[5-8].高寶玉等人對聚鋁硅酸鹽的形態及帶電特征進行了研究[9],也有人對處理過程中的動力學機理做過研究[10].但從熱力學的角度來研究混凝機理尚未見報道.本文采用測溫和控溫精度均較高(1×10-3K)、且具有恒溫環境的溶解-反應量熱計(SRC-100)[11]測定了不同條件下聚鋁硅酸鹽在水處理過程中的焓變情況,用均勻設計法對各因素的影響進行了比較.
1 實驗
1.1 儀器與試劑
SRC-100型具有恒溫環境的溶解―反應量熱計,武漢大學化學與分子科學學院研制;WGZ-1A散射光濁度儀,上海昕瑞儀器儀表有限公司;pHS-3C酸度計,杭州雷磁分析儀器廠.
水玻璃,工業品,模數3.1~3.4,永清縣聚利得化工有限公司;鈣質膨潤土,工業品,山東膨潤土廠;硫酸(98%),硫酸鋁均為市售AR級.
1.2 實驗方法
采用均勻設計法,選取水樣濁度(X1)、聚硅酸鋁用量(X2)、pH值(X3)、鋁/硅物質的量比(X4)作為影響反應的四個因素,每個因素選取5個水平.為了實驗取得較好的重復性,取擬水平,設計表為U10(54),如表1所示.根據均勻設計表,使水樣濁度為零,在其它相同條件下做空白實驗.

表1 U10(54)均勻設計表
1.3 實驗原理
混凝是指高分子化合物對水中的膠體和懸浮顆粒架橋吸附,從而使其凝集沉降的過程.在相同條件下分別測定聚硅酸鋁處理濁度水樣的焓變(ΔH1)和處理空白水樣的焓變(ΔH2),兩者之差即為混凝過程的焓變(ΔH).
1.4 試劑的配制
1.4.1 不同物質的量比聚硅酸鋁的制備
取一定量的水玻璃稀釋到一定濃度,加入硫酸調節pH值,使其聚合,再加入硫酸鋁,即得到聚硅酸鋁混凝劑.本實驗配制了鋁/硅物質的量比為21,1.51,11,11.5,12的聚硅酸鋁.
1.4.2 不同濁度、不同pH值水樣的配制
按照均勻設計方案,用鈣質膨潤土配制了pH值分別為7,8,9,10,11,濁度分別為160,320,480,640,800 NTU的水樣.
1.4.3 不同pH值空白水樣的配制
按照均勻設計方案,配制了pH值分別為7,8,9,10,11的空白水樣.
1.5 試驗方法
使環境溫度恒定在25 ℃,取100 mL待處理水樣放入量熱計的杜瓦瓶中,恒溫.待溫度穩定后,伸入已裝好混凝劑的加樣桿,使液面浸過加樣室,開動攪拌機.待重新恒溫后,把聚硅酸鋁推入到水樣中,此時溫度的變化會以電壓的形式在屏幕上顯現.根據電標加熱階段補償反應所引起的電壓變化,采用等面積法計算,通過自動化控制程序[4]即可算出反應樣品的焓變.
2 結果與討論
按照均勻設計方案,用SRC-100量熱計測得的結果如表2所示.

表2 不同條件下測得的焓變
混凝焓變ΔH=濁度水樣焓變(ΔH1)-空白水樣的焓變(ΔH2).
在測定空白水樣的焓變ΔH2時,聚硅酸鋁在水中自身發生凝聚,因此ΔH2可定義為自凝聚焓變ΔH自凝.
把4因素5水平對ΔH的影響擬用具有交互作用的三次方數學模型表示為
ΔH=A+A1X13+A2X23+A3X33+A4X43+A5X1X2+A6X1X3
+A7X1X4+A8X2X2+A9X2X3+A10X2X4+A11X3X3+A12X3X4,
(1)
方程的項數N=13;試驗次數M=10;自變量個數B1=4;每個自變量具有的最高次數T2=3.
輸入N,M,B1,T2,得到回歸分析結果[3]為
ΔH=2.48+5.19×10-3(X1-480)+3.78(X4-1.13)-7.09(X4-1.13)3+5.40×10-3(X1-480)
(X2-0.75)-1.90×10-3(X1-480)(X3-9)+1.24(X2-0.75)(X3-9.00) ,
(2)
該方程F總>F6,3(α=0.05)=8.9,方程各項F>F1,8(α=0.05)=5.3,方程置信度為95%[3].
從方程(2)可知,影響混凝焓變ΔH的因素為水樣的濁度X1,鋁/硅物質的量比X4,濁度X1與聚硅酸鋁用量X2的交互作用,濁度X1與pH值(X3)的交互作用,聚硅酸鋁用量X2與pH值(X3)的交互作用.
當X1=160,X2=1.25,X3=7,X4=2.00時,混凝焓變ΔH=38.4 J/L.
2.1 水樣濁度對混凝焓變的影響
在X2=1.25,X3=7,X4=2.00時,解出ΔH和X1,濁度對混凝焓變ΔH的影響,可用方程(3)和圖1表示.
ΔH=-7.0+0.014X1.
(3)
從圖1可以看出,隨著濁度的增大,混凝焓變ΔH值從負變為正,即由放熱變為吸熱.這可能是由于濁度增大時,水中膠體和懸浮顆粒增多,表面自由能增大,混凝時消耗能量增大所致.即當混凝劑用量一定,焓變與H值均隨懸浮顆粒表面自由能的增大而增大.
2.2 鋁/硅物質的量比對混凝焓變的影響
在X1=160,X2=1.25,X3=7時,解出ΔH和X4,鋁/硅物質的量比對混凝焓變ΔH的影響可用方程(4)和圖2表示.
ΔH=-6.78+3.78X4-7.1(X4-1.13)3.
(4)
從圖2可以看出,當水樣濁度、混凝劑用量、pH值一定時,混凝焓變ΔH隨鋁/硅物質的量比的增加而增大.但在鋁/硅物質的量比為0.72.0范圍內出現了一放熱峰值,鋁/硅物質的量比在1.6左右時放熱出現最小值.在比值大于2.0后反應放熱急劇增大.峰值的出現可能是鋁/硅物質的量比在1.6時難自聚引起的,焓變的急劇增加可能是由聚硅酸鋁的溶解稀釋熱以及鋁離子的電中和作用等所引起的.
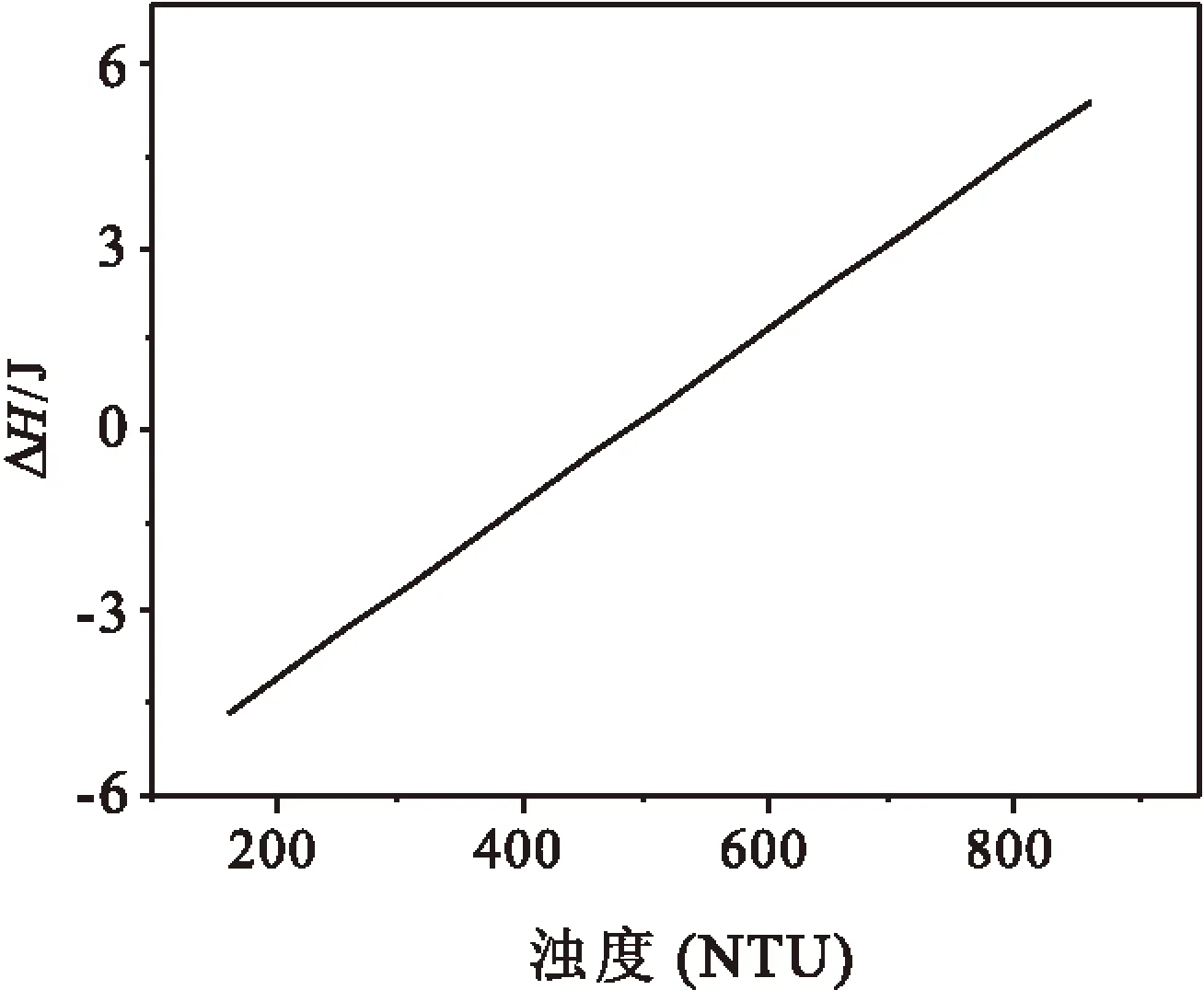
圖1 濁度與絮凝焓變的關系
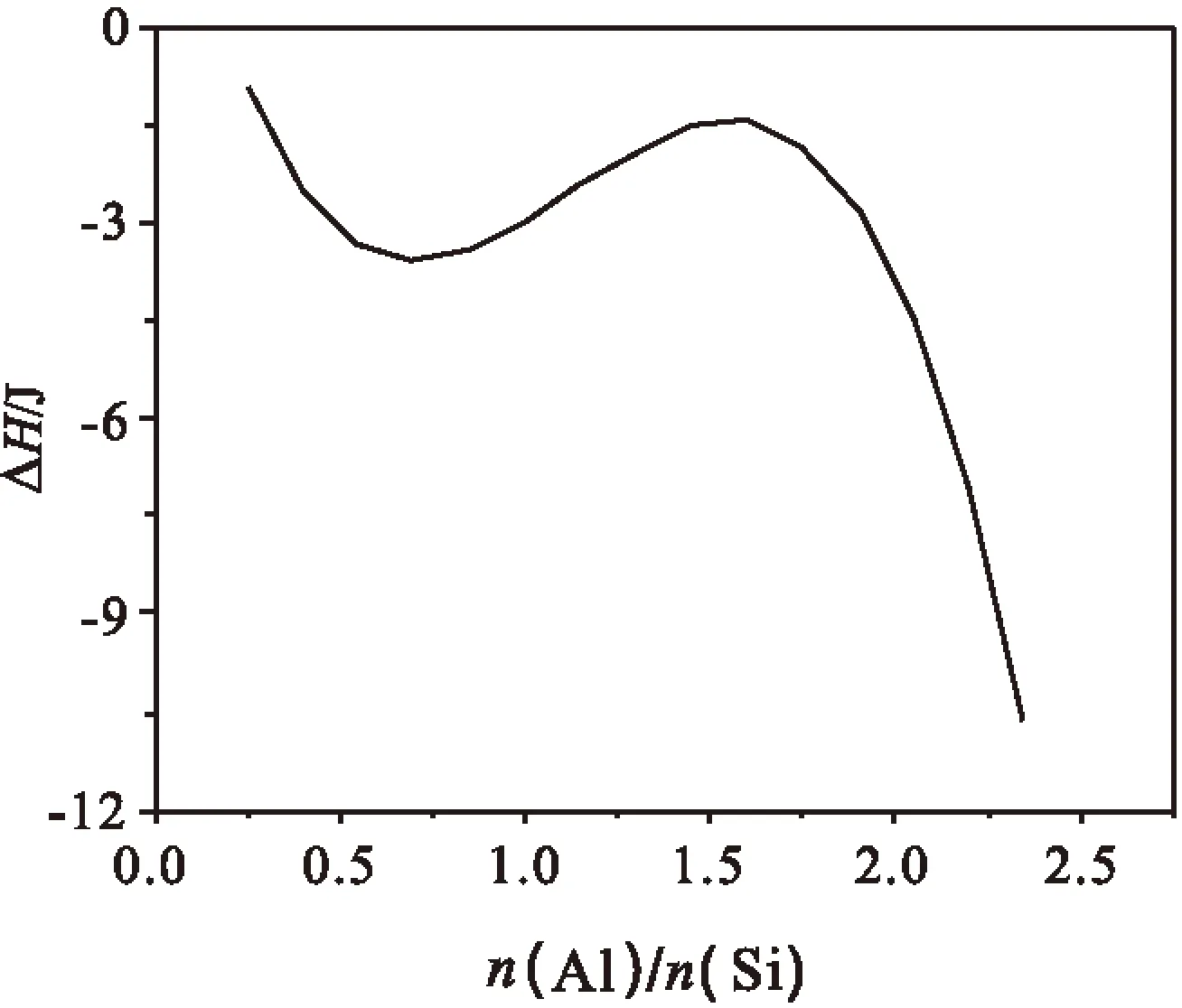
圖2 鋁/硅摩爾比與絮凝焓變的關系
2.3 水樣濁度與聚硅酸鋁用量的交互作用
在X3=7,X4=2.00時,水樣濁度(X1)與聚硅酸鋁用量(X2)之間的交互影響可分別用方程(5)和圖3表示.
(5)
從圖3可以看出,在焓變一定的條件下,隨著濁度的增加,聚硅酸鋁的用量也相應增加.ΔH越小,濁度與用量的交互作用越大;反之越小.
2.4 濁度與pH值的交互作用
在X2=1.25,X4=2.00時,濁度(X1)與pH值(X3)之間的交互影響可分別用方程(6)和圖4表示.
(6)
從圖4可以看出,隨著濁度的增大,pH值有下降趨勢.在混凝焓變ΔH越小時這種趨勢越明顯.X1與X3的交互作用隨混凝焓變ΔH增大而減小,反之增大.當混凝焓變ΔH>2.4 J時,濁度與pH值幾乎沒有交互作用.
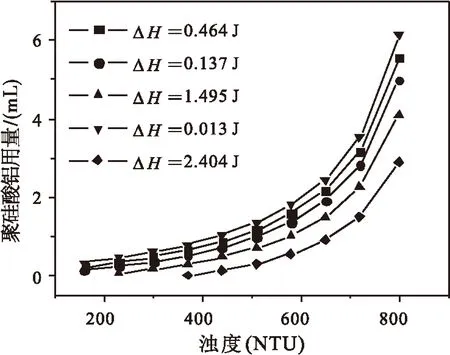
圖3 濁度與聚硅酸鋁用量的關系
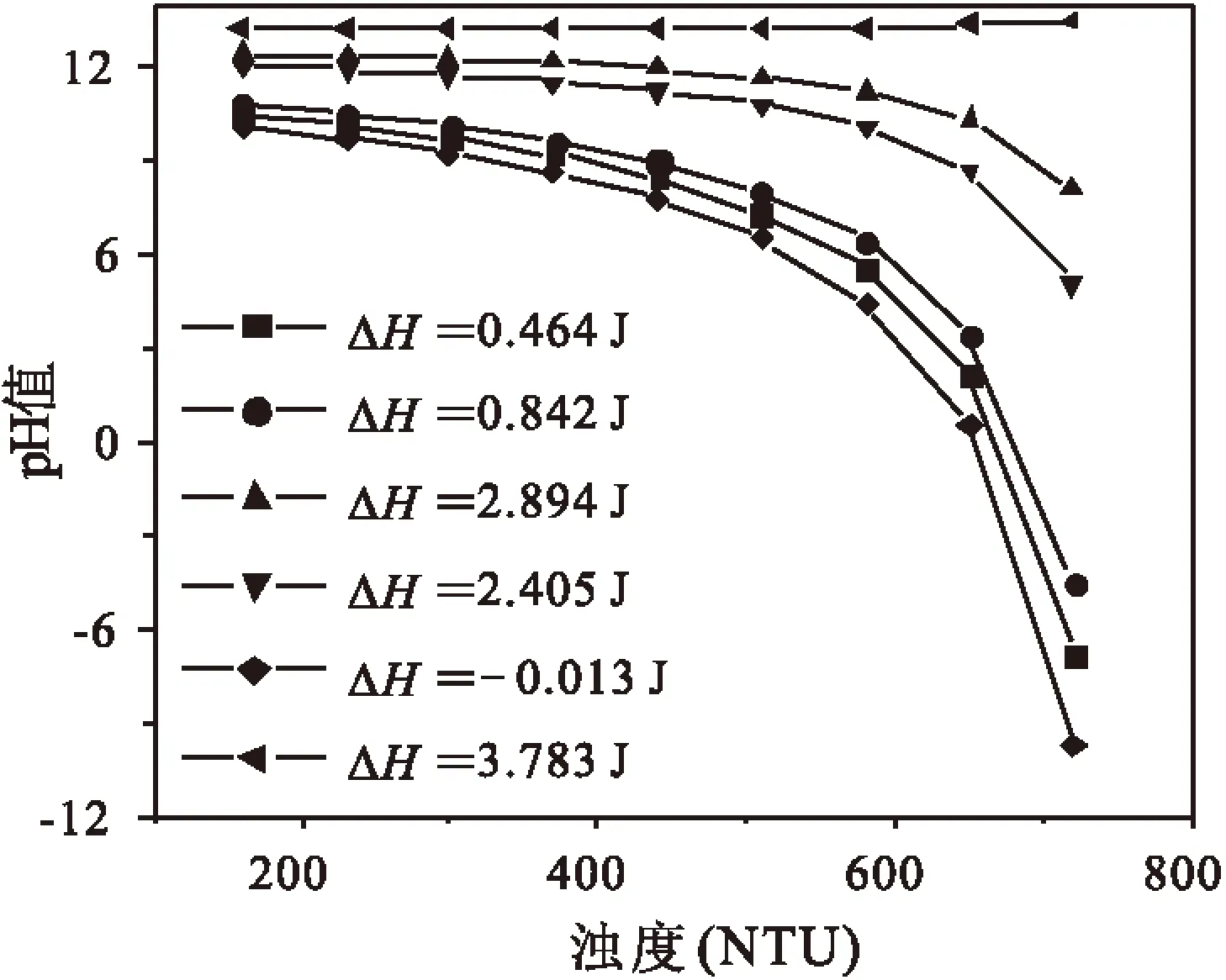
圖4 濁度與pH值的交互作用
2.5 聚硅酸鋁用量與pH值的交互作用
在X1=160,X4=2.00時,聚硅酸鋁的用量(X2)與pH值(X3)之間的交互影響可分別用方程(7)和圖5表示.
(7)
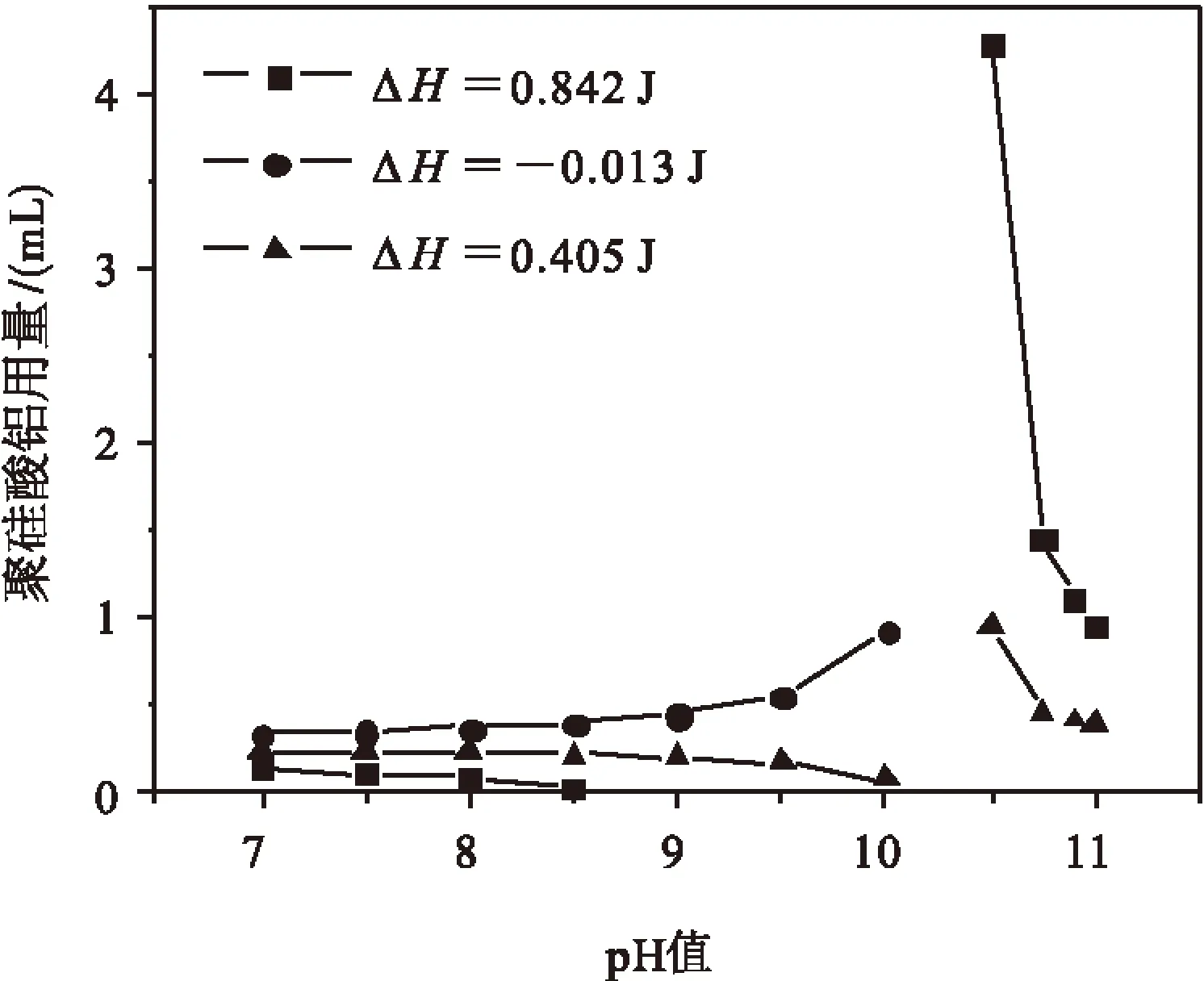
圖5 pH值與聚硅酸鋁用量的關系
從圖5可以看出,pH值小于10時,聚硅酸鋁用量不受其影響;當pH值大于10.5時,交互作用變得非常明顯,混凝焓變越大,交互作用則越強.
3 結語
試驗測得的混凝焓變ΔH>0,為正值,說明混凝本身是一個吸熱過程.把聚硅酸鋁、膠體與懸浮顆粒看成一個系統,在反應前此系統處于高分散態,混凝后懸浮顆粒隨著聚硅酸鋁的加入而凝聚沉降下來,系統分散態減小,混亂度減小;由混亂度與熵變ΔS的關系知道,該過程是一個熵減小的過程,即ΔS<0.而根據ΔG=ΔH-TΔS知道,該過程系統的吉布斯自由能ΔG系>0.根據熱力學第二定律,該過程是一個非自發過程,說明此系統不能自發進行.把聚硅酸鋁、膠體與懸浮顆粒和水看成一個系統,由于混凝過程能自發進行,則該系統ΔG混<0.ΔG混=ΔG系+ΔG水,ΔG水為聚硅酸鋁與水相互作用的自由能,為負值,并且|ΔG系|<|ΔG水|.ΔG水=ΔH水-TΔS水,其中ΔH水和ΔS水分別為聚硅酸鋁在水中的溶解稀釋焓變和熵變,而熵變遠小于稀釋焓,所以混凝過程的推動力為聚硅酸鋁在水中的溶解稀釋焓變.
[1] 李小梅,曾世東.水處理絮凝劑的種類及發展前景[J].現代農業科技,2013(24):1 558-1 562.
[2] 張振花,何玉鳳,張 俠,等.聚鐵和聚鋁類絮凝劑的改性及其在廢水處理中的應用研究進展[J].水處理技術,2010,36(9):10-15.
[3] 張瑛潔,秦 楠.聚氯化鋁鐵及其處理溶解性有機物研究進展[J].硅酸鹽通報,2015,34(5):1 290-1 295.
[4] Moussas PA, Zouboulis AI. A study on the properties and coagulation behaviour of modified inorganic polymer iccoagulant Poly-Ferric silicate sulphate(PFSiS)[J]. Separation and Purification Technology, 2008, 63(2): 475-483.
[5] 李薔薇,王淑勤,馬 垠,等.新型無機高分子混凝劑處理含氟廢水的實驗研究[J].化工時刊,2004,18(9):22-25.
[6] 陳 剛,陳 曄,周賽捷,等.鋁鹽混凝劑的制備及其在水處理中的應用研究[J].環境科學與技術,2010,33(11):156-158.
[7] 熊麗麗,高 麗,秦冬玲,等.PSAF-PD絮凝劑的研制及在造紙廢水中的應用[J].現代化工,2016,36(9):104-108.
[8] 王元宏,魏群山,張偉超,等.新型無機高分子混凝劑聚硅酸鋁鈣的制備及除濁性能的研究[J].環境工程,2015,33(增刊):320-313.
[9] 高寶玉,岳欽艷,李振東,等.聚硅氯化鋁混凝劑的形態及帶電特性研究[J].環境科學,1998,19(3):46-49.
[10] 胡 翔,周 定.聚硅酸系列混凝劑混凝過程的動力學和機理研究[J].水處理技術,1998,25(2):114-117.
[11] 武漢大學化學與分子科學學院熱化學實驗室.SRC-100型具有恒溫環境的溶解-反應量熱計用戶手冊[M].武漢:武漢大學,2004.

