CEA、CA50、CA199聯合檢測在胰腺癌診斷和預后評估中的價值
李蓉
胰腺癌是消化系統常見的死亡率最高的惡性腫瘤之一,由于其惡性程度高,病情發展迅速,其死亡率已經位居惡性腫瘤總死亡率第三位[1]。眾所周知,胰腺癌早期臨床表現不典型,容易造成誤診、漏診,所以確診時只有20%的患者有機會接受外科手術治療[2]。胰腺癌的預后效果非常差,5年生存率僅有1.3%~9.1%[3]。因而,尋找特異性的早期診斷和評估預后的標志物是降低胰腺癌死亡率、提高患者生活質量的關鍵。臨床上對胰腺癌的診斷主要借助于影像學、病理學以及血清學的檢查。目前比較認可的血清學指標的單一檢測缺乏足夠的靈敏度和特異度,很難作為有效的診斷和預后評估指標。因此,本研究主要探討癌胚抗原(CEA)、糖類抗原 50(CA50)和糖類抗原 199(CA199)三種血清學腫瘤標志物的聯合檢測在胰腺癌的診斷和預后評估中的價值。
1 材料與方法
1.1一般資料選擇我院2014年10月~2016年3月住院且根據影像學和病理學確診的胰腺疾病患者280 例,其中胰腺癌組160 例,男101例,女59例; 年齡35~81歲,平均58.3歲。根治性手術切除53例,姑息手術107例。44例術后復發患者中男31例,女13例,確診術后復發時的年齡為41~68歲。良性胰腺疾病組120例,男57例,女63例; 年齡20~77歲,包括慢性胰腺炎、胰頭黏液性囊腺瘤、胰管結石、胰腺假性囊腫等。所有患者排除胰腺癌外其他惡性腫瘤、心臟病、嚴重的炎癥、 部分自身免疫性疾病、 垂體瘤及原發性甲狀腺功能減退、腎臟疾病等。同時選取正常體檢健康對照組100例,男59例,女41例;年齡20~77歲,平均55.6歲。3組一般資料經統計學分析差異無統計學意義(P>0.05),具有可比性。
1.2檢測方法真空采血管空腹采集研究對象的 肘 正 中 靜 脈 血 4ml,靜 置 30min,3 000r/min 離心10min,分離血清立即檢測,-20℃保存。利用AutolumoA2000全自動化學發光檢測儀及其提供的配套試劑對CEA、CA50 和CA199進行檢測。CEA、CA50和CA199 正 常參考值分別為CEA<5ng/ml,CA50<25U/ml,CA199<35U/ml。
1.3統計學方法采用SPSS 18.0軟件包進行數據管理和統計學分析,計量資料以均數±標準差(±s)表示,采用單因素方差分析和t檢驗,以P<0.05為差異有統計學意義。其中敏感性和特異性的計算依據公式,敏感性=真陽性/真陽性+假陰性;特異性=真陰性/假陽性+真陰性。
2 結果
2.1 CEA、CA50和CA199在胰腺癌與良性胰腺疾病組、健康對照組中表達水平比較與良性胰腺疾病組和健康對照組相比,胰腺癌患者組CEA、CA50和CA199在血清中的表達水平顯著升高,差異有統計學意義(P<0.05)。而良性胰腺疾病組和健康對照組相比,血清CEA、CA50和CA199的表達水平差異無統計學意義(P>0.05),見表 1。
表1 3組 CEA、CA50和 CA199在血清中的表達(±s)
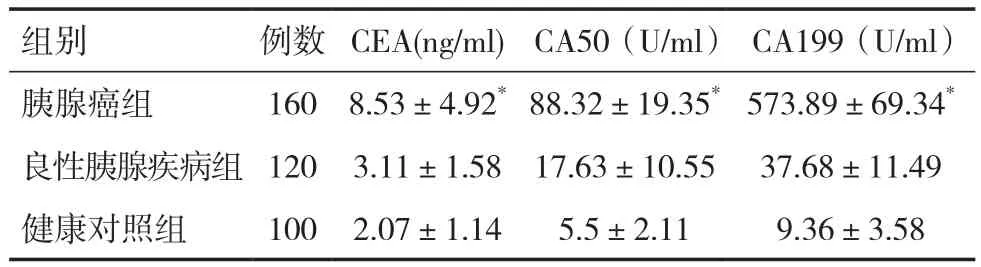
表1 3組 CEA、CA50和 CA199在血清中的表達(±s)
注:與良性胰腺疾病組、健康對照組比較,*P<0.05
組別 例數 CEA(ng/ml)CA50(U/ml) CA199(U/ml)胰腺癌組 160 8.53±4.92*88.32±19.35*573.89±69.34*良性胰腺疾病組 120 3.11±1.58 17.63±10.55 37.68±11.49健康對照組 100 2.07±1.14 5.5±2.11 9.36±3.58
2.2血清CEA、CA50和CA199在胰腺癌患者不同腫瘤分期中的表達水平CEA、CA50和CA199在胰腺癌不同腫瘤分期患者中的表達水平有顯著性差異,隨著臨床分期的變化,3種腫瘤標志物表達水平明顯發生變化。Ⅲ~Ⅳ期患者中的表達水平明顯高于Ⅰ~Ⅱ期腫瘤患者,見表2。
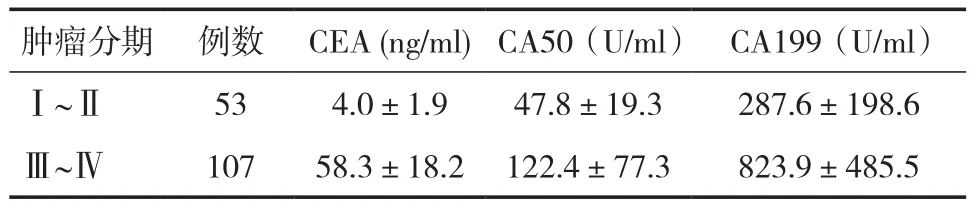
表2 CEA、CA50和CA199在胰腺癌患者不同腫瘤分期中的表達水平(x—±s)
2.3 CEA、CA50和CA199單一及聯合檢測胰腺癌的敏感性和特異性CEA、CA50和CA199在胰腺癌診斷中的敏感性達到了72.7%、51.5%、82.6%,特異性為87.8%、72.3%、76.0%。聯合檢測的敏感性和特異性均高于單一檢測,為93.1%和82.8%。
2.4胰腺癌切除術后CEA、CA50和CA199表達水平在未復發組與復發組中表達水平的比較胰腺癌患者術后復發組中CEA、CA50和CA199的表達水平與未復發組相比顯著性升高(P<0.05),見表3。
表3 CEA、CA50和CA199在復發組與未復發組中表達水平的比較 (±s)

表3 CEA、CA50和CA199在復發組與未復發組中表達水平的比較 (±s)
組別 例數 CEA(ng/ml) CA50(U/ml) CA199(U/ml)復發組 44 8.97±5.14 109.23±38.15 473.41±111.32未復發組 9 3.28±0.97 3.72±2.17 18.40±6.68
2.5 CEA、CA50和CA199單一及聯合檢測對胰腺癌術后復發診斷的敏感性和特異性53例手術切除組術后隨訪期在復發的44例患者中,CEA、CA50、CA199的敏感性分別為74.2%、53.0%、80.3%,特異性為89.9%、73.4%、74.0%。聯合檢測后敏感性和特異性分別達到了95.5%和86.3%。
3 討論
胰腺癌是致死率較高的癌癥之一,盡管現在臨床上多采取多峰性治療,但由于其復發率較高,所以5年生存率仍不到5%[4]。目前外科手術是唯一可以治愈的機會,但是只有20%的患者可以進行手術切除腫瘤[5]。而這些患者中只有15%的患者有早期癌癥的表現,一旦有手術機會并且進行輔助治療后,5年生存率就會增加到20%~30%[6]。所以及早確診對治愈率和生存率的提高尤為重要。
CEA、CA50、CA199是腫瘤細胞表面的黏蛋白物質,而這種黏蛋白與腫瘤的發生發展有密切的聯系。在臨床中,這3種物質被公認為是腫瘤血清標志物,而且廣泛用于胰腺癌的輔助診斷。CEA是一種酸性糖蛋白,胚胎時期主要在胰腺、肝臟等部位合成,CEA在大多數上皮性腫瘤中的表達,特別是內胚層來源的腫瘤如胰腺癌、消化道腫瘤、乳腺癌、肺癌中均有明顯升高[7],是臨床中常被用來輔助診斷胰腺癌的腫瘤標志物。CA50 是以唾液酸脂和唾液酸糖蛋白為主的糖蛋白,同時也是一種腫瘤抗原,它與CA199有一定的交叉抗原性,多用于胰腺癌、腸癌等的輔助診斷。CA199是一種Lewisa血型抗原,它作為腫瘤相關標志物在胰腺癌和膽囊癌中的檢出陽性率最高,對胰腺癌的診斷敏感性為68%~93%,特異性也可達到60%以上,是迄今對胰腺癌輔助診斷最有價值和最主要的一種腫瘤血清標志物,近年來逐漸有證據表明它可以成為胰腺癌預后評估以及預測治療后生存率的一項指標[8]。然而,這3者中任何一個指標單獨檢測時均不能達到足夠的敏感性和特異性,多數研究者認為聯合檢測能夠增加胰腺癌診斷的敏感性及特異性[9,10]。
本研究通過聯合檢測CEA、CA50、CA199在胰腺癌、良性胰腺疾病及健康對照組中的表達水平,發現CEA、CA50、CA199在胰腺癌中的表達均明顯增高;與良性胰腺疾病以及健康對照組相比,差異有統計學意義。在聯合檢測3種指標后對胰腺癌的診斷敏感性可達到93.1%,特異性達到82.8%。因此通過本研究我們可以得出聯合檢測CEA、CA50、CA199對胰腺癌的診斷是一種快捷、無創、有效的途徑。在本研究中我們同時對實施胰腺癌外科手術的患者進行連續監測,對術后患者聯合檢測CEA、CA50、CA199這3種標志物的表達,發現胰腺癌根治性切除術后復發組血清中CEA、CA50、CA199的表達水平與未復發組相比有明顯的增高。在評估術后復發情況的觀察中,聯合檢測(指3項檢測任一指標陽性)對復發患者的診斷陽性率為95.5%(42/44),特異性達到了86.3%(3項檢測指標均陽性),在滿足特異性診斷的前提下,診斷的敏感性得到了提高。
有研究報道CEA、CA50和CA199對細胞間的粘附發揮著重要的作用, 細胞的粘附參與了腫瘤的轉移過程,本研究同時檢測了3種指標在胰腺癌患者不同腫瘤分期中的表達差異,發現CEA、CA50和CA199的表達水平與腫瘤的臨床分期有關,在Ⅲ~Ⅳ期患者中的表達水平明顯高于Ⅰ~Ⅱ期腫瘤患者。所以證實CEA、CA50和CA199與胰腺癌的增殖、浸潤及轉移有一定的相關性。所以在胰腺癌復發轉移的監測和評估中發揮的具體機制,我們將在后續的實驗中進一步研究探討。
綜上,通過對CEA、CA50、CA199三種血清腫瘤標志物的聯合檢測,對胰腺癌診斷的敏感性和特異性均高于單一指標的檢測,并且可以較好地對胰腺癌患者預后進行有效的評估,從而有助于胰腺癌患者的療效觀察、復發預測,為改善患者生存及生活質量提供幫助。
1 Imaoka H, Mizuno N, Hara K, et al. Prognostic impact of carcinoembryonic antigen (CEA) on patients with m etastatic pancreatic cancer: A retrospective cohort study[J]. Pancreatology,2016,16(5):859-864
2 Deng T, Yuan Y, Zhang C , et al. Identification of Circulating MiR-25 as a Potential Biomarker for Pancreatic Cancer Diagnosis[J]. Cell Physiol Biochem,2016,39(5):1716-1722
3 Siegel RL, Miller KD, Jemal A. Cance r statistics, 2016. CA a Cancer J Clin,2016,66(5):7-30
4 Zhao J, Liang Y, Yin Q, et al. Clinical and prognos tic significance of serum transforming growth factor-beta1 levels in patients with pancreatic ductal adenocarcinoma [J]. Braz J M ed Biol Res,2016,49(8):1414-1431
5 Hidalgo M,Plaza C,Musteanu M,et al.SPARC Expression Did Not Predict Efficacy of nab-Paclitaxel plus Gemcitabine or Gemcitabine Alone for Metastatic Pancreatic Cancer in an Exploratory Analysis of the Phase Ⅲ MPACT Trial[J].Clin Cancer Res,2015,21(21):4811-4818
6 Sultana A, Cox T, Ghaneh P, et al. Adjuvant therapy for pancreatic cancer [J]. Recent Results Cancer Res,2012,196(7):65-88
7 黃紅莉,周剛,牛立志,等.胰腺癌患者冷凍消融治療前后血清CD44V6和整合素β1的變化及在預后評估中的意義[J]. 檢驗 醫學,2013,28(12):1083-1087
8 Hernandez JM, Cowgill SM, Al-Saadi S, et al. CA 19-9 velocity predicts disease-free survival and overall s urvival after pancreatectomy of curative intent [J].J Gastrointest Surg ,2009,13(6):349-353
9 田力, 王 曉艷, 沈 守榮 . 腫 瘤標志物 CA199、CA242、CEA、CA125聯合檢測在胰腺癌診斷中的意義[J]. 世界華人消化雜志,2012,20(31):3047-3050
10 謝煥琴, 鐘 武裝. 血 清CA199、CA242及CEA聯合檢測對胰腺癌的診斷價值 [J]. 廣西醫科大學學報,2013,30(5):75-76

