定量磁敏感圖黑質“燕尾征”在帕金森病診斷中的應用價值
管曉軍 謝非 徐曉俊
帕金森病(PD)是老年人群常見的神經變性病。流行病學調查顯示,我國≥65歲的老年人群患病率達1.7%[1]。由于缺乏客觀生物學標志物,帕金森病的診斷主要依靠臨床醫師對患者臨床癥狀與體征的評價[2],很大程度受主觀因素的干擾,故近20年來帕金森病的診斷準確性無明顯提高[3?4]。積極探尋可以提示帕金森病的客觀生物學標志物,將有助于提高疾病診斷水平。黑質致密部多巴胺能神經元缺失是臨床期帕金森病的特征性病理改變。尸體解剖研究顯示,黑質致密部背外側區即Nigrosome 1區是帕金森病多巴胺能神經元缺失最早、最嚴重的區域[5?6];且該區域鐵沉積(加重局部神經元氧化應激負荷)與多巴胺能神經元缺失密切相關[7]。因此,黑質致密部背外側區鐵沉積有助于提示帕金森病。作為磁性物質,鐵元素可以影響MRI信號。正常人群磁敏感加權成像(SWI)顯示黑質致密部背外側區呈現“燕尾”狀高信號即“燕尾征”,而帕金森病患者該區域高信號消失,稱為“燕尾征”消失[8]。研究顯示,“燕尾征”消失征象用于診斷帕金森病的靈敏度較高(>88%),而特異度變化較大(37% ~ 95%)[7?11]。定量磁敏感圖(QSM)是在SWI基礎上的進一步發展,具有更清晰的信號對比度和分辨力[12?15]。在本研究中,我們采用QSM觀察帕金森病患者黑質致密部背外側區“燕尾征”,探討該項技術是否有助于提高“燕尾征”在帕金森病診斷中的應用價值。
資料與方法
一、臨床資料
1.納入標準 (1)帕金森病的診斷符合英國帕金森病學會腦庫帕金森病臨床診斷標準[16]。(2)均行頭部MRI檢查。(3)本研究經浙江大學醫學院附屬第二醫院道德倫理委員會審核批準,所有患者或其家屬均知情同意并簽署知情同意書。
2.排除標準 (1)其他中樞神經系統疾病病史、精神病病史和顱腦創傷史。(2)臨床資料或影像學資料不全。(3)由于震顫等原因造成運動偽影較大,影響圖像質量而無法進一步處理。
3.一般資料 (1)帕金森病組:根據納入與排除標準,選擇2010年10月-2016年10月在浙江大學醫學院附屬第二醫院明確診斷的帕金森病患者共計76例,男性38例,女性38例;年齡35~77歲,平均(55.69±8.94)歲;病程0.25~17.10年,中位病程2.92(1.58,6.50)年;統一帕金森病評價量表第三部分(UPDRSⅢ)評分為 7~72分,平均為(28.75±15.53)分;Hoehn?Yahr分期 1~4級、平均(2.28±0.69)級,其中1級9例、1.5級5例、2級17例、2.5級30例、3級12例、4級3例。(2)正常對照組:選擇同期在我院進行體格檢查的健康志愿者共47例,頭部MRI均未見明顯異常,男性22例,女性25例;年齡37~79歲,平均(57.53±9.69)歲。兩組受試者性別(χ2=0.118,P=0.731)和年齡(t=1.077,P=0.284)比較,差異均無統計學意義,具有可比性。
二、研究方法
1.頭部MRI檢查 采用美國GE公司生產的Signa EXCITE 3.0T MRI掃描儀,8通道頭部線圈,梯度場強50 mT/m。受試者以醫用海綿墊固定頭部、佩戴耳塞降低噪音,以提高舒適度、減少運動偽影,首先進行T2?FLAIR成像掃描,以排除潛在病變,如占位性病變、畸形、軟化灶或腦白質高信號(WMH)等,再行三維高分辨力 MRI(3D?HRMRI)、擴散張量成像(DTI)、靜息態fMRI(rs?fMRI)、多回波采集的增強T2*加權血管成像(ESWAN)掃描。(1)3D?HRMRI:重復時間(TR)5.10 ms、回波時間(TE)1.20 ms,掃描視野(FOV)240 mm×240 mm,矩陣256×256,激勵次數(NEX)1次,層厚1.20 mm、層間距為零,掃描時間160 s,共掃描124層,掃描范圍覆蓋大腦和小腦。(2)DTI:重復時間 12 000 ms、回波時間 105 ms,掃描視野240 mm×240 mm,矩陣128×128,激勵次數1次,b值為1000 s/mm2,層厚3 mm、層間距為零,掃描時間170 s,共37層,掃描范圍覆蓋大腦和小腦。(3)rs?fMRI:重復時間 2000 ms、回波時間 30 ms,掃描視野240 mm×240 mm,矩陣64×64,激勵次數1次,層厚5 mm、層間距1 mm,掃描時間370 s,共掃描23層,掃描范圍覆蓋大腦和小腦。(4)ESWAN序列:重復時間45 ms,回波次數8次,首次回波時間為5 ms,間隔 5.02 ms,末次回波時間 40.14 ms,翻轉角(FA)25°,帶寬頻率31.25 kHz,平面內分辨率0.78×0.78,掃描視野200 mm×200 mm,重建后矩陣256×256,激勵次數1次,層厚2.80 mm、層間距為零,加速因子為2,掃描時間210 s,共52層,掃描范圍覆蓋大腦和小腦。
2.圖像處理 由同一位經驗豐富的放射科醫師采用盲法獨立完成。參照文獻[13?14]方法,采用STI Suite軟件包(美國加利福尼亞大學伯克利分校研發)[17?18]進行 QSM 圖像處理。(1)采用 Laplacian 法對相位圖去包裹,該方法可以較好地保留所有腦組織空間低頻成分,如灰質、白質和腦脊液。(2)由于未去包裹的相位圖背景相位掩蓋腦組織相位信息,采用V?SHARP法將球形半徑由0.60 mm(腦邊界處)擴大至25 mm(腦中心處),以去除背景相位。(3)由于重建單方向的QSM圖可能出現線狀偽影,導致細微結構(微病灶)丟失,采用iLSQR公式[17]估算磁化率邊界,迭代評價僅來自異常K空間填充引起的磁化偽影,以獲得剩余腦組織相位圖和磁化率,最終獲得QSM圖。與SWI圖不同,QSM圖顯示,正常人群由于黑質致密部背外側區鐵含量較低,故磁化率較低,表現為細條形或卵圓形低信號;帕金森病患者由于黑質致密部背外側區鐵沉積明顯,故磁化率較高,表現為低信號消失,即“燕尾征”消失。雙側黑質致密部背外側區低信號均存在為正常;單側或雙側黑質致密部背外側區低信號消失為異常,即“燕尾征”消失[7?11]。為便于比較幾種技術對黑質的成像,選擇同一層面的QSM圖、SWI圖、幅度圖(magnitude image)和R2*圖。
3.統計分析方法 采用SPSS 19.0統計軟件進行數據處理與分析。呈正態分布的計量資料以均數±標準差(x±s)表示,采用兩獨立樣本的t檢驗;呈非正態分布的計量資料以中位數和四分位數間距[M(P25,P75)]表示。計數資料以相對數構成比(%)或率(%)表示,采用χ2檢驗;計算帕金森病患者和正常對照者黑質致密部背外側區“燕尾征”出現率和消失率;計算“燕尾征”消失征象診斷帕金森病的靈敏度、特異度和準確度。以P≤0.05為差異具有統計學意義。
結 果
QSM圖具有極高的磁化率對比,可以清晰顯示黑質部位,準確評價“燕尾征”的存在或消失,而SWI圖、幅度圖和R2*圖分辨力較低,在本研究中無法達到診斷意義(圖1~3)。
76例帕金森病患者中73例(96.05%)出現單側或雙側“燕尾征”消失,包括單側22例和雙側51例;47例正常對照者中28例(59.57%)出現單側或雙側“燕尾征”消失,包括單側15例和雙側13例,組間差異有統計學意義(χ2=26.311,P=0.000)。“燕尾征”消失診斷帕金森病的靈敏度為96.05%、特異度為40.43%、準確度為74.80%。
討 論
本研究結果顯示,QSM圖具有極高的磁化率對比,是目前較為先進的黑質成像技術,可以滿足“燕尾征”定性分析的需要;QSM圖黑質致密部背外側區“燕尾征”消失診斷帕金森病的靈敏度較高(96.05%)、特異度較低(40.43%),準確度為74.80%。
病理學研究顯示,帕金森病患者腦組織多巴胺能神經元缺失進程具有明顯的梯度變化,即隨著疾病進展由外至內逐漸增多,其中影響最早且最嚴重的區域是黑質致密部背外側區[5?6]。2008 年,Martin等[19]采用R2*技術定量測量黑質致密部鐵含量,結果顯示,帕金森病早期黑質致密部背外側區即有明顯的鐵沉積,且該部位鐵含量與帕金森病運動癥狀嚴重程度呈正相關(r2=0.270,P=0.010)。此后,研究者們采用不同MRI鐵成像技術如SWI圖、相位圖(phase image)和幅度圖等證實,大多數帕金森病患者黑質致密部背外側區存在與鐵元素相關的MRI信號改變[7?11]。Blazejewska 等[7]將 MRI與病理學相結合,進一步揭示MRI信號改變位置為黑質致密部背外側區,且“燕尾征”消失與該區域鐵沉積、黑色素減少和神經元缺失密切相關。本研究采用QSM技術觀察帕金森病患者黑質MRI信號改變,96.05%(73/76)的患者黑質致密部背外側區“燕尾征”消失,即存在鐵沉積導致的局部磁敏感性改變,與既往研究結果相一致[7?11]。
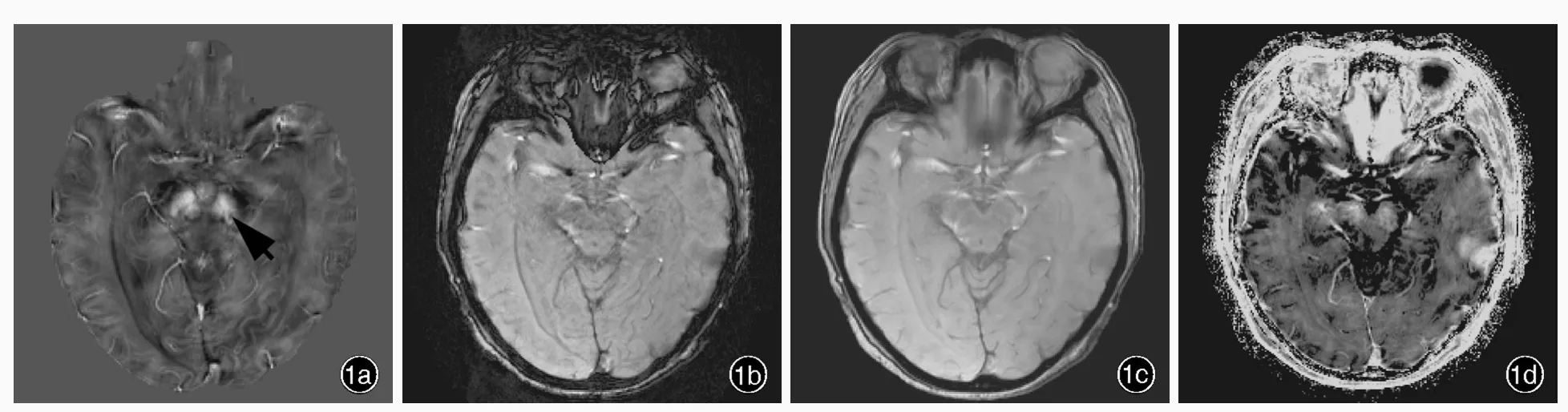
圖1 女性患者,53歲,臨床診斷為帕金森病。頭部MRI檢查所見 1a 橫斷面QSM圖顯示,左側黑質致密部背外側區卵圓形低信號影(箭頭所示) 1b~1d 同層面SWI圖、幅度圖和R2*圖均顯示不佳Figure 1 A 53 ?year?old female patient was diagnosed as PD.Head MRI findings Axial QSM showed an oval hypointensity in dorsolateral part of left substantia nigra pars compacta(arrow indicates,Panel 1a).SWI,magnitude image and R2*image in the same level failed to visualize"swallow tail sign"(Panel 1b-1d).
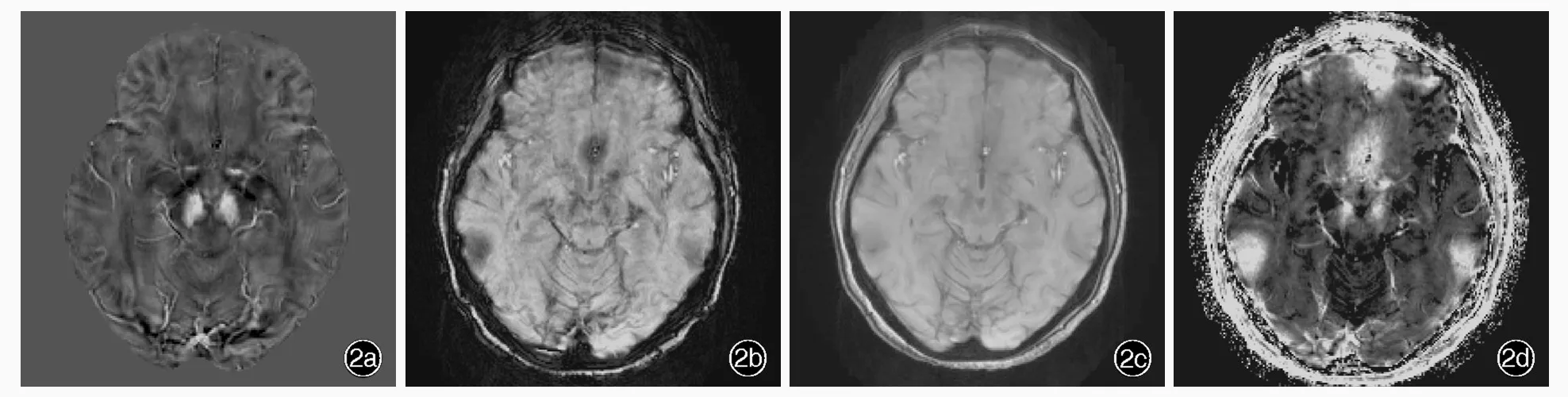
圖2 女性患者,57歲,臨床診斷為帕金森病。頭部MRI檢查所見 2a 橫斷面QSM圖未見黑質致密部背外側區低信號影 2b~2d 同層面SWI圖、幅度圖和R2*圖均顯示不佳Figure 2 A 57?year?old female patient was diagnosed as PD.Head MRI findings Axial QSM showed the absence of hypointensity in dorsolateral part of substantia nigra pars compacta(Panel 2a).SWI,magnitude image and R2*image in the same level failed to visualize"swallow tail sign"(Panel 2b-2d).
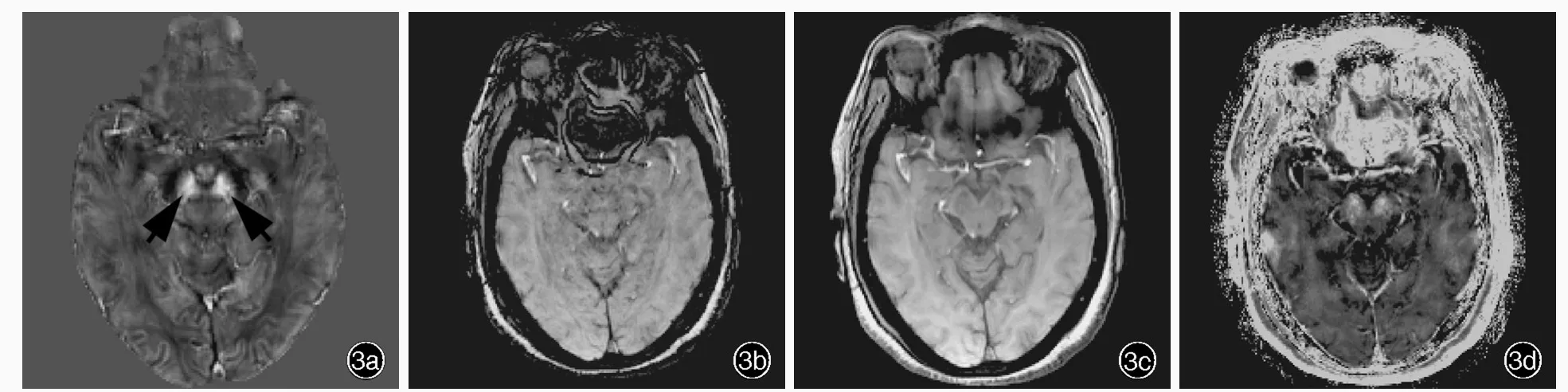
圖3 正常女性,60歲。頭部MRI檢查所見 3a 橫斷面QSM圖顯示,雙側黑質致密部背外側區可見卵圓形低信號影(箭頭所示) 3b~3d 同層面SWI圖、幅度圖和R2*圖均顯示不佳Figure 3 Head MRI findings of a 60?year?old normal female Axial QSM showed bilateral oval hypointensity in dorsolateral part of substantia nigra pars compacta(arrows indicate,Panel 3a).SWI,magnitude image and R2*image in the same level failed to meet the diagnostic requirement(Panel 3b-3d).
盡管MRI在體研究和體外研究均證實帕金森病患者存在黑質致密部背外側區鐵沉積,且該區域鐵沉積與多巴胺能神經元缺失密切相關,但能否根據黑質致密部背外側區MRI信號改變以診斷帕金森病尚存爭議。研究顯示,正常老年人群“燕尾征”消失較為罕見,根據該征象鑒別診斷帕金森病患者與正常對照者的特異度高達 83% ~ 85%[7?9,11]。亦有研究顯示,“燕尾征”消失診斷帕金森病的特異度僅為37%[10],與本研究特異度為40.43%相近。究其原因,可能包括以下幾方面:(1)腦組織正常老化可以導致黑質?紋狀體多巴胺能神經元缺失和黑質致密部鐵沉積[20],“燕尾征”存在與否可能不足以區分腦組織正常老化與神經退行性變,定量測量鐵含量可能有助于鑒別二者。(2)有文獻報道,“燕尾征”消失也可見于多發性硬化(MS)和進行性核上性麻痹(PSP)等帕金森疊加綜合征患者[11],因此,該征象可能是黑質?紋狀體多巴胺能神經元變性的共同表現而并非原發性帕金森病的特征性表現。本研究正常對照者未經嚴格的神經內科醫師評價,可能混有前驅期帕金森病患者[21]或其他神經變性病高危人群,如原發性快速眼動睡眠期行為障礙(RBD)[22]。(3)黑質致密部背外側區體積較小,但本研究圖像采集層厚較大(層厚2.80 mm),部分容積效應可能影響黑質致密部背外側區MRI信號的判斷。
綜上所述,本研究采用QSM技術觀察到大多數帕金森病患者黑質致密部背外側區存在磁化率差異導致的MRI信號改變,即“燕尾征”消失,但僅根據“燕尾征”消失診斷帕金森病的特異性較低。本研究為回顧性研究,無法嚴格控制研究對象和針對性地調整MRI參數,尚待前瞻性研究采用更高分辨力的MRI掃描儀(避免部分容積效應)、更優化的MRI參數提高圖像分辨力、更精確的定量分析方法提高QSM技術在帕金森病診斷中的應用價值。
[1]Zhang ZX,Roman GC,Hong Z,Wu CB,Qu QM,Huang JB,Zhou B,Geng ZP,Wu JX,Wen HB,Zhao H,Zahner GE.Parkinson's disease in China:prevalence in Beijing,Xi'an,and Shangha[iJ].Lancet,2005,365:595?597.
[2]Postuma RB,Berg D,Stern M,Poewe W,Olanow CW,Oertel W,Obeso J,Marek K,Litvan I,Lang AE,Halliday G,Goetz CG,Gasser T,Dubois B,Chan P,Bloem BR,Adler CH,Deuschl G.MDS clinical diagnostic criteria for Parkinson's disease[J].Mov Disord,2015,30:1591?1601.
[3]Adler CH,Beach TG,Hentz JG,Shill HA,Caviness JN,Driver?Dunckley E,Sabbagh MN,Sue LI,Jacobson SA,Belden CM,DuggerBN.Low clinicaldiagnostic accuracy ofearly vs advanced Parkinson disease: clinicopathologic study [J].Neurology,2014,83:406?412.
[4]RajputAH,Rozdilsky B,RajputA.Accuracy ofclinical diagnosisin parkinsonism:a prospective study[J].Can J Neurol Sci,1991,18:275?278.
[5]Damier P,Hirsch EC,Agid Y,Graybiel AM.The substantia nigra of the human brain.Ⅱ:patterns of loss of dopamine?containing neurons in Parkinson's disease[J].Brain,1999,122:1437?1448.
[6]Fearnley JM,Lees AJ.Ageing and Parkinson's disease:substantia nigra regional selectivity[J].Brain,1991,114:2283?2301.
[7]Blazejewska AI,Schwarz ST,Pitiot A,Stephenson MC,Lowe J,Bajaj N,Bowtell RW,Auer DP,Gowland PA.Visualization of nigrosome 1 and its loss in PD:pathoanatomical correlation and in vivo 7T MRI[J].Neurology,2013,81:534?540.
[8]Schwarz ST,Afzal M,Morgan PS,Bajaj N,Gowland PA,Auer DP.The'swallow tail'appearance of the healthy nigrosome:a new accurate test of Parkinson's disease.A case?control and retrospective cross?sectional MRI study at 3T[J].PLoS One,2014,9:E93814.
[9]Reiter E,MuellerC,Pinter B,Krismer F,Scherfler C,Esterhammer R,Kremser C,Schocke M,Wenning GK,Poewe W, Seppi K. Dorsolateral nigral hyperintensity on 3.0T susceptibility?weighted imaging in neurodegenerative Parkinsonism[J].Mov Disord,2015,30:1068?1076.
[10]He N,Ling H,Ding B,Huang J,Zhang Y,Zhang Z,Liu C,Chen K,Yan F.Region?specific disturbed iron distribution in early idiopathic Parkinson's disease measured by quantitative susceptibility mapping[J].Hum Brain Mapp,2015,36:4407 ?4420.
[11]Bae YJ,Kim JM,Kim E,Lee KM,Kang SY,Park HS,Kim KJ,Kim YE,Oh ES,Yun JY,Kim JS,Jeong HJ,Jeon B,Kim SE.Loss of nigral hyperintensity on 3 Tesla MRI of Parkinsonism:comparison with(123)I?FP?CIT SPECT[J].Mov Disord,2016,31:684?692.
[12]Liu C,Li W,Tong KA,Yeom KW,Kuzminski S.Susceptibility?weighted imaging and quantitative susceptibility mapping in the brain[J].J Magn Reson Imaging,2015,42:23?41.
[13]Guan X,Xuan M,Gu Q,Huang P,Liu C,Wang N,Xu X,Luo W,Zhang M.Regionally progressive accumulation of iron in Parkinson's disease as measured by quantitative susceptibility mapping[J].NMR Biomed,2017,30:E3489.
[14]Guan X,Xuan M,Gu Q,Xu X,Huang P,Wang N,Shen Z,Xu J,Luo W,Zhang M.Influence of regional iron on the motor impairments of Parkinson's disease:a quantitative susceptibility mapping study[J].J Magn Reson Imaging,2017,45:1335?1342.
[15]Guan X,Xu X,Zhang M.Region?specific iron measured by MRI as a biomarker for Parkinson's disease[J].Neurosci Bull,2017,33:561?567.
[16]Hughes AJ,Daniel SE,Kilford L,Lees AJ.Accuracy of clinical diagnosis of idiopathic Parkinson's disease: a clinico?pathologicalstudy of100 cases[J].J NeurolNeurosurg Psychiatry,1992,55:181?184.
[17]LiW,WangN,Yu F,Han H,CaoW,RomeroR,Tantiwongkosi B,Duong TQ,Liu C.A method for estimating and removing streaking artifacts in quantitative susceptibility mapping[J].Neuroimage,2015,108:111?122.
[18]Li W,Avram AV,Wu B,Xiao X,Liu C.Integrated Laplacian?based phase unwrapping and background phase removal for quantitative susceptibility mapping[J].NMR Biomed,2014,27:219?227.
[19]Martin WR,Wieler M,Gee M.Midbrain iron content in early Parkinson disease:a potential biomarker of disease status[J].Neurology,2008,70:1411?1417.
[20]XuX,WangQ,ZhangM.Age,gender,andhemispheric differences in iron deposition in the human brain:an in vivo MRI study[J].Neuroimage,2008,40:35?42.
[21]Berg D,Postuma RB,Adler CH,Bloem BR,Chan P,Dubois B,Gasser T,Goetz CG,Halliday G,Joseph L,Lang AE,Liepelt?Scarfone I,Litvan I,Marek K,Obeso J,Oertel W,Olanow CW,Poewe W,Stern M,Deuschl G.MDS research criteria for prodromal Parkinson's disease[J].Mov Disord,2015,30:1600?1611.
[22]De Marzi R,Seppi K,Hogl B,Muller C,Scherfler C,Stefani A,Iranzo A,Tolosa E,Santamaria J,Gizewski E,Schocke M,Skalla E,Kremser C,Poewe W.Loss of dorsolateral nigral hyperintensity on 3.0 tesla susceptibility?weighted imaging in idiopathic rapid eye movement sleep behavior disorder[J].Ann Neurol,2016,79:1026?1030.

