糖尿病前期與高血壓發病風險的相關性研究
史 榮
(貴州省遵義市第一人民醫院內分泌科 563000)
糖尿病前期是指血糖處于正常范圍到糖尿病診斷界值之間的過渡水平,包括兩類人群:空腹葡萄糖調節受損(impaired fasting glucose,IFG)和糖耐量受損(impaired glucose tolerance,IGT)。IGT與IFG通常同時存在,并與2型糖尿病以及動脈硬化相關性心血管疾病發生風險升高相關[1-4]。隨著現代社會工業化、城市化不斷加深,人類的飲食結構及生活習慣等也發生著相應改變,高血壓作為當今社會最常見的心血管疾病之一,在世界范圍內的流行程度也處于不斷攀升的狀態[5]。
既往研究表明,高血壓患者中糖尿病前期的患病率較血壓正常人群顯著升高[6-7]。2016年來自于湖北省的一項橫斷面研究顯示,與糖代謝正常人群相比,糖尿病患者的高血壓患病風險顯著升高(OR=3.87,95%CI:3.30~4.52)[8]。值得注意的是,同為代謝綜合征的重要組分,血糖調節異常與高血壓具有共同的危險因素,互相影響,互相促進[9]。2016年發表在《BMC Endocr Disord》雜志的一項橫斷面研究表明,在中國大于或等于65歲的老年人群中,IFG與高血壓患病風險升高顯著相關[10]。另外一項來自伊朗的隨訪研究同樣表明,基線水平處于糖尿病前期的患者不論血壓處于正常水平還是處于高血壓前期水平,未來高血壓的發生風險均顯著升高[11]。因此,本研究旨在通過臨床隨訪隊列人群探討糖尿病前期狀態與新發高血壓風險的相關性。
1 資料與方法
1.1一般資料 在2010年2月至2011年4月在本院內分泌科門診及病房就診患者以及來院體檢者中,根據75 g口服葡萄糖耐量測試(oral glucose tolerance test,OGTT)結果,分別收集既往無高血壓病史、目前血壓正常且無降壓藥服用史的糖耐量正常者以及糖尿病前期患者(包括IFG和/或IGT患者)各200例。既往有腎臟疾病(包括急慢性腎炎、腎衰竭)、肝功能異常[血清丙氨酸氨基轉移酶(alanine aminotransferase,ALT)、天冬氨酸氨基轉移酶(aspartate aminotransferase,AST)或者谷氨酰轉肽酶(gamma-glutamyltransferase,GGT)升高大于正常值3倍]、腎功能異常(血肌酐大于或等于 134 μmol/L)以及有惡性腫瘤病史的患者不納入到本研究當中。2014年3月至2015年5月對研究對象進行隨訪調查,糖尿病前期組共隨訪到146例研究對象,其中69例仍處于糖尿病前期的研究對象被納入到本研究的分析當中。糖耐量正常組共隨訪到140例研究對象,其中102例研究對象仍處于糖耐量正常狀態被納入到本研究的分析當中。
1.2方法 問卷調查:本研究對每一位入組的研究對象通過問卷調查形式進行信息采集,收集研究對象的性別、出生日期、聯系方式等基本信息以及基本臨床信息,包括家族史、既往病史、用藥史、生活方式(主要包括吸煙飲酒情況、體育活動情況等)。
人口學指標:研究對象接受常規體格檢查,包括腰圍、臀圍、身高、體質量、靜息狀態血壓等。
實驗室檢查:本研究于入組時及隨訪時分別對每位研究對象進行2次75 g OGTT檢測,要求研究對象于夜間空腹至少10 h后進行。并對研究對象的空腹血糖,OGTT 2 h血糖、空腹胰島素、OGTT 2 h胰島素、糖化血紅蛋白、三酰甘油、總膽固醇、高密度脂蛋白膽固醇、低密度脂蛋白膽固醇等生化指標進行了測定。胰島素敏感性的評估采用的是胰島素抵抗指數穩態模型評估法(homeostasis model of assessment for insulin resistence index,HOMA-IR),計算公式為:HOMA-IR=空腹血糖×空腹胰島素/22.5。

表1 基線臨床指標比較

續表1 基線臨床指標比較
1.3診斷標準 糖尿病前期根據世界衛生組織1999年發布的診斷標準[12]:6.1 mmol/L≤空腹血糖<7.0 mmol/L和/或7.8 mmol/L≤OGTT 2 h血糖<11.1 mmol/L,且既往無糖尿病病史,無口服降糖藥或胰島素使用史。高血壓是根據國際聯合委員會發布的第7版指南(Joint national committee,JNC7)進行診斷:收縮壓(SBP)≥140 mm Hg和/或舒張壓(DBP)≥90 mm Hg。新診斷高血壓定義為隨訪調查時血壓測量結果符合上述任一指標或者隨訪期間有降壓藥用藥史。胰島素抵抗定義為HOMA-IR≥2.5[13]。
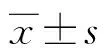
2 結 果
2.1基線臨床指標比較 本研究共納入171例研究對象,平均隨訪時間為3.76年,其中102例研究對象隨訪期間處于糖耐量正常水平,69例研究對象隨訪期間處于糖尿病前期狀態。研究對象平均年齡為(56.5±8.5)歲,男50例(29.2%),女121例(70.8%)。兩組人群年齡、性別構成差異無統計學意義。通過對兩組研究對象的基本臨床特征及生化指標比較,結果顯示,持續處于糖尿病前期狀態的人群具有更高的體質量指數(body mass index,BMI)、SBP水平、空腹及OGTT 2 h血糖、空腹及OGTT 2 h胰島素水平、糖化血紅蛋白水平、三酰甘油、總膽固醇水平以及胰島素抵抗患病率(P<0.05)。另外,與糖耐量正常組相比,糖尿病前期人群吸煙者比例較低(P<0.05),見表1。
2.2糖尿病前期狀態與新發高血壓風險的相關性 隨訪結果表明,持續處于糖尿病前期組高血壓發病率為30.4%,顯著高于糖耐量正常組的12.8%(P<0.05),見表2。在新發高血壓人群中,糖尿病前期以及胰島素抵抗的患病率(分別為61.76%和29.41%)均顯著高于未發生高血壓人群(分別為35.04%和9.49%,P<0.05)。Logistic回歸模型分析表明,持續處于糖尿病前期狀態可以顯著增加高血壓發病風險,OR(95%CI):2.99(1.38~6.51)。在矯正年齡、性別、BMI、腰圍、高血壓家族史、吸煙飲酒狀態、體育活動、總膽固醇、三酰甘油水平等混雜因素后,結果保持顯著:OR(95%CI):2.76(1.08~7.03),見表2。

表2 Logistic回歸分析糖尿病前期與新發高血壓發生風險相關性
模型1:未校正;模型 2:矯正了基線年齡;模型3:在模型2的基礎上校正了基線性別,體質量指數,腰圍;模型4:進一步校正了高血壓家族史、吸煙、飲酒狀態,體育活動,總膽固醇,三酰甘油
3 討 論
本研究通過對臨床病例的收集和隨訪,發現糖尿病前期狀態與高血壓發生風險升高顯著相關。與此同時,本研究還發現新發高血壓患者中糖尿病前期及胰島素抵抗的患病率均顯著高于未發生高血壓的人群。既往有關持續處于糖尿病前期與高血壓發生風險相關性的研究尚少,本研究結果提示,即便未達到糖尿病診斷標準,長期處于糖尿病前期狀態仍是高血壓發病的重要危險因素,與持續處于血糖正常者相比,糖尿病前期狀態及其伴隨的胰島素抵抗狀態均與高血壓發病風險升高相關。
糖尿病前期是機體對胰島素利用率下降的臨床表現之一,其中IFG主要與肝臟胰島素抵抗有關,而糖耐量減低主要與肌肉組織胰島素抵抗有關。上述復雜的病理生理機制可能參與到糖尿病前期增加高血壓發生風險的作用當中。FAGOT等[14]的一項研究表明,高胰島素血癥以及血糖調節異常均是高血壓發病的危險因素。另外一項來自日本的前瞻性研究也發現IFG是高血壓發病的危險因素[15]。然而,中國香港一項評估心血管疾病危險因素的人群隊列研究則發現IFG與高血壓發病風險無顯著相關性[16]。VACCARO等[17]對IGT與高血壓發病風險相關性進行了分析,結果也提示,IGT在基線橫斷面水平與血壓升高相關,但并不能預告高血壓發病風險。上述既往研究結論尚具爭議,本研究通過臨床隨訪觀察,排除隨訪期間糖耐量狀態的變化,有針對性地將持續處于糖尿病前期狀態的患者與隨訪期間糖耐量正常者進行比較,探討兩種糖代謝狀態與高血壓發病風險的相關性,為進一步人群調查研究及機制研究提供參考。
本研究發現,新發高血壓人群胰島素抵抗的患病率顯著高于血壓正常人群,且糖尿病前期患者胰島素抵抗患病率也顯著高于糖耐量正常人群。越來越多的研究提示,胰島素抵抗對腎臟及水鈉代謝平衡的不良影響在高血壓發病的病理過程中扮演重要角色。胰島素可以加強遠曲小管對鈉的重吸收,主要是通過提高鈉轉運通道的表達,并降低鈉的排出[18]。水鈉潴留是高血壓發病的病理過程中的重要環節,高胰島素血癥還可以通過對近端小管鈉-氫交換作用的加強促進水鈉潴留的發生和發展,并最終導致高血壓的發生[18]。與此同時,尿酸與鈉在腎臟代謝途徑類似,水鈉潴留同樣導致尿酸排泄降低,而高尿酸血癥在高血壓患者中十分常見,進一步成為高血壓發病過程中的促進因素之一[19]。另外,高胰島素血癥所致的氧化應激狀態對高血壓的發生也產生一定促進作用[20]。主要是通過使機體對血管收縮及加壓物質如血管緊張素Ⅱ等反應增強從而促進收縮壓的升高[21-22]。血管內皮細胞如上皮細胞、平滑肌細胞等可以通過作用于黃嘌呤氧化酶及一氧化氮合酶,產生不同種類的過氧化物,這些物質可以通過直接組織損傷、降低具有生物活性一氧化氮水平及其相關的血管舒張功能等途徑對血管內皮功能造成損傷[23]。而慢性炎癥狀態及氧化應激可以促進脂肪組織中血管緊張素原及血管緊張素Ⅱ的釋放,從而激活體內ROS系統,最終導致血壓升高[24]。
本研究也有一些不足:研究對象為院內收集病例,主要為中老年人群,故尚不能代表普通人群。本研究人群以女性為主,可能與男性和女性在社會參與度及配合度方面存在差異所致,但在本研究中,NGR及IGR人群無性別比例差異(P>0.05)。另外,本研究隨訪率相對偏低,可能是由于研究對象為中老年人群,依從性不高所致。綜上所述,本研究可為糖尿病前期人群高血壓的防治策略提供一定參考,但仍需長期隨訪的大樣本隨機抽樣隊列研究進一步探討。有關糖尿病前期與高血壓發生風險升高的內在機制仍有待進一步研究。
高血壓是心血管疾病以及慢性腎病的重要危險因素之一,如同時伴有糖尿病則其升高心血管疾病風險的作用尤為加強,給社會和家庭帶來沉重的醫療負擔[25]。眾所周知,糖尿病前期是糖尿病發生風險升高的重要預告因子,本研究發現,持續處于糖尿病前期的患者較糖耐量正常者高血壓發生風險顯著升高。因此,雖然未達到糖尿病診斷標準,醫生在臨床工作中仍應提高對糖尿病前期患者的重視,加強其血糖的監測及控制力度,積極采取飲食、鍛煉等方式改善糖代謝狀態,降低其糖尿病及高血壓等心血管系統疾病的發生風險,提高患者的長期生活質量。
[1]VEGT F,DEKKER J M,JAGER A,et al.Relation of impaired fasting and postload glucose with incident type 2 diabetes in a Dutch population:The Hoorn Study[J].Jama,2001,285(16):2109-2113.
[2]FERRANNINI E,NANNIPIERI M,WILLIAMS K,et al.Mode of onset of type 2 diabetes from normal or impaired glucose tolerance[J].Diabetes, 2004, 53(1):160-165.
[3]BARR E L,BOYO E J,ZIMMET P Z,et al.Continuous relationships between non-diabetic hyperglycaemia and both cardiovascular disease and all-cause mortality:the Australian Diabetes,Obesity,and Lifestyle (AusDiab) study[J].Diabetologia,2009,52(3):415-424.
[4]NAKAGAMI T,GROUP D S.Hyperglycaemia and mortality from all causes and from cardiovascular disease in five populations of Asian origin[J].Diabetologia,2004,47(3):385-394.
[5]YACH D,HAWKES C,GOULD C L,et al.The global burden of chronic diseases:overcoming impediments to prevention and control[J].Jama,2004,291(21):2616-2622.
[6]CARNEVALE G P,FRA G P.Impaired glucose metabolism in hypertensive patients with/without the metabolic syndrome[J].Europ J Int Med,2014,25(5):477-481.
[7]MOZAFFARIAN D,MARFISI R,LEVANTESI G,et al.Incidence of new-onset diabetes and impaired fasting glucose in patients with recent myocardial infarction and the effect of clinical and lifestyle risk factors[J].Lancet,2007,370(9588):667-675.
[8]潘琦,郭立新,劉薇,等.湖北省15歲以上居民高血壓患病狀況分析[J].重慶醫學,2016,45(18):2532-2534.
[9]丁賢彬,馮連貴,王豫林,等.重慶市部分農村居民高血壓與糖尿病患病率及影響因素分析[J].重慶醫學,2015,44(35):5112-5115.
[10]YAN Q,SUN D,LI X,et al.Association of blood glucose level and hypertension in Elderly Chinese Subjects:a community based study[J].BMC Endocr Disord,2016,16(1):40.
[11]DERAKHSHAN A,BAGHERZADEH KF,ARSHI B,et al.Different combinations of glucose tolerance and blood pressure status and incident diabetes,hypertension,and chronic kidney disease[J].J Am Heart Assoc,2016,5(8):e003917.
[12]GABIR M M,HANSON R L,DABELEA D,et al.The 1997 American Diabetes Association and 1999 World Health Organization criteria for hyperglycemia in the diagnosis and prediction of diabetes[J].Diabet Care,2000,23(8):1108-1112.
[13]YAMADA C,MITSUHASHI T,HIRATSUKA N,et al.Optimal reference interval for homeostasis model assessment of insulin resistance in a Japanese population[J].J Diabet Investig,2011,2(5):373-376.
[14]FAGOT C A,BALKAU B,SIMON D,et al.Is insulin an independent risk factor for hypertension? The Paris prospective study[J].Int J Epidemiol,1997,26(3):542-550.
[15]SUEMATSU C,HAYASHI T,FUJII S,et al.Impaired fasting glucose and the risk of hypertension in Japanese men between the 1980s and the 1990s[J].Diabet Care,1999,22(2):228-232.
[16]CHEUNG B M,WAT N M,MAN Y B,et al.Relationship between the metabolic syndrome and the development of hypertension in the Hong Kong Cardiovascular Risk Factor Prevalence Study-2 (CRISPS2)[J].Am J Hypertens,2008,21(1):17-22.
[17]VACCARO O,IMPERATORE G,IOVINO V,et al.Does impaired glucose tolerance predict hypertension? A prospective analysis[J].Diabetologia,1996,39(1):70-76.
[18]SONG J,HU X,RIAZI S,et al.Regulation of blood pressure,the epithelial sodium channel (ENaC),and other key renal sodium transporters by chronic insulin infusion in rats[J].Am J Physiol Renal Physiol,2006,290(5):1055-1064.
[19]MUSCELLI E,NATALI A,BIANCHI S,et al.Effect of insulin on renal sodium and uric acid handling in essential hypertension[J].Am J Hypertens,1996,9(8):746-752.
[20]COOPER S A,WHALEY-CONNELL A,HABIBI J,et al.Renin-angiotensin-aldosterone system and oxidative stress in cardiovascular insulin resistance[J].Am J Physiol Heart Circ Physiol,2007,293(4):2009-2023.
[21]JIA G,DEMARCO V G,SOWERS J R.Insulin resistance and hyperinsulinaemia in diabetic cardiomyopathy[J].Nat Rev Endocrinol,2016,12(3):144-153.
[22]ZHOU M S,LIU C,TIAN R,et al.Skeletal muscle insulin resistance in salt-sensitive hypertension:role of angiotensin II activation of NFkappaB[J].Cardiovasc Diabetol,2015,14:45.
[23]TANIYAMA Y,GRIENDLING K K.Reactive oxygen species in the vasculature:molecular and cellular mechanisms[J].Hypertension,2003,42(6):1075-1081.
[24]MASSIERA F,BLOCH-FAURE M,CEILER D,et al.Adipose angiotensinogen is involved in adipose tissue growth and blood pressure regulation[J].FASEB J,2001,15(14):2727-2729.
[25]EADDY M T,SHAH M,LUNACSEK O,et al.The burden of illness of hypertension and comorbid diabetes[J].Curr Med Res Opin,2008,24(9):2501-2507.

