大豆粗蛋白含量測定的催化條件初探
么曉黎
摘要:大豆作為重要的口糧與飼料原料,被廣泛的用于各類食品與飼料加工中,由于其營養價值均衡、附加值高等特點,應用領域越來越廣泛。筆者總結了實際工作內容,對大豆的粗蛋白含量的催化條件進行較為深刻的比較,使用了一種較為先進的催化方法,有效的加快了測定速度,同時保證了大豆粗蛋白含量的檢測方法的準確性。
關鍵詞:大豆;粗蛋白;凱氏定氮;催化劑
中圖分類號:S565.1
文獻標識碼:B
文章編號:2095-9737(2018)08-0025-01
1 樣品情況
大豆含有豐富的蛋白質和脂肪,具有營養均衡的特點。一般來說,黑龍江地產大豆的生產條件與施藥情況優于全國其他地區,大豆中的粗蛋白含量較高。為了了解大豆不同粗蛋白含量對檢測結果的影響,本次實驗采用了10個特殊含量樣本,自然樣本來源于哈爾濱市區域內收獲的大豆樣本,生長環境為普通農業生長環境。
2 實驗方法
本實驗主要針對凱氏定氮法中催化條件進行分析。蛋白質含有大量的氮,加入硫酸和催化劑時可被加熱消化,蛋白質被分解,分解產物與硫酸發生酸堿反應,生成硫酸鹽。生成的硫酸鹽經堿化蒸餾后,以硼酸吸收,最后以酸標準溶液滴定,根據酸的消耗量乘以換算系數,即為蛋白質含量。本實驗中實驗一的條件采用了普通凱氏定氮催化體系,即使用硫酸銅、硫酸鉀催化體系,而實驗二催化體系除傳統催化劑外,在樣品預處理中采用碳化鈣進行預處理,同時減少催化劑用量,考察兩種實驗方法的結果差異。
2.1 樣品處理
實驗一:準確稱取0. 20 g粉碎后大豆樣品,移入干燥的定氮燒瓶中,加入0.2 g硫酸銅,3g硫酸鉀及20 mL硫酸,搖勻后靜置,用小漏斗放置于瓶口,燒瓶以45°角斜支于有小孔的石棉網上。加熱至內容物全部炭化,澄清后,加大火力,并保持瓶內液體微沸,至液體呈藍綠色澄清透明后,再繼續加熱半小時。冷卻后,加入20 mL水。再次冷卻后,完全移人100 mL容量瓶中,混勻備用。取與處理樣品相同量的硫酸銅、硫酸鉀、硫酸按同一方法做試劑空白試驗[1]引用。
實驗二:準確稱取0. 20 g粉碎后大豆樣品,加入0.05 g碳化鈣后放入玻璃研缽進行研磨,研磨后移入干燥的100 mL定氮瓶中,加入0.1 g硫酸銅,1.5 g硫酸鉀及20 mL硫酸,搖勻后靜置,用小漏斗放置于瓶口,燒瓶以45°角斜支于有小孔的石棉網上。加熱至內容物全部炭化,澄清后,加大火力,并保持瓶內液體微沸,至液體呈藍綠色澄清透明后,再繼續加熱半小時。冷卻后,加入20 mL水。再次冷卻后,完全移入100 mL容量瓶中,混勻備用。取與處理樣品相同量的硫酸銅、硫酸鉀、硫酸按同一方法做試劑空白試驗[1]引用。
2.2 測定
根據標準連接定氮裝置,水蒸氣發生瓶內裝水至約2/3以上,加人數滴甲基紅指示液及,以保持發生瓶內酸性,加入0.5g分子篩,控制加熱溫度,加熱煮沸水蒸氣發生瓶內的水。向接收瓶內加入10 mL硼酸溶液及1滴混合指示液,吸取10.0 mL樣品消化稀釋液由小玻杯流入反應室,并以10 mL水洗滌小燒杯使流入反應室內,塞緊玻璃塞。將10 mL 40%氫氧化鈉溶液倒入小玻杯,提起玻璃塞使其緩緩流入反應室,立即蓋緊,液封以防漏氣。夾緊螺旋夾,開始蒸餾。蒸氣通入反應室使氨通過冷凝管而進入接收瓶內,蒸餾5 min。移動接受瓶,使冷凝管下端離開液面,再蒸餾1 min。然后用少量水沖洗冷凝管下端外部。取下接收瓶,以硫酸或鹽酸標準溶液滴定至灰色或藍紫色為終點。同時吸取10.0 mL試劑空白消化液重復以上實驗并計算[1]。
3 結果與討論
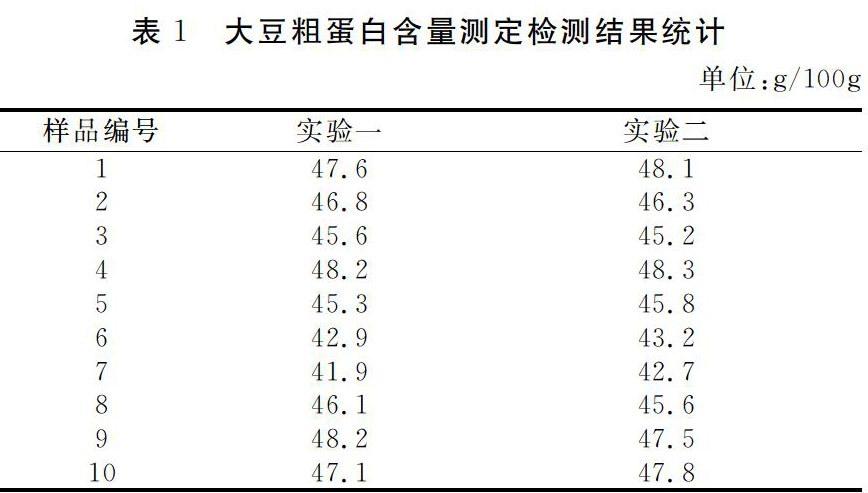
表1結果可以看出,實驗一與實驗二的檢測結果的絕對差值算數平均值的10%,符合國家標準5009.5的精密度要求,實驗表明使用碳化鈣對樣品進行預處理后,可將傳統催化劑使用量減半,同時反應時間減半,這不僅降低了催化劑使用量,同時能夠大幅加快實驗進程。經過初步分析,主要原因可能是由于碳化鈣的強吸水性使得樣品在消化過程前有一個預脫水過程,使得反應速度加快,具體反應機理還將在今后的實驗進一步進行討論。
4 結語
通過以上實驗結果,改善凱氏定氮的催化劑體系后,反應速度明顯加快,這也為大豆加工企業提供了一個準確的檢測手段,但相關企業還應盡量提高檢測水平。
參考文獻:
[1]國家標準GB 5009. 5- 2016《食品安全國家標準食品中蛋白質的測定》

