黃顙魚Wnt家族4個基因的克隆、組織表達及對銅的響應
張麗晗 羅 智 有文靜 李丹丹 吳 坤 徐異桓
(華中農業大學水產學院,動物遺傳育種與繁殖教育部重點實驗室, 武漢 430070)
Wnt家族的基因最初是由Nusse和Varmus于1982年在鼠類乳腺癌病毒誘導的小鼠乳腺癌中克隆得到的, 并被命名為Int-1, 該基因由于與后來報道的果蠅無翅基因Wingless (Wg)同源, 故將兩者合并命名為Wnt[1]。自從Wnt家族在1982年被發現以來, 科學工作者已經陸續在哺乳動物基因組中發現了19種Wnt家族成員基因[2]。進一步的研究證實,Wnt基因家族與其他相關基因組成了一條復雜的信號傳導途徑——Wnt信號途徑(Wnt signaling pathway)。Wnts可以通過經典的Wnt/β-catenin信號通路或者非經典Wnt信號通路(包括Wnt/Ca2+信號通路和Wnt/PCP信號通路)調節靶基因的表達, 在動物胚胎發育、細胞分化和器官發育等多種生命過程中發揮作用[3—5]。
Wnt通路是機體重要的信號轉導通路之一, 在細胞增殖、分化、胚胎發育和卵泡生成方面具有重要的調節作用[6,7]。因此, Wnt信號轉導通路的錯誤調節可導致包括卵巢發育失調在內的多種病理變化[3,8]。研究已證實, 以Wnt基因為配體的Wnt信號通路在進化中非常保守, 從低等的無脊椎動物到高等的哺乳動物都可以明顯檢測到該信號通路成員的表達[5]。在魚類, 目前僅在一些模式魚類克隆得到了Wnt家族部分成員的cDNA序列, 如斑馬魚(Danio rerio)[9,10]和青鳉(Oryzias latipe)[11]等。最近,曹梅等[12]基于斑點叉尾鮰(Ictalurus punctatus)的基因組數據庫, 通過與NCBI中存在的人(Homo sapiens)、小鼠(Mus musculus) 和斑馬魚等Wnt蛋白氨基酸序列進行比較, 發現斑點叉尾鮰Wnt基因家族成員共20種。然而, 在其他魚類, 還沒有有關Wnt家族成員cDNA序列克隆的報道, 也沒有關于這些基因mRNA組織表達的研究。
銅是包括魚類在內的所有脊椎動物必需的微量元素之一, 廣泛地參與體內的許多生化過程, 然而, 過量的銅對生物體是有毒的[13]。與其他脊椎動物不同, 魚類可以經由鰓從水中吸收銅。我們前期研究發現水體銅暴露能影響黃顙魚的卵巢發育和激素分泌[14], 然而相關機制尚不清楚。對哺乳動物的研究表明, Wnt介導的通路在卵巢發育和激素分泌過程中起著重要作用[15]。Wnt通路能通過激活βcatenin提高FSH的作用效果, 因而促進腔前卵泡的生長, 然而, 過度活化β-catenin對LH激素誘導的排卵和黃體化產生不利的影響[16]。
鑒于Wnt家族基因和蛋白對卵巢發育的重要作用, 我們假設Wnt家族成員介導了銅影響黃顙魚卵巢發育和激素分泌的調控。所以, 作為深入解析這些成員功能的第一步, 本研究首先克隆了黃顙魚Wnt家族4個基因(Wnt5a、Wnt5b、Wnt7a和Wnt9b)全長的cDNA序列, 探討了它們的組織表達模式; 在此基礎上研究了水體銅暴露對這些基因mRNA表達的影響, 為深入研究Wnt家族基因在銅影響魚類卵巢發育和激素分泌中所起的作用奠定基礎, 并為解析魚類Wnt家族基因的功能提供科學依據。
1 材料與方法
1.1 實驗魚
本實驗的黃顙魚為一齡黃顙魚, 均購自武漢市上涉湖養殖場(東經114°15′, 北緯30°8′), 分為2組。第一組黃顙魚用于Wnt家族4個基因cDNA序列的克隆和組織表達水平的測定。用于基因克隆的黃顙魚組織樣品為肝臟和卵巢組織。用于基因表達譜測定的組織包括黃顙魚的腦、脾臟、腎、鰓、心臟、肌肉、脂肪、肝臟和卵巢組織。取樣參照本實驗室的方法[17,18]。
第二組黃顙魚用于檢測水體銅暴露對Wnt家族4個基因表達水平的影響。實驗策略參照[14]。簡單說來, 216尾規格均一的健康黃顙魚[平均體重:(10.2±0.2) g, 平均值±標準誤]隨機放入9個300 L玻璃纖維缸中, 每缸24尾。分別暴露在銅濃度為0(對照)、30(低)和60(高) μg/L的水體中, 每個處理設3個重復(即3個缸), 每天換水1次。水中銅濃度通過電感耦合等離子體質譜儀(ICP-MS)測定[14], 每周測定2次, 實測值分別為(3±1)、(31±2)和(62±3) μg Cu/L (平均值±標準誤,n=16)。實驗期間, 黃顙魚每天飽食投喂商業飼料2次[飼料Cu含量: (3.1±1) mg Cu/kg, 平均值±標準誤,n=3], 每天換水1次。實驗持續8周, 在28d和56d時進行取樣, 每缸取6尾黃顙魚提RNA用于基因表達測定。
1.2 實驗藥品
RNA提取試劑盒(Trizol Reagent)、逆轉錄試劑盒、3′-Full RACE Kit試劑盒、5′-Full RACE Kit試劑盒、熒光定量試劑盒、凝膠純化回收試劑盒、Taq酶、DNA Marker(2000)、dNTP等試劑購自大連寶生物公司(TaKaRa), 胰蛋白胨和酵母粉購自Sigma公司, 無水乙醇、氯仿、異丙醇等為中國國藥分析純產品。
1.3 Wnt家族基因cDNA序列的克隆
參照本實驗室已有的方法[17,18]。簡要步驟如下: 總RNA的提取參照Invitrogen公司的Trizol說明書進行。總RNA的質量通過瓊脂糖凝膠電泳進行檢測, 其濃度及A260/A280通過Nanodrop ND2000分光光度計測定。然后, 以提取的總RNA為模板, 用TaKaRa公司的反轉錄試劑盒(PrimeScriptTMII 1st Strand cDNA Synthesis Kit)合成第一鏈cDNA。
根據GenBank及Ensembl數據庫中已報道的魚類Wnt家族基因序列, 設計簡并引物(表 1), 以擴增Wnt5a、Wnt5b、Wnt7a和Wnt9b基因cDNA核心片段。PCR反應程序如下: 94℃預變性4min; 94℃30s, 55℃ 30s, 72℃ 1min, 30個循環; 72℃延伸5min。PCR體系包括500 ng cDNA template、0.2 μmol/L primer、5 μL 10×ExTaqBuffer、2.5 mmol/LdNTP和1.25 U ExTaqpolymerease (TaKaRa, 日本)。然后分別設計3′和5′ RACE特異性引物(表 1)進行巢式PCR反應, Outer-PCR反應參數為: 94℃預變性3min; 然后94℃ 30s, 55℃ 30s, 72℃ lmin, 共25個循環; 最后72℃再延伸10min。Inner-PCR反應參數為:94℃預變性3min; 然后94℃ 30s, 55℃ 30s, 72℃1min, 共30個循環; 最后72℃終延伸10min。
1.4 序列分析
用DNAStar軟件將擴增得到的核心片段、3′和5′末端序列拼接, 從而獲得基因的cDNA全長序列。獲得的核苷酸序列經NCBI進行BLAST, 以確定該序列對應的基因亞型(http://blast.ncbi.nlm.nih.gov/)。同時, 運用DNAStar軟件找出開放閱讀框(ORF)并翻譯成氨基酸序列。序列比對和氨基酸同源性分析使用Clustal-W軟件。進化樹用MEGA 5.0軟件采用鄰接法(NJ)構建[19], 選擇的最適進化模型為JTT+G[20], 每個節點的可信值進行1000次重復計算。
1.5 基因的組織分布和表達分析
參照文獻[17, 18]采用實時熒光定量PCR (qPCR)方法檢測, 熒光定量引物見表 2。qPCR反應參數為: 95℃預變性30s; 95℃ 5s, 57℃ 30s, 72℃ 30s,共40個循環。相對表達水平采用2-ΔΔCt方法計算[21]。選用雙內參(β-actin和gapdh)進行標準化。我們的預實驗表明這2個內參組合在黃顙魚不同組織及不同銅暴露濃度下的表達水平沒有顯著差異。

表 1 Wnt5a、Wnt5b、Wnt7a和Wnt9b基因克隆的引物序列Tab. 1 Primers used for the cDNAs cloning of Wnt5a, Wnt5b,Wnt7a and Wnt9b genes
1.6 數據分析
結果采用平均值±標準誤(Mean±SEM) 進行表示。統計分析之前, 采用Kolmogorov-Smirnov檢驗所有數據的正態分布性。不同處理間方差的同質性使用Bartlett檢驗。實驗處理組之間進行單因素方差分析和Duncan’s多重比較檢驗。顯著性水平取0.05。采用SPSS 19.0軟件(SPSS, Michigan Avenue, Chicago, IL, USA) 進行數據分析處理。
2 結果
2.1 Wnt5a、Wnt5b、Wnt7a和Wnt9b序列的分子特征及進化分析
本研究通過RT-PCR和RACE方法獲取Wnt5a、Wnt5b、Wnt7a和Wnt9b基因的cDNA全長序列, 長度分別為1984、2905、2158和1622 bp。序列分析顯示,它們的cDNA序列ORF長度分別為1124、1124、1049和1073 bp, 翻譯成蛋白所得到的氨基酸數分別為375、375、350和358。黃顙魚除WNT7A以外, WNT5A、WNT5B和WNT9B氨基酸序列都有信號肽酶切位點。黃顙魚WNT5A和WNT5B都有24個保守的半胱氨酸殘基, 4個保守的天冬酰胺殘基和1個酪氨酸硫酸化位點(圖 1)。黃顙魚WNT7A蛋白有24個保守的半胱氨酸殘基(圖 2)。黃顙魚WNT9B有23個保守的半胱氨酸殘基和1個N糖基化位點(圖 3)。
多肽序列比對發現黃顙魚WNT5A、WNT5B、WNT7A和WNT9B氨基酸序列與其他魚類和哺乳類的同源性分別為78.6%—83.4%、76.3%—88.4%、85.9%—89.3%和58.9%—85.9%。
黃顙魚和其他脊椎動物WNTs氨基酸的進化樹見圖 4。在進化樹中, 所有硬骨魚WNTs獨立聚集成一簇, 而兩棲類和哺乳類WNTs聚集成另外一簇。與其他硬骨魚類相比, 黃顙魚WNT5A與墨西哥麗脂鯉(Astyanax mexicanus) 比較接近, 黃顙魚WNT9B與青鳉(Oryzias latipe) 最近。黃顙魚WNT5B與 墨西哥麗脂鯉(Astyanax mexicanus) 和斑馬魚(Danio rerio)比較接近。硬骨魚類WNT7A先與青鳉(Oryzias latipes)和斑馬魚(Danio rerio) 聚成一簇, 再與黃顙魚WNT7A共同聚成一簇。

表 2 熒光定量引物Tab. 2 Primers used for real-time PCR

圖 1 黃顙魚(Pf: Pelteobagrus fulvidraco)WNT5A和WNT5B氨基酸序列與斑馬魚(Dr: Danio rerio)、墨西哥麗脂鯉(Am: Astyanax mexicanus)和人類(Hs: Homo sapiens)比對分析Fig. 1 Alignment of P. fulvidraco (Pf: Pelteobagrus fulvidraco) WNT5A and WNT5B amino acid sequences with other species (Dr: Danio rerio; Am: Astyanax mexicanus; Hs: Homo sapiens)

圖 2 黃顙魚(Pf: Pelteobagrus fulvidraco) WNT7A氨基酸序列與斑馬魚(Dr: Danio rerio)、青鳉(Ol: Oryzias latipes)和人類(Hs: Homo sapiens)和其他硬骨魚類比對分析Fig. 2 Alignment of P. fulvidraco (Pf: Pelteobagrus fulvidraco) WNT7A amino acid sequences with other species (Dr: Danio rerio; Ol:Oryzias latipes; Hs: Homo sapiens)
2.2 Wnt5a、Wnt5b、Wnt7a和Wnt9b序列的組織表達模式
Wnt5a的mRNA在肌肉表達最高, 其次是脂肪組織, 而在其他組織(如腦、脾臟、腎臟、鰓、心臟、肝臟和卵巢)中無顯著差異(圖 5A);Wnt5b在脾臟中的表達最高, 而在其他組織中無顯著性差異(圖 5B);Wnt7a在肌肉中表達最高, 其次是腦、卵巢、脂肪和鰓, 而在其他組織中無顯著性差異(圖5C);Wnt9b在肌肉中表達最高, 而其他組織無顯著性差異(圖 5D)。
2.3 水體銅暴露對Wnt5a、Wnt5b、Wnt7a和Wnt9b基因表達水平的影響
在暴露28d時,Wnt7amRNA水平在30 μg Cu/L組最高, 其他2組差異不顯著 (圖 6A)。Wnt5a、Wnt5b和Wnt9b基因的mRNA表達各個處理組無顯著性差異。在暴露56d (圖 6B),Wnt5b在60 μg Cu/L組最低, 其他2個組差異不顯著;Wnt9bmRNA水平在30 μg Cu/L組最高, 其他2組差異不顯著。
3 討論
3.1 Wnt5a、Wnt5b、Wnt7a和Wnt9b序列的分子特征與進化分析
本研究克隆得到了黃顙魚Wnt5a、Wnt5b、Wnt7a和Wnt9b基因的cDNA全長序列。分析這4個基因的蛋白序列發現, 它們具有一些保守的結構域,如N-糖基化位點、信號肽酶切位點和保守的半胱氨酸殘基等[22—25]。本研究指出, WNT蛋白富含半胱氨酸, 這些半胱氨酸之間形成的二硫鍵對其正確折疊非常重要。N-糖基化是Wnt蛋白的一個重要修飾, 它們對Wnt的分泌和行使正常功能至關重要[26]。多肽序列比對發現, 黃顙魚WNT5A、WNT5B、WNT7A和WNT9B氨基酸序列與其他魚類和哺乳類的同源性分別為78.6%—83.4%、76.3%—88.4%、85.9%—89.3%和58.9%—85.9%, 這與在哺乳動物中的報道相近[22,23,27,28]。進化樹分析進一步發現,黃顙魚WNT5A、WNT5B、WNT7A和WNT9B多肽與其他魚類的親緣關系與物種的分類地位相符,與曹梅等[12]在斑點叉尾鮰中的研究結果相似。

圖 3 黃顙魚(Pf: Pelteobagrus fulvidraco) WNT9B氨基酸序列與斑馬魚(Dr: Danio rerio)、墨西哥麗脂鯉(Am: Astyanax mexicanus)和人類(Hs: Homo sapiens)比對分析Fig. 3 Alignment of P. fulvidraco (Pf: Pelteobagrus fulvidraco) WNT9B amino acid sequences with other species (Dr: Danio rerio; Am:Astyanax mexicanus; Hs: Homo sapiens)
3.2 Wnt5a、Wnt5b、Wnt7a和Wnt9b序列的組織表達模式
研究基因的組織分布模式有助于我們初步了解這些基因的生理功能。Wnt家族成員作為一種信號分子普遍存在于生物體各個組織中, 并參與生物體多種組織細胞的生命過程。然而, 先于我們的研究, 目前在魚類還沒有有關這些基因mRNA組織表達模式的報道。我們的研究表明這4個Wnt基因在黃顙魚各組織中均有表達, 但不同組織間的表達水平差異很大, 一方面表明Wnt家族的這4個基因在各個組織中起著廣泛的作用, 另一方面不同組織差異性的表達模式可能反映了不同組織特有的生物學作用。因此, 這種表達差異被認為是Wnt基因功能的多樣性造成的。相似地, 周春婭等[25]指出海蜇Wnt5基因在不同的發育階段均有表達, 但存在著明顯的發育表達差異。此外, 在卵巢中的表達表明這些基因可能在卵巢發育和成熟中起著重要的調控作用, 相似的結果在Sanchez等[15]的研究中得到了證實。
3.3 水體銅暴露對Wnt5a、Wnt5b、Wnt7a和Wnt9b基因表達水平的影響
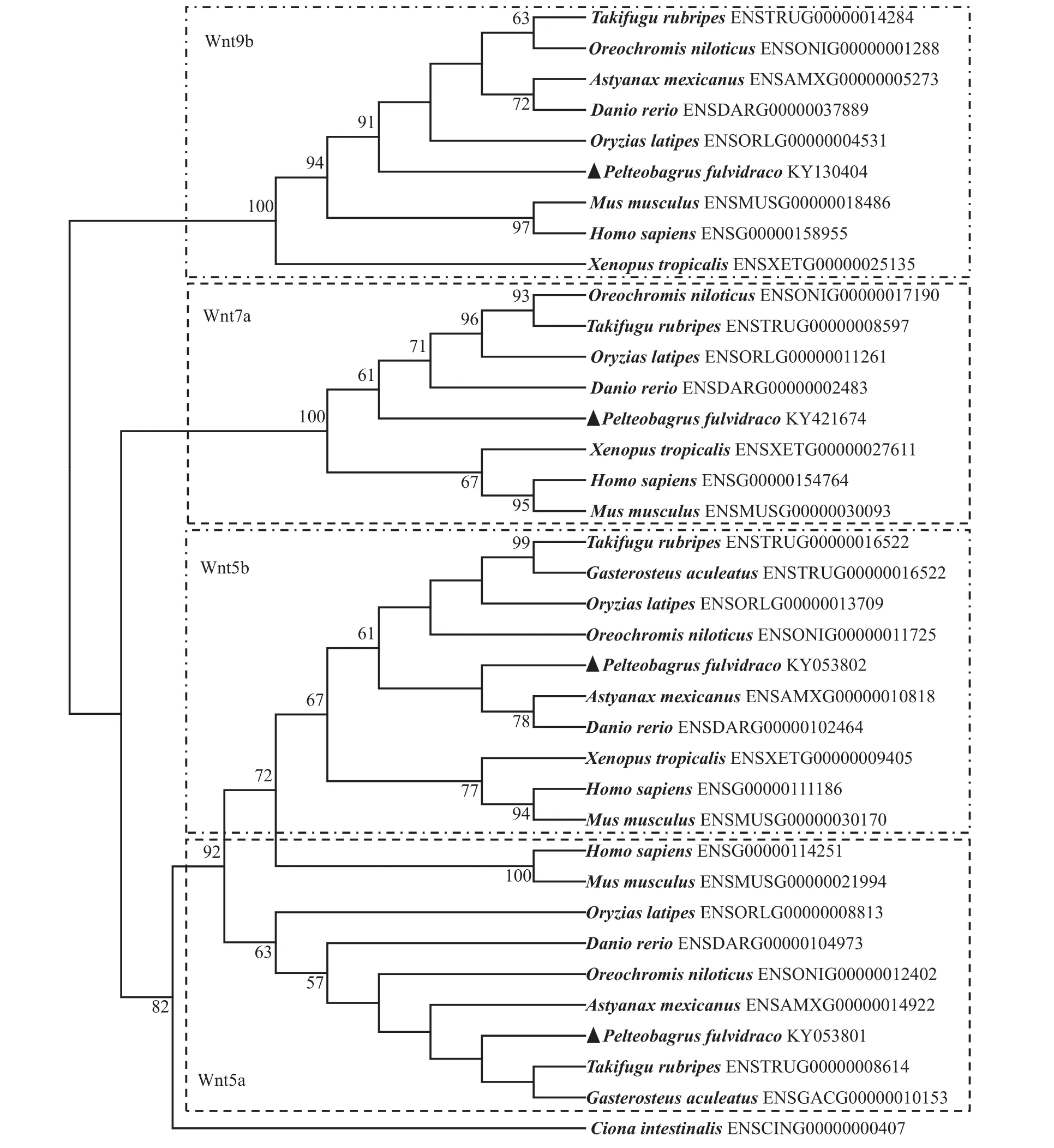
圖 4 脊索動物Wnts系統進化樹Fig. 4 Phylogenetic tree based on the protein sequences of Wnts from P. fulvidraco (▲) and other chordate species using the neighborjoining (NJ) method with 1000 bootstrap replicates
在本研究中, 我們假設銅對黃顙魚卵巢發育和激素合成的影響與Wnt通路的變化有關。然而, 無論是在陸生(包括哺乳動物)還是水生動物, 目前還沒有關于銅影響這些基因表達水平的報道; 而且,目前僅見Wnt5a在哺乳動物卵巢發育和激素分泌過程中所起生物學作用的研究, 沒有Wnt5b、Wnt7a和Wnt9b生物學功能的類似報道, 因此要進行深入的討論非常困難。我們的研究表明: 在28d時, 黃顙魚卵巢中的Wnt7amRNA水平在30μg Cu/L組最高, 其他2組差異不顯著;Wnt5a、Wnt5b和Wnt9b基因的mRNA表達各個處理組無顯著性差異。而在56d,卵巢中的Wnt5b在60 μg Cu/L組最低, 其他2個組差異不顯著;Wnt9bmRNA水平在30 μg Cu/L組最高,其他2組差異不顯著。Wnt家族成員是一類富含半胱氨酸的分泌型糖脂蛋白, 可以通過經典的Wnt/βcatenin信號通路或者非經典Wnt信號通路 (包括Wnt/Ca2+信號通路和Wnt/PCP信號通路) 調控機體的生命活動。有限的研究指出, Wnt5a是非經典Wnt信號通路的配體, 在哺乳動物雌性生殖系統發育過程中發揮了重要的作用。過表達Wnt5a能夠抑制顆粒細胞的β-catenin信號[29]。Wu等[7]在黑鯛(Acanthopagrus schlegeli)的研究表明,Wnt4基因的上調和cyp19a基因的下調伴隨著卵巢的生長, 說明Wnt信號通路參與并調控卵巢組織的生長與發育。本研究初步發現Wnt5b、Wnt7a和Wnt9b可能介導了銅影響黃顙魚卵巢發育和激素合成的變化, 因此,深入闡明Wnt5b、Wnt7a和Wnt9b在銅影響黃顙魚卵巢發育和激素合成中的作用機制, 有助于揭示銅影響黃顙魚卵巢發育和激素合成的機理, 這將為研究銅的繁殖營養和毒性效應提供一個新的思路。
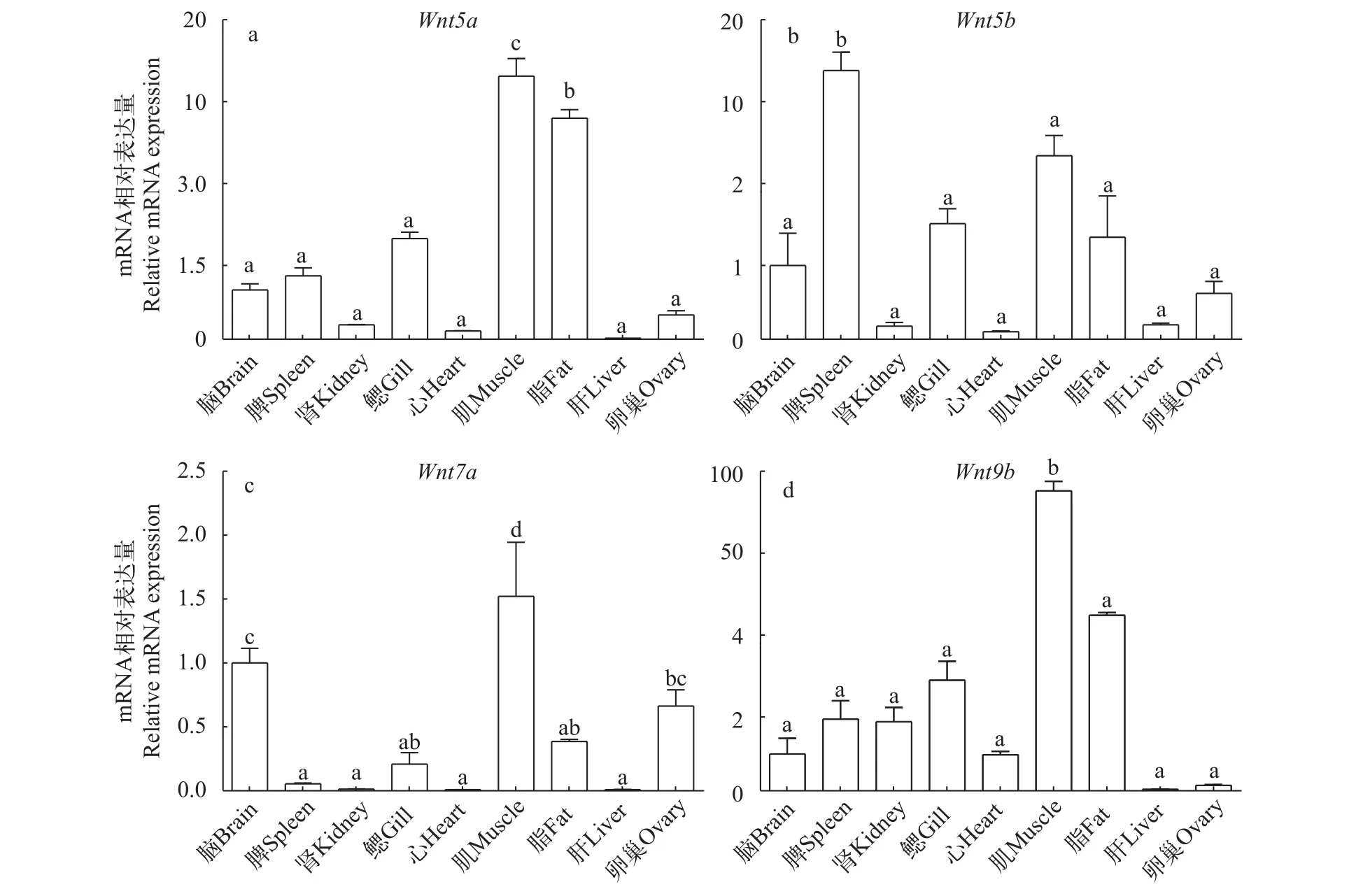
圖 5 黃顙魚Wnts組織特異性表達分析Fig. 5 The mRNA level of Wnts in the brain, spleen, kindey, gill, heart, muscle, fat, liver and ovary
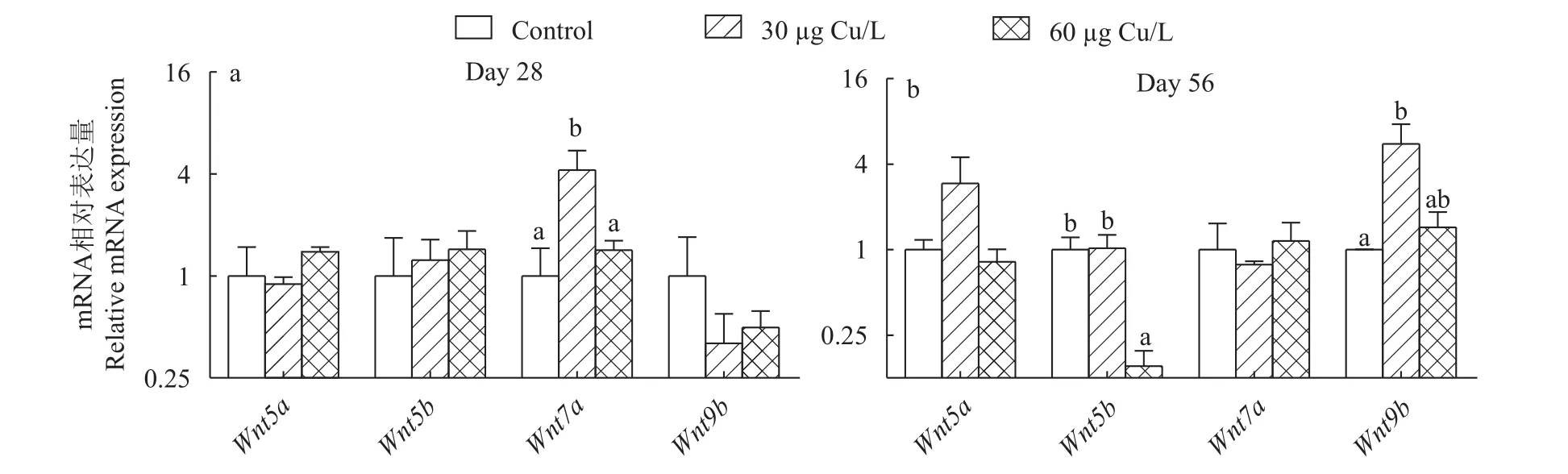
圖 6 第28天和第56天銅暴露對黃顙魚卵巢中Wnts基因(Wnt5a、Wnt5b、Wnt7a和Wnt9b)mRNA表達的影響Fig. 6 Effect of Cu exposure on the mRNA levels of genes (Wnt5a, Wnt5b, Wnt7a and Wnt9b) in the ovary of P. fulvidraco on days 28 and 56
本研究獲取了Wnt5a、Wnt5b、Wnt7a和Wnt9b基因的cDNA全長序列, 為深入解析它們的功能奠定了基礎; 這些基因在檢測的9個組織中都有表達,但表達水平相同, 表明它們會以信號分子的形式參與多種組織細胞的生命過程; 銅暴露差異性影響了Wnt家族4個基因的mRNA水平, 表明它們的基因功能發生了分化, 并可能介導了銅影響黃顙魚卵巢發育的調控。
參考文獻:
[1] Cabrera C V, Alonso M C, Johnston Pet al. Phenocopies induced with antisense RNA identify the wingless gene[J].Cell, 1987, 50(4): 659—663
[2] Huelsken J, Behrens J. The Wnt signalling pathway [J].Journal of Cell Science, 2002, 115(21): 3977—3978
[3] Logan C Y, Nusse R. The Wnt signaling pathway in development and disease [J].Annual Review of Cell and Developmental Biology, 2004, 20(1): 781—810
[4] MacDonald B T, Tamai K, He X. Wnt/β-catenin signaling: components, mechanisms, and diseases [J].Developmental Cell, 2009, 17(1): 9—26
[5] Yin D Z, Song H Y. Regulation of Wnt Signaling: Mechanisms and biological significance [J].Chinese Journal of Cell Biology, 2011, 33(2): 103—111 [尹定子, 宋海云.Wnt信號通路: 調控機理和生物學意義. 中國細胞生物學學報, 2011, 33(2): 103—111]
[6] Komiya Y, Habas R. Wnt signal transduction pathways[J].Organogenesis, 2008, 4(2): 68—75
[7] Wu G C, Chang C F. Wnt4 is associated with the development of ovarian tissue in the protandrous black Porgy,Acanthopagrus schlegeli[J].Biology of Reproduction,2009, 81(6): 1073—1082
[8] Boerboom D, Paquet M, Hsieh Met al. Misregulated Wnt/β-catenin signaling leads to ovarian granulosa cell tumor development [J].Cancer Research, 2005, 65(20):9206—9215
[9] Hua F, Sun W B, Gei J Y. Molecular cloning of Shh,Wnt5b and Catnb specific gene fragments from zebrafish embryos [J].Journal of Oral Science Research, 2009,25(2): 129—131 [華芳, 孫衛斌, 葛久禹. 斑馬魚Shh,Wnt5b和Catnb特異性基因片段的克隆. 口腔醫學研究,2009, 25(2): 129—131]
[10] Liu A, Majumdar A, Schauerte H E,et al. Zebrafish wnt4b expression in the floor plate is altered in sonic hedgehog and gli-2 mutants [J].Mechanisms of Development, 2000, 91(1): 409—413
[11] Li J Z, Liu Q, Wang D S,et al. Molecular cloning and identification of twoWNT4genes from the medaka(Oryzias latipes) [J].Acta Hydrobiologica Sinica, 2012,36(5): 983—986 [李建中, 劉瓊, 王德壽等. 日本青鳉2種WNT4基因的克隆及鑒定. 水生生物學報, 2012, 36(5):983—986]
[12] Cao M, Wang X, Cui C,et al. Sequence analysis ofWntgene family from catfish [J].Journal of Huaihai Insititute of Technology(Natural Science Edition), 2017, 26(1):76—81 [曹梅, 王興強, 崔春輝, 等. 鯰魚Wnt基因家族序列分析. 淮海工學院學報(自然科學版), 2017, 26(1):76—81]
[13] Watanabe T, Kiron V, Satoh S. Trace minerals in fish nutrition [J].Aquaculture, 1997, 151(1): 185—207
[14] Zhang L H, Luo Z, Song Y Fet al. Effects and mechanisms of waterborne copper exposure influencing ovary development and related hormones secretion in yellow catfishPelteobagrus fulvidraco[J].Aquatic Toxicology,2016, 178: 88—98
[15] Sanchez A M, Viganò P, Quattrone F,et al. The WNT/βcatenin signaling pathway and expression of survival promoting genes in luteinized granulosa cells: endometriosis as a paradigm for a dysregulated apoptosis pathway [J].Fertility and Sterility, 2014, 101(6): 1688—1696
[16] Fan H Y, O’Connor A, Shitanaka M,et al. Beta-catenin(CTNNB1) promotes preovulatory follicular development but represses LH-mediate ovulation and luteinization [J].Molecular Endocrinology, 2010, 24(8):1529—1542
[17] Wu K, Zheng J L, Luo Z,et al. Carnitine palmitoyltransferases I gene inSynechogobius hasta: cloning, mRNA expression and transcriptional regulation by insulin in vitro [J].Gene, 2016, 576(1): 429—440
[18] Wei C C, Luo Z, Song Y F,et al. Identification of autophagy related genes LC3 and ATG4 from yellow catfishPelteobagrus fulvidracoand their transcriptional responses to waterborne and dietborne zinc exposure [J].Chemosphere, 2017, 175: 228—238
[19] Tamura K, Peterson D, Peterson Net al. MEGA5: molecular evolutionary genetics analysis using maximum likelihood, evolutionary distance, and maximum parsimony methods [J].Molecular Biology and Evolution,2011, 28(10): 2731—2739
[20] Jones D T, Taylor W R, Thornton J M. The rapid generation of mutation data matrices from protein sequences [J].Computer Applications in the Biosciences: CABIOS,1992, 8(3): 275—282
[21] Livak K J, Schmittgen T D. Analysis of relative gene expression data using real-time quantitative PCR and the 2–ΔΔCTmethod [J].Methods, 2001, 25(4): 402—408
[22] Clark C C, Cohen I, Eichstetter Iet al. Molecular cloning of the human proto-oncogene Wnt-5A and mapping of the gene (WNT5A) to chromosome 3p14-p21 [J].Genomics,1993, 18(2): 249—260
[23] Qian J, Jiang Z, Li Met al. Mouse Wnt9b transforming activity, tissue-specific expression, and evolution [J].Genomics, 2003, 81(1): 34—46
[24] Fradkin L G, van Schie M, Wouda R Ret al. The Drosophila Wnt5 protein mediates selective axon fasciculation in the embryonic central nervous system [J].Developmental Biology, 2004, 272(2): 362—375
[25] Zhou C Y, Zhu L, Pan Y,et al.Wnt5 gene fromRhopilema Esculentum: cDNA cloning, genomic organization and mRNA expression [J].Oceanologia Et Limnologia Sinica, 2013, 44(4): 1115—1122 [周春婭, 朱玲, 潘瀅, 等. 海蜇(Rhopilema esculentum)Wnt5基因: cDNA克隆、基因組結構與表達. 海洋與湖沼, 2013, 44(4): 1115—1122]
[26]Mason J O, Kitajewski J, Varmus H E. Mutational analysis of mouse Wnt-1 identifies two temperature-sensitive alleles and attributes of Wnt-1 protein essential for transformation of a mammary cell line [J].Molecular Biology of the Cell, 1992, 3(5): 521—533
[27] Lejeune S, Huguet E L, Hamby A,et al. WNT5A cloning,expression and upregulation in human primary breast cancers [J].Clinical Cancer Research, 1995, 1(2): 215—222
[28] Bui T D, Lako M, Lejeune Set al. Isolation of a fulllength WNT7A gene implicated in limb development and cell transformation, and mapping to chromosome 3p25[J].Gene, 1997, 189(1): 25—29
[29] Topol L, Jiang X, Choi Het al. Wnt-5a inhibits the canonical WNT pathway by promoting GSK-3-independent beta-catenin degradation [J].The Journal of Cell Biology,2003, 162(5): 899—908

