市售蒲公英片HPLC特征圖譜建立及其單咖啡酰酒石酸、菊苣酸含量測定
,3 ,3 ,3 ,5*
1.云南省昆蟲生物醫藥研發重點實驗室,云南 大理 671000;2.藥用特種昆蟲開發國家地方聯合工程研究中心,云南 大理 671000;3.中國西南藥用昆蟲及蛛形類資源開發利用協同創新中心,云南 大理 671000;4.四川好醫生藥業集團,四川 成都 610000;5.云南民族大學南亞東南亞輻射研究中心,云南 昆明 650504
蒲公英又名婆婆丁、黃花地丁、黃花三七等,為菊科植物蒲公英TaraxacummongolicumHand.-Mazz、堿地蒲公英TaraxacumborealisinenseKitag.或同屬數種植物的干燥全草。蒲公英中含有黃酮類、酚酸類、萜類、色素類植物甾醇類等化合物[1],具有抗炎、抑菌、保肝、抗腫瘤、抗氧化、降糖等作用[2-5],常用于治療疔瘡腫毒、乳癰、目赤、肺癰、腸癰、濕熱黃疸和熱淋澀痛等癥[6]。蒲公英片是以蒲公英水提醇沉干浸膏制得,具有清熱解毒的功效,主要用于咽喉腫痛(急性扁桃體炎)、瘡癤[1],收載于部頒標準中藥成方制劑第三冊,但該標準中未對蒲公英片做相關的含測要求,對該品種的質量控制缺乏全面性和客觀性[7]。中藥特征圖譜可以通過系統性、整體性和特征性等特點評價蒲公英中所含化學成分的種類及數量,對于蒲公英片的質量控制具有重要意義[8]。近年來,有部分關于蒲公英藥材的特征圖譜研究相繼報道,分別以其藥材中綠原酸、咖啡酰、阿魏酸、蘆丁、木犀草素等常見酚酸類化學成分進行特征圖譜指認[9-10],但是尚未建立蒲公英片主要特征峰的HPLC特征圖譜及含量測定方法。
筆者對市售7個廠家的蒲公英片展開特征圖譜研究,采用“中藥特征圖譜相似度評價系統”(2012版)對其進行相似度評價,并首次確認蒲公英片特征圖譜中的特征峰單咖啡酰酒石酸和菊苣酸,對其進行含量測定,為蒲公英片的質量控制提供參考,同時為后續藥理活性研究提供參考依據。
1 儀器與材料
1.1 儀器 BSA124S分析天平(賽多利斯科學儀器有限公司);AKSW-V-16艾柯實驗室超純水機(成都艾柯水處理設備有限公司);Agilent 1260型高效液相色譜系統(美國Agilent 公司);Sepax Gp-C18色譜柱(4.6×250mm,5μm,美國賽分); 已腈、三氟乙酸為色譜純,水為超純水,其他試劑均為分析純。
1.2 材料 對照品菊苣酸(批號:20140704,99.3%,中國計量科學研究院);單咖啡酰酒石酸(批號:PRF8052505,純度>98%,成都柯瑞法科技開發有限公司)。市售7個廠家的蒲公英片,均執行部頒標準中藥成方制劑第三冊WS3-B-0648-91,標示量均為每片含干浸膏0.3克,分別產自河南A廠(批號:1607023)、河南B廠(批號:160509)、河南C廠(批號:160301)、河南D廠(批號:160305)、廣西E廠(批號:150420)、山西F廠(批號:20151002)、吉林G廠(批號:04160303)。
2 方法與結果
2.1 單咖啡酰酒石酸與菊苣酸含量測定
2.1.1 混合對照品溶液的制備 精密稱取單咖啡酰酒石酸5.1 mg、菊苣酸5.0 mg于25 mL棕色量瓶中,加入超純水定容至刻度,搖勻,即得204 μg/mL的單咖啡酰酒石酸和200 μg/mL菊苣酸的對照品溶液,分別取混標溶液0.5、1、2、4、6、8、10 mL于10 mL量瓶中,加入超純水定容致刻度線,搖勻,既得系列標準品溶液。
2.1.2 供試品溶液的配制 取各廠家蒲公英片20片,去除包衣后研碎,精密稱取該粉末400.0 mg于具塞錐形瓶中,精密加入70 %乙醇10 mL,稱重,超聲處理(功率300 W,頻率54 Hz)30 min,放冷,稱重,用70%乙醇補足差重,搖勻,過濾,取續濾液1.0 mL過0.22 μm微孔濾膜,即得濃度為40 mg/mL供試品溶液。
2.1.3 色譜條件 色譜柱:Sepax Gp-C18(4.6×250 mm,5μm);流速1.0 mL/min;檢測波長:323 nm;柱溫:40 ℃;進樣量:10 μL;流動相A為0.1%三氟乙酸-乙腈,流動相B為0.1%三氟乙酸-水,洗脫梯度:0~13 min,11%A 等梯度洗脫;14~22 min,17%A等度洗脫;22~29 min,17%~27%A梯度洗脫;29~43 min,27%~34%A梯度洗脫;43~50 min,34%~95%A梯度洗脫。理論塔板數按菊苣酸峰計算應不低于4000。取混合對照品溶液、空白溶液及供試品溶液進樣檢測,結果表明,供試品及混合標準品中各峰分離度及對稱性良好,色譜圖如圖1所示。
2.1.4 線性關系試驗 取系列標準品溶液10 μL進樣,測定其峰面積。以峰面積為縱坐標,對照品濃度為橫坐標(μg),繪制標準曲線,計算單咖啡酰酒石酸和菊苣酸的線性回歸方程及相關系數見表1。

表1 單咖啡酰酒石酸、菊苣酸的回歸方程、相關系數及線性范圍

待測成分回歸方程r線性范圍/μg單咖啡酰酒石酸Y=2857 3X-27 210 999910 2~204 0菊苣酸Y=2899 2X-29 170 999910 00~200 0
2.1.5 精密度試驗 取混合對照品溶液,進樣10 μL,連續進樣6次,記錄峰面積。結果顯示單咖啡酰酒石酸和菊苣酸的峰面積的RSD分別為1.09%、1.44%,表明精密度良好。
2.1.6 重復性試驗 取山西F廠(批號:20151002)蒲公英片,各精密稱量6份,按2.1.2項下配制供試品溶液,分別進樣10 μL,記錄峰面積并代入表1標準方程計算樣品中單咖啡酰酒石酸和菊苣酸的含量(μg/mg)。結果顯示單咖啡酰酒石酸和菊苣酸的平均含量分別為1.43 μg/mg、1.29 μg/mg,RSD值分別為0.99%、1.09%,表明重復性良好。
2.1.7 穩定性試驗 取山西F廠(批號:20151002)蒲公英片供試品溶液,分別于室溫下放置0、4、8、12、16、20、24 h進行進樣分析,記錄峰面積。結果顯示24 h內單咖啡酰酒石酸峰面積的RSD為0.67%;菊苣酸峰12h內的面積的RSD為0.61%,即供試品溶液在室溫條件下12 h內穩定。
2.1.8 加樣回收試驗 取山西F廠(批號:20151002)蒲公英片,各精密稱量6份,精密加入對照品溶液,按2.1.2項下配制供試品溶液,測定單咖啡酰酒石酸和菊苣酸的含量,計算回收率,結果見表2。
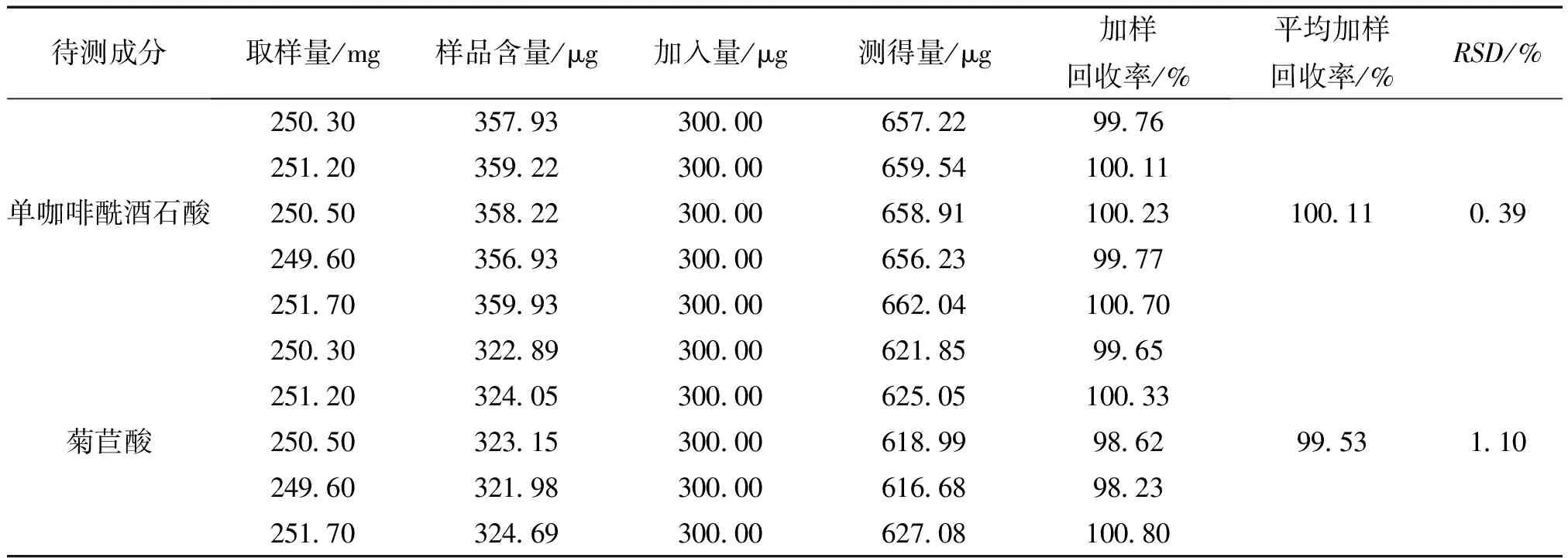
表2 蒲公英片中單咖啡酰酒石酸、菊苣酸的加樣回收實驗 (n=6)
2.1.9 供試品測定 取7個廠家的蒲公英片,按“2.1.2”項下方法配置供試品溶液,精密吸取各供試品溶液10 μL,按“2.1.3”項下色譜條件記錄單咖啡酰酒石酸和菊苣酸的峰面積,并計算其含量,見表3。

表3 不同廠家蒲公英片中單咖啡酰酒石酸和菊苣酸的含量測定 (mg/g)
2.2 特征圖譜的測定與相似度分析
2.2.1 色譜條件 色譜柱:Sepax Gp-C18(4.6×250mm,5μm);流速:1.0 mL/min;檢測波長:323 nm;柱溫:40 ℃;流動相A為0.1%三氟乙酸-乙腈,流動相B為0.1%三氟乙酸-水,洗脫梯度:0~13 min,11%A 等梯度洗脫;14~22 min,17%A等度洗脫;22~29 min,17%~27%A梯度洗脫;29~43 min,27%~34%A梯度洗脫;43~50 min,34%~95%A梯度洗脫。
2.2.2 精密度實驗 取山西F廠(批號:20151002)蒲公英片,各精密稱量1份,按“2.1.2”項下配制供試品溶液,平行測定6次,以單咖啡酰酒石酸峰和菊苣酸峰為參照峰,計算其余各特征峰的相對保留時間和相對峰面積。結果各特征峰相對峰面積和相對保留時間無明顯變化,RSD<2%,符合HPLC特征圖譜檢驗要求,表明儀器精密度良好。
2.2.3 穩定性實驗 取山西F廠(批號:20151002)蒲公英片供試品溶液,分別于室溫下放置0、4、8、12、16、20、24 h進行進樣分析,記錄峰面積。以單咖啡酰酒石酸峰和菊苣酸峰為參照峰,計算其余各特征峰的相對保留時間和相對峰面積。結果各特征峰相對峰面積和相對保留時間在12 h內無明顯變化,RSD<2%,表明供試品溶液在室溫條件下12 h內穩定。
2.2.4 重復性實驗 取山西F廠(批號:20151002)蒲公英片,各精密稱量6份,按“2.1.2”項下配制供試品溶液,平行測定,以單咖啡酰酒石酸峰和菊苣酸峰為參照峰,計算其余各特征峰的相對保留時間和相對峰面積。結果各特征峰相對峰面積和相對保留時間無明顯變化,RSD<2%,符合HPLC特征圖譜檢驗要求,表明重復性良好。
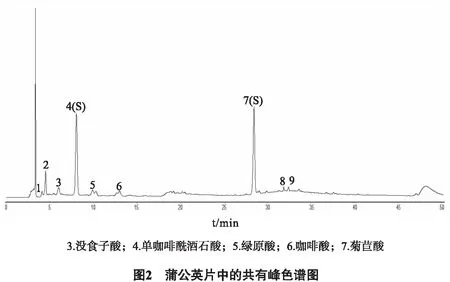
2.2.5 蒲公英片特征圖譜測定 按“2.1.3”項色譜條件對7個廠家生產的蒲公英片進行測定,記錄色譜圖,見圖2。采用“中藥特征圖譜相似度評價系統(2012版)”軟件得出色譜峰1~9為7個不同廠家蒲公英片的共有峰,依次確認色譜峰1~9為蒲公英片的特征峰,并且在相同HPLC條件下,3、4、5、6、7的保留時間分別與沒食子酸、單咖啡酰酒石酸、綠原酸、咖啡酸、菊苣酸對照品的保留時間一致,其中單咖啡酰酒石酸和菊苣酸分離度較好,且含量較高、穩定,故選擇單咖啡酰酒石酸和菊苣酸為參照峰(S)。
2.2.6 特征圖譜的相關性分析 將“2.2.1”項下所得色譜數據導入“中藥特征圖譜相似度評價系統(2012版)”軟件,采用多點校正將譜峰自動匹配,平均數法設置參照圖譜,峰匹配模式得出樣品特征譜圖的共有峰,并計算相似度,結果見圖3和表4。由表4可見,7個廠家生產的蒲公英片中,除河南D廠樣品相似度為0.831外,其余樣品相似度均>0.90,差異不明顯,并且1~9色譜峰在7個廠家生產的蒲公英片中均能全部檢出,表明各廠家生產的蒲公英片成分相關性良好,該色譜條件建立的蒲公英片的特征圖譜指標穩定。
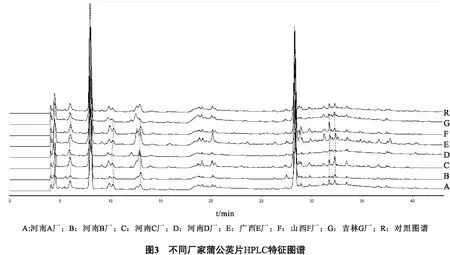

表4 蒲公英片特征圖譜的相似度評價結果
3 討論
3.1 單咖啡酰酒石酸和菊苣酸作為指標峰用于蒲公英片的特征圖譜 在蒲公英原料藥材及其制劑的相關報道檢索中少見有對單咖啡酰酒石酸和菊苣酸的報道[11],實驗發現在蒲公英片中,單咖啡酰酒石酸和菊苣酸有較高的含量、特征性良好,故選取單咖啡酰酒石酸和菊苣酸作為蒲公英片的含測指標及蒲公英片特征圖譜的指標峰。結果表明,蒲公英片在0.1%的TFA乙腈和0.1%TFA水作為流動相時具有較好的分離效果,能夠保證樣品良好的分離度和出峰數。特征圖譜研究中發現,蒲公英片中富含酚酸類物質,其中沒食子酸、單咖啡酰酒石酸、綠原酸、咖啡酸、菊苣酸的含量較高,且均為咖啡酸類衍生物,故選取咖啡酸的特征吸收波長323 nm作為檢測波長,且在該波長下各峰分離度良好,特征性強,峰數目較多。
3.2 市售7個廠家蒲公英片的特征圖譜比較分析 對比分析7個廠家的蒲公英片發現,除河南D廠外,其余6個廠家的蒲公英片具有較高的相似度。通過“中藥特征圖譜相似度評價系統(2012版)”軟件進行峰匹配發現7個廠家生產的蒲公英片中均含有沒食子酸、單咖啡酰酒石酸、綠原酸、咖啡酸、菊苣酸,且單咖啡酰酒石酸和菊苣酸含量較高,特征性明顯,特征指紋峰的相對保留時間一致,表明該方法用于蒲公英片的特征圖譜具有較高的穩定性。河南D廠相似度相對較低可能是原料藥材的選取、原料藥材的質量控制或原料藥材的采收季節、產地、儲存方式等方面的原因,但缺乏實驗論證。
3.3 單咖啡酰酒石酸和菊苣酸的含量比較 《中國藥典》2015版僅在蒲地藍消炎口服液中有測定蒲公英中菊苣酸含量的記載,尚無單咖啡酰酒石酸的相關指標考察[7]。研究表明,蒲公英中的單咖啡酰酒石酸和菊苣酸具有增強免疫、抗炎、抗氧化等作用[11]。測定蒲公英片中單咖啡酰酒石酸和菊苣酸含量發現,河南D廠生產的片劑中單咖啡酰酒石酸和菊苣酸含量分別為0.39 mg/g和0.12 mg/g,其余6個廠家的蒲公英片中單咖啡酰酒石酸和菊苣酸含量均高于1.00 mg/g和0.80 mg/g,這可能也是導致河南D廠與其余6廠相似度差別較大的原因之一。單咖啡酰酒石酸和菊苣酸在蒲公英片中有較高的含量和明顯的HPLC特征圖譜,因此,可將單咖啡酰酒石酸和菊苣酸作為蒲公英及其相關制劑的質量控制指標之一,但是單咖啡酰酒石酸和菊苣酸的含量與蒲公英片的療效之間的關系尚需藥理實驗加以證實。
參考文獻
[1]李超,董自波,蔣金來,等. HPLC法測定蒲公英中菊苣酸,咖啡酸與綠原酸[J].中草藥, 2015, 46(23): 3577-3580.
[2] 肖潮勇,張宇,王宇亮.蒲公英總多糖的提取,純化及其體外抗炎活性分析[J].中國實驗方劑學雜志, 2016, 22(11): 25-28.
[3] 任麗平, 杜鋼軍, 崔新萍. 蒲公英對酒精性肝損傷的影響[J]. 中國實驗方劑學雜志, 2011, 17(11): 179-181.
[4] 劉磊磊, 陳娟, 師彥平. 清熱解毒中藥抗腫瘤作用研究進展[J]. 中草藥, 2012, 43(6): 1203-1212.
[5] 李雪石, 張彥文. 蒲公英水提取物對鏈脲佐菌素致糖尿病大鼠的降血糖作用及其機制[J]. 中草藥, 2013, 44(7): 863-868.
[6] 張詠梅,張淑慧,王朝卿,等.不同產地蒲公英中總黃酮的測定[J]. 中草藥, 2009, 40(2): 169-170
[7] 國家藥典委員會.中華人民共和國藥典(一部)[M].北京:中國醫藥科技出版社,2015.
[8] 田宇柔,甄亞欽,王鑫國,等.半枝蓮配方顆粒HPLC指紋圖譜及含量測定方法研究[J].中國藥學雜志, 2016, 51(20):1795-1799.
[9]李喜鳳,孟璐,陳隨清.蒲公英藥材高效液相色譜特征圖譜研究[J].中國醫院藥學雜志,2010(8):643- 645.
[10]蘇英,彭章明,劉燕,等.宜賓地區蒲公英藥材HPLC特征圖譜定性研究[J].中國藥學雜志, 2009 (24): 1858-1861.
[11] 占遠,黎田兒,黃文平,等. HPLC法同時測定二丁顆粒中的單咖啡酰基酒石酸,秦皮乙素和菊苣酸[J]. 中成藥, 2015,37(10):2190-2193.

