物質結構與性質的命題特點及應對策略
■鄭州外國語學校 包 軍
物質結構與性質屬于選考內容,占15分左右。試題從考查內容可分為三部分:一是原子結構與性質,二是分子結構與性質,三是晶體結構與性質。該部分內容較好體現化學學科核心素養之一且為第一條的“宏觀辨識與微觀探析”。下面談一下它的命題特點及應對策略。
一、命題特點
(1)從問題設置的數量看一般在10個空左右。
(2)從問題考查內容看,不回避高頻考點,如基態原子的核外電子排布(價電子排布式)、軌道表達式、共價鍵類型、中心原子雜化方式、分子的空間構型、分子的物理性質的判斷及解釋、晶胞的有關計算等幾乎年年考查。
(3)從區分度的角度看,高考題也會通過考查絕大多數考生在某一知識點上的短處,達到為高水平大學選拔優秀學生的目的,部分試題的難度遠遠超出高中課本的內容,這點在2013年之后的高考試題中皆有體現。
(4)取材來自全球科技發展中的重要化學材料,如熱點石墨烯、半導體材料砷化鎵、鈦合金、鋰材料等,尤其是中國科學家近幾年在科技領域中取得的具有較強影響力的成果也會作為命題素材,以凸顯中國優秀文化的強大,從而達到立德樹人的目的。比如2017年新課標Ⅱ第35題“我國科學家最近成功合成了世界上首個五氮陰離子鹽(N5)6(H3O)3(NH4)4Cl(用 R 代表)”,這個材料選自2017年1月27日南京理工大學胡炳成團隊的科研成果,題中的圖片和發表的文章中的幾乎一模一樣。
(5)從失分點來看,依然是利用原理解釋物質結構與性質,有關晶胞的識別和計算。
二、備考應對策略
(1)理解物質結構與性質內容中的每一個概念。
(2)全覆蓋仔細閱讀課本,對知識不遺漏。
(3)對高頻考點進行重點訓練。
(4)精心訓練近五年全國各省份的高考真題,并進行總結。
三、高頻考點
1.原子結構與性質中的高頻考點。
原子核外電子的排布原理及能級分布,能用電子排布式或電子排布圖表示常見元素(1~36號)原子核外電子、價電子的排布,原子核外電子的運動狀態。
例1(1)基態K原子中,核外電子占據最高能層的符號是____,占據該能層電子的電子云輪廓圖形狀為____。K和Cr屬于同一周期,且核外最外層電子構型相同,但金屬K的熔點、沸點等都比金屬Cr的低,原因是____。
(2)我國科學家最近成功合成了世界上首個五氮陰離子鹽(N5)6(H3O)3(NH4)4Cl(用R代表)。回答下列問題:氮原子價層電子對的軌道表達式(電子排布圖)為____。
(3)研究發現,在CO2低壓合成甲醇反應(CO2+3H2→CH3OH+H2O)中,CO氧化物負載的Mn氧化物納米粒子催化劑具有高活性,顯示出良好的應用前景。回答下列問題:CO基態原子核外電子排布式為____。元素Mn與O中,第一電離能較大的是____,基態原子核外未成對電子數較多的是____。
(4)東晉《華陽國志·南中志》卷四中已有關于白銅的記載,云南鎳白銅(銅鎳合金)聞名中外,曾主要用于造幣,亦可用于制作仿銀飾品。鎳元素基態原子的電子排布式為____,3d能級上的未成對的電子數為____。
(5)Cu+基態核外電子排布式為____。
答案:(1)N 球形 K的原子半徑較大,且價電子較少,金屬鍵較弱
(2)
(3)1s22s22p63s23p63d74s2或[Ar]3d74s2OMn
(4)1s22s22p63s23p63d84s2或[Ar]3d84s22
(5)1s22s22p63s23p63d10
2.元素的性質與電負性、電離能的關系,并能用以說明元素的某些性質。
例2(1)光催化還原CO2制備CH4反應中,帶狀納米Zn2GeO4是該反應的良好催化劑。Zn、Ge、O電負性由大至小的順序是____。
(2)單質銅及鎳都是由____鍵形成的晶體。元素銅與鎳的第二電離能分別為:ICu=1959kJ·Mol-1,INi=1753kJ·mol-1,ICu>INi的原因是____。
(3)砷化鎵(GaAs)是優良的半導體材料,可用于制作微型激光器或太陽能電池的材料等。回答下列問題:根據元素周期律,原子半徑Ga____As,第一電離能Ga____As。(填“大于”或“小于”)
(4)A、B、C、D為原子序數依次增大的四種元索,A2-和B+具有相同的電子構型;C、D為同周期元索,C核外電子總數是最外層電子數的3倍;D元素最外層有一個未成對電子。回答下列問題:四種元素中電負性最大的是____(填元素符號),其中C原子的核外電子排布式為____。
(5)科學家正在研究溫室氣體CH4和CO2的轉化和利用。CH4和CO2所含的三種元素電負性從小到大的順序為____。
答案:(1)O>Ge>Zn(2)金屬銅失去的是全充滿的3d10電子,鎳失去的是4s1電子 (3)大于 小于 (4)O1s22s22p63s23p3(或[Ne]3s23p3) (5)H、C、O
3.化學鍵與物質的性質。
理解離子鍵的形成、共價鍵的形成、配位鍵的形成、金屬鍵的形成,能用化學鍵理論解釋晶體的一些物理性質、雜化軌道理論及常見的雜化軌道類型(sp、sp2、sp3),能用價層電子對互斥理論或者雜化軌道理論推測常見的簡單分子或者離子的空間結構。
例3(1)用X射線衍射測定發現,I3AsF6中存在I3+離子,I3+離子的幾何構型為
____,中心原子的雜化形式為____。
(2)我國科學家最近成功合成了世界上首個五氮陰離子鹽(N5)6(H3O)3(NH4)4Cl(用R代表)。經X射線衍射測得化合物R的晶體結構,其局部結構如圖1所示。
①從結構角度分析,R中兩種陽離子的相同之處為____,不同之處為____。(填標號)
A.中心原子的雜化軌道類型
B.中心原子的價層電子對數
C.立體結構
D.共價鍵類型
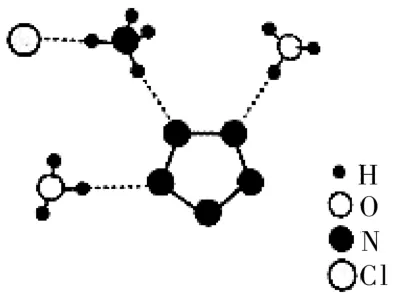
圖1
②R中陰離子中的σ鍵總數為個。分子中的大π鍵可用符號表示,其中m代表參與形成的大π鍵原子數,n代表參與形成的大π鍵電子數(如苯分子中的大π鍵可表示為),則中的大π鍵應表示為____。
③圖1中虛線代表氫鍵,其表示式為(NH4+)N—H…Cl____、 、____。
(3)硝酸錳是制備上述反應催化劑的原料,Mn(NO3)2中的化學鍵除了σ鍵外,還存在____。
(4)HOCH2CN的結構簡式為。
[Zn(CN)4]2-在水溶液中與HCHO發生如下反應:
4HCHO+[Zn(CN)4]2-+4H++4H2O══[Zn(H2O)4]2++4HOCH2CN
①1molHCHO分子中含有σ鍵的數目為____mol。
②HOCH2CN分子中碳原子軌道的雜化類型是____。
③與H2O分子互為等電子體的陰離子為____。
④[Zn(CN)4]2-中Zn2+與CN-的C原子形成配位鍵。不考慮空間構型,[Zn(CN)4]2-的結構可用示意圖表示為____。
解析:(1)I3+的中心原子為I,有2對σ鍵電子對(m=2);中心原子上的孤電子對數==2(n=2)。由價層電子對互斥理論,價層電子總對數為2+2=4,中心I原子為sp3雜化,由于孤電子對數為2,分子的空間構型為V形。
(2)①有4個H的陽離子為NH4+,有3個H的陽離子為H3O+。NH4+中心原子N含有4個σ鍵,其中一個是配位鍵,孤電子對數為(5-1-4×1)=0,價層電子對數為4,雜化類型為sp3,空間構型為正四面體;H3O+中心原子是O,含有3σ鍵,其中一個是配位鍵,孤電子對數為=1,價層電子對數為4,為sp3雜化,空間構型為三角錐形。
②方法1:根據圖1可知,N5-中的σ鍵總數為5個,根據信息,N5-有6個電子可形成大π鍵,可用符號Π65表示。
方法2:也可以類比苯分子形成Π66的方法分析,先研究N5,每個N原子進行了sp2雜化,3個未成對電子中2個形成了σ鍵,每個N原子都剩余1個未成對電子,5個N原子共用5個電子形成Π55,N5-可以看作N5得到一個電子形成N5-,所以5個N原子共用了6個電子。
③O、N的非金屬性較強,對應的O—H、N—H都可與H形成氫鍵,還可表示為(H3O+)O—H…N、(NH4+)N—H…N。
(3)硝酸錳是離子化合物,硝酸根和錳離子之間形成離子鍵,硝酸根中N原子與3個O原子形成3個σ鍵,硝酸根中有一個氮氧雙鍵,所以還存在π鍵。
(4)①甲醛的結構式是,由于單鍵都是σ鍵,雙鍵中有一個σ鍵和一個π鍵,因此在一個甲醛分子中含有3個σ鍵和1個π鍵,所以在1molHCHO分子中含有σ鍵的數目為3mol。
②根據HOCH2CN的結構簡式可知在HOCH2CN分子中,連有羥基—OH的碳原子形成4個單鍵,因此雜化類型是sp3雜化,含有—CN的碳原子與N原子形成三鍵,則其軌道的雜化軌道類型是sp雜化。
③原子數和價電子數分別都相等的是等電子體,H2O含有10個電子,則與H2O分子互為等電子體的陰離子為NH2-。
④在[Zn(CN)4]2-中Zn2+與CN-的N原子形成配位鍵,N原子提供一對孤對電子,Zn2+的空軌道接受電子對,因此若不考慮空間構型,[Zn(CN)4]2-的結構可用示意圖表示為
答案:(1)V形 sp3(2)①ABDC②5Π65③(H3O+)O—H…N (NH+4)N—H…N(3)π鍵、離子鍵(4)①3②sp③NH-2④
4.分子晶體、原子晶體、離子晶體、金屬晶體的結構微粒、微粒間作用力的區別;根據晶胞確定晶體的組成并進行相關的計算;晶格能的概念及其對離子晶體性質的影響。
例4KIOO3晶體是一種性能良好的非線性光學材料,具有鈣鈦礦型的立方結構,邊長為a=0.446nm,晶胞中K、I、O分別處于頂角、體心、面心位置,如圖2所示。
(1)K與O之間的最短距離為____nm。
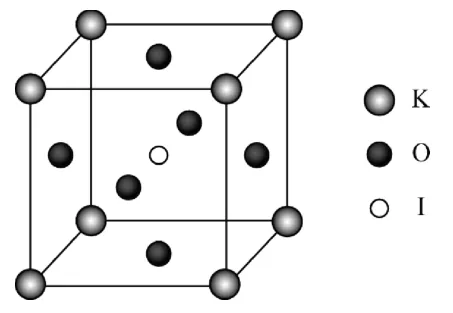
圖2
(2)與K緊鄰的O的個數為____。
(3)在KIOO3晶胞結構的另一種表示中,I處于各頂角位置,則K處于____位置,O處于____位置。
解析:(1)最近的K和O是晶胞中頂點的K和面心的O,其距離為邊長的倍。故最短距離為0.446nm×=0.315nm。
(2)從晶胞中可以看出,在一個晶胞中與頂點K緊鄰的O為含有該頂點的三個面面心的O,即為3×個。由于一個頂點的K被8個晶胞共用,故與一個K緊鄰的O有3××8=12(個)。
(3)KIO3晶體以K、I、O分別處于頂角、體心、面心位置的鄰近4個晶胞,如圖3,并對K、I作相應編號。由圖3得,以I處于各頂角位置的KIO3晶胞如圖4。由圖4得,K處于體心位置,O處于棱心位置。
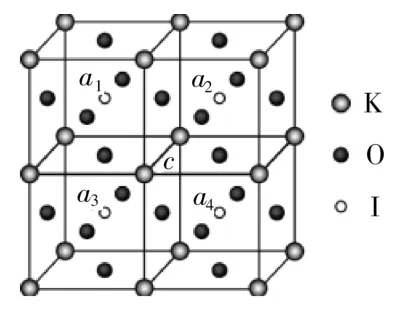
圖3
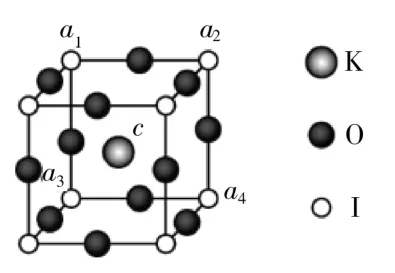
圖4
例5M是第四周期元素,最外層只有1個電子,次外層的所有原子軌道均充滿電子。元素Y的負一價離子的最外層電子數與次外層的相同。單質M的晶體類型為____,晶體中原子間通過____作用形成面心立方密堆積 A1,其中M原子的配位數為____。
解析:M是金屬Cu,屬于金屬晶體,晶體中原子間通過金屬鍵形成面心立方密堆積,面心立方密堆積的配位數都是12。
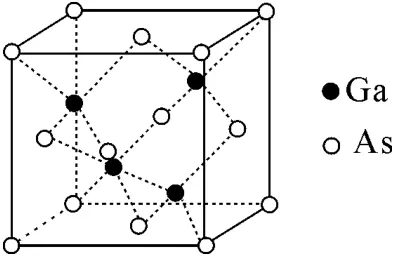
圖5
例6砷化鎵(GaAs)是優良的半導體材料,可用于制作微型激光器或太陽能電池的材料等。GaAs的熔點為1238℃,密度為ρg·cm-3,其晶胞結構如圖5所示。該晶體的類型為____,Ga與As以____鍵結合。Ga和As的摩爾質量分別為MGag·mol-1和MAsg·mol-1,原子半徑分別為rGapm和rAspm,阿伏加德羅常數值為NA,則GaAs晶胞中原子的體積占晶胞體積的百分率為____。
解析:由于GaAs的熔點為1238℃,熔點較高,屬于原子晶體,原子晶體中原子之間以共價鍵結合。GaAs晶胞中原子的體積占晶胞體積的百分率為×100%=×100%。
策略:晶胞的計算是難點,但有法可循。一是熟悉教材中各類晶體中的堆積方式,二是掌握典型模型中粒子之間的位置以及數值關系,三是注意單位換算。


