物質結構與性質易錯綜合題剖析
■鄭州外國語學校 李晉峰
例1已知A、B、C、D和E5種分子所含原子數目依次為1、2、3、4和6,且都含有18個電子。又知B、C和D是由兩種元素的原子組成。請回答:
(1)組成A分子的原子的核外電子排布式是____。
(2)B和C的分子式分別是____和____;C分子的立體結構呈____形,該分子屬于____分子。
(3)若向D的稀溶液中加入少量二氧化錳,有無色氣體生成。則D的分子式是____,該反應的化學方程式為____。
(4)若將1molE在氧氣中完全燃燒,只生成1molCO2和2molH2O,則E的分子式是____。
(5)前四周期元素中,基態原子中未成對電子與其所在周期數相同的元素有____種。
(6)第ⅢA、ⅤA族元素組成的化合物GaN、GaP、GaAs等是人工合成的新型半導體材料,其晶體結構與單晶硅相似。Ga原子的電子排布式為____。在GaN晶體中,每個Ga原子與____個N原子相連,與同一個Ga原子相連的N原子構成的空間構型為____。在四大晶體類型中,GaN屬于____晶體。
(7)在極性分子NCl3中,N原子的化合價為-3,Cl原子的化合價為+1,請推測NCl3水解的主要產物是____(填化學式)。
解析:此題是建立在對含有18電子的物質熟悉的基礎上的。含有18個電子又只含有一個原子,所以A為稀有氣體Ar,核外電子排布式是1s22s22p63s23p6。B、C中分別含有2個或3個原子并且有18個電子,所以分別為HCl、H2S,H2S與水分子結構相似,均是V形結構,屬于極性分子。D是含有4個原子的18電子分子,則可能是PH3和H2O2,據題意,加入二氧化錳會產生無色氣體,則D物質是H2O2,反應的化學方程式為2H2O2。前四周期元素中,基態原子中未成對電子與其所在周期數相同的元素有H、C、O、P、Fe五種。Ga是第四周期31號元素,所以核外電子排布式為1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1),從題給信息可知GaN、GaP、GaAs晶體結構與單晶硅相似,所以它們均屬于原子晶體,原子之間是以共價鍵結合的,所以在GaN晶體中,每個Ga原子與4個N原子相連,其中一個是Ga原子提供空軌道、N原子提供孤對電子形成的配位鍵,所以與同一個Ga原子相連的N原子構成的空間構型為正四面體形。NCl3中N原子的化合價為-3,Cl原子的化合價為+1,所以與水發生水解時,N原子結合水電離的氫離子形成一水合氨,放出氨氣,氯結合氫氧根離子形成次氯酸。
答案:(1)1s22s22p63s23p6(2)HCl H2SV 極性 (3)H2O22H2O22H2O+O2↑
(4)CH4O (5)5
(6)1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1)4正四面體形 原子 (7)HClO、NH3·H2O
例2氮是地球上極為豐富的元素。
(1)Li3N晶體中氮以N3-存在,基態N3-的電子排布式為____。
(2)N≡N的鍵能為942kJ·mol-1,N—N單鍵的鍵能為247kJ·mol-1,計算說明N2中的____鍵比____鍵穩定(填“σ”或“π”)。
(3)N的氧化物中被稱為“笑氣”同時又可以充當麻醉劑的是____,它的等電子體有____(任寫一種),它的空間構型為____。
(4)(CH3)3NH+和AlCl4-可形成離子液體。離子液體由陰、陽離子組成,熔點低于100℃,其揮發性一般比有機溶劑____(填“大”或“小”),可用作____(填代號)。
a.助燃劑 B.“綠色”溶劑
c.復合材料 d.絕熱材料
(5)X+中所有電子正好充滿K、L、M三個電子層,它與N3-形成的晶體結構如圖1所示。X的元素符號是____,與同一個N3-相連的X+有____個。

圖1
(6)X元素可作乙醇轉化為乙醛的催化劑,則乙醛中碳元素的雜化方式為____,乙醛分子中H—C—O的鍵角____(填“<”“=”或“>”)乙醇分子中H—C—O的鍵角。乙醛又可以氧化為乙酸,乙酸的沸點明顯高于乙醛,其主要原因是____。
(7)X元素的氯化物與N元素的氣態氫化物的水溶液反應可形成配合物[X(NH3)4]Cl2,1mol該配合物中含有σ鍵的數目為____個。X的氨基乙酸鹽分子結構如圖2,氮原子的雜化方式為____。在X的硫酸鹽溶液中加入過量K CN,生成配合物[X(CN)4]2-,則CN-中含有的σ鍵與π鍵的數目之比為____。

圖2
(8)X元素與H元素可形成一種紅色化合物,其晶體結構單元如圖3所示。則該化合物的化學式為____。

圖3
(9)X單質形成的晶體類型為____,晶體中原子間通過____作用形成面心立方密堆積,其中M原子的配位數為____。
解析:(1)N原子的原子序數為7,N3-核外共有10個電子,且最外層達穩定結構,所以基態N3-的電子排布式為1s22s22p6。(2)NN≡中有一個σ鍵、兩個π鍵,N—N單鍵的鍵能為247kJ·mol-1,1個π鍵的鍵能是0.5×(942-247)kJ·mol-1=347.5kJ·mol-1,則氮氣中的π鍵鍵能大于σ鍵鍵能,所以π鍵比較穩定。(3)笑氣是N2O,它的等電子體有CO2、CNO-、SCN-等,所以空間結構與二氧化碳一樣是直線形。(4)離子液體的作用力是離子鍵,盡管微弱但是強于氫鍵和分子間作用力,所以其揮發性小,不會污染環境,因此是綠色溶劑。(5)X+所含的電子數為2+8+18=28,所以X為29號元素銅,結合化學式Cu3N可知白球為N,以白球為定點結合空間結構來看,周圍有六個黑球,則N3-周圍有6個X+。(6)乙醛中有甲基、醛基,甲基上的碳原子sp3雜化,醛基上的碳原子sp2雜化,sp3雜化的鍵角大于sp2雜化的平面三角形鍵角。乙醛分子中氫原子都與碳原子相連,而乙酸分子中有一個氫原子與氧原子相連,因此,乙醛分子之間不能形成氫鍵,而乙酸分子之間可以形成氫鍵,所以,乙酸的沸點明顯高于乙醛。(7)配合物[X(NH3)4]Cl2中,氯和絡離子之間形成離子鍵,氨氣分子內是σ鍵,4個氨氣分子共12個σ鍵,氨氣中的氮原子提供孤對電子與銅形成配位鍵,也屬于σ鍵,共有4個,所以σ鍵總共16個;N原子周圍有兩個N—H鍵,一個N—C鍵,還有一對孤對電子,所以是sp3雜化;CN-與N2是等電子體,所以含有的σ鍵與π鍵的數目之比為1∶2。(8)據均攤法,位于頂點的原子每個提供給結構單元個,面心提供給結構單元個,內部原子以1個計,棱上提供個,則銅共有12×+2×+3=6(個),氫有6×+4=6(個),所以化學式為Cu H。(9)銅晶體是金屬晶體,形成晶體的作用力是金屬鍵,因為晶胞是面心立方結構,所以一個銅原子周圍的配位數為12。
答案:(1)1s22s22p6(2)πσ(3)N2OCO2(或 CNO-、SCN-) 直線形
(4)小B(5)Cu6(6)sp3、sp2>乙醛分子之間不能形成氫鍵,而乙酸分子之間可以形成氫鍵(7)16sp31∶2(8)XH(9)金屬晶體金屬鍵12
例3C和Si元素在化學中占有極其重要的地位。
(1)寫出Si的基態原子核外電子排布式:____。從電負性角度分析,C、Si和O元素的非金屬活潑性由強至弱的順序為____。
(2)SiC的晶體結構與晶體硅的相似,其中C原子的雜化方式為____,微粒間存在的作用力是____。
(3)氧化物MO的電子總數與SiC的相等,則M為____(填元素符號),MO是優良的耐高溫材料,其晶體結構與NaCl晶體相似,MO的熔點比Ca O的高,其原因是____。
(4)C、Si為同一主族的元素,CO2和SiO2化學式相似,但結構和性質有很大不同。CO2中C與O原子間形成σ鍵和π鍵,SiO2中Si與O原子間不形成上述π鍵。從原子半徑大小的角度分析,為何C、O原子間能形成上述π鍵,而Si、O原子間不能形成上述π鍵:___。
(5)碳元素的單質有多種形式,金剛石、石墨、C60、碳納米管等都是碳元素的單質形式,它們互為____;金剛石、石墨烯(指單層石墨)中碳原子的雜化形式分別為____、____;石墨晶體中,層內C—C鍵的鍵長為142pm,而金剛石中C—C鍵的鍵長為154pm。其原因是金剛石中只存在C—C間的____共價鍵,而石墨層內的C—C間不僅存在____共價鍵,還有____鍵。最新研究表明生命可能起源于火山爆發,因為火山爆發產生的氣體中含有1%的羰基硫(COS),已知羰基硫分子中所有原子的最外層都滿足8電子結構,結合已學知識,判斷有關說法正確的是____。
A.羰基硫屬于非極性分子
B.羰基硫的電子式為∶
C.羰基硫的沸點比CO2的低
D.羰基硫分子中三個原子處于同一直線上
(6)過渡金屬配合物N i(CO)n的中心原子價電子數與配體提供電子總數之和為18,則n=____。CO與N2結構相似,CO分子內σ鍵與π鍵個數之比為____。CO作為N i(CO)n配合物中的配體可以提供孤電子對進入中心原子的空軌道中,則提供孤電子對的元素是____。
(7)碳和硅的有關化學鍵鍵能如表1所示。

表1
簡要分析和解釋下列有關事實:
①硅與碳同族,也有系列氫化物,但硅烷在種類和數量上都遠不如烷烴多,原因是____。
②SiH4的穩定性小于CH4的穩定性,更易生成氧化物,原因是____。
③單質硅可通過甲硅烷(SiH4)分解反應來制備。工業上采用Mg2Si和NH4Cl在液氨介質中反應制得SiH4,該反應的化學方程式為____。
(8)在硅酸鹽中,SiO44-四面體(如圖4)通過共用頂角氧離子可形成島狀、鏈狀、層狀、骨架狀四大類結構形式。圖5為一種無限長單鏈結構的多硅酸根,其中Si原子的雜化形式為____。Si與O的原子數之比為____,化學式為____。

圖4
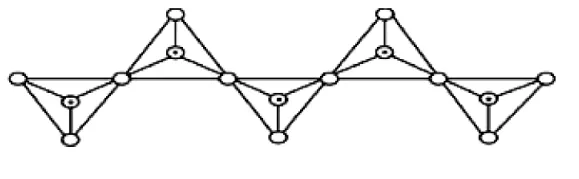
圖5
解析:(1)硅是14號元素,則核外電子排布式為1s22s22p63s23p2;非金屬活潑性O>C>Si。(2)SiC晶體中C原子與Si原子之間用單鍵相連,均有四個共價鍵,所以C原子是sp3雜化。(3)SiC有20個電子,由此可以推斷M元素是Mg,因為Mg2+的半徑比Ca2+的小,所以MgO的晶格能大、熔點高。(4)由于C的原子半徑較小,所以C、O原子能充分接近,p—p軌道肩并肩重疊的程度較大,形成較穩定的π鍵;而Si原子半徑較大,Si、O原子間距離較大,p—p軌道肩并肩重疊程度較小,不能形成穩定的π鍵。(5)這幾種物質都是由碳原子構成的結構不相同的單質,所以相互之間屬于同素異形體,金剛石中只含有碳碳單鍵,所以是sp3雜化,石墨層中有碳碳雙鍵,所以C原子屬于sp2雜化,而金剛石中鍵長比較長就是因為只含有碳碳σ鍵,石墨中鍵長較短與它既存在碳碳σ鍵也存在π鍵有關。羰基硫與二氧化碳屬于等電子體,碳原子分別與氧原子和硫原子形成兩對共用電子對,屬于極性分子,沸點高于二氧化碳。(6)N i的價電子數為10,CO提供8個電子形成配位鍵,所以CO分子數為4。CO分子與氮氣分子屬于等電子體,所以含有的σ鍵與π鍵個數比為1∶2;由于O的電負性強于C原子,所以C原子對電子的吸引力弱,C原子更容易提供孤對電子形成配位鍵。(7)①C—C鍵和C—H鍵較強,所形成的烷烴穩定;而硅烷中Si—Si鍵和Si—H鍵的鍵能較低,易斷裂,導致長鏈硅烷難以生成,所以硅烷在種類和數量上都遠不如烷烴多。②C—H鍵的鍵能大于C—O鍵的鍵能,C—H鍵比C—O鍵穩定;而Si—H鍵的鍵能卻遠小于Si—O鍵的鍵能,所以Si—H鍵不穩定而傾向于形成穩定性更強的Si—O鍵。③工業上采用Mg2Si和NH4Cl在液氨介質中反應制得SiH4,該反應產物除了生成SiH4外,還放出NH3,所以化學方程式為Mg2Si+4NH4Cl══SiH4+4NH3+2MgCl2。
(8)硅酸鹽中的硅酸根(SiO4-4)為正四面體結構,所以中心原子Si原子采取了sp3雜化方式;根據圖5所示,直線上的原子為兩個結構單元所共有,所以一個結構單元中含有1個硅原子和3個氧原子,化學式為SiO2-3。
答案:(1)1s22s22p63s23p2O>C>Si(2)sp3共價鍵 (3)MgMg2+半徑比Ca2+小,MgO的晶格能大(4)C的原子半徑較小,C、O原子能充分接近,p—p軌道肩并肩重疊程度較大,形成較穩定的π鍵;而Si原子半徑較大,Si、O原子間距離較大,p—p軌道肩并肩重疊程度較小,不能形成穩定的π鍵(5)同素異形體 sp3sp2σσπ
D(6)41∶2C(7)①C—C鍵和C—H鍵較強,所形成的烷烴穩定;而硅烷中Si—Si鍵和Si—H鍵的鍵能較低,易斷裂,導致長鏈硅烷難以生成②C—H鍵的鍵能大于C—O鍵的鍵能,C—H鍵比C—O鍵穩定;而Si—H鍵的鍵能卻遠小于Si—O鍵的鍵能,所以Si—H鍵不穩定而傾向于形成穩定性更強的Si—O鍵 ③Mg2Si+4NH4Cl══SiH4+4NH3+2MgCl2(8)sp31∶3
例4ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表現出多種氧化態,含ⅥA族元素的化合物在研究和生產中有許多重要用途。請回答下列問題:

圖6
(1)S單質的常見形式為S8,其環狀結構如圖6所示,S原子采用的軌道雜化方式是____。
(2)原子的第一電離能是指氣態電中性基態原子失去一個電子轉化為氣態基態正離子所需要的最低能量,O、S、Se原子的第一電離能由大到小的順序為____。
(3)H2Se的酸性比H2S的酸性____(填“強”或“弱”)。氣態SeO3分子的立體構型為____,SO離子的立體構型為____。
(4)已知Li2Ti5O15中有過氧鍵,Ti的化合價為+4價,其中過氧鍵的數目為____。
解析:(1)S8分子中每個S原子形成兩個共價鍵,此外還有兩對孤對電子存在,所以S8分子中硫原子是sp3雜化。(2)O、S、Se三個元素是同一主族,從上到下原子半徑逐漸增大,原子核對核外電子的吸引力減小,非金屬性逐漸減弱,所以第一電離能逐漸減小,O>S>Se。(3)中氫化物的穩定性 H2S比H2Se強。氣態SeO3分子的立體構型與等電子體SO3結構一樣是平面三角形,S離子中S是sp3雜化,所以其立體構型為三角錐形。(4)Li2Ti5O15中,Ti的化合價為+4價,Li的化合價為+1價,O原子既有-2價又有-1價,根據化合價代數和為零,設過氧鍵的數目為x,則2+4×5-2(15-2x)-2x=0,x=4。
答案:(1)sp3(2)O>S>Se(3)強平面三角形三角錐形 (4)4

