從晶胞結構層面談創新姚
■鄭州外國語學校 姚衛民
自2006年江蘇卷率先在選擇題里出現晶胞結構以來,各種晶胞結構陸續在全國及各省市高考題中出現。有關晶體的部分可謂是年年創新,下面我們分別從以下幾個方面舉例探究。
一、晶胞中原子的位置互換
例1鈣鈦礦結構材料廣泛應用于壓電、超導、催化、磁電阻等領域。回答下列問題:
(1)元素鈣的焰色反應呈磚紅色,其中紅色對應的輻射波長為____nm(填標號)。
A.324.7 B.404.4 C.460.7
D.553.5 E.657.3
(2)基態Ca原子中,核外電子占據的第三層符號是____,占據該能層最高能級電子的電子云輪廓形狀為____。Ti和Cu屬于同一周期,Ti的原子半徑大于Cu的,但金屬Ti的熔沸點比Cu的高,說明金屬的熔沸點與金屬原子半徑、____和晶體結構中原子堆積方式等因素有關。
(3)被譽為“生命元素”的元素Se和Ca處于同一周期,我國科學家嘗試用Na2SeO3清除人體內的活性氧,離子的幾何構型為____,中心原子的雜化類型為____。
(4)鈣鈦礦晶胞為立方結構,邊長為anm,晶胞中Ti、Ca、O分別處于頂角、體心、棱中心位置,如圖1所示。Ca與O間最短距離為____nm,與Ti緊鄰的O的個數為____。

圖1
(5)在鈣鈦礦晶胞結構的另一種表示中,Ca處于各頂角位置,則Ti處于____位置,O處于____位置。
答案:(1)E
(2)M 啞鈴形(或紡錘形) 金屬原子的價電子結構
(3)三角錐形 sp3雜化
(4)a6
(5)體心 面心
分析:在高中課本中主要介紹了四種晶胞類型:簡單立方晶胞、體心立方晶胞、面心立方晶胞和六方晶胞,對于離子晶體晶胞類型也只是提到CsCl型、NaCl型、ZnS型、CaF2型等四種類型,并沒有講過鈣鈦礦型,當然高考并沒有超綱,這恰恰是高考源于課本又高于課本的體現,是對考生處理未知信息能力的考查。然而站在考生的角度,如何去做這種題呢?其實仔細研究不難發現,鈣鈦礦晶胞結構其實是把CsCl型晶胞和NaCl型晶胞嵌套在一起形成的。所以此題其實是在變相考查考生對CsCl型晶胞和NaCl型晶胞特點的掌握情況。
新編題:(1)F-與Mg2+、K+形成一種立方晶系的離子晶體,此晶體應用于激光領域,結構如圖2所示。晶胞邊長為anm,晶胞中Mg2+、K+、F-分別處于頂角、體心、棱中心位置。該晶體的化學式為____,與K+緊鄰的F-的個數為____。

圖2
(2)在該離子晶胞結構的另一種表示中,F-處于各頂角和部分面心位置,則Mg2+處于____位置,K+處于____位置。
答案:(1)KMgF312(2)棱中心面心
二、原子坐標
例2(1)Na+與Ne互為等電子體,電離能I2(Na)___I1(Ne)(填 “<”“=”或“>”)。
(2)第四周期中,與Al原子未成對電子數相同的金屬元素有____種。氣態氯化鋁的分子組成為(AlCl3)2,分子中所含的化學鍵類型有____,Al原子的雜化方式為____。
(3)可燃冰是天然氣水合物,具有籠形結構如圖3(表面的小球是水分子,內部的大球是甲烷分子)。水分子成籠的作用力是____,圖3中最小的環中連接的原子總數是____。可燃冰晶體具有多種籠狀結構,其中一種由1個圖3所示籠分別用2個面與另外兩個相同的籠共面而成,則中間籠實際占有____個水分子。

圖3
(4)金屬鎂晶體中原子的堆積方式為六方最密堆積,如圖4所示,晶胞可用圖5表示。設金屬鎂的原子半徑為acm,晶胞的高為bcm,則該晶體的空間利用率為____(寫出計算式);設晶胞中A點原子的坐標為(0,0,0),C點原子的坐標為(2a,0,0),D點原子的坐標為(0,0,b),則B點原子的坐標為____。
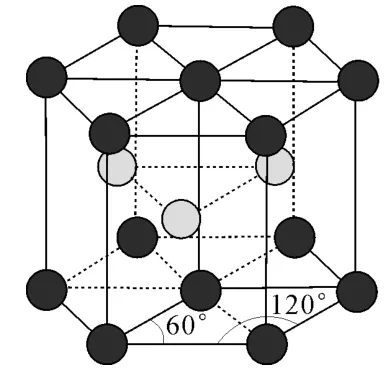
圖4

圖5
答案:(1)> (2)4共價鍵、配位鍵sp3(3)氫鍵 1015 (4)× 100%
分析:從歷年各省份高考題來看,還從未考查過有關六方晶胞中的距離、空間占有率以及晶胞參數。這可能成為未來晶體結構出題的一個重要方向。
三、粒子填隙和替換
粒子填隙和替換,是晶體結構豐富多樣的原因之一。
例3研究發現,在CO2低壓合成甲醇反應(CO2+3H2══CH3OH+H2O)中,CO氧化物負載的Mn氧化物納米粒子催化劑具有高活性,顯示出良好的應用前景。回答下列問題:
(1)CO基態原子核外電子排布式為____。元素Mn與O中,第一電離能較大的是____,基態原子核外未成對電子數較多的是____。
(2)CO2和CH3OH分子中C原子的雜化形式分別為____和____。
(3)在CO2低壓合成甲醇反應所涉及的4種物質中,沸點從高到低的順序為____,原因是____。
(4)硝酸錳是制備上述反應催化劑的原料,Mn(NO3)2中的化學鍵除了σ鍵外,還存在____。
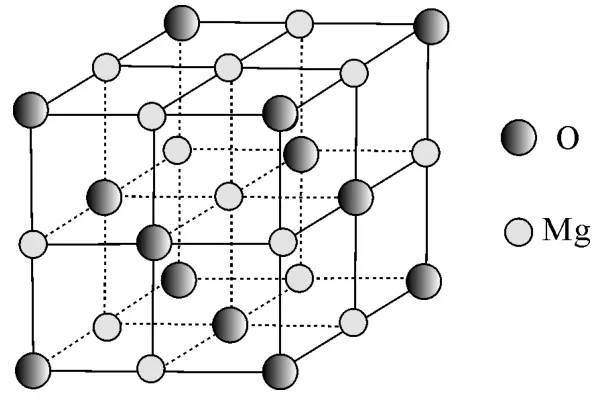
圖6
(5)MgO具有NaCl型結構(如圖6),其中陰離子采用面心立方最密堆積方式,X射線衍射實驗測得MgO的晶胞參數為a=0.420nm,則r(O2-)為____nm。MnO也屬于NaCl型結構,晶胞參數為a'=0.448nm,則r(Mn2+)為____nm。
答案:(1)1s22s22p63s23p63d74s2或[Ar]3d74s2OMn
(2)sp sp3
(3)H2O>CH3OH>CO2>H2H2O與CH3OH均為極性分子,H2O中氫鍵比甲醇多;CO2與H2均為非極性分子,CO2分子量較大,范德華力較大
(4)離子鍵和π鍵
(5)0.1480.076
分析:在離子晶體中,一般陰離子體積比陽離子的大,所以離子晶體的形成,一般看成陰離子先密堆積,然后陽離子來填充陰離子堆積所形成的空隙。而只有當正、負離子完全緊密接觸時,晶體才是穩定的。在不同構型的離子晶體中,要使正負離子完全接觸,則正負離子的半徑比值必須滿足一定的條件,如表1所示。這也是離子晶體比較多變的原因之一。所以這方面應該引起我們的關注和深入研究。
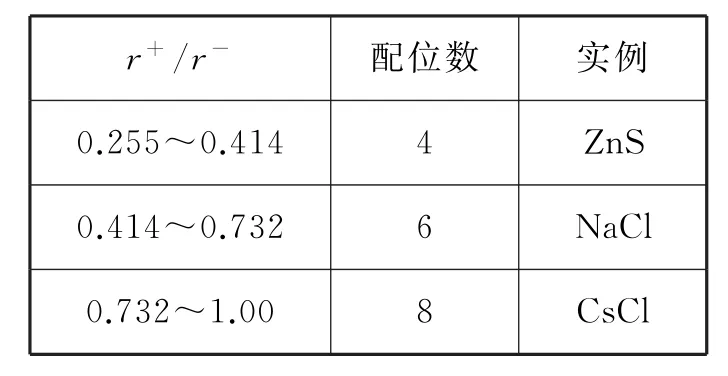
表1
填隙又分為恰好填隙(不改變原有陰離子的最密堆積)和填隙之后使陰離子相離兩種情況。例3就是在考查這兩種情況。從空隙對稱性來看,簡單立方、面心立方和六方晶胞的空隙都是對稱性的,而體心立方空隙是不規則的,所以通常對具有對稱性空隙晶體的考查較多。簡單立方填隙為CsCl型晶胞,面心立方填隙分別得到NaCl型晶胞、立方ZnS型晶胞和CaF2型晶胞,六方晶胞填隙能得到六方ZnS型晶胞。
總結:化學的創新實質上就是通過一個新穎的載體,把知識有機地結合到一起,從而達到考查認知的目的。從上述例題分析來看,結合近幾年出題類型,無論是創新題還是改編題,無論是原子坐標還是原子互換,其實都是對課本知識的深入挖掘,有的甚至能在大學無機化學教材里找到出處。不只是晶體部分,很多其他的創新題也很多來源于大學課本或是文獻,這充分體現了對考生讀題能力,對陌生信息處理能力的考查。所以要想創新必須深入研究課本知識,特別是大學教材,找到其與高中課本知識相銜接的地方,巧妙設計,融為一體。

