物質結構與性質方面的競賽知識歸納
■鄭州外國語學校 陳 寧
物質結構與性質知識涉及三個模塊:原子結構與性質、分子結構與性質、晶體結構與性質。下面以自主招生真題和部分競賽試題為例,將可能需要儲備的知識點和思維方法加以介紹。通過這些介紹,希望同學們不僅可以對高考中的一些難點重新突破,同時也可以掌握一些自主招生考試解題方法。
一、原子結構與性質
問題1:一般情況下,電子離核越遠能量越高,但為什么按照構造原理圖,離核較遠的第四個能層的4s能級卻比離核較近的第三個能層的3d能級能量更低?
問題2:為什么周期表中有的原子核外電子排布不符合核外電子填充的三個規律(構造原理、洪特規則、泡利原理)?例如Pd、Pt、Ru等。
問題3:Fe原子價電子構型是3d64s2,為什么Fe2+價電子構型是3d6而非3d44s2?
要解決這些問題必須具有以下知識儲備。
1.屏蔽效應。
在多電子的中性原子中,每個電子除了受原子核(核電荷數Z)的吸引外,同時還受其他Z-1個電子的排斥。如不考慮電子間的相互作用,多電子原子中的電子僅受核電荷的吸引,那么此電子離核越遠能量越高;當考慮其他電子排斥作用時,其他電子對此電子的排斥作用相當于部分抵消(或削弱)了原子核對此電子的吸引,其他Z-1個電子的電子云分散在核周圍,像一個“罩”屏蔽掉了一部分原子核的正電荷吸引,使此電子離核距離有所增加,能量升高。
電子的屏蔽效應有以下幾個規則:(1)n+1層電子對n層及n層以內電子無屏蔽效應;(2)同層電子間屏蔽效應比內層電子對其屏蔽效應弱;(3)n能層上的電子受到n-2層電子屏蔽效果比n-1層電子屏蔽效果更強;(4)相鄰兩組電子,內層電子對外層s和p電子的屏蔽效應弱于對d和f電子的屏蔽效應。
2.鉆穿效應。
由于不同能級電子云形狀不同,電子穿過內層鉆穿到核附近回避其他電子屏蔽的能力不同,從而使其能量不同的現象稱為鉆穿效應。鉆穿能力一般是ns>np>nd>nf。鉆穿能力越強表示電子回避其他電子屏蔽能量越強,受核吸引越強,離核越近,能量越低。鉆穿與屏蔽效應是相互聯系的,二者共同作用決定了核外電子的能量以及原子半徑的大小。
問題1解答:以19K和20Ca元素為例,E4s<E3d。因為4s和3d電子云形狀不同,雖然4s電子最大概率密度距核比3d電子遠,但由于4s鉆穿效應比3d強,其上電子鉆穿到核附近回避其他電子的能力大,大大降低了4s電子的平均能量,使得4s比3d電子能量還低。
問題3解答:21Sc以后的元素,以26Fe為例,其E4s>E3d。原因是4s電子云從整體看比3d離核遠得多,與Ca相比,當6個電子填入以后,核電荷同時增加了6個單位,作用于3d的核電荷增加使3d能量降低。此時內層3d上的電子對4s的屏蔽又起作用,相比之下4s鉆穿作用不再突出,4s電子能量又高于3d。因此Fe→Fe2+,失去的是4s上的2個電子。
問題2解答:由上面兩個問題可以看出,決定基態中性原子或離子的核外電子排布時,最根本的是考慮整個原子或離子在哪一種狀態能量最低,而不是任何情況下只看軌道的能量高低。周期表中原子的核外電子排布是光譜實驗的測定結果。
例1鑭系元素從左向右,原子半徑減小的幅度減小,這種現象稱為鑭系收縮,說說出現這一現象的原因。
解答:對比短周期,從左向右電子都增加在同一外層,電子在同一層內的相互屏蔽作用比較小,所以隨原子序數增大,核電荷對電子吸引力增強,導致原子收縮,半徑減小;第四周期過渡元素從左到右,電子逐一填入(n-1)d層,d電子處于次外層,對核的屏蔽作用較大,所以隨著核電荷增大,半徑減小的幅度不如主族元素那么大;鑭系元素電子填入再次外層,即(n-2)f層,其對核的屏蔽作用更大,原子半徑從左到右收縮的平均幅度更小。
二、分子結構與性質
例2寫出NH3、NF3、PF3分子的構型,鍵角順序。
解答:均為三角錐形。鍵角:NH3>NF3>PF3。
點撥:分子構型的推斷依據是選修3中介紹的價層電子對互斥理論(VSEPR)(雜化軌道理論無法預測分子構型),而如何比較鍵角的大小,高中教材并未講解。但若能理解VSEPR理論的基本思想:在共價分子或共價型離子中,中心原子周圍所占空間盡可能采用使其本身受到靜電排斥最小的理想幾何構型,即盡可能使中心原子周圍的各電子對距離達到最大,便可將此思想遷移到鍵角大小的比較上來。
在相同的雜化類型和孤電子對的條件下,中心原子的電負性越大,成鍵電子對離中心原子越近,成鍵電子對之間距離變小,排斥力增大,鍵角變大。N原子電負性大于P,因此NF3中鍵角大于PF3中鍵角。與其相反,中心原子相同,端位原子的電負性越大,鍵角越小。F電負性大于H,因此NF3中鍵角小于NH3的鍵角。
影響鍵角的因素很多,除了上面提到的兩點以外,還有以下幾個方面。
a.共價分子中雙鍵、叁鍵的影響:由于叁鍵與叁鍵之間的排斥力>雙鍵與雙鍵之間的排斥力>雙鍵與單鍵之間的排斥力>單鍵與單鍵之間的排斥力。例如乙烯分子中,∠HCC>∠HCH。
b.不同雜化類型,鍵角不同。
c.在相同的雜化類型條件下,中心原子上孤對電子越多,成鍵電子對之間的鍵角越小。例如CH4、NH3、H2O,因為中心原子上孤對電子越多,成鍵電子對受到的排斥力越大,所以鍵角依次減小。孤對電子與孤對電子之間的排斥力>孤對電子與成鍵電子之間的排斥力>成鍵電子與成鍵電子之間的排斥力。
三、晶體結構中的多面體
晶體結構中涉及的問題多種多樣,本文無法全部分析。但筆者對晶體類試題研究發現,晶胞中包含的多面體模型是眾多高考、自主招生、競賽出題頻率最高的題型,因此我將選擇這個問題作為重點突破。
(一)四面體。
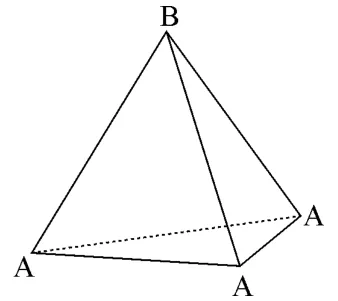
圖1
圖1為正四面體的幾何圖形,幾何結構上可看作四個正三角形面兩兩共棱的組合或者任意兩條異面直線的組合,若考慮晶體中原子堆積則可看作A、B兩層:A層正三角形和正對A層三角形中心的B。
密堆積的原子單層排列如圖2,A球密堆積,將該層稱為A層,留下兩種三角形空隙B和C。

圖2
若要緊密堆積,第二層的球只能填入B空隙或C空隙,一旦有一個球入B空隙,剩余的球只能入B空隙,可將該層稱為B層,若一開始球入C空隙,該層稱為C層(B、C取向只是相對而言的,假設第二層為B層)。則A層三個相鄰的構成正三角形方位的原子與其上方填入B空隙的1個原子構成一個正四面體,如圖3,其體心即四面體空隙中心;同樣,若A層取一個原子與其正上方B層成正三角形方位的三個原子也可形成一個正四面體,如圖4,其體心也是四面體空隙中心。

圖3

圖4
倘若把三原子所在三角形當作底面,單原子中心稱作頂點,那么頂點到底面中心的距離即此四面體的高,此高線方向與密置層所在面垂直,四面體空隙的中心O在此高線上。
以圖3所示四面體為例,其構型如圖5所示,A所在面為密置層面,X為三角形中心,B為四面體頂點,BX垂直于A面,O為四面體空隙中心,O在B X上,且d(BO)=d(BX)。

圖5
例3圖6為六方ZnS的晶胞圖,頂點與晶胞內為S原子,請寫出Zn原子的坐標。
注:箭頭所指S原子坐標為(1,1,1)。

圖6
解答:S按照六方最密堆積ABABA……,六方晶胞共三層S原子。

圖7
從圖7中比較容易看出來B層一個S原子與相鄰A層三個S原子構成的四面體,此四面體高線與z軸平行,長度等于相鄰層間距(晶胞z軸方向棱長的一半)。1號Zn填在此四面體空隙中,它距離頂點B的距離為四面體高的(晶胞z軸方向棱長的),因此坐標為(,1-),即(,)。
還有一種四面體,B層三個相鄰呈三角形位置的S原子與相鄰密置A層的一個S構成的四面體,雖然這種四面體底面三個原子并未都在此晶胞中出現,但能確定的是AB層距為這個四面體的高,四面體空隙中心一定在A的正下方,距A高度為四面體高的。2,3,4,5號Zn原子中z軸方向坐標為1,完整坐標分別為(1,0,),(0,0),(0,1),(1,1)。
(二)八面體。
正八面體的觀察有三種不同方式,最常規的如圖8所示,四個B組成正方形與過該正方形中心并垂直于該平面的軸(兩個A的連線)。

圖8

圖9
第二種如圖9所示,可看作由三個A和3個B構成的正三角形組成,兩個三角形所在面互相平行。若將頂點處六個原子沿著兩個平行三角形中心連線投影,所得投影圖如圖10所示,投影圖為六芒星形狀。
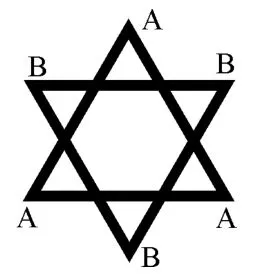
圖10
第三種如圖11所示,相互交叉的兩個三角形,三個A構成的三角形底邊與三個B構成的三角形底邊垂直相交,交點為正八面體體心。

圖11
例4圖12為Mg的晶胞圖,請寫出其中八面體空隙中心的坐標。其中O(0,0,0)。

圖12
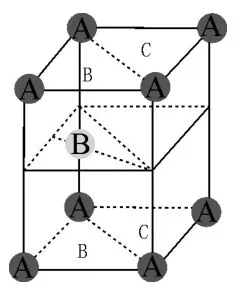
圖13
解答:如圖13所示,一個六方最密晶胞共由ABA三個密置層構成,層在水平面上。A密置層共有兩種三角形空穴B和C(字體不加粗,分別已標注于圖13A層相應位置),第二層填充了對應的B空穴,則B層三個原子與A層三個原子必然在對應C空穴的位置存在一個八面體空隙,如圖14所示。

圖14
圖14中雙向箭頭所連接的三個A構成的三角形與下面B層三個原子構成的三角形所在面平行,大小相等,取向相反,正好構成一個正八面體,其中心即為八面體空隙中心。該中心沿著堆積方向投影剛好與C空穴位置重合,其縱向位置恰好在相鄰兩個A、B層中間,因此坐標為,同理在B層與下面一個A層之間也存在一個八面體空隙中心,其坐標為。
(三)六元環。
圖15為金剛石的結構圖,其中灰色小球代表碳原子,每個碳原子均為sp3雜化,價層電子對呈正四面體構型,每六個碳原子構成一個六元環,這六個碳原子并不在同一個平面內,而是呈現一個椅形的狀態。

圖15

圖16
例5金剛烷(C10H16)是一種重要的脂肪烷烴,其結構高度對稱(如圖16所示)。金剛烷能與鹵素發生取代反應,其中一氯一溴金剛烷(C10H14ClBr)的同分異構體數目是( )。
A.4B.6 C.8 D.10
解答:金剛烷中的碳可分為兩類,一類是(CH—)結構中的C,共有4個,相互之間呈四面體構型,記為1號碳;一類是(CH2—)中的C,共有6個,呈八面體構型,記為2號碳。此題的同分異構可分為三類來解決問題。第一類,將Cl連在1號碳上,然后在同一個六元環上連Br,有鄰、間、對三種情況;第二類,將Cl連在2號碳上,然后在同一個六元環上連Br,有同一碳原子和鄰、間、對四種情況;第三類,將Cl連在2號碳上,然后在不同的六元環上連Br,只有一種情況。若將Cl連在1號碳上,找不到與其在不同的六元環上的碳,故沒有此類型的同分異構體。
如圖17所示,共8種。答案為C。

圖17
【晶體中的多面體問題小結】由于自然界中晶體的廣泛存在,從晶體結構與性質出發,可引申出形式各樣的題目,但目前高考與自主招生在這一模塊出題常常會從晶體中蘊含的經典多面體角度出題,筆者認為要想突破此難點,需要先將經典多面體本身從多個角度(結合其對稱性)深入認識并剖析,然后從原子堆積層中找尋經典多面體基本模型,進而將較為復雜的題目轉變為解決經典多面體模型的基本問題上來,最終順利解決問題。

