甲狀旁腺切除術(shù)對(duì)終末期腎病合并繼發(fā)性甲狀旁腺功能亢進(jìn)患者冠狀動(dòng)脈鈣化及鈣磷代謝的影響
曲立枝
終末期腎病(end stage renal disease, ESRD)是指各種腎臟疾病進(jìn)展至腎功能、腎臟結(jié)構(gòu)不可逆的最終階段,隨著透析技術(shù)的發(fā)展,患者生存時(shí)間得到明顯延長(zhǎng),但是影響患者生活質(zhì)量及長(zhǎng)期生存率的并發(fā)癥問(wèn)題日益凸顯[1-2]。其中心血管不良事件發(fā)生及繼發(fā)性甲狀旁腺功能亢進(jìn)(secondary hyperparathyroidism, SHPT)是最為常見(jiàn)且嚴(yán)重的并發(fā)癥。由于ESRD患者存在骨和鈣磷代謝異常,又可誘發(fā)心血管疾病,會(huì)對(duì)患者的預(yù)后造成嚴(yán)重影響[3]。冠狀動(dòng)脈鈣化(coronary artery calcification, CAC)是心血管事件的病理基礎(chǔ),研究報(bào)道,CAC和鈣磷乘積水平、甲狀腺旁腺激素(iPTH)、血磷等密切相關(guān)[4]。臨床認(rèn)為在早期應(yīng)用擬鈣劑、活性維生素D3、磷結(jié)合劑可降低iPTH水平,減輕CAC,改善鈣磷代謝,并可縮小增大的甲狀旁腺,但是部分患者經(jīng)活性維生素D3沖擊或其他藥物治療后仍然可進(jìn)展為難治性的SHPT或鈣磷代謝紊亂加重[5]。故對(duì)于晚期ESRD合并SHPT患者,甲狀旁腺切除術(shù)治療是唯一有效的治療方法[6]。本研究探討甲狀旁腺切除術(shù)對(duì)ESRD合并SHPT患者CAC及鈣磷代謝的影響,旨在為其治療提供理論基礎(chǔ),現(xiàn)報(bào)告如下。
1 資料與方法
1.1一般資料 選擇2006年1月—2016年2月在我院擇期行甲狀旁腺切除術(shù)的300例ESRD合并SHPT患者的臨床資料,并進(jìn)行回顧性分析。①納入標(biāo)準(zhǔn):頸部彩色超聲均顯示甲狀旁腺增大,且經(jīng)術(shù)后病理證實(shí);均伴有SHPT,即iPTH>800 pg/ml;均給予活性維生素D3沖擊等內(nèi)科保守治療無(wú)效或療效較差,均符合甲狀旁腺切除術(shù)手術(shù)指征;均經(jīng)放射學(xué)檢查顯示高度骨代謝指標(biāo)轉(zhuǎn)運(yùn)。②排除標(biāo)準(zhǔn):近期應(yīng)用過(guò)免疫抑制劑或糖皮質(zhì)激素治療者;伴有血液系統(tǒng)疾病或急性感染患者;合并惡性腫瘤患者;伴有嚴(yán)重肝、腦功能障礙患者;近1年來(lái)有心肌梗死、心絞痛、心力衰竭等心血管疾病病史者。其中男120例,女180例;年齡35~65(43.26±3.52)歲;透析時(shí)間2~10(6.12±1.41)年;原發(fā)病類(lèi)型:高血壓腎病82例,慢性腎小球腎炎118例,糖尿病腎病100例。并根據(jù)有無(wú)發(fā)生CAC分為CAC組210例和無(wú)CAC組90例。
1.2方法
1.2.1治療方法:所有患者入院后均給予血液透析、飲食控制、營(yíng)養(yǎng)支持、降壓等對(duì)癥治療,待病情平穩(wěn)后再行甲狀旁腺切除術(shù),具體如下:采用全身麻醉方式,于頸部做一橫向切口,將上下皮瓣游離,再分開(kāi)頸前肌群,確定甲狀腺上下極后方的甲狀旁腺腺體,常規(guī)行甲狀旁腺切除術(shù),術(shù)后放置引流管。所有患者術(shù)后均常規(guī)將切除的甲狀旁腺腺體進(jìn)行病理檢測(cè),結(jié)果證實(shí)為甲狀旁腺組織增生。
1.2.2觀(guān)察指標(biāo):記錄所有患者的年齡、性別、透析時(shí)間、血鈣、血磷、鈣磷乘積、iPTH、C反應(yīng)蛋白、甘油三酯、高密度脂蛋白膽固醇、低密度脂蛋白膽固醇、白蛋白、血紅蛋白以及CAC積分等臨床資料。
1.2.3隨訪(fǎng):所有患者隨訪(fǎng)12個(gè)月,觀(guān)察術(shù)前、術(shù)后6和12個(gè)月的CAC積分、iPTH、血鈣、血磷、鈣磷乘積、甘油三酯水平變化。
1.3CAC積分評(píng)估標(biāo)準(zhǔn) 參照Agatston積分法對(duì)CAC進(jìn)行定量分析[7],鈣化的閾值定為CT值130 Hu,并要求所檢測(cè)的鈣化灶面積>0.5 mm2。將CT值130~199 Hu定為1分,200~299 Hu定為2分,300~399 Hu定為3分,≥400 Hu定為4分。各鈣化灶積分=鈣化灶面積×CT值積分。CAC積分等于右冠狀動(dòng)脈、左冠狀動(dòng)脈、左回旋支、左前降支的各鈣化灶積分之和。CAC積分<10分則表明心血管疾病發(fā)生率較低;CAC積分在10~400分,則表明存在冠狀動(dòng)脈狹窄,臨床應(yīng)當(dāng)引起重視;CAC積分>400分則表明存在冠心病。
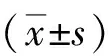
2 結(jié)果
2.1單因素分析 兩組的血鈣、血磷、鈣磷乘積、C-反應(yīng)蛋白、iPTH水平、透析時(shí)間和CAC積分比較差異有統(tǒng)計(jì)學(xué)意義(P<0.01),而年齡、性別、甘油三酯、高密度脂蛋白膽固醇、低密度脂蛋白膽固醇、血紅蛋白和白蛋白水平比較差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05)。見(jiàn)表1。
2.2多因素Logistic回歸分析 將上述有統(tǒng)計(jì)學(xué)差異的因素納入多因素Logistic回歸分析,結(jié)果顯示透析時(shí)間長(zhǎng)、CAC積分高是影響ESRD合并SHPT患者發(fā)生CAC的獨(dú)立危險(xiǎn)因素(P<0.05)。見(jiàn)表2。
2.3不同時(shí)間點(diǎn)相關(guān)指標(biāo)的變化 術(shù)后6和12個(gè)月,血鈣、血磷、鈣磷乘積、甘油三酯、iPTH水平及CAC積分均低于術(shù)前(P<0.05)。術(shù)后12個(gè)月,iPTH水平及CAC積分低于術(shù)后6個(gè)月(P<0.05),術(shù)后12個(gè)月與術(shù)后6個(gè)月的血鈣、血磷、鈣磷乘積、甘油三酯水平比較差異均無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05)。見(jiàn)表3。
3 討論
SHPT是ESRD患者對(duì)于鈣磷代謝紊亂的適應(yīng)性反應(yīng),iPTH是一種尿毒癥毒素,與ESRD患者免疫功能、肌肉功能、睡眠狀況、皮膚瘙癢及心血管不良事件密切相關(guān),這些均可對(duì)患者的生存質(zhì)量及預(yù)后造成影響[8]。ESRD患者由于腎功能衰竭引起活性維生素D3生成減少、高磷血癥、低鈣血癥,這些因素均可引起甲狀旁腺增大,過(guò)度釋放iPTH,增加破骨細(xì)胞的活性,從而導(dǎo)致鈣、磷水平過(guò)高發(fā)生高鈣、高磷血癥[9-10]。大部分患者在ESRD早期通過(guò)擬鈣劑、透析、活性維生素D3、降磷藥物、飲食控制等對(duì)癥治療,可有效地改善鈣磷代謝紊亂,縮小甲狀旁腺腺體,但是仍有小部分患者可發(fā)展為難治性的SHPT[11]。ESRD患者具有“傳統(tǒng)的”和“非傳統(tǒng)的”心血管不良事件危險(xiǎn)因素,“傳統(tǒng)的”危險(xiǎn)因素包括高血壓、糖尿病、高齡、高脂血癥等[12],“非傳統(tǒng)的”危險(xiǎn)因素包括血管鈣化、炎性反應(yīng)、鈣磷代謝紊亂等[13]。

表1 ESRD合并SHPT患者發(fā)生CAC的單因素分析
注:ESRD為終末期腎病,SHPT為繼發(fā)性甲狀旁腺功能亢進(jìn),CAC為冠狀動(dòng)脈鈣化,iPTH為甲狀腺旁腺激素

表2 ESRD合并SHPT患者發(fā)生CAC的多因素Logistic回歸分析
注:ESRD為終末期腎病,SHPT為繼發(fā)性甲狀旁腺功能亢進(jìn),CAC為冠狀動(dòng)脈鈣化,iPTH為甲狀腺旁腺激素

表3 300例ESRD合并SHPT患者隨訪(fǎng)不同時(shí)間點(diǎn)相關(guān)指標(biāo)變化
注:ESRD為終末期腎病,SHPT為繼發(fā)性甲狀旁腺功能亢進(jìn),CAC為冠狀動(dòng)脈鈣化,iPTH為甲狀腺旁腺激素;與術(shù)前比較,aP<0.05;與術(shù)后6個(gè)月比較,cP<0.05
在ESRD患者中發(fā)現(xiàn)CAC的現(xiàn)象較為常見(jiàn),CAC可引起心律失常、心肌缺血、心肌梗死等不良心血管事件的發(fā)生,也是引起ESRD患者死亡的重要因素[14-15]。CAC發(fā)生是多種因素共同作用結(jié)果,本研究結(jié)果顯示,透析時(shí)間長(zhǎng)、CAC積分高是影響ESRD合并SHPT患者發(fā)生CAC的獨(dú)立危險(xiǎn)因素。近20年,在國(guó)外30項(xiàng)有關(guān)軟組織鈣化臨床研究中發(fā)現(xiàn)ESRD患者發(fā)生血管鈣化主要與透析持續(xù)時(shí)間、年齡大相關(guān)[16]。還有相關(guān)研究發(fā)現(xiàn),透析時(shí)間是引起CAC發(fā)生的獨(dú)立危險(xiǎn)因素[17-19],本研究結(jié)果也與之相符。CAC積分越高發(fā)生不良心血管事件的危險(xiǎn)性越大,冠心病患者CAC積分明顯高于正常人[20]。在關(guān)于心血管疾病危險(xiǎn)性和CAC積分相關(guān)性研究中,CAC積分越高心肌梗死、心絞痛發(fā)生率也越高,預(yù)后也越差[21],也符合本研究結(jié)果。
在歐洲慢性腎臟病骨代謝及其疾病臨床實(shí)踐中建議對(duì)于難治性SHPT或合并高鈣、高磷血癥的ESRD合并SHPT患者可行甲狀旁腺切除術(shù)治療,可有效地改善患者生活質(zhì)量[22]。本研究結(jié)果顯示,術(shù)后6和12個(gè)月,血鈣、血磷、鈣磷乘積、甘油三酯、iPTH水平及CAC積分均低于術(shù)前,其中iPTH水平及CAC積分在術(shù)后12個(gè)月達(dá)到最低。符合既往黃瑩等[23]的研究結(jié)果。安全有效的手術(shù)可使ESRD合并SHPT患者iPTH水平快速下降至正常,從而緩解因iPTH引起的相關(guān)臨床癥狀及死亡率[24-25]。
綜上所述,甲狀旁腺切除術(shù)可有效地改善ESRD合并SHPT患者鈣磷代謝紊亂、降低iPTH水平,抑制CAC進(jìn)展。
[參考文獻(xiàn)]
[1] 闞森,張倩,王夢(mèng)婧,等.甲狀旁腺切除術(shù)對(duì)血液透析患者冠狀動(dòng)脈鈣化進(jìn)展的影響[J].中國(guó)血液凈化,2015,14(7):408-411.
[2] 薛玉仿,郝麗,王德光,等.甲狀旁腺全切并自體前臂移植術(shù)對(duì)難治性繼發(fā)性甲狀旁腺功能亢進(jìn)患者骨代謝的影響[J].安徽醫(yī)科大學(xué)學(xué)報(bào),2015,50(7):1008-1011.
[3] 張衡.甲狀旁腺切除術(shù)后并發(fā)癥原因分析及護(hù)理對(duì)策[J].中國(guó)血液凈化,2017,16(3):211-213.
[4] 羅麗花,管保章,黃盛玲,等.維持性血液透析患者鈣磷代謝紊亂治療進(jìn)展[J].臨床腎臟病雜志,2015,15(9):567-570.
[5] 侯終君.高通量血液透析對(duì)血清β2-微球蛋白和甲狀旁腺激素的影響[J].中國(guó)實(shí)驗(yàn)診斷學(xué),2015,19(3):444-446.
[6] 曹娟,趙彩霞,李海濤,等.甲狀旁腺切除術(shù)治療尿毒癥繼發(fā)性甲狀旁腺功能亢進(jìn)的療效觀(guān)察[J].實(shí)用臨床醫(yī)藥雜志,2015,19(21):200-201,210.
[7] 王喆,魏芳,陳海燕,等.西那卡塞對(duì)終末期腎病患者繼發(fā)性甲狀旁腺功能亢進(jìn)影響的Meta分析[J].天津醫(yī)藥,2016,44(5):642-648.
[8] Neves P D, Bridi R A, Elias R M,etal. Coronary artery calcification seen through chest radiography[J].J Clin Med Res, 2015,7(9):724-725.
[9] 程晨,張麗娜,王寧寧,等.超聲引導(dǎo)下微創(chuàng)治療嚴(yán)重繼發(fā)性甲狀旁腺功能亢進(jìn)癥[J].中華骨質(zhì)疏松和骨礦鹽疾病雜志,2016,9(4):428-433.
[10] 王妍妮,楊小娟,劉延,等.成纖維細(xì)胞生長(zhǎng)因子23(FGF23)在終末期腎病患者繼發(fā)性甲狀旁腺功能亢進(jìn)中的作用[J].現(xiàn)代生物醫(yī)學(xué)進(jìn)展,2016,16(32):6336-6338,6289.
[11] 于嬋媛,王紅月,劉麗,等.尿毒癥繼發(fā)性甲狀旁腺功能亢進(jìn)的發(fā)病機(jī)制及治療研究進(jìn)展[J].國(guó)際泌尿系統(tǒng)雜志,2017,37(3):467-470.
[12] 賈鴻雁,張曉蕾,劉景峰,等.早期慢性腎臟病患者社區(qū)-家庭-自我管理的效果觀(guān)察[J].山西醫(yī)藥雜志,2015,44(7):828-830.
[13] 段麗萍,鄭朝霞,胡天曉.邯鄲地區(qū)應(yīng)用生理鈣透析液對(duì)持續(xù)性腹膜透析患者鈣磷代謝的影響[J].臨床腎臟病雜志,2016,16(4):228-231.
[14] 陳續(xù)紅,劉帝,劉燁歆,等.維持性血液透析患者鈣磷代謝紊亂的影響因素及其與腎性貧血的相關(guān)性[J].臨床腎臟病雜志,2016,16(12):728-733.
[15] 邢昌贏,沈冬云.慢性腎臟病患者骨-礦物質(zhì)代謝異常的診斷與治療[J].中華全科醫(yī)學(xué),2015,13(7):1040-1041.
[16] 吳美軍,葉麗萍,郝麗,等.單中心維持性血液透析患者的鈣磷代謝調(diào)查[J].臨床腎臟病雜志,2015,15(3):155-160.
[17] 黃琳,于暢,王曉中,等.尿毒清顆粒對(duì)老年腹膜透析患者透析充分性及營(yíng)養(yǎng)狀態(tài)效果分析[J].中國(guó)中西醫(yī)結(jié)合腎病雜志,2015,16(10):886-888.
[18] Jing Y, Zhao H, Ge Y,etal. Application of total parathyroidectomy with auto-transplantation for uremia secondary hyperparathyroidism treatment[J].Int J Cli Exp Med, 2015,8(7):11188-11194.
[19] 李懷魚(yú),楊軍,王振興,等.血液透析患者血清中骨硬化蛋白和DKK1蛋白表達(dá)與腹主動(dòng)脈鈣化程度的相關(guān)性分析[J].中國(guó)藥物與臨床,2017,17(1):79-81.
[20] 崔杰,董勤,葉春林,等.醋酸鈣聯(lián)合低鈣透析液對(duì)老年高鈣、高磷腹膜透析患者鈣磷代謝和左心功能的影響[J].上海醫(yī)學(xué),2016,39(5):306-308.
[21] 賈英民,霍延紅,楊永紅,等.左卡尼汀治療終末期腎病維持性血液透析患者心功能不全的臨床效果[J].中國(guó)醫(yī)藥,2015,10(10):1499-1501.
[22] 袁戎,楊瑩,彭輝,等.甲狀旁腺素與2型糖尿病腎臟病相關(guān)性研究進(jìn)展[J].臨床腎臟病雜志,2016,16(9):567-570.
[23] 黃瑩,肖龍,梁劍波,等.甲狀旁腺切除對(duì)終末期腎病并繼發(fā)性甲旁亢患者鈣磷代謝的影響[J].廣州醫(yī)科大學(xué)學(xué)報(bào),2017,45(2):45-48.
[24] Dural C, Okoh A K, Sinziana A,etal. A pilot study investigating the effect of parathyroidectomy on arterial stiffness and coronary artery calcification in patients with primary hyperparathyroidism[J].Surgery, 2016,159(1):218-224.
[25] 柳詩(shī)意,張寧,劉世巍,等.慢性腎臟病血管鈣化機(jī)制研究進(jìn)展及中醫(yī)藥研究概況[J].中國(guó)中西醫(yī)結(jié)合腎病雜志,2015,16(4):352-356.
- 解放軍醫(yī)藥雜志的其它文章
- 丙泊酚和七氟烷麻醉對(duì)老年胸外科手術(shù)患者術(shù)后認(rèn)知功能的影響
- 帕瑞昔布鈉超前鎮(zhèn)痛對(duì)老年髖骨骨折患者術(shù)后應(yīng)激反應(yīng)、鎮(zhèn)痛和譫妄的影響
- 高劑量纈沙坦治療慢性腎小球腎炎合并高血壓的臨床效果及對(duì)TGF-β1、MMP-9和TIMP-1的影響
- 前列地爾聯(lián)合高壓氧治療糖尿病周?chē)窠?jīng)病變的臨床效果觀(guān)察
- 間苯三酚對(duì)腸易激綜合征患者腸道痙攣的應(yīng)用分析
- 布地奈德/福莫特羅治療咳嗽變異性哮喘的臨床效果及對(duì)血清IL-4、TNF-α的影響

