新型陽離子光固化活性單體3,3-[氧基雙亞甲基]-雙[3-甲基]氧雜環丁烷的合成
蘇建宇,汪魯焱,鄭怡倩,劉 敏,卜凡樂,劉安昌
新型反應器與綠色化學工藝湖北省重點實驗室(武漢工程大學),湖北 武漢 430205
如今,隨著污染問題的日益嚴重,環保問題越來越被重視,開發實用的工業化轉化的環保工藝成為當今的重要考慮問題。傳統的固化技術是用電子束固化設備,由于設備復雜、成本較高而且可見光固化的材料難以保存,所以開發一種新型光固化技術和材料尤為必要。氧雜環丁烷是一類四元環醚的化合物,包括單官能團氧雜環丁烷、雙官能團氧雜環丁烷以及改性氧雜環丁烷,在UV下可進行陽離子開環聚合,且這類化合物黏度低,固化后膜的附著力高,固化收縮率小、固化速率快、毒性低、不易揮發,合成過程較簡單,高效節能,適用性廣等優勢越來越受到人類的青睞,吸引了眾多科研者的興趣[1-3]。
3,3-[氧基雙亞甲基]-雙[3-甲基]氧雜環丁烷是近年來應用廣泛的陽離子光固化活性單體,其合成方法國內還沒有報道,目前文獻報道的合成方法由3-甲基-3-氯甲基氧雜環丁烷與3-甲基-3-羥甲基氧雜環丁烷醚化而制得,該工藝在制備3-甲基-3-氯甲基氧雜環丁烷時需要使用昂貴的氯化鋰,我們在文獻[4-15]的基礎上,對3,3-(氧基雙亞甲基)-雙-(3-甲基)氧雜環丁烷的合成工藝進行了改進。本工作是以三羥甲基乙烷和碳酸二甲酯為原料經環化裂解生成3-甲基-3-羥甲基氧雜環丁烷。然后與磺酰化試劑對甲苯磺酰氯反應,得到3-甲基-3-(對甲基苯磺酸氧基甲基)氧雜環丁烷,在堿性條件下,3-甲基-3-(對甲基苯磺酸氧基甲基)氧雜環丁烷與3-甲基-3-羥甲基氧雜環丁烷醚化得到目的產物3,3-[氧基雙亞甲基]-雙[3-甲基]氧雜環丁烷。該工藝縮短了合成路線,省去了中間體3-甲基-3-氯甲基氧雜環丁烷的合成步驟,所用原料易得,工藝簡單,無需格外精制,可滿足3,3-[氧基雙亞甲基]-雙[3-甲基]氧雜環丁烷的大規模工業化生產的需要。其合成路線如下:
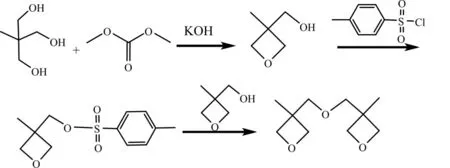
1 實驗部分
1.1 試劑和儀器
三羥甲基乙烷(山西科頂化學試劑,分析純);碳酸二甲酯(國藥集團化學試劑有限公司,化學純);對甲苯磺酰氯(上海麥克林生化科技有限公司,化學純);氫化鈉(質量分數60%,南京化學試劑股份有限公司),其它試劑均為化學純。
日本島津IR-408型紅外分光光度計(KBr壓片);UNI-TY-400核磁共振儀(瑞士BrukerA?vance)。
1.2 3-甲基-3-羥甲基氧雜環丁烷的合成
在裝溫度計、攪拌器和蒸餾裝置的1 000 mL的三口反應瓶中,加入192 g(1.6 mol)三羥甲基乙烷,201.6 g(2.24 mol)的碳酸二甲酯,再加入 3 g氫氧化鉀用少量的甲醇做溶劑,加熱至頂部溫度62℃~64℃,反應5 h~6 h,至無甲醇餾出,拆掉蒸餾裝置,升溫至158℃~170℃,進行裂解反應,此時有大量的二氧化碳放出。當二氧化碳氣泡明顯減少時,裂解基本完畢,減壓蒸餾,收集84℃~86℃及400 Pa條件的餾分130.2 g,收率79.7%高于文獻[2]收率 77%。
1.3 3-甲基-3-(對甲基苯磺酸氧基甲基)氧雜環丁烷的合成
在裝有溫度計、攪拌器和滴液漏斗的500 mL的三口反應瓶中,加入 42.8 g(0.42 mol)的 3-甲基-3-羥甲基氧雜環丁烷,64.5 g(0.63 mol)三乙胺和150 mL二氯甲烷,冷卻至-5℃~0℃,在0℃以下滴加103.7 g(0.55 mol)對甲苯磺酰氯的50 mL二氯甲烷溶液。滴加完畢,升至室溫繼續反應16 h。加入250 mL蒸餾水至反應瓶中,分層,水層用80 mL的二氯甲烷萃取2次,合并有機層,用80 mL的5%稀鹽酸洗滌,然后用80 mL的質量分數5%碳酸氫鈉水溶液洗滌3次,再用蒸餾水洗至中性,濃縮得棕紅色液體,放置變成固體。用25 mL四氫呋喃和75 mL正己烷的混合溶劑重結晶,得到96.4 g白色針狀結晶,熔點為61℃~62℃,收率89%高于文獻[5]收率75%。
1.4 3-(氧基雙亞甲基)-雙-(3-甲基)氧雜環丁烷的合成
在裝溫度計、攪拌器和回流冷凝管的500 mL的三口反應瓶中,將13 g(0.33 mol)質量分數60%的氫化鈉分散于250 mL DMF中,在0℃以下滴加33.2 g(0.33 mol)的3-甲基-3-羥甲基氧雜環丁烷,滴加時間不低于45 min,繼續攪拌1 h,直到不再有氫氣放出為止,然后滴加64 g(0.25 mol)溶于50 mL DMF中的3-甲基-3-(對甲基苯磺酸氧基甲基)氧雜環丁烷溶液。滴完后升溫至100℃下繼續反應64 h。減壓蒸出大部分溶劑,然后冷卻,倒入500 mL的冰水中,用150 mL的二氯甲烷萃取3次,合并有機層,用150 mL蒸餾水洗3次,濃縮得淡黃色液體,減壓蒸餾,收集(110℃~112℃)/400 Pa的餾分34.8 g的無色油狀物,收率75.0%與文獻[8]相同。
2 結果與討論
2.1 3-(氧基雙亞甲基)-雙-(3-甲基)氧雜環丁烷的紅外吸收和核磁共振譜圖
采用溴化鉀壓片,將少量樣品涂抹于壓片上烘干,進行紅外光譜吸收測試,見圖1(a)。
從圖中可知2 958 cm-1,2 868 cm-1分別是CH3中C-H鍵的反對稱伸縮振動吸收峰;1 457 cm-1,1 378 cm-1分別是C-H的反對稱變形振動峰和對稱變形振動峰;1 112 cm-1為非四圓環主鏈中C-O-C的伸縮振動峰,1 038 cm-1為氧雜環丁烷四元環的特征峰,主要結構紅外中均有體現,結構基本一致。
圖1(b)為目標產物400 MHz的核磁共振氫譜圖,溶劑為 CDCl3,化學位移δ:1.208(6H,CH3),3.425(4H,CH2O),4.2(4H,CH2,ring),4.4(4H,CH2,ring)共18個H,參照標準譜圖,結構一致。
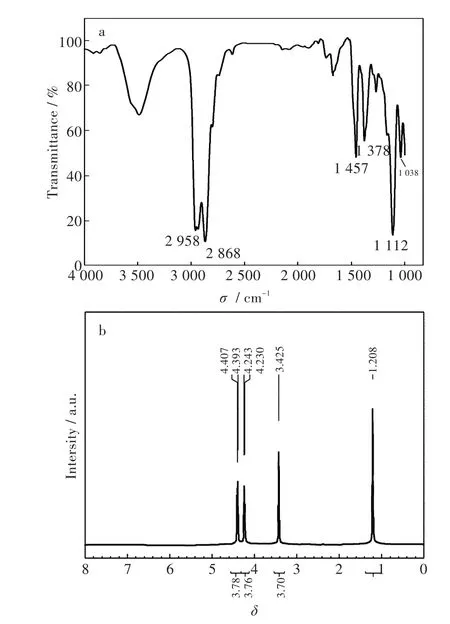
圖1 3-(氧基雙亞甲基)-雙-(3-甲基)氧雜環丁烷:(a)紅外吸收譜圖和(b)核磁共振氫譜譜圖Fig.1 Spectra of(a)IR and(b)1HNMR of bis(3-methyloxetan-3-yl)methyl ether
3-甲基-3-羥甲基氧雜環丁烷的合成過程分兩個階段進行,環化和裂解如下所示:
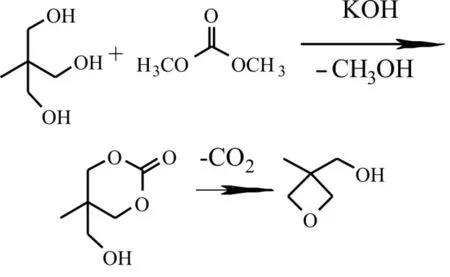
從反應機理中可以得知,蒸餾出副產物甲醇可以促進酯交換向正反應方向移動,而原料碳酸二甲酯容易和甲醇形成共沸物一起被蒸出,所以碳酸二甲酯應該過量。此外,通過安裝精餾柱控制共沸物回流比可以減少碳酸二甲酯的損失,從而提高反應收率。裂解需要在高溫的條件下脫去二氧化碳完成,再通過減壓蒸餾,可以直接得到產物,在此過程中我們發現蒸出產物的后期會有大量白色固體吸附于蒸餾裝置上,文獻報道該白色固體為原料三羥甲基乙烷升華所致,所以蒸出產物時壓力應該盡量減小,從而降低出料溫度,減小三羥甲基乙烷的損失。
在合成3-甲基-3-(對甲基苯磺酸氧基甲基)氧雜環丁烷的過程中,所采用對甲苯磺酰氯為反應試劑,引入對甲苯磺酰基,該基團是較好的離去基團,為后續反應的順利進行提供了可靠的保證。
在 3-(氧基雙亞甲基)-雙-(3-甲基)氧雜環丁烷的合成過程中,采用堿金屬氫氧化物或堿金屬氫化物與3-甲基-3-羥甲基氧雜環丁烷的羥基反應,拔掉羥基上的氫離子,形成氧負離子,和含有磺酰基的離去基團的3-甲基-3-(對甲基苯磺酸氧基甲基)氧雜環丁烷反應,脫掉對甲苯磺酰基得到目標產物,但該實驗反應過程較長,需要64 h才能完成,原因有可能是反應過程中生成了大量的鹽使攪拌難以進行。
3 結 語
以三羥甲基乙烷和碳酸二甲酯為原料,經環化裂解生成3-甲基-3-羥甲基氧雜環丁烷。然后經磺酰化,得到3-甲基-3-(對甲基苯磺酸氧基甲基)氧雜環丁烷,在堿性條件下與3-甲基-3-羥甲基氧雜環丁烷醚化得到目的產物3,3-[氧基雙亞甲基]-雙[3-甲基]氧雜環丁烷。該方法收率較高,合成路線短,省去了中間體3-甲基-3-氯甲基氧雜環丁烷的合成步驟,直接醚化得到目標產物,產物經紅外光譜和核磁共振譜得到確證,具有工業化應用價值。
[1]MASAKI K.Active energy ray curable resin composition with low viscosity foropticalstereolithography for forming a cured product with excellent curability,Young's modulus, swelling degree, warpage and surface smoothnessofa three-dimensionalobject:JP 2018058978[P].2018-04-12.
[2]DAEWON L,YOUNGo-WOO L,HYEON-GYUN I,et al.Bioinspired transparent laminated composite film for flexible green optoelectronics[J].Applied Materials&Interfaces,2017,9(28),24161-24168.
[3]鄧沖,謝王付,黃筆武,等.氧雜環丁烷/丙烯酸酯混合體系的光固化性能研究[D].南昌:南昌大學,2014.
[4]ZHDANKO A G,NENAJDENK O V G.Nonracemizable Isocyanoacetates for multicomponent reactions[J].Journal of Organic Chemistry,2009 ,74(2):884-887.
[5]JONAS M ,TIM B.Synthesis and polymerization of alkyl halide-functional cyclic carbonates[J].Polymer,2011,52(25):5716-5722.
[6]ULF A ,NICOLA R.Process for production of an oxetane by cyclization of a polyhydric alcohol:WO2000035895[P].2000-06-22.
[7]SANIAY K.Preparation ofphenylalkanoic acid derivativesasGPR agonists:WO2013128378 [P].2013-09-06.
[8]NOBUYUKI N.Optimization of(2,3-dihydro-1-benzofuran-3-yl)acetic acids:discovery of a non-free fatty acid-like,highly bioavailable g protein-coupled receptor 40/free fatty acid receptor 1 agonist as a glucose-dependent insulinotropic agent[J].Journal of Medicinal Chemistry,2012,55(8):3960-3974.
[9]OLIVIER B.Preparation oftriazole compoundsas T-type calcium channel blockers[P].World patent,WO2016041892,2016-5-24.
[10]JOHANNES D, SIW B F.Synthesis of branched polyether ligands designed for selective complexation of small cations[J].Acta Chemica Scandinavica,1992,46(3):271-7.
[11]THOMAS G A ,ROLAND P C,ASLAM A M,et al.Preparation and polymerization of initiators containing multiple oxetane rings for preparation of star polymers:US5362848[P].1994-11-8.
[12]劉安昌,夏強,張良,等.陽離子光固化活性單體氧雜環丁烷的合成[J].武漢工程大學學報,2010,32(9):14-16.
[13]TAKEHIKO S, HISATO N.Cation-polymerizable compositions with good curability and low viscosity,recorded articles and image formation using the same,their ink sets for ink-jet printing,and ink-jet printing method:JP 2008031316[P].2008-02-14.
[14]ALFRED B,EDWIN T.UV or EB curing screen printing inks containing a high amount of renewable/sustainable material :WO 2010012818[P].2010-02-04.
[15]ALFRED B,EDWIN T.Uv or eb curing screen printing inks containing a high amount of renewable/sustainable material:US 8419847[P].2013-04-16.

