鐵屑用于電鍍污泥減量工藝優化研究
羅 文
(太原市環境科學研究院, 山西 太原 030002)
電鍍行業為國內外各行各業服務,是不可或缺的產業。一般而言,電鍍行業屬于勞動密集型企業,在電鍍過程中,會產生大量的廢水,且電鍍廢水水質復雜,廢水中含有各種有毒有害物質,因此,電鍍行業被認為是當今全球三大污染工業之一[1]。我國電鍍企業的主要特征為耗能高、排污量大、產品附加值低,據不完全統計,全國電鍍廢水總排量已經達到80×109t。我國電鍍廢水主要來源于鍍件清洗水、堿性除油液等,主要污染物質為重金屬離子,如鉻、鎳、銅等,這些有毒有害物質不僅會污染環境,還可以以空氣、水體、食物等為介質,危害人類健康。目前我國電鍍行業正在不斷開拓新技術、新工藝[2],研究新的電鍍廢水處理工藝,以減少其對環境的污染和對人類的危害。
電鍍污泥是電鍍行業中廢水處理過程中產生的沉淀物,這些重金屬污泥成分復雜,很難處理和利用[3],被列入國家危險廢物名單中的第十七類危險廢物。為此,對于電鍍廢水處理尤其對于電鍍污泥的優化處理對電鍍行業發展及人類生存環境的保護具有重要的意義。
1 試驗材料與方法
1.1 試驗用水
選擇某電鍍工業園廢水為研究對象,經長期調研與檢測,其水質如表1所示。
1.2 試驗主要藥劑及儀器與設備
本試驗中用到的主要試劑為:濃硫酸,98%;聚丙烯酰胺(PAM),粉末狀;次氯酸鈉溶液,10%;高錳酸鉀,分析純;過氧化氫,27.5%;重鉻酸鉀,分析純;丙酮,分析純;氫氧化鈉,分析純;七水合硫酸亞鐵,分析純;硫化鈉,分析純。

表1 試驗用水水質
試驗中用到的主要試驗儀器設備有:COD消解儀,DR200,青島明博環保科技有限公司;電子天平,JA2003N,上海精科天美儀器有限公司;pH計,PHS-25,上海精密科學儀器有限公司;原子吸收分光光度計,日立Z-2000,日立高科技貿易(上海)有限公司;氣泵,海利ACO-308AC交流電磁式空氣壓縮機;混凝試驗攪拌機,ZR4-6,上海標卓科學儀器有限公司;曝氣生物濾池,Φ250 mm×1 800 mm,山東濰坊譽德環保科技有限公司。
1.3 試驗方法與原理
據調研顯示,多數研究者對酸性電鍍廢水的處理采用投入石灰以提高廢水的pH,加入硫酸亞鐵引進具有還原作用的Fe2+,但硫酸亞鐵中含有硫酸根等雜質與石灰易生成硫酸鈣,增加了廢水在后續處理過程中結垢的風險。
本試驗主要以廢水pH與Cr6+體積分數為研究對象,由于Fe2+是還原Cr6+的真正起作用的部分,加之原水為酸性廢水,因此可直接采用鐵屑與酸性廢水反應,不僅可以消耗H+,提高廢水的pH,生成可以還原Cr6+的Fe2+,還可減少因硫酸亞鐵的投入而帶來的硫酸根及為調高pH所投入的石灰量,最終減少污泥量。
1.3 檢測項目和測試分析方法
本試驗檢測項目均采用標準分析方法,具體如表2所示。

表2 試驗主要檢測項目及分析方法
2 試探性基礎試驗
試探性試驗步驟如下:首先,將100 g鐵屑投入5 L酸性廢水中,并對其進行攪拌,使之充分反應,同時每隔3 h測廢水pH值的變化,并記錄pH值;其次,在鐵屑與原酸性廢水充分反應,也就是廢水pH值穩定后,記下穩定后的pH值;第三,將含鉻廢水分別與1倍、2倍、3倍、4倍、5倍、6倍及7倍體積的經鐵屑充分反應pH值穩定后的酸性廢水混合;最后,比較原含鉻廢水(未混合酸性廢水)及含鉻廢水與1倍、2倍、3倍、4倍、5倍、6倍及7倍體積的酸性廢水混合廢水的鉻離子的剩余含量,考察混合后對鉻離子的去除情況。
2.1 pH值變化結果
100 g鐵屑投入5 L酸性廢水中,廢水pH值的變化如圖1所示。

圖1 加入鐵屑后原廢水pH值隨時間變化
由圖1可知,酸性廢水初始pH值為2.5,加入鐵屑經過反應穩定后的pH值約為5.5。具體的,在加入鐵屑的0~24 h之內,隨著時間的推移及反應的不斷進行,廢水的pH值不斷升高,且基本呈線性關系;而當廢水pH值在反應進行24 h時,pH值達到5.5左右,之后,隨著時間的延長,酸性廢水pH值保持穩定,變化不大。可能是因為鐵屑被氧化需要一定的時間,當反應24 h后,鐵屑被完全氧化為Fe2+,不再消耗H+,因此,24 h之后,酸性廢水pH值保持穩定。
2.2 鉻離子含量變化結果
不同體積比的經鐵屑處理后的酸性廢水與含鉻廢水混合后的鉻離子含量變化結果如圖2所示。

圖2 含鉻廢水與加鐵屑后酸性廢水不同體積比混合后鉻含量
由圖2可知,隨著V含鉻廢水與V酸性廢水之比的逐漸減小,即V酸性廢水的不斷增大,混合液中鉻含量逐漸降低,在體積比小于1∶5時,在V酸性廢水大于5份時,廢水鉻含量達到國家排放標準。具體的,當V含鉻廢水∶V酸性廢水為 1∶1~1∶3 之間時,隨著體積比的逐漸減小,鉻含量的下降幅度最大;當體積比小于1∶3時,隨著體積比的逐漸減小,鉻離子剩余含量下降緩慢,最后基本保持不變。同時,在體積比小于1∶4時,即V酸性廢水大于4份之后,總鉻與六價鉻離子濃度趨于一致。
3 系統性優化試驗
3.1 pH值和Fe2+隨反應時間的變化規律
由試探性基礎試驗結果可知,直接采用鐵屑與酸性廢水反應,確實可以提高廢水的pH,并降低鉻含量,試驗思路可行。而為了進一步明確試驗條件,提高鐵屑對鉻的去除率,本試驗對pH值和Fe2+隨反應時間的變化規律作了研究。即,取25 L酸性廢水,將其平均分成5份,并將pH值分別調至1、2、3、4、5,之后將5份200 g的鐵屑分別投入不同pH值的廢水中,測量和記錄pH值和Fe2+隨反應時間的變化規律,結果如圖2、圖3所示。

圖3 不同初始pH值的酸性廢水加入鐵屑后pH值變化規律
圖3表明,水樣pH值都是隨著時間的延長先快速增加,后趨于平穩,且當初始pH值越大,趨穩后越廢水pH值接近中性,但廢水初始pH值對趨穩后pH值影響差距較小,結果不大。圖4顯示,初始pH值為1時,Fe2+產生最快,產生量也最大,具體的,在前 10 h 之內 ρ(Fe2+)迅速躍升到 425 mg/L,而初始pH值為2、3、4、5時,Fe2+產生速度及產生量明顯不及初始pH值為1時的情況。原因可能是由于初始pH值越大,生成的Fe2+較少,部分Fe2+被空氣氧化為Fe3+的緣故。

圖4 不同初始pH值的酸性廢水加入鐵屑后Fe2+變化規律
3.2 鉻離子的去除對比試驗
由3.1試驗結果可知,初始pH值為1時,水樣pH的提升和產生Fe2+的綜合效果最好,為此,將其與含鉻廢水以不同的體積比混合,測定鉻的剩余含量,結果如表3所示。同時,將本試驗結果與不同投加量的硫酸亞鐵對鉻離子的去除效果(如表4所示)作對比。
由表3和表4可知,總體而言,加鐵屑后酸性廢水混合反應對鉻離子的去除效果要好于加硫酸亞鐵對鉻離子的去除效果,且達到相同去除率的加鐵屑后酸性廢水混合反應的石灰投加量也遠遠小于加硫酸亞鐵反應的,也就是說鐵屑與酸性廢水的混合反應能大大減少污泥量。
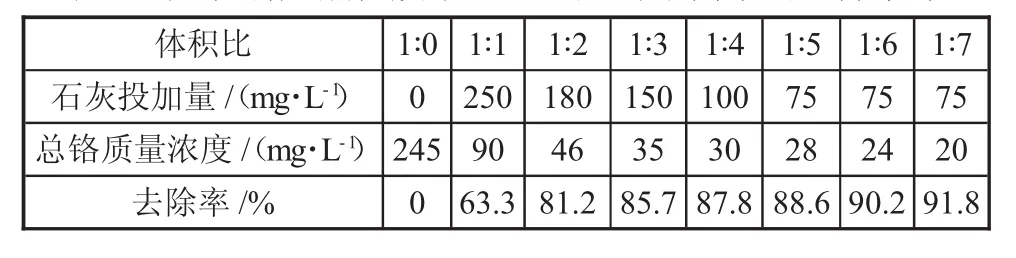
表3 加鐵屑后酸性廢水混合反應對鉻離子的去除效果

表4 加硫酸亞鐵對鉻離子的去除效果
4 結語
現階段,電鍍重金屬污泥的處置方法主要有水泥、鐵氧體固化,填海或焚燒等。而本試驗證明,在電鍍廢水處理中可以在酸性廢水池中投入一定量的鐵屑,在提高pH值,產生亞鐵離子之后,收集電鍍廢水中的酸性廢水,并以逆流的形式將其向上進水,通入含鉻等原水池中進行混合,以達到降低鉻等含量,和減少電鍍廢水處理所產生的污泥量的效果,降低廢水處理成本。
[1]Ying Xu,Tianyi Xu.Heavy Metal Complexes Wastewater Treatment with Chelation[J].Precipitation,2008(2):2 789-2 793.
[2]郁祖湛.電子電鍍中若干新工藝和新技術[J].電鍍與涂飾,2006,25(9):4-7.
[3]彭昌盛,盧壽慈,徐玉琴,等.電鍍廢水處理過程中的二次污染[J].電鍍與涂飾,2002,21(2):41-43.

