磷尾礦循環酸浸試驗的研究
楊 成,李 防,潘志權,張華麗*
1.武漢工程大學化學與環境工程學院,湖北 武漢 430205;2.湖北興發化工集團股份有限公司,湖北 宜昌 443000
我國磷礦資源儲量豐富,但約80%以上為中低品位磷礦[1],為了滿足優質磷酸和濃度高的磷肥生產需求,必須經過選礦富集后才能加以利用[2]。浮選工藝原理表明,磷礦經浮選后會產生大量的尾礦,其中質量分數w(MgO)≥15%,w(P2O5)≤10%[3]。目前這些尾礦的隨意堆放,不僅會浪費資源,并且會造成環境污染[4],因此,對磷礦資源的二次開發綜合利用極其重要[5]。綜合開發利用磷尾礦中的有用成分不僅能改善生態環境和可持續利用資源,而且能產生巨大的經濟和社會效益[6]。
黃芳等[7]對磷礦浮選尾礦在硫酸中的酸解行為進行了研究。黃芳等[8]對磷尾礦的酸解動力學過程介微觀現象進行了研究,解釋了硫酸酸解過程的反應機理。趙琦[9]以高鎂磷尾礦為研究對象,對其進行新藥劑再浮選,得到了品位為19.06%、回收率為91.19%的鎂精礦。吳夢[10]以磷尾礦為原料,采用氨水沉淀法制備納米氫氧化鎂,團聚現象明顯,可作為添加型高效抑煙阻燃劑應用于塑料、橡膠等領域。馬會娟等[11]以磷尾礦為原料,采用工業鹽酸分解高鎂磷尾礦并制備硫酸鎂產品,制得的七水硫酸鎂產品符合國家行業一等品標準。馬會娟等[12]以磷尾礦為原料,采用循環酸浸-復鹽結晶法制備磷酸二銨,制得的磷酸二銨產品符合國家標準優等品的要求。高金鋒等[13]以改性后的鐵礦尾礦為原料,采用干壓成型方法制備出蒸壓磚;羅力等[14]以鐵尾礦、石灰石為原料制備出硅酸鹽水泥熟料;Onuaguluchi等[15]利用銅尾礦制備混凝土;Shettima等[16]對采用鐵尾礦作為細料制備混凝土的可行性進行了研究;張龍等[17]針對沙柳木粉對添加造孔劑法制備粉煤灰基多孔陶瓷的影響進行了研究等。
試驗選取湖北某地高鎂磷尾礦作為原料,對此尾礦進行物相及化學全元素分析后發現,該尾礦的主要物相為白云石[CaMg(CO3)2]和氟磷灰石[Ca5(PO4)3F],其中P2O5質量分數為8.0%,MgO為14.6%,而CaO為33.2%,可看作高鎂磷尾礦。
試驗采用工業鹽酸對高鎂磷尾礦進行酸解預處理,得到酸解濾液和渣相,對得到的渣相進行水洗,水洗液與酸解濾液混合后產生固體1,再對其固液分離后的液體進行酸化處理,酸化濾液進行濃縮產生固體2,濃縮濾液通過循環酸解使濾液中的磷和鎂得到富集[18]。
1 實驗部分
1.1 實驗原料
該磷尾礦來自于湖北某選礦企業,化學成分分析(質量分數,%)CaO,49.506;MgO,19.498;P2O5,15.992;SiO2,7.654;Al2O3,1.797;K2O,0.420;TiO2,0.186;MnO,0.110;Fe2O3,0.957;Na2O,0.116;SrO4,0.039。
用X射線衍射(X-ray diffraction,XRD)對尾礦進行物相分析,XRD檢測結果見圖1。

圖1 尾礦XRD圖譜Fig.1 XRD pattern of phosphate tailing
經圖1分析可知,該磷礦尾礦主要以白云石[CaMg(CO3)2]和氟磷灰石[Ca5(PO4)3F]等礦相組成,其質量分數分別為93.53%、6.47%。
1.2 實驗方法
取適量工業鹽酸倒入3000 mL圓底燒瓶中,系統升溫至某一溫度,用加料漏斗連續性加入一定量的磷尾礦。待加完畢反應一段時間后停止攪拌,保溫抽濾,濾餅為未參加反應的硅渣,用適量的水連續分別洗滌3次,烘干,測定硅渣的質量及其CaO,MgO和P2O5含量,計算其分解率[18]。所得濾液為酸解液,將其與礦渣一次水洗液均勻混合靜置,次日離心過濾,離心濾液測定鈣鎂磷含量后轉入2000 mL燒杯,用恒壓滴液漏斗連續緩慢滴加與鈣離子等摩爾的濃硫酸進行酸化除鈣,待濃硫酸滴加完畢后繼續反應一段時間使硫酸鈣熟化完全,停止反應靜置陳化。次日抽濾,用適量的水連續分別洗滌濾餅3次,測定石膏的質量及其CaO,MgO和P2O5質量分數,計算其夾帶率[12]。所得濾液為酸化液,與石膏一次水洗液混合后進行水平衡,過濾,測定濾液中CaO,MgO和P2O5含量,以及濾液的酸度。測量其體積,轉入3000 mL三口燒瓶中,補加工業鹽酸使混酸的氫離子總物質的量與起初酸解磷尾礦所加工業鹽酸氫離子總物質的量相等,如此循環分解,流程圖如圖2。
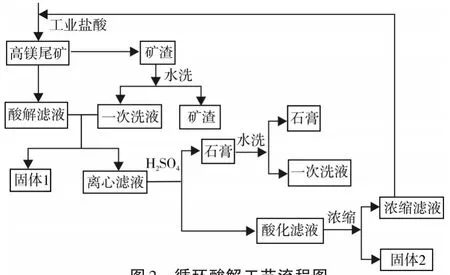
圖2 循環酸解工藝流程圖Fig.2 Process flowchart of multicyclical acid immersion
2 結果與討論
2.1 循環次數對CaO、MgO、P2O5分解率的影響
循環次數對CaO、MgO和P2O5分解率的影響的實驗結果如圖3(a)所示。
由圖3(a)可知,MgO分解率隨著循環次數的增加基本保持不變,CaO、P2O5分解率均隨著循環次數的增加先有所降低,循環到第9次后有所增加,這是因為在前8次循環的酸化過程中加入的酸的量都是根據鈣的總摩爾量加入等摩爾的濃硫酸,當鈣以硫酸鈣的形式沉淀下來后,酸化濾液中仍有部分游離的硫酸根及微溶硫酸鈣返回到下一次分解過程中,在酸解過程中,有大量的鈣離子產生,于是硫酸根與鈣離子反應產生的硫酸鈣沉淀包裹在未來的及與工業鹽酸反應的尾礦上,影響其分解過程的進行,隨著循環次數增加,鎂離子逐漸富集,濃度增加,所以每次進行下一次循環之前系統中游離的硫酸根越來越多,在酸解過程中產生的硫酸鈣沉淀也越來越多,故包裹效應越來越嚴重,因此前8次礦渣的分解率隨著循環次數的增加逐漸降低;而后進行的循環分解率又有所增加是因為在循環過程中,隨著循環的次數不斷增加,雜質含量不斷的累積,致使在第9次循環分解時,進行水平衡濃縮出來的固體最多,而導致部分硫酸鈣沉淀被帶出,硫酸鈣的包裹現象減弱[12]。總體來說,MgO分解率均達到了99%以上,循環分解效果比較好。
2.2 循環次數對酸解濾液及一次水洗液中CaO、MgO、P2O5濃度的影響
循環次數對酸解濾液及一次水洗液中CaO、MgO、P2O5濃度的影響的實驗結果如圖3(b)。
從圖3(b)中可以看出,隨著循環次數的增加,酸解濾液加一次水洗液混合液中MgO、P2O5濃度是逐漸升高的,因為高鎂磷尾礦中的CaMg(CO3)2和(Ca5(PO4)3F)隨著每次循環酸解的進行被分解,有效成分磷、鎂在酸解濾液中得到了有效富集,故檢測到P2O5、MgO濃度是逐漸升高的。酸解濾液中的CaO濃度是逐漸降低且趨于平衡的,這是因為在酸化過程中每次加入的濃硫酸的量都是根據鈣的總摩爾量加入等摩爾的濃硫酸,除鈣是徹底的,每次分解的氟磷灰石也是一定的,因此測得的CaO濃度趨于平衡。這說明循環酸浸能夠有效富集有效元素磷、鎂,硫酸除鈣徹底。
2.3 循環次數對酸化濾液及一次水洗液中CaO、MgO和P2O5濃度的影響
循環次數對酸化濾液及一次水洗液中CaO、MgO、P2O5濃度的影響的實驗結果如圖3(c)所示。
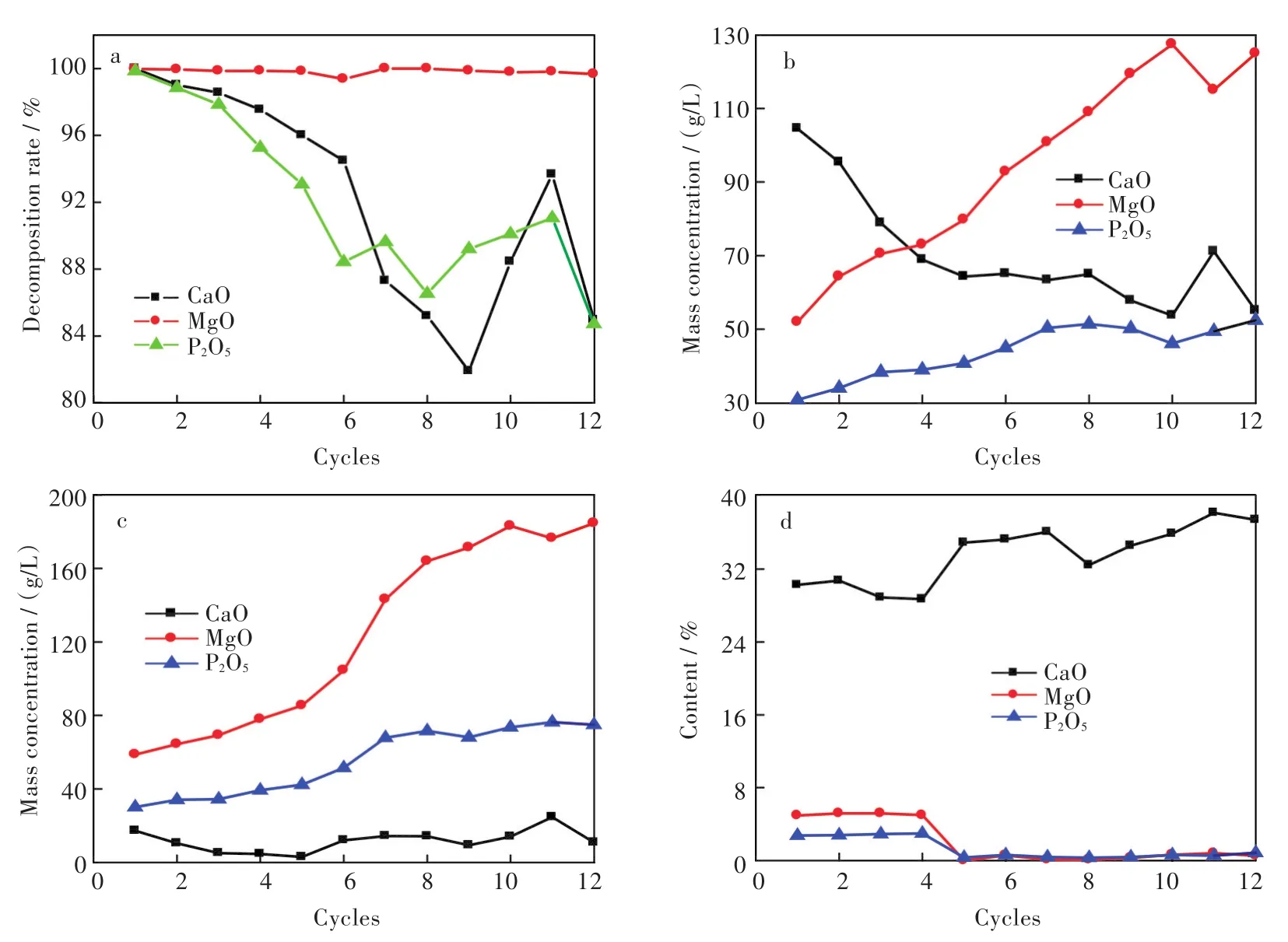
圖3 循環次數對(a)分解率,(b)酸解濾液濃度,(c)酸化濾液濃度,(d)石膏中CaO,MgO和P2O5含量的影響Fig.3 Effect of cycles on(a)decomposition rate,(b)concentration of acid solution,(c)concentration of acidizing fluid,(d)content of CaO,MgO and P2O5in gypsum
從圖3(c)可以看出,隨著循環次數的增加,酸化濾液中MgO、P2O5濃度均是逐漸增加的,并且進行第6次循環后增加的程度明顯大于前面5次循環過程增加的程度,這是因為前5次循環未加石膏一次水洗液,6次~12次循環加了石膏一次水洗液;第6次循環后,隨著循環次數的增加,增加的幅度便不大,是因為隨著循環次數的增加,酸化濾液中P2O5、MgO濃度都隨著增加,進行水平衡操作時,則會有大量的磷、鎂析出,因此后面的循環濃度增加幅度不大。CaO濃度隨著循環次數的增加,均保持在較低濃度的平衡狀態,說明在酸化除鈣過程中,除鈣操作穩定徹底。
2.4 循環次數對石膏中CaO、MgO、P2O5含量的影響
循環次數對石膏中CaO、MgO、P2O5含量的影響的實驗結果如圖3(d)。
從圖3(d)可以看出,在循環過程中,石膏中MgO、P2O5的含量隨著循環次數的增加而逐漸趨于最低平衡狀態,在第5次循環過程中,MgO、P2O5的含量突然降低,是因為前4次循環過程中未水洗石膏,在隨后的循環過程中,均水洗石膏,致使石膏中夾帶的MgO、P2O5被水洗出來,因此,石膏中的MgO、P2O5下降并趨于平衡。說明水洗石膏是必要的,可以大大降低損失。
2.5 產品的檢測
所得固體經XRD物相分析,XRD檢測結果見圖4。
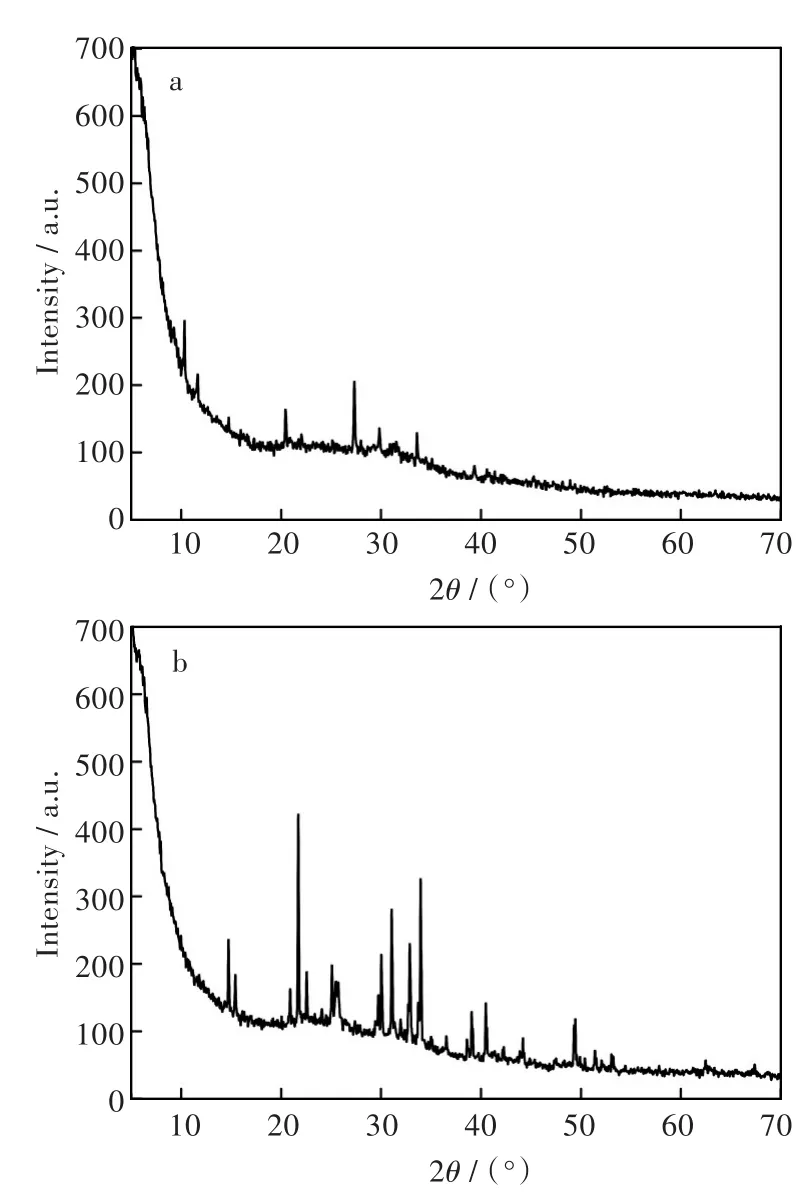
圖4 (a)固體1,(b)固體2的XRD圖譜Fig.4 XRD patterns of solids:(a)No.1,(b)No.2
所得固體經XRF全元素分析,XRF檢測結果見表1。

表1 固體化學成分分析Tab.1 Chemical compositions of solid
經圖4和表1可知,該固體1的主要物質為CaClH2PO4·H2O和 CaSO4·2H2O。固體 2的主要物質為 MgCl2和 Ca(PO3)2,還含部分 CaSO4·2H2O,MgSO4和 FeCl2等。
3 結 語
分別利用XRD、XRF對高鎂磷尾礦進行分析可知:該尾礦的主要物相為白云石[CaMg(CO3)2]和氟磷灰石[Ca5(PO4)3F],其中P2O5質量分數為8.0%,MgO為14.6%,而CaO為33.2%,可看做高鎂磷尾礦。
循環酸浸能夠有效富集有效元素磷、鎂,酸解循環過程中,酸解液加一次水洗液中MgO和P2O5分別可達到116.07 g/L和49.99 g/L,酸化液加一次水洗液中MgO和P2O5分別可達到170.37 g/L和72.06 g/L,且這些數據基本保持穩定。
固體1主要物質為CaClH2PO4·H2O以及CaSO4·2H2O,固體 2主要物質為 MgCl2和 Ca(PO3)2,此兩種物質可作為生產磷鎂肥原料或制備高端鎂系材料的原材料。

