可切除性食管癌的外科治療療效分析
付伸伸 鄭于臻
食管癌(esophageal cancer, EC)是源自食管上皮細胞異常增殖的惡性疾病。根據病理, 可分為鱗癌、腺癌及其他少見類型(小細胞癌等);根據部位, 可分為頸段、胸上段、胸中段、胸下段及胃食管交界處;根據首選治療, 可分為可切除性和不可切除性。在世界范圍內, 隨著人口老齡化及不良生活習慣的影響, 食管癌的發病率逐年增加, 其中, >50%的食管癌患者是中國人[1,2]而且治療效果不好預后較差, 已成為我國的第四大死因[3]。目前, 雖然食管癌的治療效果較過去有了很大的改善, 但總體上大部分患者仍屬不可治愈性, 自然生存期仍然較短, 其治療目標在于緩解癥狀、提高生活質量、減少復發和延長總生存時間。對于可切除性食管癌來說,仍然主張以手術治療為基礎, 并根據腫瘤分期決定是否進行多學科綜合治療。本研究旨在分析手術治療在可切除性食管癌的療效。現報告如下。
1 資料與方法
1.1 一般資料 本研究納入2001年1月1日~2011年1月1日在福建省腫瘤醫院診斷為可切除性食管癌并接受頸、胸、腹三切口外科治療317例患者的臨床資料。納入標準:①組織學診斷為可切除性食管癌;②接受頸、胸、腹三切口外科手術治療;③切緣陰性切除(R0切除) ;④沒有接受術前新輔助治療;⑤基本臨床病理資料健全。患者存在既往腫瘤病史或在診斷是并發其他腫瘤疾病被排除在外。腫瘤分期采用第7版食管癌分期系統進行。
1.2 方法 手術治療操作包括切除原發瘤和清掃淋巴結。先經右胸游離食管全段, 再經上腹切口游離胃, 制備管狀胃后, 經左頸部胸鎖乳突肌前緣斜切口游離頸段食管, 切除腫瘤后將胃上提至頸部吻合(McKeown)。所有患者均接受至少二野淋巴結清掃術, 即清掃后縱隔區及腹部淋巴結;三野淋巴結清掃術只在少數患者中開展。
通常對伴發淋巴結轉移或遠處轉移的食管癌患者開展輔助治療, 包括輔助化療或輔助放療。治療決策是基于腫瘤分期、醫生觀點、患者體制以及患者需求制定。大多情況下,輔助治療在術后4~8周內開始進行。經典化療方案是含鉑兩藥4~6個療程。術后放療包括吻合口、鎖骨上及縱隔引流淋巴結區, 總劑量約45~60 Gy。
治療結束后, 患者將在被要求在門診接受規律的隨訪,包括2年內1次/3個月, 3~5年1次/6個月, 而后1次/年。對于無法規律隨訪的患者, 采用電話隨訪或信件隨訪。隨訪檢查包括體格檢查、抽血、內鏡、胸片以及超聲檢查。頸、胸、腹CT至少檢查1次/年。
1.3 觀察指標及判定標準 分析患者的生存率及預后風險因素。總生存期(overall survival, OS):從手術到死亡或末次隨訪的時間;刪失:失訪或在末次隨訪的時間仍然存活的狀況。
1.4 統計學方法 采用SPSS22.0統計學軟件對研究數據進行統計分析。雙側檢驗且P<0.05表示差異具有統計學意義。生存率的統計采用Kaplan-Meier方法;采用單因素及多因素Cox模型確定獨立預后風險因素, 其中在單因素模型中發現P<0.05的患者被認定為具備潛在預后價值而被納入多因素模型中進行進一步的研究。多因素Cox模型采用backward方式實現變量篩選。
2 結果
2.1 臨床資料 317例患者中男244例、女73例;平均年齡(58.2±9.0)歲;清掃淋巴結個數為(32.0±15.6)枚;輔助治療在74例患者中開展, 其中有63例接受輔助化療, 7例接受輔助放療, 4例接受輔助同步放化療。T1、T2、T3、T4患者分別為30、57、225、5例;N0、N1、N2、N3患者分別為141、97、56、23例;胸上段、胸中段和胸下段腫瘤部位的患者分別為53、157、107例。見表1。
表1 317例患者的臨床資料分析(n, ±s)

表1 317例患者的臨床資料分析(n, ±s)
?
2.2 風險因素 在末次隨訪時, 有149例(47.0%)患者死亡,患者的中位生存時間為59.7個月, 1、3、5年生存率分別為83.6%、61.2%、49.8%。在單因素Cox模型中, 輔助治療、T分期和N分期均具有潛在的預后價值(P<0.05);在多因素回歸模型顯示, T分期和N分期為獨立預后風險因素(P<0.05)。見表2。
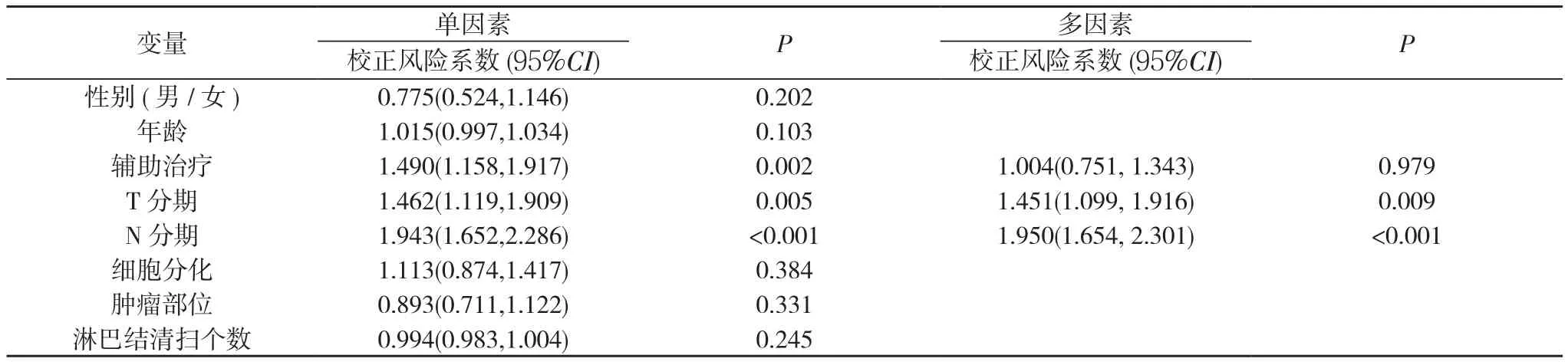
表2 單因素、多因素預后分析
3 討論
目前常用的食管癌手術有多種方案可供選擇, 包括:①內鏡下食管黏膜切除術;②傳統左胸食管癌切除術:經左胸游離食管, 開左側膈肌游離胃, 切除腫瘤后將胃上提至左胸腔/左頸部進行吻合;③右胸-上腹兩切口食管癌切除術(Ivor-Lewis):經上腹部切口游離胃, 制備管狀胃后, 經右胸游歷食管全段, 切除腫瘤后經膈肌裂孔上提至右胸腔進行吻合;④右胸-上腹-左頸三切口食管癌切除術:先經右胸游離食管全段, 再經上腹切口游離胃, 制備管狀胃后, 經左頸部胸鎖乳突肌前緣斜切口游離頸段食管, 切除腫瘤后將胃上提至頸部吻合(McKeown)。
胸段食管癌切除的手術方式有多種選擇, 相對其他開放性手術方式而言, 經左胸食管癌根治術因為對于患者創傷較小且術后生存質量較高而廣泛開展, 但也因其受限的淋巴結清掃范圍而遭受詬病。盡管有少數學者對這種手術方式提出支持, 如楊瑞森等[4]回顧性總結分析1992~2002年2058例采用左胸頸兩切口食管癌切除術的臨床資料后發現, 術后痊愈出院2025例, 臨床治愈率98.4%, 圍手術期死亡33例(1.6%), 術后3、5年生存率分別為61.22%、36.45%。但大多數文獻仍指出, 左胸食管癌切除因難以保證足夠的淋巴結清掃范圍并不適合于大部分的胸段食管癌患者。相對于左胸手術而言, McKeown術式均采用右胸+上腹部的切口, 能夠實現更加徹底淋巴及清掃, 更加符合根治術的要求, 因此越來越多地被采用作為食管癌的首選手術方案。Tan等[5]回顧性分析三切口食管癌切除術, 發現采用全縱膈二野淋巴結清掃術的胸段食管癌患者, 其5年總生存率及無瘤生存率分別為50.7%、35.3%。常規認為三切口術式創傷較大, 對心肺的干擾大于其他術式, 但從綜合療效來看, 也不失為一種較好的術式。經左頸、右胸、腹部食管癌切除術越來越多的被專家學者推薦應用, 其優點在于術野暴露清晰, 腫瘤容易被完全切除, 區域淋巴結清掃更便捷、更徹底, 適用于任何部位胸段食管癌[6]。
本研究結果顯示, 對于可手術的食管癌患者, 開展積極的三切口食管癌根治術, 搭配積極的淋巴結清掃, 可以實現良好的預后, 5年生存率近50%, 此結果與中山大學腫瘤防治中心的結果相近。
此外, 腫瘤轉移機制的更新不斷刷新著人們的認識, 食管癌逐漸被看成是一種全身性疾病, 治療也由過去單純切除逐步過渡到現在多學科綜合治療。術后化療的理論基礎主要是清除手術未及的微轉移灶, 減少腫瘤復發的幾率。相關臨床試驗最早在上世紀90年代由Pouliquen和Ando等學者提出, 但是都未能發現輔助化療的積極療效。但是值得注意的是, 在這些臨床研究中, Pouliquen入組了非R0切除的食管癌患者, Ando雖然入組R0切除患者, 但是其采用的化療方案則是在后續研究中證實對食管癌不敏感的順鉑+長春地辛方案。因此, 二十世紀以來, 后續臨床試驗在總結既往研究的基礎上, 為了更客觀地體現輔助化療的療效, 一致將入組條件設定為R0切除患者并采用了對于食管癌更加敏感的化療方案。這些結果肯定了輔助化療對于伴發淋巴結轉移的進展期食管癌的療效, 可以有效減少復發, 延長無病生存期。Ando等學者入組242例胸段食管癌患者發現, 對于那些伴發淋巴結轉移的患者, 相比單純手術而言, 輔助化療可以有效減少復發(5年無瘤生存率, 52% VS 38%, P=0.041<0.05)。但是,在改善總生存方面, 盡管近期有一系列回顧性研究暗示其在這方面的積極作用, 但仍無明確共識[7,8]。輔助放療在食管癌治療方面也無相關共識。在該研究中, 很遺憾, 也未能觀察到輔助治療在實現三切口根治性切除術的食管癌患者的額外療效。
綜上所述, 盡管放療、化療技術不斷發展, 可切除性食管癌的治療仍然是以手術治療為基礎。頸胸腹三切口食管癌切除搭配積極的淋巴結清掃有助于獲得良好的治療效果。

