流感病毒疫苗原液制備中不同品種胚蛋對原液制備的影響研究
蔡鶴鳴 徐宇虹
【摘要】目的:通過選用3種不同的胚蛋(海蘭白父母代、海蘭白商品代和京白系,其中海蘭白父母代胚蛋為對照品)進行流感病毒接種,觀察病毒在三種胚蛋中的培養(yǎng)情況,在海蘭白商品代和京白系中選出適合生產(chǎn)用的胚蛋。方法:原液的生產(chǎn)方式按照現(xiàn)行的生產(chǎn)工藝進行生產(chǎn),比較原液的蛋白含量、血凝素含量、內毒素含量等各項數(shù)據(jù)。結果:兩種實驗胚蛋的內毒素含量都低于海蘭白父母代,蛋白質含量和血凝素含量都高于海蘭白父母代。結論:兩種候選胚蛋都適合于生產(chǎn)流感病毒疫苗。
【關鍵詞】流感病毒疫苗;蛋白質;血凝素;內毒素
流行性感冒病毒,簡稱流感病毒,是有包膜的RNA病毒,屬正粘病毒科m主要通過人類談話時的飛沫、與患有流感的病人的接觸或與被流感病毒污染的物品接觸而傳播。流感病毒包括了人流感病毒和動物流感病毒,而人流感病毒根據(jù)病毒核蛋白的抗原性又可以分為甲(A)、乙(B)、丙(C)三種類型,都是流感的病原體。在流感流行期,無論成人還是兒童,通常咳嗽和發(fā)熱是患流感的基本特征[2-4],發(fā)熱一般在38-40度范圍,但可能會更高。
在前面提到的3種類型的病毒中,甲型流感病毒抗原性極其容易發(fā)生變異,因此曾引起過多次世界性的大流行.在20世紀時就爆發(fā)了三次流感大流行,分別是1918-1919年的西班牙大流感、1957-1958年的亞洲流感以及1968-1969年的香港流感。僅僅1918-1919年的”西班牙大流感”,根據(jù)歷史記載,當年全世界至少有2500-4000萬人死于這次大流行[5]。乙型流感病毒對人類也有比較強的致病性,但是到目前為止還沒有發(fā)現(xiàn)因乙型流感病毒而引起的大流行;丙型流感病毒到目前為止只引起人類輕微的上呼吸道感染,相對來說也比較穩(wěn)定,所以也就很少造成流行。由于流感病毒非常容易發(fā)生變異,導致流行反復地發(fā)生。當出現(xiàn)新毒株,人類免疫水平就會下降,WHO每年也會根據(jù)流感病毒的變異規(guī)律推薦出用于下一年疫苗生產(chǎn)用流感病毒毒株,因此每年人們都有必要來接種流感疫苗[6-8]。
在我國,目前廣泛使用的是流感病毒在雞胚尿囊腔中生長的方式來制備流感疫苗(組分包含甲1型、甲3型以及乙型病毒的三價裂解疫苗)。所以,生產(chǎn)中使用的雞胚質量如何,是否能達到各項要求就顯得十分的重要了。本人所在的公司流感疫苗生產(chǎn)所用胚蛋為海蘭白父母代,而近些年由于禽流感疫情經(jīng)常發(fā)生,所以從2013年開始國內海關禁止從國外引進活禽,何時解除禁令不得而知,2017年本公司流感疫苗生產(chǎn)用海蘭白父母代雞胚蛋將無貨供應,同時國內的公司這幾年來通過不斷的努力也研發(fā)培育出了不錯的種雞和胚蛋,所以一方面為了降低禽流感的風險,同時也為了擴大本公司流感疫苗生產(chǎn)用胚蛋品種的選擇范圍,2016年對海蘭白商品代和京白系胚蛋進行了試驗,海蘭白父母代胚蛋作為對照。經(jīng)生產(chǎn)部、質保部開會討論,選擇2016年生產(chǎn)的3批甲1型、2批甲3型、2批乙型單價病毒原液(共7批)進行變更驗證,3種胚蛋每批原液生產(chǎn)時各投入約2.5萬枚進行生產(chǎn)。生產(chǎn)過程中,試驗蛋與對照蛋嚴格分開,分別完成原液各生產(chǎn)步驟,獨立形成單價原液,對生產(chǎn)工藝各階段與胚蛋質量及產(chǎn)品得率相關的數(shù)據(jù)進行統(tǒng)計和比對。
1 材料與方法
1.1 雞胚
原液制備使用的10日齡雞胚由寧波威達龍禽業(yè)有限公司提供,由上海家禽育種有限公司孵化。
1.2 病毒
3個流行性感冒病毒毒株A/California/7/2009(甲1型)、A/Hongkong/4801/2014(甲3型)、B/Brisbane/60/2008(乙型),由英國國家生物制品檢定所(NIBSC)提供。
1.3 設備及儀器
TKA自動胚蛋接種機、TKA自動尿囊液收獲機、Millipore超濾系統(tǒng)、MettlerToledo DM40密度計、日立CP80WX超速離心機、金達HD-93-1核酸蛋白檢測儀、Beckman J6離心機。
1.4 接種
用含有最終濃度為500 9g/ml硫酸慶大霉素的0.01mol/L的PBS溶液稀釋毒種。將胚蛋放到接種機上,每胚接種病毒。接種了病毒的胚蛋置孵,房孵育50-60小時。
1.5 收獲
用檢蛋器檢查已經(jīng)孵育到期的胚蛋,去除死胚、雞胚生長不良、胚蛋污染等不合格的胚蛋。然后將合格的胚蛋移入冷庫冷卻。冷卻到期后將胚蛋放置于收獲機上,收獲尿囊液的同時檢查是否有不合格胚蛋,收獲合格胚蛋的尿囊液。
1.6 濃縮
通過Millipore超濾系統(tǒng)對收獲尿囊液進行濃縮,濃縮后的尿囊液通過MilliporePellicon-2超濾系統(tǒng)進一步濃縮,然后加入PB溶液后繼續(xù)濃縮并回收。最后回收的濃縮尿囊液量控制在原收獲尿囊液液量的1/30至1/40。
1.7 純化
量取濃縮后的尿囊液并倒入燒杯內,通過蠕動泵把樣品導入?yún)^(qū)帶轉頭。同樣的方法依次導入30-33_%w/w飛蔗糖溶液、55-56_%w/w蔗糖溶液,當轉頭中心孔硅膠管流出樣品時,停止導入55-56%訣幾蔗糖溶液。量取0.125 mol/L的PB溶液,通過蠕動泵把PB溶液從中心孔導入?yún)^(qū)帶轉頭內。設定離心速度開始離心。離心結束后收集病毒液。
1.8 裂解及滅活
用0.25_mol/L的PB溶液回收稀釋,使裂解前病毒液蛋白質含量在600-900_μg/ml范圍內。將病毒液導入裂解罐,加入10_%w/v,聚山梨酯80溶液,攪拌。加入與裂解前病毒液等量的乙醚,攪拌。將病毒裂解液分裝于離心瓶中并離心。離心好之后加入4甲醛,使其最終濃度為80_μg/ml。于2-8℃放置18小時。
1.9 裂解液純化
按照1.7的方法對病毒裂解液進行區(qū)帶離心,離心結束后收集病毒液。
1.10 透析脫糖
用0.01_mol/L的PBS溶液10倍稀釋病毒液。通過超濾膜包透析去除蔗糖,10倍濃縮后結束第一次透析。再次用0.01_mol/L的PBs溶液10倍稀釋,進行第二次透析。
1.11 除菌過濾
壓濾桶內倒入一定量0.01_mol/L的PBS溶液,使PBS溶液依次通過澄清過濾濾膜和除菌濾膜。將待濾樣品倒入壓濾桶,使樣品依次通過澄清過濾濾膜和除菌濾膜。等待濾樣品過濾完后,在壓濾桶內倒入適量0.01_mol/L的PBS溶液清洗濾膜,清洗液體和之前的病毒液都通過濾膜收集在收液瓶內,并加入已除菌過濾的4_%w/v甲醛溶液。
2 結果
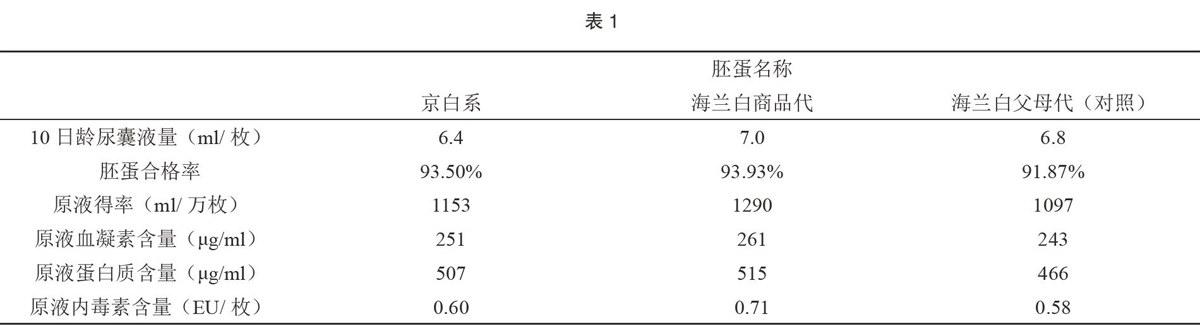
數(shù)據(jù)匯總(數(shù)據(jù)為平均值)見表1。
3 討論
本次胚蛋變更驗證試驗,每批試生產(chǎn)同時投入三種胚蛋進行平行比對,三種胚蛋來源均符合企標要求,使用的流感毒種一致,生產(chǎn)過程使用的原輔材料均一致。病毒接種、收獲、濃縮工段使用同一套設備,所以在生產(chǎn)時間上進行了分割,前一種胚蛋相關生產(chǎn)清場后,再開始后一種胚蛋的相關生產(chǎn)。純化和裂解液純化兩個工段所使用的部分離心機都是相同型號的離心機。綜上,我們認為三種胚蛋所對應的原液數(shù)據(jù)是客觀的。
對比表1數(shù)據(jù),在10日齡尿囊液量、胚蛋合格率、原液得率、原液血凝素含量、原液蛋白質含量的數(shù)據(jù)中海蘭白商品代的數(shù)據(jù)是最高的,京白系胚蛋在胚蛋合格率、原液得率、原液血凝素含量、原液蛋白質含量上高于海蘭白父母代(對照品),三者的內毒素含量也無太大差異,因此,我們認為兩種候選胚蛋(海蘭白商品代、京白系)都可以用于2017年的流感病毒疫苗生產(chǎn)。
參考文獻
[1]Ron FouchierAm,MunsterV,WallensterA,etal.Characterizatior of a novelinfluenza A virus hemagglutininsubtype(H16)obtained fromblack-headed gulls[J].JVirol,2005,79(05):2814-22.
[2]Monto AS,Gravenstein S,Elliott M,et al.Clinical signs and symptomspredicting influenza infection.Arch Intern Mod 160(21):3243-3247,2000.
[3] BoivinG,HardyI,TellierG,MaziadeJ.Predicting influenza infectionsduring epidemics with use of aclinical case definition.ClinInfect Dis 31(05):1166-1169,2000.
[4]OhmitSE,MontoAs.Symptomati。predictions of influenza viruspositivity in children during theinfluenza season.Clin Infect Dis43(05):564-568,2006.
[5]Tumpey T M,Basler C F,AguilarP V,eral.Characterization ofthe reconstructed 1918 Spanishinfluenza pandemic virus[J].Science,2005,310(5745):77-80.
[6]Beyer WE,deBruijnIA,PalacheAM,etal.The Plea against annualinfluenza vaccination?TheHoskinsparadoxrevisited.Vaccine 16(20):1929-1932,1998.
[7]Hoskins TW,Davies dR,α-chinA,etal.Controlled trial ofinactivated influenza vaccinecontaining the a-Hong Kong strainduring an outbreak of influenzadue to the a-England-42-72 strain.Lancet 2(7821):116-120,1973.
[8]Hoskins TW,Davies.TA,Smith A7,Miller CL,Allchin A,Assessment ofinactivated influenza-A vaccineafter three outbreaks of influenzaA at Christs Hospital.Lancet1(8106):33-35,1979.

