赤霞珠葡萄酒生產廢棄物資源化利用*
毛建利李 艷
1(河北科技大學生物科學與工程學院,河北石家莊050018)1(河北省發酵工程技術研究中心,河北石家莊050018)
我國是世界上葡萄酒生產大國,年產量達到100多萬千升,約剩余20萬噸皮渣,其中分離葡萄籽6萬噸、葡萄皮10萬噸、葡萄梗4萬噸,這些皮渣大多被用于生產飼料、肥料或者做填埋處理,利用率極低,不僅造成資源浪費,也給生態環境造成了一定破壞。
Harman在20世紀50年代中期第一次提出了衰老自由基學說,認為衰老是細胞內成分被氧自由基損害而造成的,維持體內正常水平的自由基,可以延緩人體細胞的衰老。研究還發現,目前威脅著人體健康的癌癥、帕金森綜合征、糖尿病和艾滋病等多種重大疾病,都與生物大分子的氧化損傷有關。
單寧是一類水溶性多元酚化合物,分子量在500 Da~3 000 Da之間,性質活潑,單寧的酚羥基與苯環直接相連的化學結構使其具有很好的抗氧化活性。單寧在葡萄梗中含量較多,縮合單寧中最有代表性的原花青素是所發現的有效的自由基清除劑之一,對多種疾病具有直接或間接的預防治療作用。本研究通過對葡萄梗中單寧的提取及抗氧化性研究,為今后這些資源的利用提供參考。
1 材料與方法
1.1 材料
昌黎產區赤霞珠葡萄釀酒廢棄物,包括葡萄皮、葡萄梗、葡萄籽;石家莊地區產巨峰葡萄釀酒廢棄物,包括葡萄皮、葡萄梗、葡萄籽。采用傳統工藝釀制葡萄酒后的皮渣,經55℃烘干,磨粉,過40目篩,備用。
1.2 儀器與設備
SP-756紫外可見分光光度計,上海光譜儀器有限公司;101-0AB電熱鼓風干燥箱,天津市泰斯特儀器有限公司;DELTA 320pH數字酸度計,梅普勒-托利多儀器有限公司;JJ1000電子天平,常熟市雙杰測試儀器廠;SHZ-HI真空泵,上海知信實驗儀器技術有限公司。
1.3 方法
1.3.1 單寧成分測定
單寧(以單寧酸計):采用福林-丹尼斯法測定。
1.3.2 花色苷含量的測定
稱取1.5 g樣品溶于20 mL體積濃度60%的酸化乙醇溶液(鹽酸體積濃度為0.5%),50℃水浴3 h離心得到上清液。再加入15 mL酸化乙醇,50℃水浴3 h離心取上清液,重復第3次,合并3次上清液定容50mL備用,采用pH值示差法測定。
1.3.3 原料的選擇
分別稱取10 g不同樣品于250mL瓶中,加水50mL放入60℃水浴鍋中12 h,將清液濾至250mL容量瓶中;殘渣加入30mL熱水,80℃水浴20min,清液濾入容量瓶;殘渣再加30mL熱水,80℃水浴20min重復3~4次,直至提取液與10 g/L三氯化鐵溶液不生成藍色產物為止。定容至刻度,采用福林-丹尼斯方法測定提取液中單寧的含量,求出樣品中單寧的質量分數即為樣品中單寧的提取得率。
1.3.4 提取劑的選擇
分別選取去離子水、體積濃度50%乙醇溶液,體積濃度50%丙酮溶液作為提取劑,葡萄皮渣粉按料液比為1 g∶25mL置于試劑瓶中密封,于60℃恒溫水浴中提取6 h,測定提取液中單寧提取得率。
1.3.5 單因素試驗
以料液比、提取溫度、提取時間和丙酮體積濃度為變化因素,以單寧提取得率為評價指標進行單因素試驗。料液比分別為:1 g∶15mL、1 g∶20mL、1 g∶25mL、1g∶30mL、1g∶35mL;溫度為:40℃、50℃、60℃、70℃、80℃;提取時間為:4 h、5 h、6 h、7 h、8 h;丙酮體積濃度設定為:30%、40%、50%、60%、70%。
1.3.6 正交試驗優化單寧的提取工藝
在單因素試驗基礎上,采用L9(34)正交設計,優化單寧的提取工藝。
1.3.7 抗氧化性能
1.3.7.1 ABTS自由基清除試驗清除ABTS自由基能力測定采用分光光度法。
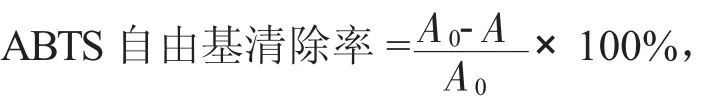
式中:A0——不加樣品時的吸光度;
A——加入不同量樣品時的吸光度。
樣品溶液:取1mL提取液,用提取溶劑稀釋成與Vc溶液同等濃度的溶液。
Vc溶液:用去離子水配制成質量濃度為80μg/mL、90μg/mL、100μg/mL、110μg/mL、120 μg/mL、140 μg/mL、160μg/mL的溶液。
取4mL ABTS+·工作液,加入100μL樣品溶液,混勻反應6min,黑暗環境下放置6min后于734 nm下測定吸光值,記為A。用提取劑替代樣品溶液的記為A0。
1.3.7.2 DPPH自由基清除試驗
清除DPPH自由基能力的測定采用分光光度法。

式中:A空白——不加樣品時的吸光度;
A樣品——加入不同量的樣品時的吸光度。
樣品溶液:取1mL提取液,用提取溶劑稀釋成與Vc同等濃度的溶液。
Vc溶液:用去離子水配制質量濃度為10μg/mL、20μg/mL、30μg/mL、40μg/mL、50μg/mL、60μg/mL、70μg/mL的溶液。
分別吸取2mL的樣品溶液和Vc溶液于試管中,加入2mLDPPH溶液,每個樣品做3個平行對照,搖勻后避光,室溫放置30min,517 nm下測定吸光值,記為A樣品。用2mL提取溶劑代替樣品溶液,吸光值記為A空白。
1.3.7.3 鐵離子還原能力的測定鐵離子還原能力的測定采用分光光度法:

式中:A0—加入樣品和試劑時的吸光度;
A1—不加樣品時的吸光度。
樣品溶液:取1mL提取液,用提取溶劑稀釋成與Vc同等濃度的溶液。
Vc溶液:用去離子水配制質量濃度為10μg/mL、20μg/mL、30μg/mL、40μg/mL、50μg/mL、60μg/mL、80μg/mL、120μg/mL、140μg/mL的溶液。
吸取2.5mL磷酸鹽緩沖溶液、2.5mL鐵氰化鉀溶液以及不同質量濃度的2.5mL樣品溶液,充分混勻。50℃水浴20min后快速冷卻,加2.5mL三氯乙酸混勻,3 000 r/min離心10min,取上清液2.5mL,加2.5mL體積分數0.1%的氯化鐵溶液,反應10min后在700 nm波長下測定吸光值(A0)。用同等體積的提取溶劑替代樣品溶液,測定吸光度A1。
1.3.7.4 羥自由基清除能力的測定
羥基清除能力的測定采用分光光度法:
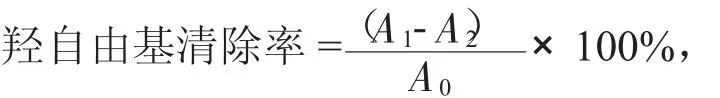
式中:A1——加入樣品和羥基母體溶液時的吸光度;
A2——不加入羥基母體溶液時的吸光度;
A0——只加入羥基母體溶液時的吸光度。
樣品溶液:取1mL提取液,用去離子水稀釋成與Vc同等濃度的溶液。
Vc溶液:用去離子水配制質量濃度為0.05mg/mL、0.10 mg/mL、0.15mg/mL、0.2 mg/mL、0.25 mg/mL、0.3mg/mL的溶液。
取3 mL的羥基母體溶液,分別加入1 mL不同濃度的樣品溶液,充分混勻,37℃恒溫水浴15min,用分光光度計在530 nm測定各組的吸光值A1(分光光度計校零時用去離子水),將羥基母體溶液用等量的提取溶劑代替,吸光值記為A2,將樣品溶液用等量的提取溶劑代替,吸光值記為A0。
1.3.8 數據處理
采用Excel 2003、Origin8.5、SPSS18.0進行試驗數據的匯總與統計分析處理。
2 結果與分析
2.1 葡萄酒廢棄物單寧提取得率
研究了不同品種葡萄釀酒廢棄物各組織的單寧提取得率,結果見圖1。
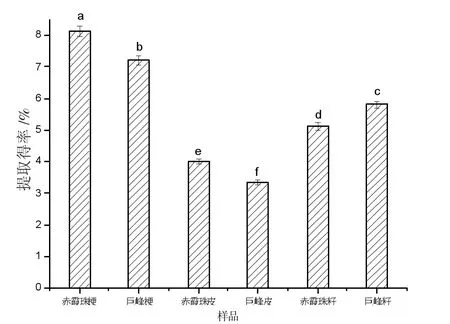
圖1 葡萄廢棄物中單寧的提取得率
由圖1可知,不同品種葡萄釀酒廢棄物的單寧提取得率差異顯著,且同一品種的葡萄釀酒廢棄物各組織之間的單寧提取得率也有顯著差異。其中赤霞珠葡萄梗的單寧提取得率達到了8.14%,巨峰梗的單寧提取得率達到了7.21%。
2.2 葡萄酒廢棄物中花色苷的提取得率
研究了不同品種葡萄釀酒廢棄物各組織的花色苷提取得率,結果見下頁圖2。
由圖2可知,不同品種葡萄釀酒廢棄物的花色苷提取得率差異顯著,同一品種不同組織部位的花色苷提取得率差異性不顯著。其中赤霞珠葡萄皮和赤霞珠葡萄籽的花色苷提取得率最高,均為0.10%。巨峰葡萄梗和皮的差異性呈現顯著性,其提取得率分別為0.022%和0.018%。根據上述數據,后續試驗選擇赤霞珠葡萄梗作為提取原料。
2.3 提取劑的選擇
選擇水、體積濃度50%乙醇溶液、體積濃度50%丙酮溶液為試劑,以葡萄梗為原料提取單寧,結果如圖3所示。
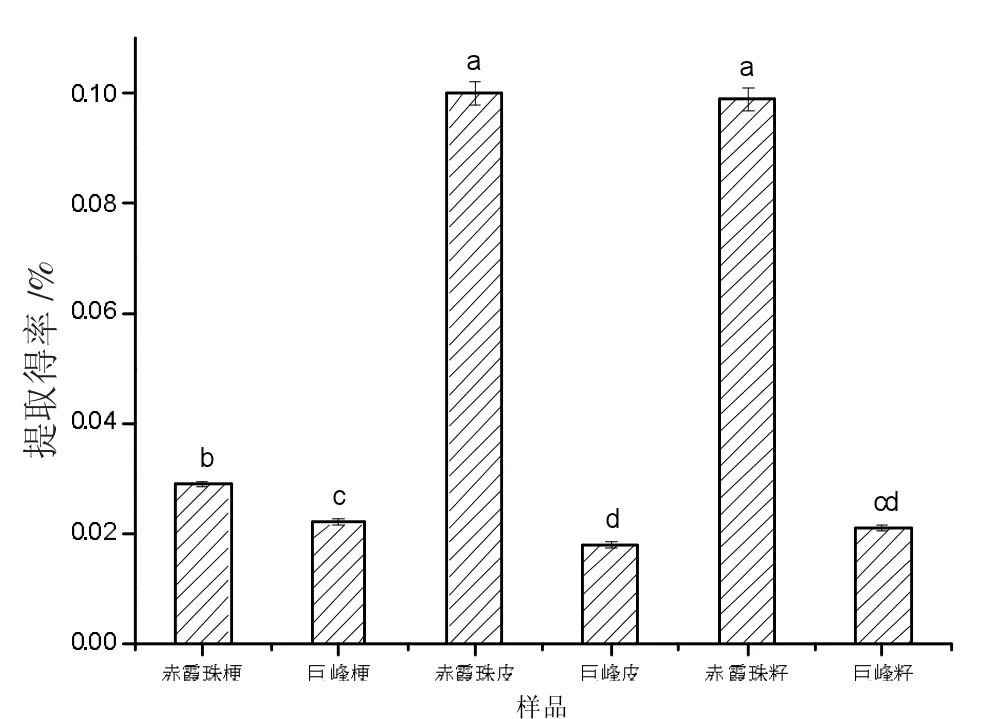
圖2 樣品花色苷的提取得率
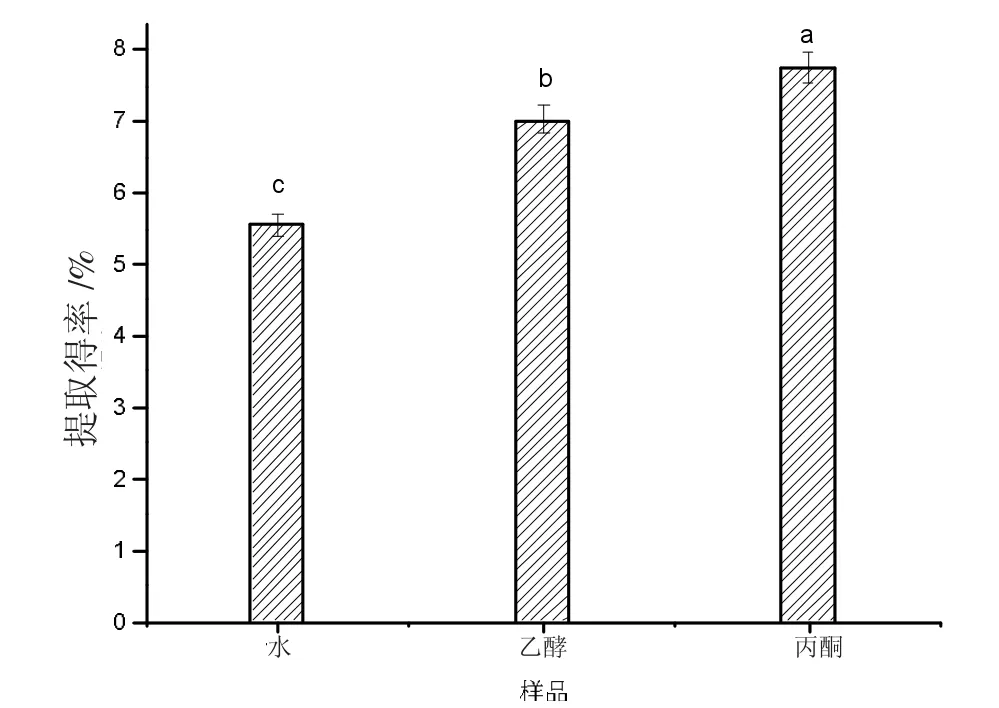
圖3 不同提取劑對赤霞珠葡萄梗中單寧的提取得率
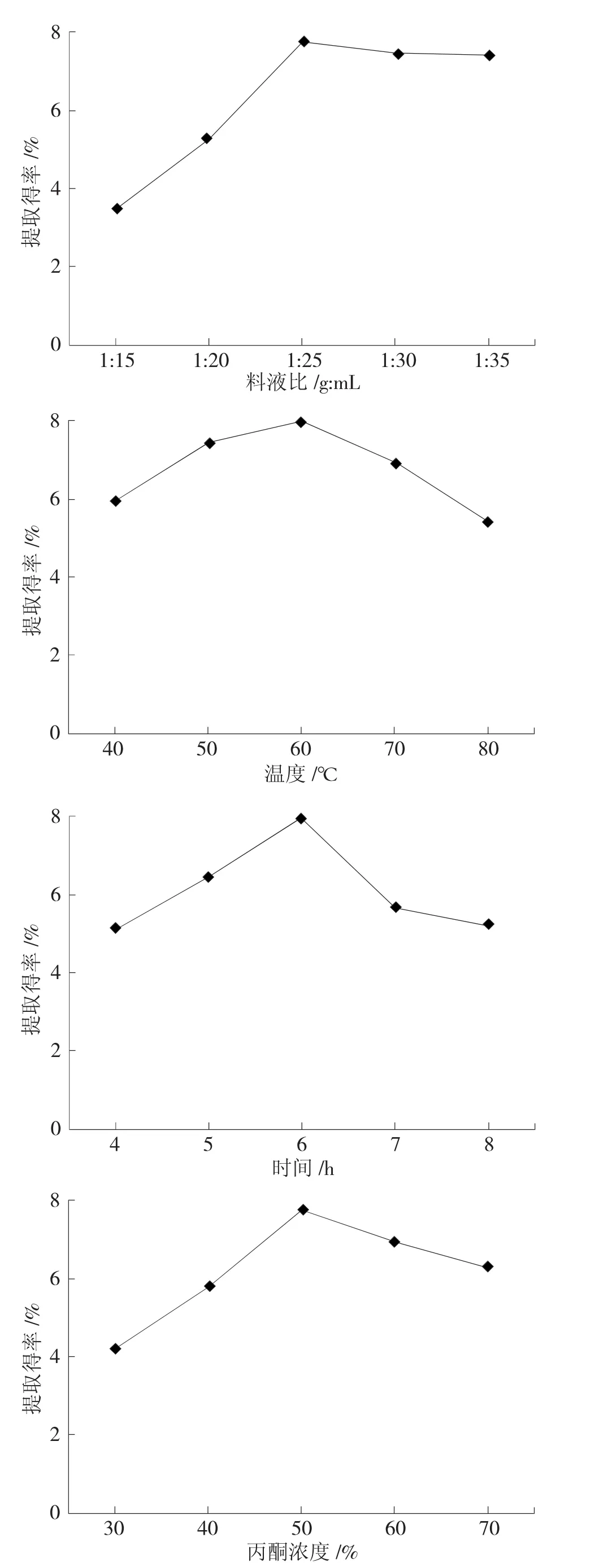
圖4 赤霞珠葡萄梗中單寧提取條件的單因素試驗
由圖3可知,不同的提取劑對赤霞珠葡萄梗中單寧的提取得率差異顯著,其中體積濃度50%的丙酮對赤霞珠葡萄梗的單寧提取得率最高為7.75%。不同的溶劑極性不同,單寧的溶解率變化很大,水的提取得率最低為5.56%。因此選用提取得率較高的丙酮作為優化提取赤霞珠葡萄梗的提取劑。
2.4 赤霞珠葡萄梗中單寧提取的單因素試驗
分別進行料液比、提取溫度、提取時間、丙酮體積濃度對單寧提取率的影響單因素試驗,結果見圖4。
從圖4看,在料液比1 g∶25mL附近,單寧的提取得率最高,為7.75%,繼續提高料液比,提取率沒有明顯增加。在浸提過程中,溫度會影響分子運動的速率,隨著溫度提高,可溶性物質分子運動加劇,單寧迅速滲出、溶解和擴散至溶液中,60℃時單寧提取得率最高,到70℃時降低,溫度過高會破壞單寧或加速單寧的氧化分解。在恒定溫度下,提取時間延長會促使物質溶出,因此呈現上升趨勢,達到高峰值后下降,提取6 h時單寧的提取得率最高,時間再長導致提取液中單寧成分在較高溫度下被破壞。丙酮體積濃度的改變,會影響到提取劑的極性,從而改變單寧的溶解度,單寧在體積分數50%的丙酮溶劑中提取得率最高。
2.5 赤霞珠葡萄梗中單寧提取正交試驗
根據單因素試驗結果,通過正交設計對赤霞珠葡萄梗中單寧提取條件進行優化。因素水平見表1,正交試驗結果見表2。
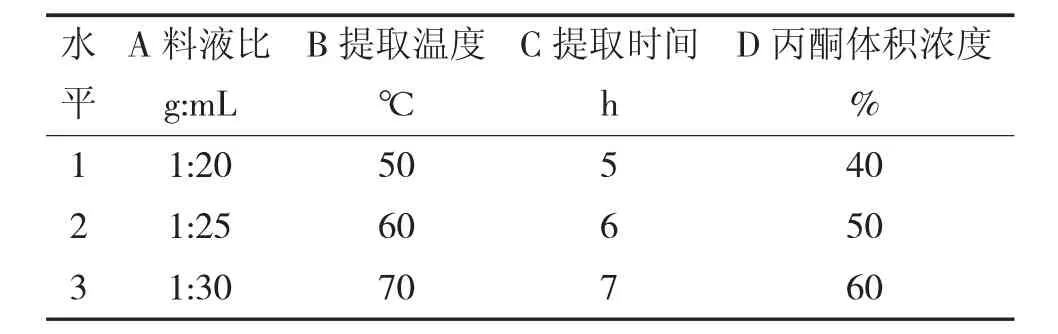
表1 正交試驗因素水平表

表2 正交試驗優化葡萄梗中單寧的提取條件
由表2可知,各因素的極差大小順序為A>B>C>D,由此可得出,影響赤霞珠葡萄梗中單寧提取率的4個因素先后順序為:料液比>溫度>時間>丙酮體積濃度,最優的提取工藝條件為:A2B2C2D2,即料液比1 g∶25mL,提取溫度60℃,提取時間6 h,丙酮體積濃度為50%。
在最優正交試驗條件下,進行驗證和擬合試驗,試驗平行3次求得平均值,單寧的平均提取得率為7.75%,比正交表中最佳提取得率提高6.71%。
2.6 赤霞珠葡萄梗中單寧提取物體外抗氧化試驗
2.6.1 赤霞珠葡萄梗中單寧提取物對ABTS自由基的清除試驗
以Vc為對照,研究赤霞珠葡萄梗單寧提取液對ABTS自由基的清除率,對比效果見圖5。
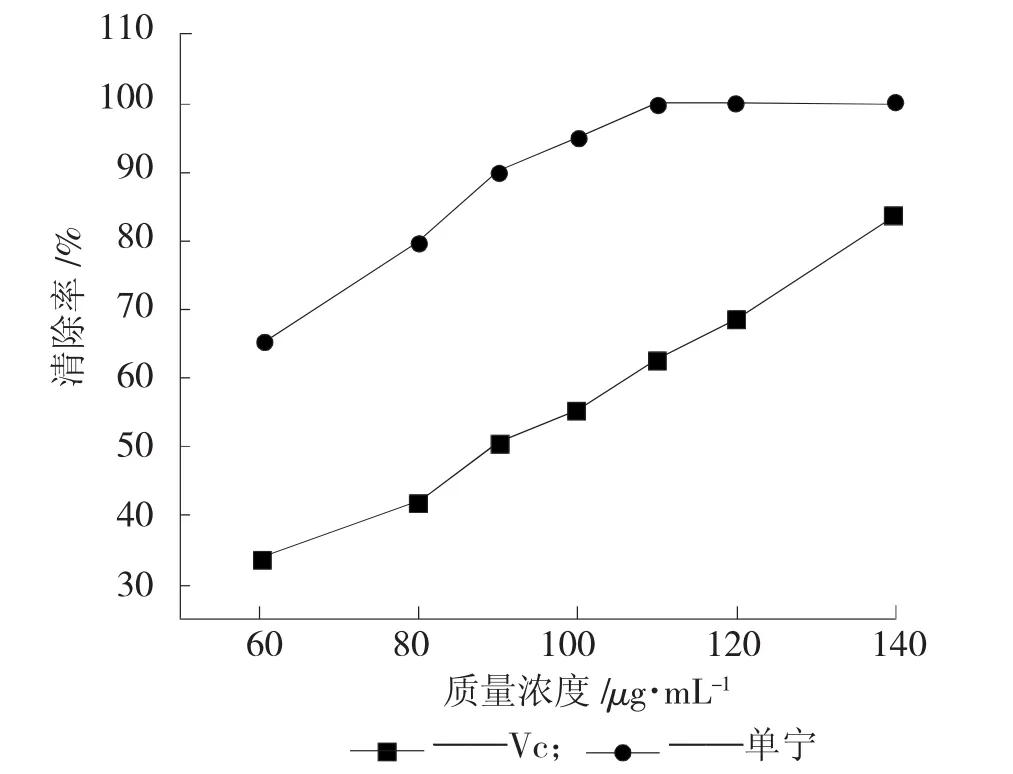
圖5 赤霞珠葡萄梗中單寧提取物對ABTS自由基的清除試驗
由圖5可知,單寧提取物對ABTS自由基的清除能力明顯高于Vc。Vc質量濃度在90μg/mL,對ABTS自由基的清除率達到了50.92%,而單寧提取物在此濃度下對ABTS自由基的清除率達到了90.01%。當單寧提取物的質量濃度達到了110μg/mL時,對ABTS自由基的清除率就能達到100%。由試驗結果分析可知,赤霞珠葡萄梗單寧提取物對ABTS自由基的清除效果明顯。
2.6.2 赤霞珠葡萄梗中單寧提取物對DPPH自由基的清除試驗
以Vc為對照研究赤霞珠葡萄梗單寧提取液對DPPH自由基的清除率,對比效果見圖6。

圖6 赤霞珠葡萄梗中單寧提取物對DPPH自由基的清除試驗
由圖6可知,赤霞珠葡萄梗中單寧提取物對DPPH自由基的清除能力要明顯高于Vc。當Vc的質量濃度為30μg/mL,對DPPH自由基的清除率達到了48.30%,而同等濃度的單寧提取液對DPPH自由基的清除率達到了97.00%。當單寧質量濃度增加到40μg/mL時,其對DPPH自由基的清除率就能達到100%。由試驗結果分析可知,赤霞珠葡萄梗中單寧提取物對DPPH自由基的清除效果明顯。
2.6.3 赤霞珠葡萄梗中單寧提取物對鐵離子的還原能力試驗
以Vc為對照,研究赤霞珠葡萄梗中單寧提取液對鐵離子還原能力,對比效果見圖7。
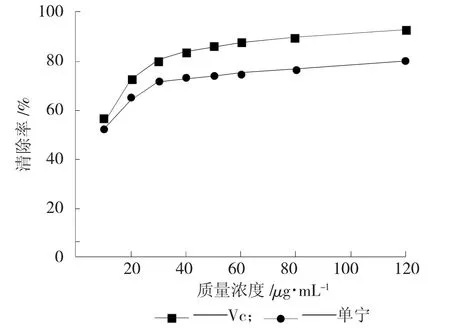
圖7 赤霞珠葡萄梗中單寧提取物對鐵離子的清除試驗
由圖7可知,赤霞珠葡萄梗中單寧提取物對鐵離子的還原能力略低于Vc。當Vc的質量濃度為10μg/mL時,對鐵離子的清除率為55.46%,同等濃度下的單寧提取物對鐵離子的清除率為52.24%。隨著Vc和單寧提取物質量濃度的增加,對鐵離子的還原能力也明顯增加。由試驗結果分析可知,赤霞珠葡萄梗中單寧提取物對鐵離子的還原效果良好。
2.6.4 赤霞珠葡萄梗中單寧提取物對羥自由基的清除試驗
以Vc為對照,研究赤霞珠葡萄梗中單寧提取液對羥自由基的清除率,對比效果見圖8。
由圖8可知赤霞珠葡萄梗中的單寧提取物對羥自由基的清除能力略弱于Vc。當Vc質量濃度為0.25 mg/mL時,對羥自由基的清除率達到了54.44%,同等濃度下的單寧提取液對羥自由基的清除率也達到了50.12%。隨著Vc和單寧提取液質量濃度的增加,對羥自由基的清除率都呈現上升的趨勢。由試驗結果分析可知,赤霞珠葡萄梗對羥自由基的清除作用明顯。
3 結論
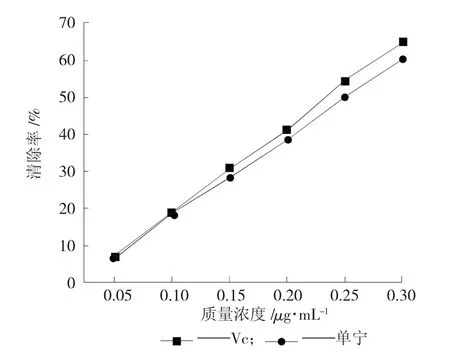
圖8 赤霞珠葡萄梗中單寧提取物對羥自由基的清除試驗
a)不同品種的葡萄釀酒廢棄物的單寧提取得率差異顯著,同一品種的葡萄釀酒廢棄物各組織之間的單寧提取得率差異也顯著。其中葡萄梗的單寧提取得率最高,赤霞珠葡萄梗的單寧提取得率為8.14%,巨峰葡萄梗的單寧提取得率為7.21%。
b) 在正交試驗最優條件下,即:料液比為1∶25(g/mL),提取溫度60℃,丙酮濃度為50%,浸提時間為6 h,進行驗證和擬合試驗,試驗平行3次求得平均值,單寧的平均提取得率為7.75%。
c)試驗結果分析可知,以Vc為陽性對照并對赤霞珠葡萄中的單寧提取液進行ABTS、DPPH、羥自由基、鐵離子的清除試驗,明顯看出赤霞珠葡萄梗中單寧提取物對4種自由基的清除效果良好,由此說明赤霞珠葡萄梗具有開發抗氧化產品的潛力。

