藥物溶出試驗儀計量校準方法研究
阮 俊,張紹旺,饒 杰,龔 榕
(云南省計量測試技術研究院,云南 昆明 650228)
0 引 言
藥物溶出試驗儀(以下簡稱溶出度儀)是檢測藥物成分從片劑、膠囊劑或顆粒劑等制劑在規定條件下溶出情況的一種體外試驗裝置[1]。我國新版《藥品生產質量管理規范》規定,所有關系到藥品生產質量控制的儀器都必須經過校準。校準是在規定條件下,為確定計量儀器或測量系統的示值,或實物量具或標準物質所代表的值,與相對應的被測量的已知值之間關系的一組操作,而溶出度儀的校準則是保障藥品質量的一個重要的措施。美國是該領域的開拓者和發展者,已有50年的研發歷史,擁有多種校準用標準片。我國市場上溶出度儀品牌種類較多,各儀器廠商根據自家儀器制定內部操作規程進行自校準,適用范圍窄,所用工具、測量方式、測量成本差異程度大[2-3]。國內校準溶出度儀的方法現有機械方法和化學方法2種。機械方法主要是對儀器的外觀檢查、攪拌槳擺動幅度和轉籃擺動幅度的檢查、轉桿垂直度的檢查;化學方法國內廠家目前是用水楊酸標準片來進行自校準。我國目前尚無該設備的國家校準規范,究其原因是還沒有確定校準該設備的國家級標準物質。本文從設備的物理性能即溫度[4-5]、轉速[6]、時間[7-9]著手來探討其校準方法。
1 設備原理
溶出度是指在規定條件下活性藥物從制劑中溶出的速率和程度[1]。溶出度儀是為溶出度測定法提供一種微機控制的機電一體化試驗設備,是測量藥品溶解程度,模擬口服固體制劑在胃腸道中崩解和溶出的體外簡易試驗設備,是在體外對體內藥物生物利用度進行研究和評價的有效的替代儀器,也是保證和衡量固體口服制劑生產工藝及質量是否合理和穩定的一項重要手段。其主要由電動機、恒溫裝置、轉籃、攪拌槳、溶出杯及杯蓋等組成,如圖1所示。該儀器采用四柱支撐結構形式,有雙排十二杯十二桿、雙排八杯八桿、雙排四杯四桿、單排六杯六桿等結構;機頭有固定式和電動升降式,機械性能穩定;具備溫度的控制、轉速的調節、時間的設定3項基本功能。

圖1 溶出度儀實物圖
2 校準條件
2.1 環境條件
溫度為10~35 ℃;相對濕度不大于85%;操作環境應潔凈無塵。
2.2 校準用設備條件
溫度計或測溫裝置至少2套,測溫范圍30~40 ℃,溫度修正值的擴展不確定度不大于0.1 ℃(k=2),分辨力不大于0.05 ℃;轉速表不低于0.1級;秒表10 min內最大允許誤差±0.07 s。
2.3 被校準儀器的前期檢查
根據儀器說明書的要求,檢查電源電壓是否為220V±22 V,操作環境應潔凈無灰塵,儀器不應受強光直射,周圍無強磁場、電場干擾,無強氣流及腐蝕性氣體,應避免其他冷、熱源影響。
檢查并確認是否所有用于校準該設備的標準器其計量性能都符合要求。
檢查溶出度儀外殼是否平整、清潔,無影響其功能的缺陷,儀器應標明制造單位名稱、型號、出產編號、制造日期,國產儀器還應有計量器具制造許可證標志及編號,儀器的轉籃、攪拌槳、溶出杯等應符合《中華人民共和國藥典》[1]要求,無影響計量特性的缺陷。
3 校準項目及方法
3.1 控溫誤差的校準
溶出度儀主要模擬人體內環境進行測量,如水浴溫度超出人體正常值則會影響藥物的溶出度,導致測量結果不準確,因此要對該指標進行校準[10]。
使用溫度計或測溫裝置,向溶出度儀水浴槽中加入蒸餾水至刻度線后開機,將溫度設定為37.0 ℃并加熱,將溫度計插入溶出度儀A溶出杯擺放區域內,達到熱平衡后溫度計測量該處溫度3次,取平均值得到。采用同樣方法依次測量每個溶出杯擺放區域,得到溫度值,按下式計算各點的溫度誤差:
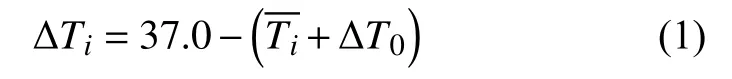
式中:ΔTi——溫度誤差,℃;
ΔT0——溫度計的修正值,℃;
i——溶出杯擺放區域(A~M)。
取偏離37 ℃最大值的ΔTi作為該溶出儀的最大溫度誤差[11]。按照CFDA2016指導原則/FDA(DAPLOP.002)要求,各溶出杯內溶出介質的溫度均應為 37 ℃±0.5 ℃。
3.2 溫度場均勻性及波動度的校準
溶出度儀的水浴箱處于額定溫度,并已達到熱穩定狀態,箱內各溶出杯之間的溫度差異及單杯中的溫度波動十分重要,直接影響藥物在各溶出杯中的溶出速率,所以應對其進行校準[12-13]。
3.2.1 溫度場均勻性
溫度設定為37.0 ℃,將溫度計Ⅰ插入溶出度儀工作區域任意位置固定,另一支溫度計Ⅱ插入溶出度儀溶出杯擺放區域A,熱平衡后測量水溫,測量順序為Ⅰ→Ⅱ→Ⅱ→Ⅰ,不少于2個循環,取平均值得到溫度計測量值。將溫度計II插入溶出度儀溶出杯擺放區域B,按上述方法得到和,則位置A和B之間的溫差為
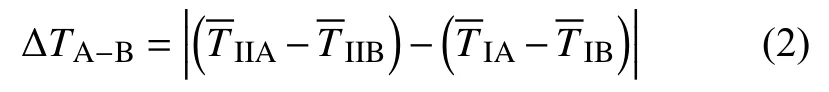
按上述方法還可以得到工作區域中A和C之間的溫差ΔTA?C,位置B和位置C之間的溫差可按下式計算:

依此類推,可以得到所選全部位置之間的溫差,取其中最大溫度差值作為該溶出儀的溫度場均勻性。按照CFDA2016指導原則/FDA(DAP-LOP.002)要求,各溶出杯內溶出介質的溫度均勻性應為0.5 ℃。
3.2.2 溫度波動度
溫度設定為37.0 ℃,將溫度計Ⅰ放置在有代表性的溶出杯擺放區域,熱平衡后每隔1 min測量1次溫度,不少于16組數據(并不少于一個溫度波動循環),取其中最小值與最大值的范圍作為溶出度儀的溫度波動度 (36.7 ~ 37.3℃)。

式中:Tmin——溫度計I在同一溶出杯擺放區域最小溫度值,℃;
Tmax——溫度計I在同一溶出杯擺放區域最大溫度值,℃。
3.3 轉速相對誤差的校準
溶出度儀的轉籃(攪拌槳)轉速分別可設定為25 r/min、50 r/min、100 r/min 和 200 r/min,或其他常用轉速,其準確度也會影響藥物的溶出度,故應對該參數進行校準。
將轉籃(攪拌槳)轉速分別設定為25 r/min、50 r/min、100 r/min和 200 r/min,或其他常用轉速(最大允許誤差為±4%),不少于3點。各點用轉速表測量3次,取平均值為該點的測量值,按下式計算轉速相對誤差:

式中:Δ ω——儀器的轉速相對誤差,%;
ω——轉速表3次測量的平均值,r/min;
ω0——轉速設定值,r/min。
3.4 定時器的計時相對誤差的校準
在測量藥物溶出度的過程中,通常要設定計時器,在規定時間內進行測量,如果計時不準確,將會誤導實驗人員觀測藥物的溶出度,因此要對該參數進行校準[14]。
分別設置定時器時間點為2 min、5 min、10 min(計時誤差為±2%),各點用秒表測量3次,取平均值為該時間點的測量值,按式(6)計算計時相對誤差,取最大的Δt為該溶出儀定時器的計時相對誤差。
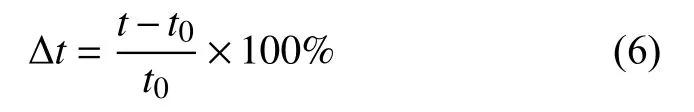
式中:Δt——定時器的計時相對誤差,%;
t——秒表3次測量的平均值,min;
t0——儀器設定值,min。
4 校準實驗
為了驗證該校準方法的可行性,對天津市天大天發科技有限公司生產的RC806D藥物溶出試驗儀按本方法進行校準,結果見表1。
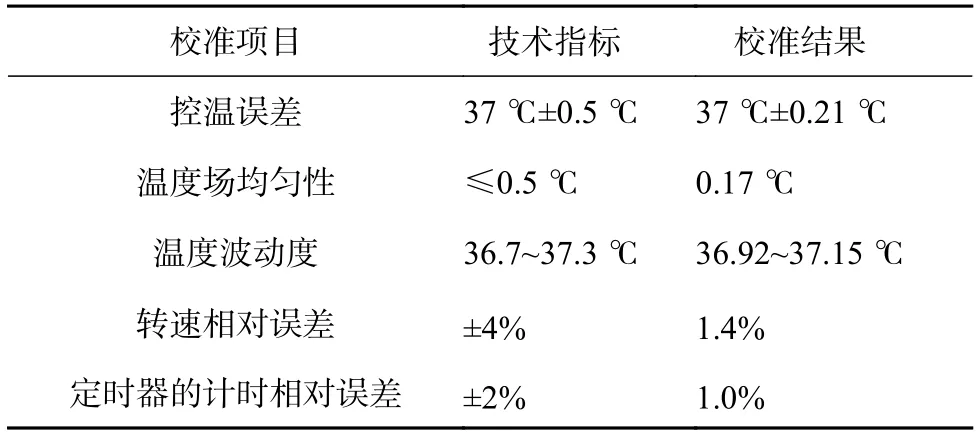
表1 藥物溶出試驗儀校準結果
使用本校準方法評定得到藥物溶出試驗儀溫度誤差的擴展不確定度為U=0.12 ℃,k=2;溫度均勻性測量結果的擴展不確定度為U=0.05 ℃,k=2;溫度波動性測量結果的擴展不確定度為U=0.08 ℃,k=2;轉速25~200 r/min示值誤差的擴展不確定度為U=0.56%~1.2%,k=2;定時器的計時 2~10 min相對誤差的擴展不確定度為U=0.15%~0.7%,k=2。
由表1可知,該儀器的各項指標均符合校準項目指標的要求,本文校準方法能夠合理、準確地評價藥物溶出試驗儀的性能,為從事該校準的技術人員提供參考。
5 結束語
本文藥物溶出試驗儀校準方法是根據儀器原理進行設計的,能有效地檢測溶出度儀的準確性和安全性,確保藥物成分從片劑、膠囊劑或顆粒等制劑在規定條件下溶出的速度和程度準確、有效、可靠。校準技術和方法已經在云南省計量校準檢測工作中得到了實施和應用,成為JJF(滇)13——2017《藥物溶出試驗儀校準規范》。但方法存在一定的問題,如只能校準設備空載的情況,無法驗證轉籃的清潔度、攪拌槳的清潔度、脫氣等因素的影響等。因此,下一步將研制藥物溶出試驗儀系列國家標準物質,將其引入校準過程,更為全面、完整地考核設備,使我國藥物溶出試驗儀校準方法取得更大突破。

