腎上腺血管瘤1例報告
趙曉風 張豫才 張然昆 楊 婕 白 偉 王順雨 潘家波
(北京市健宮醫院泌尿外科,北京 100054)
腎上腺血管瘤是一種罕見的腎上腺無功能良性腫瘤,因缺乏特征性臨床表現,術前誤診率極高,因臨床表現多樣,目前尚未統一的治療規范。我科2017年10月腹腔鏡手術切除右腎上腺腫物1例,術后病理診斷為腎上腺血管瘤,現報道如下。
1 臨床資料
患者男,57歲。因體檢發現右側腎上腺區腫物1個月于2017年10月入院。1個月前常規體檢B超發現右腎上腺區一腫物,無頭痛、頭暈、心悸,無惡心、嘔吐,飲食、二便如常,體重無明顯變化。既往無原發性高血壓、冠心病、糖尿病史,無手術及外傷史。體檢:體溫36.5 ℃,心率72次/min,呼吸20次/min,血壓135/80 mm Hg(1 mm Hg=0.133 kPa)。腹部及泌尿專科檢查無異常體征。B超:右腎上方7.3 cm×6.3 cm×6.7 cm圓形混雜回聲團,內部回聲不均,界清(圖1);CT:右腎上腺區類圓形低密度影7.5 cm×6.3 cm×6.6 cm,平掃CT值27~43 Hu,邊界清,動脈期可見腫物不均勻輕度強化,靜脈期可見腫物有向心性強化趨勢(圖2~4)。MRI:右側腎上腺7.4 cm×6.5 cm×6.5 cm異常信號影, T1W1、T2W1均為高低混雜型號,界清(圖5、6)。實驗室檢查:血漿血管緊張素Ⅱ臥位47.4 ng/L(我院正常值25~60 ng/L),立位58.74 ng/L(我院正常值50~120 ng/L);血漿醛固酮臥位10.92 ng/L (我院正常值30~160 ng/L),立位28.89 ng/L(我院正常值70~300 ng/L);腎素活性臥位0.6 μg·L-1·h-1(我院正常值0.15~2.33 μg·L-1·h-1),立位1.47 μg·L-1·h-1(我院正常值0.1~6.56 μg·L-1·h-1);促腎上腺皮質激素11.78 ng/L(我院正常值6~80 ng/L);血清皮質醇541.4 nmol/L(我院正常值51~623 nmol/L);24 h尿苦杏仁酸13 μmol/d(我院正常值10~30 μmol/d)。術前診斷:右腎上腺腫物(無功能腺瘤可能性大)。按嗜鉻細胞瘤行術前準備2周(口服特拉唑嗪2 mg,每日1次,應用特拉唑嗪后血壓無明顯變化)后,在氣管插管全麻下經腹腹腔鏡行右腎上腺腫物切除術。左側臥位,Hassan法在右側腹直肌旁臍頭側2 cm置入10 mm trocar及腹腔鏡,建立氣腹后分別于右鎖骨中線肋緣下2 cm及右腋前線臍尾側1 cm穿刺置入12、5 mm trocar,再于正中線劍突下穿刺置入5 mm trocar(置入持針器將肝臟上舉)。切開肝鐮狀韌帶,在Toldt’s線和升結腸之間切開側腹膜,銳性分離Gerota筋膜前層和融合筋膜之間的間隙,將升結腸和十二指腸向內側推移,顯露下腔靜脈及右腎靜脈。右腎上腺腫瘤位于腹膜后腎與肝臟、右腎靜脈與下腔靜脈之間,呈球形、灰褐色、邊界清楚,與右腎稍有粘連,右腎上腺被擠壓,與腫瘤分界尚清。腫瘤表面可見少量怒張血管,質韌,有彈性(圖7),沿腫瘤包膜將腫瘤游離后切除,保留右腎上腺,術中血壓平穩,術中出血10 ml,手術時間76 min。標本剖面可見大量血竇樣結構(圖8)。術后病理:右腎上腺海綿狀血管瘤(圖9)。術后3 d拔除引流管,術后8 d出院。術后隨訪6個月,未見腫瘤復發。
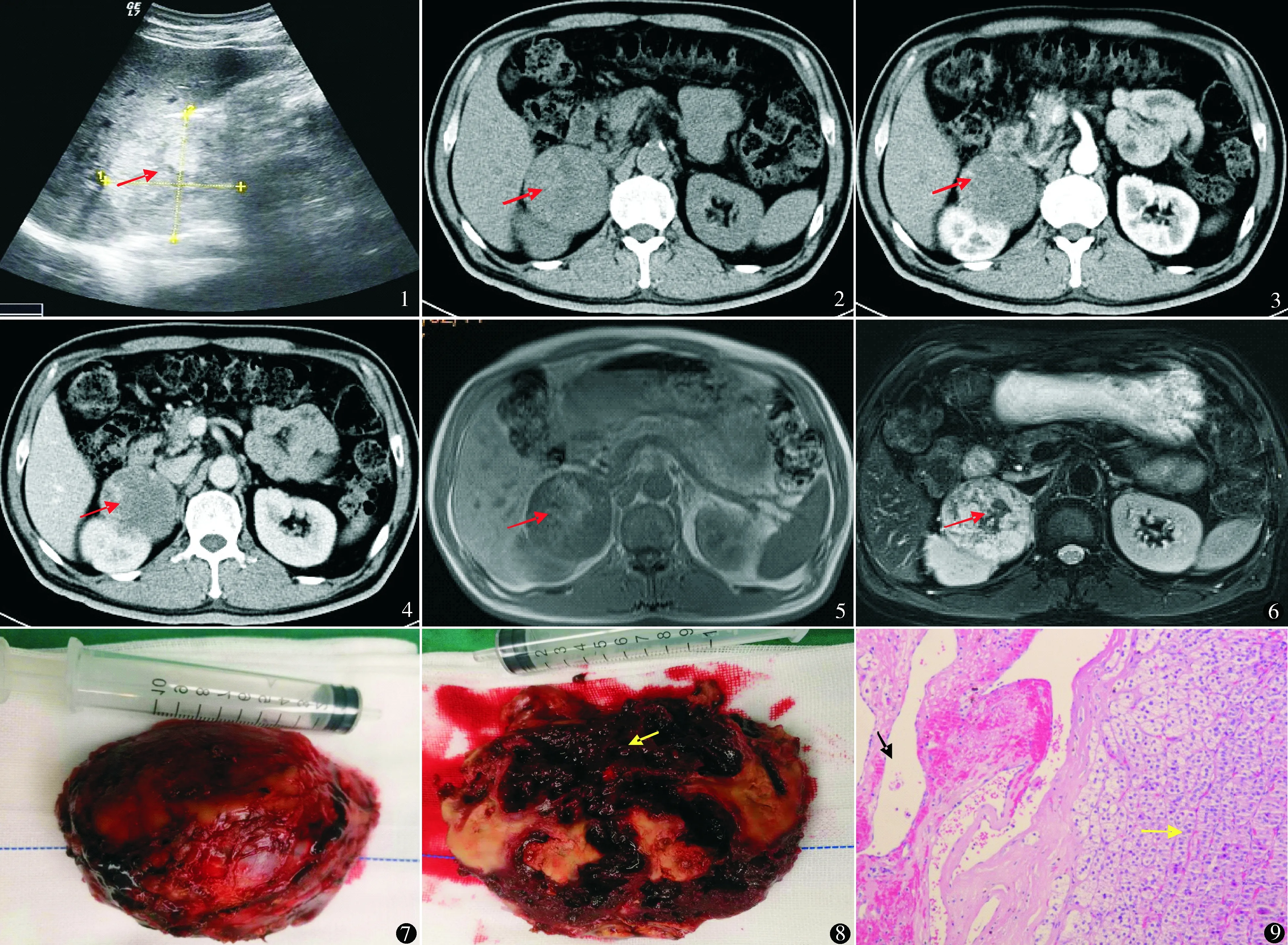
圖1 右腎上腺區彩超腎與肝之間類圓形混雜回聲 圖2 右腎上腺區腫物CT平掃 圖3 右腎上腺區腫物CT增強動脈期 圖4 右腎上腺區腫物CT增強靜脈期 圖5 右腎上腺區腫物MRI T1W1期 圖6 右腎上腺區腫物MRI T2W1期 圖7 右腎上腺血管瘤切除后整體外觀 圖8 右腎上腺血管瘤標本剖開可見血竇樣結構 圖9 腎上腺組織(黃色箭頭)旁管腔結構(黑色箭頭),被覆血管內皮細胞 (HE染色 ×10)
2 討論
隨著現代影像學技術,尤其是B超、CT和MRI的廣泛應用,腎上腺腫物偶發瘤的檢出率逐漸升高,約占總體腎上腺腫瘤的4%[1]。腎上腺血管瘤罕見,第1例由Johnson等[2]在1955年報道,至今為止國內外文獻共報道約70例[3],其中僅有1篇報道為術前即診斷為腎上腺血管瘤[4],其余均為術后病理確診,可見,此病術前誤診率極高。
大多數腎上腺血管瘤除影像學提示腎上腺區腫物外,并無其他特征性臨床表現。本例是在常規體檢時無意中發現右腎上腺腫物,無任何不適,腎上腺相關激素的血液、尿液檢測也無異常。腫瘤體積較大對周圍組織造成壓迫時,會出現患側腹脹不適,嚴重者也會有惡心、嘔吐等癥狀[5]。因腎上腺血管瘤無特異性的臨床癥狀,故其影像學表現作為術前診斷的依據尤為重要。國內外學者總結出腎上腺血管瘤的一些影像學特點: CT的特征表現包括平掃彌漫性鈣化,鈣化被認為是大量擴張靜脈內的靜脈石[6],動脈期邊緣斑片狀強化及靜脈期向心性增強[7],本例CT無鈣化,但有靜脈期向心性增強的表現;MRI表現為T1W1多樣性[8],T2W1以高信號為主,原因被認為是血管瘤內富含大量的血液[9]。但以上特點與腎上腺其他來源的腫物影像學特點重疊,難以總結其特有表現。當血管瘤伴發出血、鈣化、壞死等病理改變時,更難與其他其他性質的腫物鑒別。
因腎上腺血管瘤一般體積較大,臨床上需要與嗜鉻細胞瘤和腎上腺皮質癌相鑒別,我們認為以下幾點應考慮:①腎上腺血管瘤患者的發病年齡中位數是61.8歲[5],嗜鉻細胞瘤和腎上腺皮質癌的高發年齡在40~50歲[10]。腎上腺血管瘤患者的發病年齡較高,結合本例有可能是因為血管瘤無功能,只有當腫瘤體積較大時才被發現。②腎上腺血管瘤女性患者比例較高,與腎上腺皮質癌類似,值得注意的是,另一種常見疾病肝血管瘤也是女性占大多數[11],嗜鉻細胞瘤則是男女比例相當。③大多數腎上腺血管瘤因無分泌功能而無明顯臨床癥狀,有癥狀者往往是因為腫瘤體積較大而對周圍組織壓迫而引起。嗜鉻細胞瘤和腎上腺皮質癌是因為腫瘤強大的分泌功能而臨床癥狀明顯。
目前,尚無腎上腺血管瘤的治療標準,鄭清友等[12]認為直徑<3.5 cm腎上腺血管瘤可定期隨訪。Paluszkiewicz等[13]認為因為腎上腺血管瘤有潛在危及生命的自發性大量出血的危險,應該積極手術切除。我們的體會是當腫瘤引起臨床癥狀或是與嗜鉻細胞瘤及惡性病變難以區分時,應積極手術治療。當不能完全除外嗜鉻細胞瘤時,應按嗜鉻細胞瘤做術前準備,本例按嗜鉻細胞瘤行術前準備2周。我們認為腹腔鏡是目前腎上腺血管瘤的首選手術方式,經腹腔還是經后腹腔入路均可行,并且腫瘤的大小與手術難易程度并不成正相關[14],因為腫瘤的邊緣形成一層致密的纖維膜,在腹腔鏡放大清晰的視野下易于沿著纖維膜游離并切除瘤體[15],并且因為血管瘤是良性病變,與周圍組織分解清楚,比較容易分離,術中出血很少,有很好的安全性。
綜上所述,雖然腎上腺血管瘤臨床罕見,屬于良性病變,且不具備獨特的臨床表現,但具有潛在危及生命的自發性大量出血的危險,加強對此病的認識有助于臨床工作中對腎上腺腫物診治策略的正確指導,在腎上腺偶發瘤的鑒別診斷中,應包括腎上腺血管瘤,如果需要手術治療,腹腔鏡切除腫瘤是一種安全可行的方法。

