癌癥免疫學(xué)家斬獲諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng)
編譯 傳植
詹姆斯·艾利森和本庶佑開(kāi)創(chuàng)了全新免疫療法思路:釋放免疫系統(tǒng)自身能力攻擊癌細(xì)胞。

詹姆斯·艾利森(左)和本庶佑共獲2018年諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng)
兩位科學(xué)家因開(kāi)創(chuàng)癌癥治療的全新方法共獲2018年諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng)。
美國(guó)休斯敦德克薩斯州立大學(xué)安德森癌癥中心的詹姆斯·艾利森(James Allison)和日本京都大學(xué)的本庶佑(Tasuku Honjo)將分享900萬(wàn)瑞典克朗的獎(jiǎng)金。
兩人的研究展現(xiàn)了通過(guò)免疫細(xì)胞上的蛋白來(lái)操縱機(jī)體免疫系統(tǒng)殺傷癌細(xì)胞。以此方法為基礎(chǔ)的各式療法如今已為一些癌癥患者延長(zhǎng)了數(shù)年的生命,甚至根除了部分晚期癌癥患者的病癥。無(wú)數(shù)研究者如獲至寶,開(kāi)始嘗試這一方法,使免疫療法成為癌癥研究中的熱門(mén)。
一大早喜出望外
清晨五點(diǎn)半,艾利森被他兒子打來(lái)的電話吵醒,知道了獲諾獎(jiǎng)的好消息。這幾天他在紐約參加一個(gè)免疫學(xué)方面的會(huì)議。到了六點(diǎn)半,同事們紛紛來(lái)到他的酒店房間祝賀,買(mǎi)來(lái)香檳要給他辦一個(gè)祝賀派對(duì)。不一會(huì)兒,艾利森便接到了諾獎(jiǎng)委員會(huì)的正式通知。
“我到現(xiàn)在也沒(méi)完全明白過(guò)來(lái),”艾利森在新聞發(fā)布會(huì)上說(shuō),“我是個(gè)做基礎(chǔ)研究的,能讓我的研究成果真正影響到人類(lèi)是最好不過(guò)的了,這是我們每個(gè)人的夢(mèng)想。”
20世紀(jì)90年代,艾利森還在加州大學(xué)伯克利分校工作,他是少數(shù)著眼于“檢查點(diǎn)”蛋白CTLA-4研究的科學(xué)家,CTLA-4可視為免疫細(xì)胞中T細(xì)胞的“制動(dòng)器”。1997年,艾利森與同事們?cè)O(shè)計(jì)了一種可以結(jié)合CTLA-4的抗體,由此除去了T細(xì)胞活性的“制動(dòng)器”,釋放了它們殺傷小鼠體內(nèi)癌細(xì)胞的能力。2010年的一項(xiàng)臨床研究發(fā)現(xiàn),該抗體對(duì)晚期黑色素瘤——一種皮膚癌——有顯著的療效。
1992年,獨(dú)立于艾利森進(jìn)行研究的本庶發(fā)現(xiàn)了另一個(gè)T細(xì)胞蛋白——PD-1,同樣也是免疫系統(tǒng)的“制動(dòng)器”,運(yùn)作于不同的機(jī)制。PD-1很快成為另一個(gè)癌癥治療的目標(biāo)。2012年,臨床研究證明,該蛋白可有效對(duì)抗多種不同的癌癥,包括肺癌這一人類(lèi)的主要?dú)⑹帧;谠摰鞍椎寞煼ㄐЧ踩耍恍┺D(zhuǎn)移癌患者獲得了長(zhǎng)期緩解,使根治疾病成為可能。
松開(kāi)制動(dòng)器
“艾利森和本庶的發(fā)現(xiàn)為癌癥療法添磚加瓦。該方法體現(xiàn)了一種全新的思路,不同于以往靶向癌細(xì)胞本身的療法,它以機(jī)體免疫系統(tǒng)檢查點(diǎn)這一‘制動(dòng)器’作為目標(biāo),”諾獎(jiǎng)新聞發(fā)布會(huì)上介紹獲獎(jiǎng)成果的諾獎(jiǎng)委員會(huì)成員、斯德哥爾摩卡羅琳斯卡學(xué)院免疫學(xué)家克拉斯·卡萊(Klas Krre)說(shuō),“兩位諾獎(jiǎng)得主的重大發(fā)現(xiàn)為抗癌領(lǐng)域的研究構(gòu)建了一種新范式,具有重大意義。”
免疫助推器
幾種或能有效幫助“免疫哨兵”T細(xì)胞殺傷癌細(xì)胞的方法
檢查點(diǎn)阻滯藥物
“檢查點(diǎn)”蛋白抑制T細(xì)胞的活性,而抑制劑能夠在不同階段幫助松開(kāi)T細(xì)胞的“制動(dòng)器”
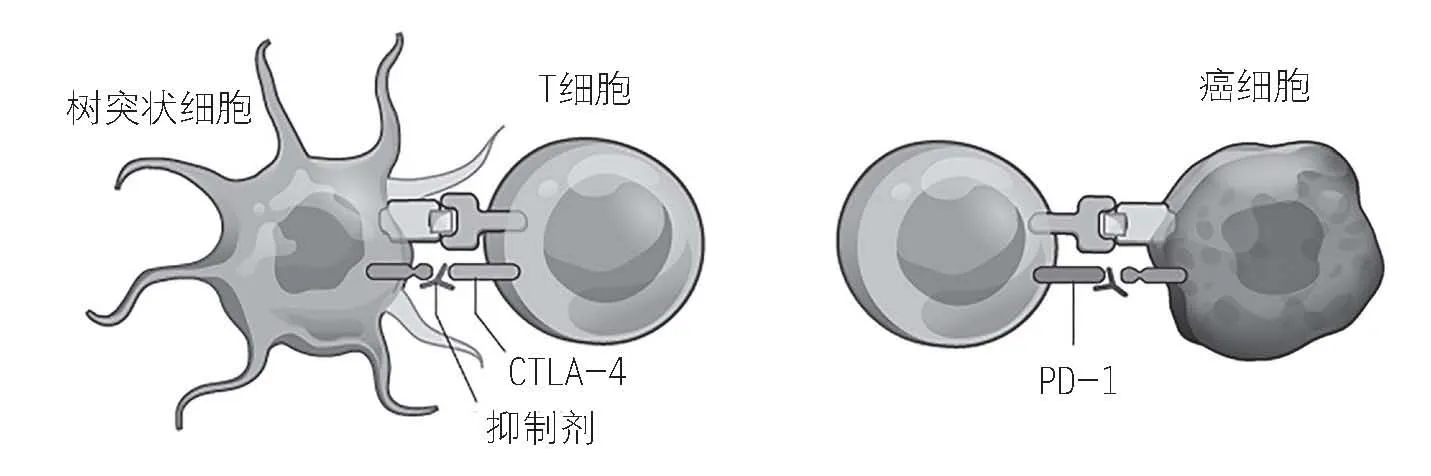
CTLA-4檢查點(diǎn)蛋白阻止了樹(shù)突狀細(xì)胞啟動(dòng)T細(xì)胞對(duì)腫瘤的識(shí)別,抑制劑可以PD-1檢查點(diǎn)蛋白阻止T細(xì)胞殺傷癌細(xì)胞,抑制劑可以使T細(xì)胞恢復(fù)活性
近年來(lái),臨床上以抑制CTLA-4和PD-1——又稱(chēng)作“免疫檢查點(diǎn)療法”——為原理的藥物研究進(jìn)展突飛猛進(jìn)。阻滯PD-1的療法經(jīng)試驗(yàn)證明在肺癌、腎癌、淋巴瘤和黑色素瘤方面有效。近期臨床試驗(yàn)對(duì)黑色素瘤患者使用靶向CTLA-1和PD-1的聯(lián)合療法,其療效優(yōu)于單一的CTLA-4療法。如今,科學(xué)家通過(guò)試驗(yàn)評(píng)估檢查點(diǎn)療法對(duì)大多數(shù)癌癥的療效,并嘗試靶向大量其他檢查點(diǎn)蛋白來(lái)測(cè)試它們是否也能作為目標(biāo)。
并非只有艾利森和本庶為此做出了貢獻(xiàn),還有一些人在檢查點(diǎn)抑制劑發(fā)現(xiàn)早期做出了貢獻(xiàn)。值得一提的有馬薩諸塞州波士頓丹娜法伯癌癥研究院的免疫學(xué)家戈登·弗里曼(Gordon Freeman),他很失望自己的貢獻(xiàn)未被諾獎(jiǎng)委員會(huì)認(rèn)可。弗里曼同波士頓哈佛大學(xué)醫(yī)學(xué)院艾琳·夏普(Arlene Sharpe)和康涅狄格州紐黑文耶魯大學(xué)陳列平兩位免疫學(xué)家研究檢查點(diǎn)蛋白,以及一個(gè)可以結(jié)合PD-1的分子PD-L1。
藥物伊匹單抗(ipilimumab)是能夠抑制CTLA-4的抗體,2011年獲得美國(guó)食品藥品管理局(FDA)的批準(zhǔn),成為第一個(gè)患者可得的檢查點(diǎn)抑制劑藥物。但弗里曼指出,CTLA-4抑制劑經(jīng)試驗(yàn)證實(shí),僅僅對(duì)黑色素瘤有效。而FDA批準(zhǔn)了靶向PD-1的藥物和PD-L1,可對(duì)13種不同的癌癥有效。“PD-1和PD-L1才是對(duì)廣大患者而言真正的福音,”弗里曼說(shuō),“而我們的研究是其基石。”
但是,弗里曼也補(bǔ)充說(shuō)CTLA-4是這方面研究的先驅(qū),正是艾利森對(duì)這一領(lǐng)域起了決定性作用。“艾利森是免疫療法真正的提倡者和擁護(hù)者,”他說(shuō),“CTLA-4是第一個(gè)真正的成功。”
不二之選
法國(guó)國(guó)家生物醫(yī)學(xué)研究所免疫學(xué)家杰羅姆·加隆(Jerome Galon)對(duì)諾獎(jiǎng)委員會(huì)的決定并不驚訝。“我認(rèn)為艾利森和本庶兩人實(shí)至名歸,”他說(shuō),“當(dāng)然會(huì)有其他人有獲獎(jiǎng)資格,但這兩位是不二之選。”
他還補(bǔ)充說(shuō),本次諾獎(jiǎng)反映了通過(guò)免疫方法抗擊癌癥已經(jīng)邁出了一大步。2012年,PD-1抑制劑被證實(shí)對(duì)肺癌有效后,這一領(lǐng)域迎來(lái)了爆發(fā)性的進(jìn)展,學(xué)術(shù)界和企業(yè)競(jìng)相為更多患者提供受益的機(jī)會(huì)。“10年前,除了一些免疫學(xué)家?guī)缀鯖](méi)有人對(duì)此感興趣,”加隆說(shuō),“如今已然天翻地覆。”
2013年,《自然》雜志采訪艾利森時(shí),他回憶起當(dāng)初這一方法并沒(méi)有引起制藥公司的興趣。“這很令人沮喪,”他說(shuō),“他們表示說(shuō)這可能對(duì)小鼠有效,但絕不適用于人。這個(gè)方法太過(guò)新穎而不尋常了。”
艾利森在多個(gè)公司奔波,嘗試尋找項(xiàng)目的投資者。最后紐約百時(shí)美施貴寶公司為伊匹單抗的誕生買(mǎi)了單。那之后,許多制藥公司都開(kāi)始了人體使用的檢查點(diǎn)抑制劑的研發(fā)。
加隆表示,焦點(diǎn)問(wèn)題在于這些藥物延長(zhǎng)患者生命的長(zhǎng)度,不應(yīng)該只以星期或月來(lái)計(jì)算,而應(yīng)以年為單位。但只有小部分患者的病癥有了較大改善,而研究者仍在爭(zhēng)相通過(guò)聯(lián)合檢查點(diǎn)抑制劑或其他一些方法來(lái)提升受益患者人數(shù)。“對(duì)比其他一些療法,該療法確實(shí)能夠?yàn)榛颊邘?lái)長(zhǎng)期生存,”加隆說(shuō),“不幸的是,僅有一小部分患者有反應(yīng)。”
“一路走來(lái),這一領(lǐng)域的發(fā)展是令人興奮的,”弗里曼說(shuō),“這一切都來(lái)自人們無(wú)限的創(chuàng)造力和精力。許多癌癥患者的狀況正越來(lái)越好,令人欣慰。”
2015年,艾利森因在癌癥免疫療法上的工作獲得了極具聲望的拉斯克獎(jiǎng)。2016年,本庶獲得京都獎(jiǎng)基礎(chǔ)科學(xué)獎(jiǎng),一項(xiàng)由稻盛基金會(huì)頒發(fā)的國(guó)際性獎(jiǎng)項(xiàng)。
資料來(lái)源 Nature

