高效液相色譜法測定桶裝水及水桶中雙酚A含量
劉 濤,黃子晏
(1. 莆田學院環境與生物工程學院,福建 莆田 351100;2. 福建省新型污染物生態毒理效應與控制重點實驗室,福建 莆田 351100)
0 引 言
雙酚A(BPA)是聚碳酸酯的生產單體,生產聚氯乙烯的穩定材料,環氧樹脂的主要組成部分,由俄國科學家Alexander P.Dianin在1891年利用兩分子苯酚和一分子丙酮在氯化氫催化下第一次合成出來[1]。由于雙酚A制品的良好機械性能、低吸水性及熱穩定性,因此被大量用于制作水管、水杯、奶瓶、玩具以及其他食品容器。然而雙酚A是一種環境類激素,能夠干擾人體內分泌系統[2],不僅能夠導致肥胖問題同時還有增加癌變[3]、畸形的可能。市場所售桶裝水,絕大部分水桶材均質為聚碳酸酯,雙酚A作為聚碳酸酯的合成單體,水桶中殘留的雙酚A有可能會從水桶遷移至飲用水中,進而進入人體內。
目前,雙酚A的殘留可通過液-液萃取[4]、固相萃取[5]進行富集,而后利用高效液相-熒光法[6]、液相色譜-質譜聯用[7]或氣相色譜-質譜聯用法[8]進行檢測,此外電化學[9-10]也是一種高靈敏檢測BPA的方法。LC-MS、GC-MS等儀器價格昂貴且操作復雜,而液相紫外檢測器在大多數實驗室都較為常見且操作簡單、維護方便。本文利用高效液相色譜-紫外檢測器建立一種簡單、高靈敏檢測桶裝水及水桶中雙酚A的檢測方法,并抽取莆田市售的桶裝水及水桶中雙酚A含量進行檢測。
1 實驗部分
1.1 實驗儀器和試劑
實驗儀器:高效液相色譜儀(LC1100),美國安捷倫公司,配備隔膜真空泵、自動進樣系統、柱溫箱、可變波長掃描紫外檢測器;純水機(ultra pure),上海和泰儀器有限公司;電子天平(Sartorius BS224S),賽多利斯;全自動固相萃取儀(Sepaths UP),萊伯泰科儀器股份有限公司;紫外可見分光光度計(UV-2500),島津;0.45 μm 有機濾膜,上海市新亞凈化器件廠。
化學試劑:甲醇,色譜純,天津市化學試劑供銷公司;無水乙醇,分析純,天津市化學試劑供銷公司;四氫呋喃,分析純,國藥集團化學試劑有限公司;乙酸乙酯,分析純,天津市鼎盛鑫化工有限公司;乙腈,色譜純,上海阿拉丁生化科技有限公司;雙酚A,分析純,上海麥克林生物制藥有限公司。
1.2 實驗方法
1.2.1 標準溶液配置
準確稱取 0.025 0 g(精確到 0.000 1 g)雙酚 A,置于燒杯中,甲醇溶解。將溶液轉移至250 mL容量瓶中,甲醇定容至刻度線,搖勻,得到0.1 mg/mL的雙酚A標準儲備溶液,密封保存。使用前根據需要吸取適量標準儲備液,用甲醇稀釋配置成質量濃度為0.4,1,2,4,5,10 μg/mL 的工作標準溶液,0.45 μm濾膜過濾備用。
1.2.2 色譜分析條件
流動相為乙腈-水,V(乙腈):V(水)=60:40,流量1 mL/min,檢測波長 224 nm,自動進樣器進樣,進樣體積 10 μL。
1.2.3 樣品處理
依次用10 mL甲醇、10 mL超純水活化C18固相萃取柱,流量為 1.5 mL/min。上樣 1 000 mL,上樣完畢后氮吹干燥3 min。分兩次用3 mL甲醇洗脫萃取柱,洗脫程序為浸泡90 s,最后氮吹干燥150 s,洗脫液氮吹定量濃縮至 1 mL,0.45 μm濾膜過濾,進樣分析。
1.2.4 水桶塑料預處理
取桶裝水塑料,超純水沖洗后,晾干將其剪碎,精密稱取1.000 g樣品置于燒杯中,加入10 mL二氯甲烷,超聲(功率 120 W;頻率 40 kHz)溶解并混勻,加入15 mL甲醇,充分震蕩搖勻,使高分子化合物沉淀,過濾,濾液在40 ℃水浴蒸干,用甲醇溶解殘渣,轉移至10 mL容量瓶中,甲醇定容至刻度,0.45 μm 濾膜過濾,備用。
1.2.5 水樣與水桶雙酚 A 含量的檢測
隨機選取莆田市售5個品牌的桶裝水,分別取常溫保留10,20,30 d的桶裝水水樣,每個時間的水樣平行測定3組。按照1.2.3方式經固相萃取濃縮至1 mL,按1.2.2色譜條件檢測分析。已提取的水桶預處理液按色譜條件進樣分析。
2 結果與討論
2.1 洗脫劑的選擇
取質量濃度為4 μg/mL雙酚A標準液1 mL置于1 000 mL容量瓶中,超純水定容至刻度線,分別用甲醇、四氫呋喃、無水乙醇、乙酸乙酯4種有機溶劑進行固相萃取,樣品經過C18萃取柱提取后用高效液相色譜檢測,計算得到4種洗脫劑的回收率,回收率結果見圖1。根據測量計算結果,4種洗脫劑中甲醇的洗脫效果最好,因此選用甲醇作為水樣固相萃取的洗脫劑。
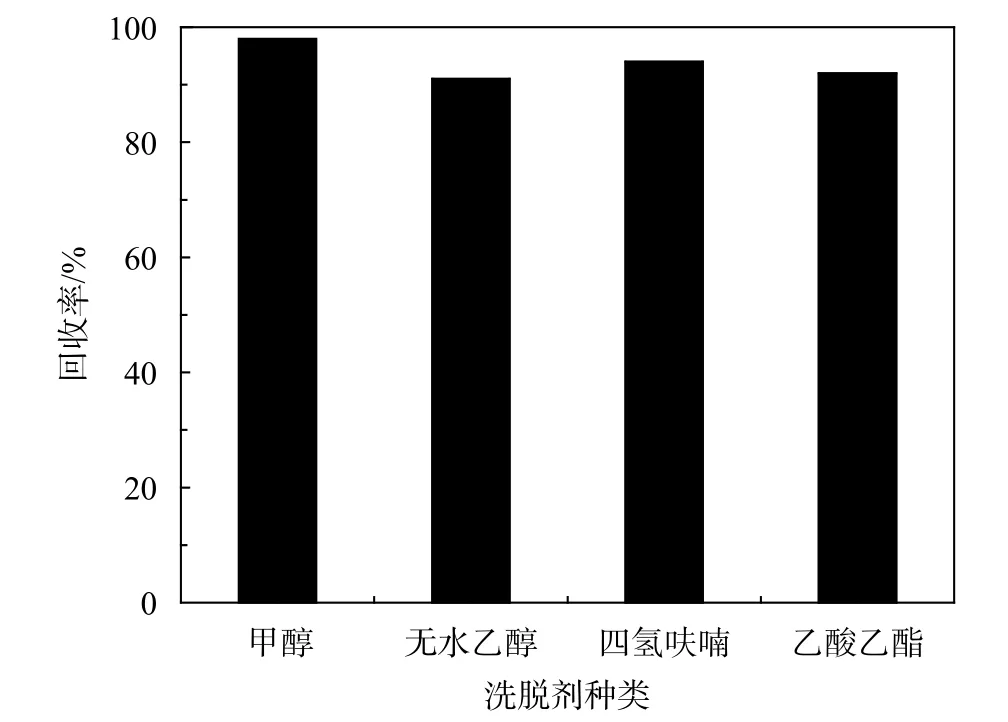
圖1 不同洗脫劑洗脫效果
2.2 HPLC紫外檢測波長的選擇
查閱相關文獻,雙酚A紫外吸收光譜在202,227,278 nm波長下有較強的吸收[11]。對雙酚A溶液在190~300 nm波長范圍內進行掃描,所得紫外吸收光譜如圖2所示,可以看到,雙酚A在224 nm和278 nm附近有強紫外吸收,且224 nm波長下紫外吸收較強,因此選擇224 nm作為液相檢測的波長。
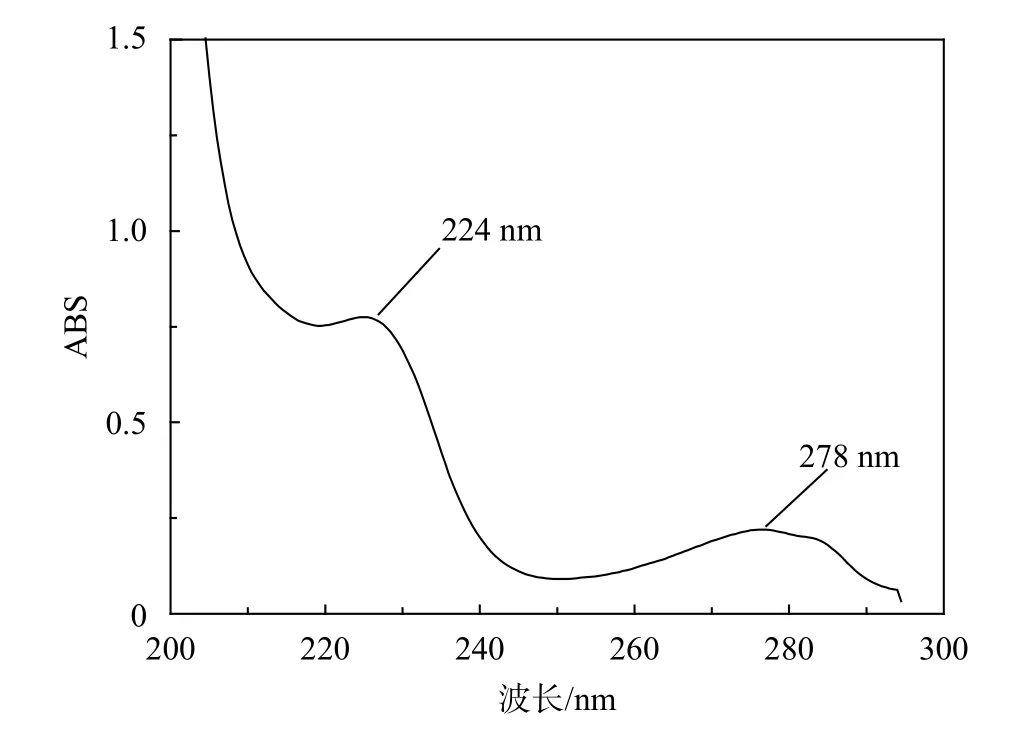
圖2 雙酚A紫外吸收光譜
2.3 流動相的選擇
考察了不同流動相對雙酚A色譜峰的影響,在高效液相色譜中常用的流動相為甲醇、乙腈和水。首先用甲醇-水為流動相,改變甲醇與水的比例,雜峰與雙酚A溶液出峰時間較近,如圖3所示。雜峰面積較大,在某些比例下會出現負峰,對目標峰的定性以及定量產生影響,且溶劑甲醇在低波長情況下存在紫外吸收。為了改善分離效果,利用乙腈-水作為流動相,調整比例,在V(乙腈):V(水)=60:40時,色譜圖良好,峰形尖銳,對稱性良好,見圖4。雜峰位置在 1~1.5 min,雙酚 A 出峰時間在 2.790 min,間隔時間長,雜峰位置不會對雙酚A產生影響;并且可以在短時間內將雙酚A分離洗脫,因此選乙腈-水(V/V,60:40)作為本實驗的流動相。
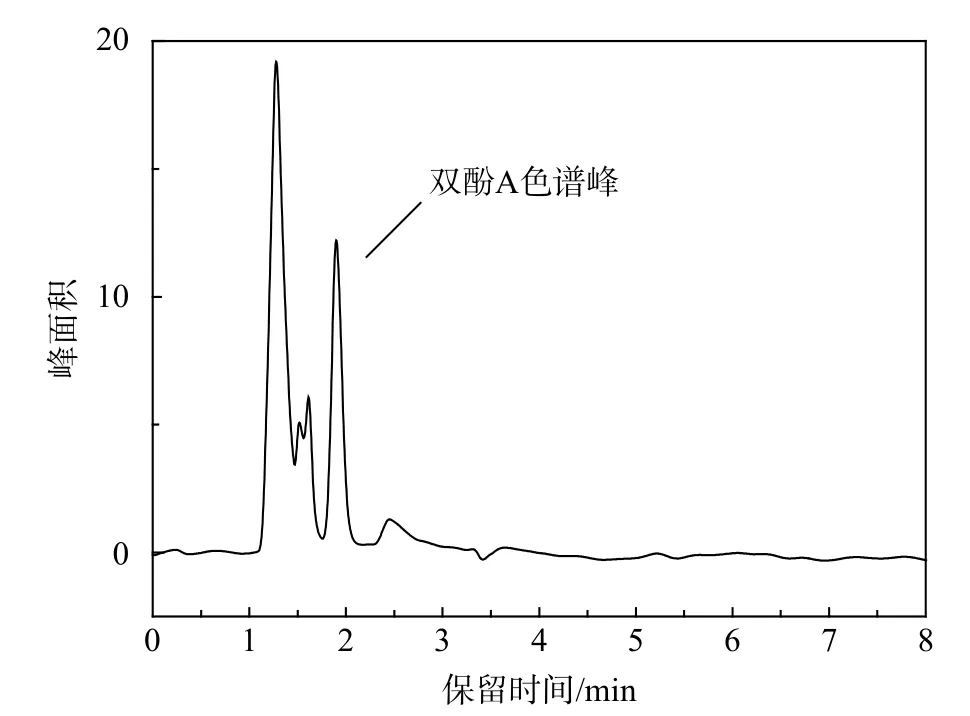
圖3 甲醇-水雙酚A色譜圖
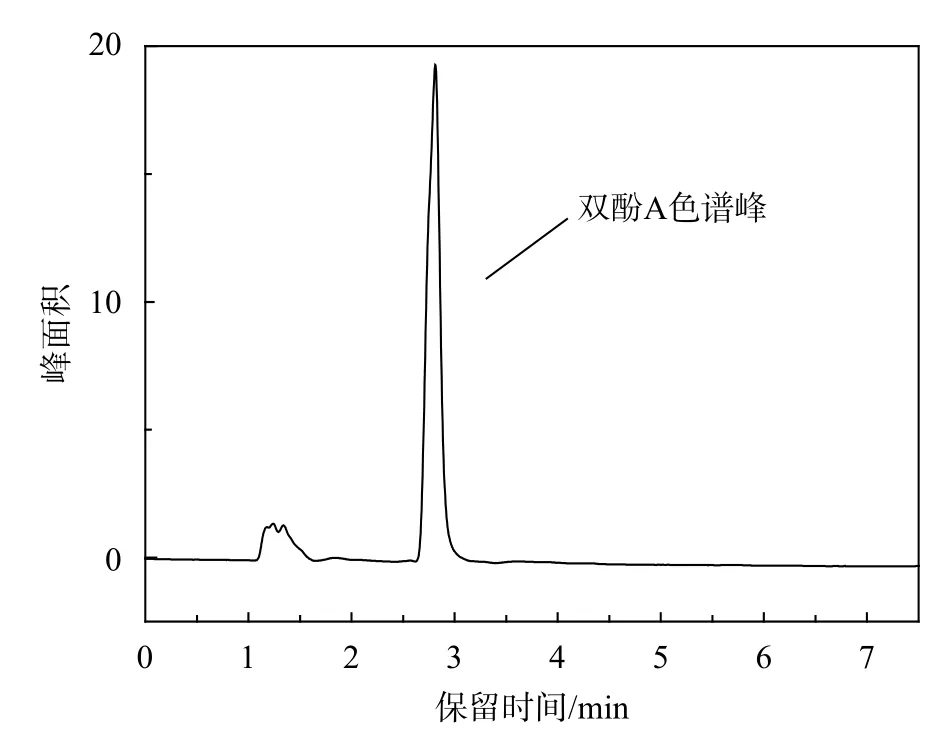
圖4 乙腈-水雙酚A色譜圖
2.4 線性關系和重現性
將1.2.1配制系列濃度梯度溶液,在選定的色譜條件下進行測定,以雙酚A標準溶液濃度為橫坐標,色譜峰面積為縱坐標,做標準曲線,如圖5所示。其線性回歸方程為Y=42.152 39X–0.175 58,線性相關系數為r2=0.999 8,且在 0.4~10 μg/mL 的濃度范圍內線性關系良好。
取質量濃度為1 μg/mL雙酚A標準樣品溶液,連續進樣5次,保留時間與峰面積如表1所示,相對標準偏差分別為2.05%、2.26%。
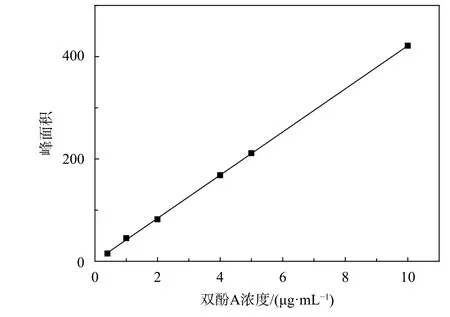
圖5 雙酚A溶液標準曲線
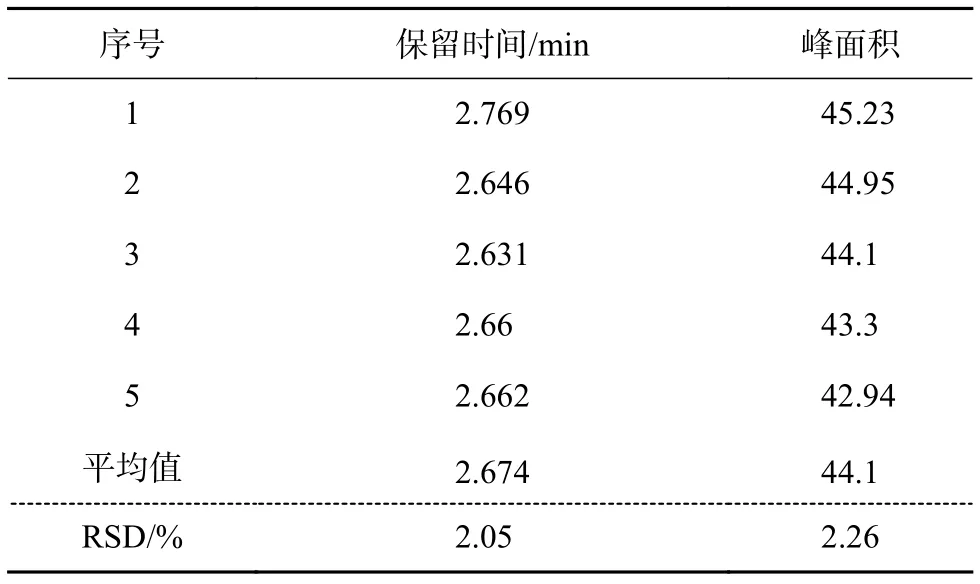
表1 保留時間與峰面積重現性
2.5 檢出限和定量限
根據方法檢出限計算方法,以質量濃度為0.4 μg/mL的純水加標樣品,按照選取的最優條件進行固相萃取-高效液相測定雙酚A的含量,平行測定6次,6次測定的標準偏差δ值為0.022,根據檢出限計算公式 MDL=3.143δ,得到檢出限為 0.069 μg/mL,定量限為 0.23 μg/mL。
相關國家標準GB4806.7-2016《食品接觸用塑料材料及制品》和GB5009.156-2016《食品接觸材料及制品遷移試驗預處理方法通則》中對水基食品模擬物中雙酚A的檢出限和定量限分別為1 μg/L和10 μg/L;本文建立的雙酚A檢測方法能夠滿足對水中痕量雙酚A的檢測。
2.6 回收率與精密度
為了驗證提取方法的可靠性,進行回收率試驗,以不含雙酚A的超純水為空白基質,在1 L容量瓶中分別加入質量濃度為 0.4,1,2,4,5 μg/mL 的1 mL雙酚A標準溶液,超純水定容至刻度線。按照選定的最佳條件進行固相萃取處理后上機檢測。計算回收率見表2,結果顯示平均回收率為98.3%,對于高、中、低濃度樣品的回收率都有滿意的效果。
選取質量濃度為1 μg/mL的純水加標樣,按照方法指定的檢測步驟,平行測試6次,檢驗該方法的精密度。結果如表3所示,相對標準偏差為1.99%,數據重現性好,精密度高。
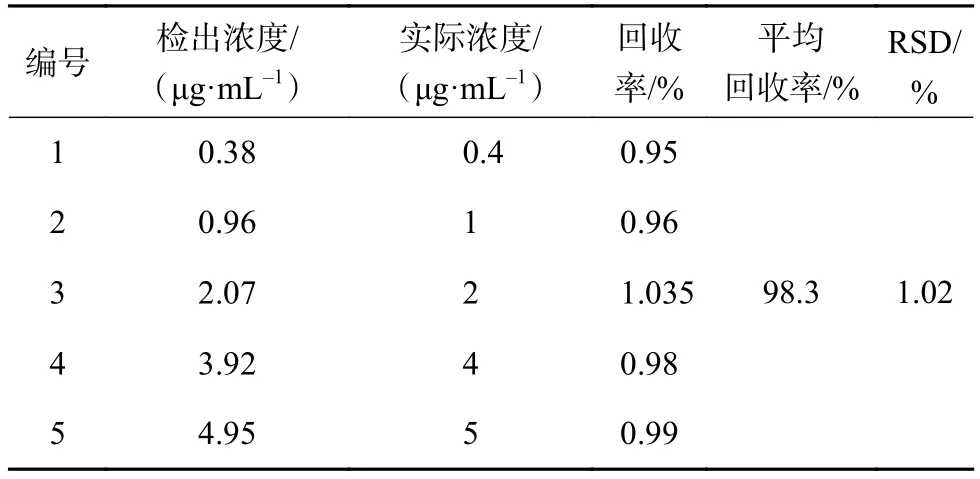
表2 回收率實驗結果

表3 精密度實驗結果
2.7 檢測結果
取5個品牌桶裝水,檢測已保留的桶裝水水樣,每個品牌分別儲存10天、20天和30天后,經檢測均未檢測到雙酚A的存在。雖然在常溫儲存、保質期內的桶裝水中并未檢測出雙酚A,但仍存在雙酚A向水中遷移的潛在危害。相關研究表明日曬、儲存溫度及生產過程中洗桶程序等因素對雙酚A的遷移都有一定的影響[12]。
水桶材料中雙酚A的平均含量為37.1 μg/g,且5個品牌的雙酚A含量大致相同,結果見表4。相關資料顯示[13]食品中雙酚A的遷移主要來自聚合物表面降解,而聚合物中雙酚A的殘余量對其遷移影響很小。因此,應針對食品包裝容器的PC材質進行限制,采用PP或其他更安全的材質。

表4 水桶檢測結果
3 結束語
本文建立了固相萃取高效液相檢測桶裝水中雙酚A含量的檢測方法,對實驗條件進行優化,以甲醇為洗脫劑對水樣進行固相萃取處理,乙腈-水(60:40)為流動相,224 nm波長下實現對水樣中BPA簡單、快速、高靈敏檢測。方法檢出限0.069 μg/mL,定量限為0.23 μg/mL,回收率為98.3%。隨機選取市售5個品牌桶裝水,在保質期內的桶裝水中并未檢測到雙酚A的存在,水桶材質中檢測出雙酚A的含量為37.1 μg/g;在水樣中雖未檢測出雙酚A,但仍有一定潛在溶出風險。根據實驗結果,針對PC食品包裝材料應更換更加健康安全的材質。

