核酸試紙條法檢測食品中小腸結腸炎耶爾森菌
張宏偉,莎日娜,鄭文杰,王碩
(1.天津科技大學食品工程與生物技術學院,天津300457;2.天津出入境檢驗檢疫局,天津300461;3.天津醫學高等專科學校,天津300222)
小腸結腸炎耶爾森菌(Yersinia enterocolitica),是腸桿菌科、耶爾森菌屬的一個種,廣泛分布于自然界的土壤、水體中,野生動物,家畜,昆蟲中均有檢出,生存溫度從0℃~40℃,在0℃~40℃環境中保持生命力可達18個月之久,-25℃能存活24 h以上,這種嗜冷性質決定了保存在4℃~5℃冰箱中的食品更具有傳染的危險性。
小腸結腸炎葉爾森氏菌是一種急性胃腸炎型食物中毒病原菌,可致人畜患病。耶爾森氏菌病典型癥狀為胃腸炎、發熱,亦可引起闌尾炎和反應性關節炎,另一個并發癥是敗血癥,死亡率較高。經典檢測方法耗時長,步驟繁多,操作復雜,成本高昂,不能滿足快速鑒定食品中是否污染該菌的要求,本研究旨在應用聚合酶鏈反應(polymerase chain reaction,PCR)技術建立檢測方法,結合免疫金試紙條檢測方法,避免PCR方法結果檢測需要電泳使用溴化乙錠(ethidium bromide,EB)、PCR產物污染等問題,探索建立一種快速準確避免污染的檢測方法,便于在實驗室推廣應用。
1 材料與方法
1.1 材料與試劑
基因組提取試劑盒:Promega公司;HS Ex Taq DNA聚合酶(5 U/μL):大連寶生物公司;引物合成由上海生物工程公司完成;核酸快速檢測試紙條:優思達公司。
菌株采用4株美國模式培養物集存庫(American type culture collection,ATCC)菌株和22株中國醫學細菌保藏管理中心(national center for medical culture collections,CMCC)小腸結腸炎耶爾森氏菌標準菌株,9株其它耶爾森氏菌屬標準菌和其它菌屬17株ATCC標準菌株,具體見表1。

表1 試驗菌株Table 1 Bacterial strains for detection
1.2 儀器與設備
PrC-200熱循環儀:MJ公司;1510核酸蛋白分析儀:賽默飛世爾科技有限公司。
1.3 方法
1.3.1 引物設計
利用細菌16s-23srDNA間區序列設計特異性引物見表2,引物組合見表3。在引物合成時,一條引物的5’端標記異硫氰酸熒光素(fluorescein isothiocyanate,FITC),另一條引物的 5’端標記地高辛(Digoxin)。

表2 引物序列Table 2 Primers sequence
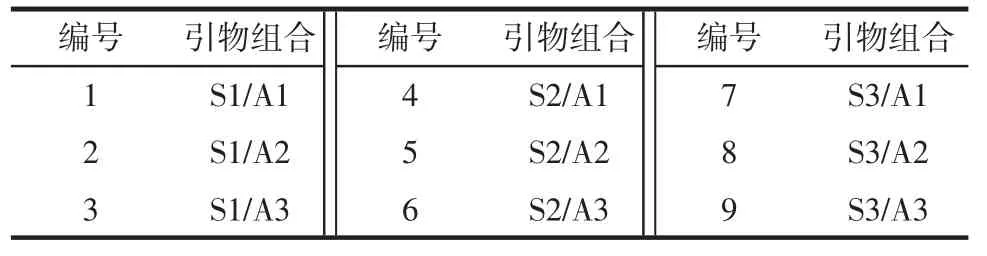
表3 16s-23s rDNA間區引物組合Table 3 Detection primer combination
1.3.2 反應體系
體系的構成如下:10×buffer,5 μL;引物(10 μmol/L)各 2 μL;dNTP(10 mmol/L),1 μL;模板 DNA,2 μL;Taq酶(5 U/μL),1 μL;ddH2O,37 μL。
反應條件:94℃預變性10 min;擴增循環:94℃30 s,56℃溫度退火 15 s,72℃延伸 60 s,進行 30個循環,72℃延伸5 min,4℃保存。
1.3.3 特異性試驗
利用表1中的標準菌株對引物分別進行特異性試驗,以篩選出通用性好,特異性強的引物。
1.3.4 靈敏度試驗
取1 mL標準菌株增菌液用于提取基因組DNA,利用紫外分光光度計檢測DNA質量及純度。將PCR模板進行10倍梯度稀釋,按建立方法擴增,同時用凝膠電泳和膠體金試紙條方法觀察檢測結果。
1.3.5 樣品加菌試驗
3份經證實未污染結腸炎耶爾森氏菌的碎肉樣品,1份作為對照樣品,2份各25 g分別接種1 mL不同濃度小腸結腸炎耶爾森氏菌液和1 mL 10倍濃度的大腸埃希菌和金葡菌菌液,混勻后進行檢測。
1.3.6 市售樣品檢測
利用建立的方法對市場購買的樣品進行檢測,并與GB 4789.8-2016《食品安全國家標食品微生物學檢驗小腸結腸炎耶爾森氏菌檢驗》進行比較。
2 結果與分析
2.1 特異性引物的確定
應用溫度梯度PCR,分別用9對引物進行PCR檢測,發現S1/A2引物組合在56℃退火時特異性最好,實驗用近緣菌株都無假陽性出現,而小腸結腸炎耶爾森氏菌都出現特異性泳帶。因此,本研究選擇S1/A2作為小腸結腸炎耶爾森氏菌PCR檢驗的特異性引物,退火溫度確定為56℃,其擴增產物為282 bp。
2.2 特異性試驗
小腸結腸炎耶爾森氏菌標準菌株檢測結果均為陽性結果,耶爾森氏菌其他屬標準菌株及對照標準菌株檢測結果均為陰性,部分檢測結果見圖1、圖2。
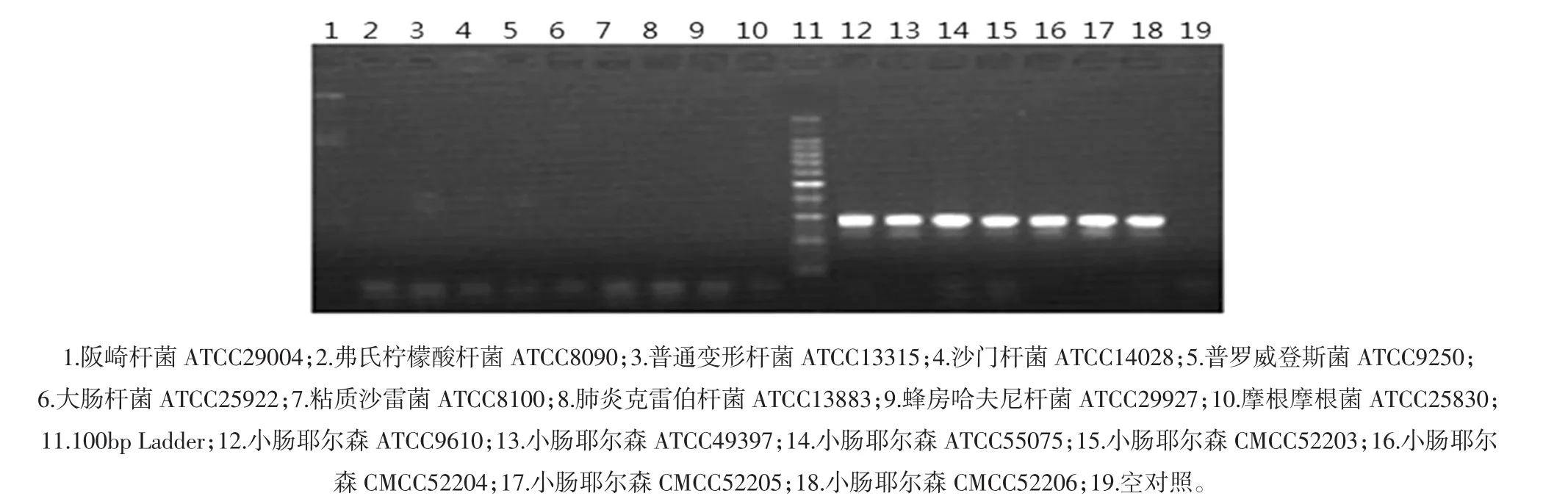
圖1 特異性檢測結果Fig.1 Detece of specificity by electrophoresis

圖2 對照菌株特異性檢測結果Fig.2 Detece of specificity by nucleic acid strips
檢測結果顯示小腸結腸炎標準菌株檢測沒有出現假陰性結果,耶爾森氏菌屬其他種的標準菌株及對照標準菌株檢測均沒有出現假陽性結果,說明引物特異性良好,試紙條顯示的檢測結果與電泳結果相符合,表明其檢測特異性良好。
2.3 靈敏度試驗
模板稀釋倍數分別為 100、10、1、10-1、10-2、10-3、10-4、10-5、10-6、10-7μg/mL,檢測結果見圖 3。

圖3 靈敏度檢測結果Fig.3 Detece of sensitivity
檢測結果表明,隨著稀釋度的增加,檢測條帶逐漸減弱,當稀釋濃度達到10-3μg/mL時,電泳檢測結果顯示為陰性,而試紙條則有淡紅色條帶出現,說明試紙條檢測靈敏度較電泳方法高一個數量級,可達到10-3μg/mL。
2.4 樣品加菌試驗
添菌靈敏度檢測結果見圖4。
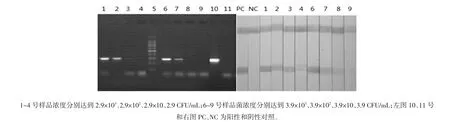
圖4 添菌靈敏度檢測結果Fig.4 Detece of sensitivity in samples
檢測結果表明,盡管有高濃度的干擾菌存在,電泳檢測靈敏度可達到101CFU/mL,而試紙條檢測靈敏度較電泳檢測高一個數量級,達到了100CFU/mL。
2.5 市售樣品檢測
用PCR-試紙條法對市售722份水產及禽畜肉進行檢測,并與國標方法檢測結果進行比較,結果見表4。
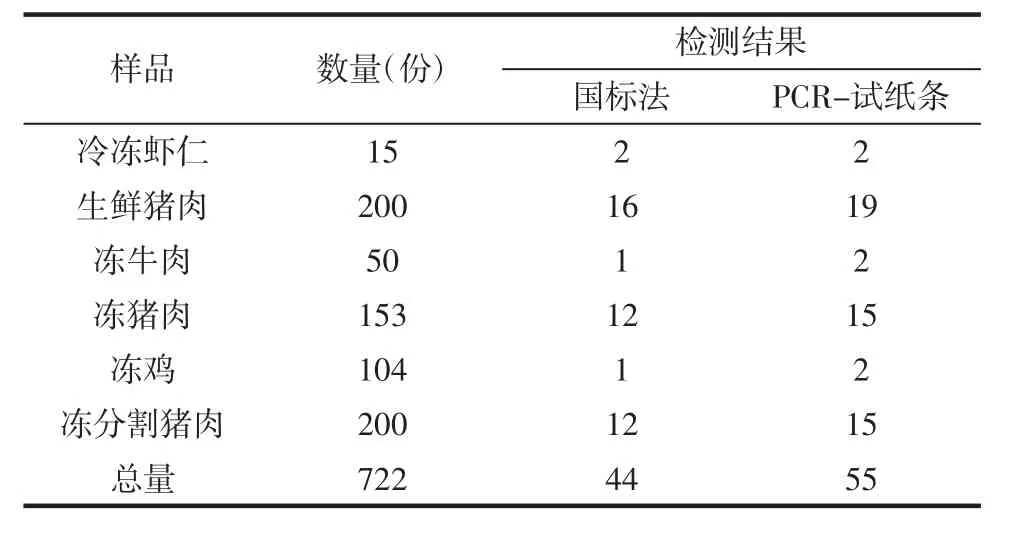
表4 市售樣品檢測結果Table 4 Detection result of samples
檢測結果表明,PCR-試紙條方法檢測陽性率高于國標方法。以國標方法為基準方法,對新建立的方法進行評估,見表5。
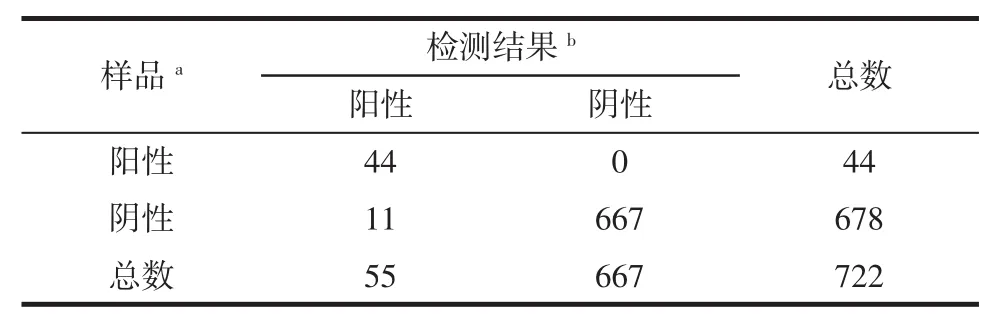
表5 PCR-試紙條方法評估表Table 5 Assessment of PCR-immunoblotting strips method
3 討論
檢測假陽性的發生可能因素包括:(1)如果檢測中多對引物相互反應,出現引物二聚體則可能導致假陽性結果。(2)樣品中存在目標菌死菌,作為較為靈敏的核酸檢測方法,檢測到死菌信號。(3)傳統的檢測方法對檢驗人員的經驗要求較高,如果檢驗人員經驗不足,則使用經典檢測方法有可能造成漏檢。使用PCR-試紙條方法作為篩選方法,可以彌補檢驗人員因經驗不足造成的漏檢情況。以本研究建立的快速方法檢測到陽性結果,需要用國標方法加以確認,以國標方法檢測作為判定依據。
國家標準小腸結腸炎耶爾森氏菌耶爾森氏檢測方法至少需要7天完成檢測、容易發生檢測人員因經驗不足造成漏檢,采用本研究建立的檢測方法特異性強,靈敏度高,可在24小時內得到檢測結果。本研究采用試紙條代替凝膠電泳,既減少了PCR產物的二次污染,又避免了EB對人體的傷害和對環境的污染,是傳統方法的有益補充。

