歐龍馬滴劑口服加超短波輔助治療小兒分泌性中耳炎
孫紅軍
(陜西省西安市兒童醫院 耳鼻咽喉科, 陜西 西安, 710003)
分泌性中耳炎(SOM)是耳鼻喉科常見的非化膿性疾病,其臨床特征主要表現為聽力下降、鼓室積液[1]。臨床常用鼓膜切開術、鼓室穿刺抽液等多種外科手術方法進行治療,但效果均欠佳[2]。本研究就歐龍馬滴劑聯合超短波治療小兒SOM的臨床效果進行了研究,現將結果報告如下。
1 資料與方法
1.1 一般資料
選擇2014年6月—2017年6月在耳鼻喉科接受診治的SOM患兒128例(193耳),患兒均經耳鏡檢查及聽力診斷確診為SOM[3]。采用隨機抽簽法將患兒均分為2組,其中對照組64例(87耳),男35例,女29例; 年齡3~14歲,平均(5.73±1.26)歲; 病程5 d~3個月,平均(1.06±0.53)個月; 聲導抗: 35耳為B型, 52耳為C型。觀察組64例(106耳),男33例,女31例; 年齡2~13歲,平均(5.52±1.33)歲; 病程7 d~3個月,平均(1.11±0.64)個月; 聲導抗: 47耳為B型, 59耳為C型。2組患兒性別、年齡、病程及聲導抗耳型間差異無統計學意義(P>0.05)。納入標準: 年齡≤14歲者; 未接受過歐龍馬滴劑及超短波治療者。排除標準: 鼻或鼻咽部病變者; 化膿性中耳炎者。所有患兒家屬自愿參與此研究,且簽署了知情協議書。
1.2 治療方法
對照組患兒口服歐龍馬滴劑(仙璐貝,批準文號Z20110001),劑量為50滴/次, 3次/d。觀察組在對照組基礎上加用超短波進行聯合治療。患兒選坐位或仰臥位,將五官超短波電療儀中的電極并列置于耳屏前和乳突部位,或將其中一支電極置于患耳外耳道口,另一側電極置于對置頰部, 15 min/次,1次/d, 連續治療5 d。
1.3 觀察指標
分別于治療前后抽取2組患兒肘靜脈血。3 000 轉/min條件下離心15 min, 將血清在-70 ℃保存,用于患兒血清免疫球蛋白(IgG、IgM、IgE)、水通道蛋白(AQP1、AQP4)及血清炎癥指標[IL-6、PCT及TNF-α]水平測定。IgE、AQP1、AQP4、IL-6及 TNF-α選擇酶聯免疫吸附法測定; IgG、IgM則采用速率散射比濁法; PCT選擇雙抗夾心免疫發光法進行測定。
1.4 療效評價標準
①聲導抗療效。治愈: 聲導抗檢查顯示鼓室曲線A型,臨床癥狀完全恢復正常; 顯效: 聲導抗檢查鼓室曲線中出現波峰,或患耳鼓室內負壓顯著下降,臨床癥狀有所改善,但未恢復到正常水平; 有效: 患耳鼓室內負壓稍下降; 無效: 聲導抗檢查鼓室曲線無改變。總有效率=(總病例數-無效數)/總病例數×100%。② 綜合療效。顯效: 治療后患兒臨床主要癥狀全部消失,鼓膜和語頻聽力完全恢復,導抗圖恢復為A型; 有效: 治療后患兒臨床主要癥狀基本消失,鼓膜有較好改善,語頻聽力提高10~15 dB, 但未完全恢復,導抗圖B型; 無效: 治療后,上述癥狀指標為顯著改善,甚至加重。總有效率=(總病例數-無效數)/總病例數×100%。
1.5 統計學方法
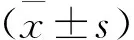
2 結 果
2.1 血清免疫球蛋白水平變化比較
治療前, 2組患兒血清免疫球蛋白IgE、IgG及IgM含量差異無統計學意義(P>0.05)。治療后, 2組患兒上述IgE含量顯著下降, IgG及IgM含量顯著上升,且觀察組患兒上述免疫球蛋白含量均優于對照組,差異有統計學意義(P<0.05)。見表1。
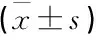
表1 2組患兒治療前后血清免疫球蛋白含量變化對比
與治療前比較, *P<0.05; 與對照組比較, #P<0.05。
2.2 血清炎癥因子水平變化比較
治療前, 2組患兒血清炎癥因子IL-6、TNF-α及PCT水平差異無統計學意義(P>0.05)。治療后, 2組患兒上述炎癥因子水平顯著下降,且觀察組患兒上述因子水平均優于對照組,差異有統計學意義(P<0.05)。見表2。
2.3 血清AQP1 及AQP4表達水平比較
治療前, 2組患兒血清中AQP1 及AQP4表達水平差異無統計學意義(P>0.05)。經治療, 2組患兒血清中上述2種水通道蛋白表達水平均顯著升高,且觀察組患兒表達水平優于對照組,差異有統計學意義(P<0.05)。見表3。
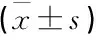
表2 2組患兒治療前后血清中炎癥指標變化情況對比
與治療前比較, *P<0.05; 與對照組比較, #P<0.05。
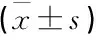
表3 2組患兒治療前后血清水通道蛋白亞型AQP1 及AQP4表達水平比較 ng/mL
與治療前比較, *P<0.05; 與對照組比較, #P<0.05。
2.4 聲導抗療效比較
對照組痊愈13例,顯效25例,有效22例,無效27例; 觀察組痊愈18例,顯效33例,有效37例,無效18例。觀察組患兒治療后聲抗檢查總有效率為83.02%,顯著高于對照組的68.97%(P<0.05)。
2.5 綜合療效比較
對照組顯效29例,有效22例,無效13例; 觀察組顯效48例,有效13例,無效3例。觀察組患兒治療綜合有效率為95.31%, 顯著高于對照組的79.69%(P<0.05)。
3 討 論
咽鼓管功能障礙是引發小兒SOM的基本原因。咽鼓管功能障礙導致患兒通氣受阻,嚴重影響中耳部位氣體交換,導致中耳腔內氧分壓與二氧化碳分壓失衡,黏膜腺體產生大量分泌物,從而導致中耳腔內出現積液。水通道蛋白是一種控制細胞水分吸收外排,調節局部液體平衡的膜蛋白。其中AQP1及AQP4表達量與SOM病程密切相關。其中AQP1在SOM患者咽鼓管及鼓室黏膜中表達量顯著低于健康患者。AQP4主要分布于內耳,患者聽力受損程度與其表達量呈反比[4]。體外實驗發現,AQP4基因敲除后,小鼠聽力嚴重受損,表明中耳腔中AQP4在維持內穩態及預防中耳積液方面具有重要作用[5]。此外,感染與免疫因素也是引發該類疾病的主要病因。姜胤輝[6]研究發現,SOM患者血清中IL-4、IL-6水平顯著高于健康組,IFN-α顯著降低,表明SOM形成與免疫反應相關。而以往報道[7]顯示,小兒SOM與Ⅰ型和Ⅲ變態反應密切相關。患兒體內Th1下降、Th2增加,導致Th1/Th2失衡,使得機體內細胞因子間相互調控發生紊亂。當Th2占優勢時,體內體液免疫功能增強,從而引發Ⅰ型變態反應。與成人比,小兒咽鼓管短直,更易發生感染,造成炎性細胞脫顆粒,分泌大量細胞因子,因此出現局部Ⅲ型變態反應。報道[8]顯示, IgE是Ⅰ型變態反應的主要抗體, SOM患者血清中IgE水平高于正常人。因此,治療SOM關鍵在于改善咽鼓管功能,促進黏液吸收或外排。
歐馬龍滴劑是一種由歐龍膽、報春花、酸模、洋接骨木及馬鞭草制備而成的重要滴劑。可通過加速上皮細胞CI轉運,促進機體水合作用及分泌物稀化,提高黏膜纖毛擺動頻率,從而加速機體分泌物化解作用。此外,還具有較強的抗病毒、抗炎及免疫調節功效。歐馬龍滴劑可通過抑制炎性介質合成,減輕患者炎癥作用。沈瑩等[9]表明,歐龍馬滴劑可提高鼻竇炎患者鼻黏膜傳輸速率; 莊麗萍等[3]指出,歐龍馬滴劑可有效降低鼻竇炎患者體內炎癥反應; 李英來等[10]指出, 6~12月SOM嬰兒采用歐馬龍滴劑進行治療,可有效降低抗菌藥物性肝損傷,提高療效,安全性高。
超短波具有很強穿透力,可直接穿透至病灶組織,病灶區離子及水分子受高頻震蕩釋放出巨大能量,促使局部組織體溫升高,血管擴張,改善血液微循環,同時促進體內白細胞增殖,增強巨噬細胞吞噬作用,加速機體代謝及炎癥吸收,從而發揮消炎、消腫及修復功效。超短波配合藥物治療可有效縮短病程,提高治療效率,降低不良反應率[11], 可有效降低急性胰腺炎患者血清炎性因子,減輕炎性反應[12]。
本研究結果顯示,聯合治療組患兒血清免疫球蛋白、水通道蛋白亞型及炎性因子水平均顯著優于對照組,表明該治療方法可通過促進水通道蛋白亞型AQP1及AQP4上調表達,改善患兒鼓室及內耳微環境,依靠免疫調節作用抑制體內炎癥反應,降低炎癥反應對患兒組織損傷。觀察組患兒治療后聲導抗有效率及綜合有效率均顯著高于對照組,表明該治療方法不僅可以減少炎癥反應對患兒機體損傷,同時促進中耳組織修復。歐龍馬滴劑加超短波可有效提高SOM患兒免疫功能,抑制炎癥反應,提高治療效率。

