4,6-二氨基-5-醛基嘧啶與間苯二甲酸為共配位的金屬鎘(Ⅱ)配合物的合成
杜曉蕊 ,楊翰文 ,樊嬌嬌 ,蘇育菲 ,趙紅昆
(1.天津師范大學 化學學院,天津 300387;2.天津師范大學 無機-有機雜化功能材料化學教育部重點實驗室,天津 300387;3.天津師范大學 天津市功能分子結構與性能重點實驗室,天津 300387)
嘧啶雜環是生物分子遺傳信息載體DNA和RNA的重要結構單元,具有特殊結構和較好生物活性的吡啶、嘧啶類氮雜環化合物在醫學、農業、化學材料和生命科學等相關領域應用廣泛[1-5].有關嘧啶雜環衍生物的相關研究已成為化學和生物化學領域的重要課題之一[6-10].根據嘧啶六元環母體上2位、4位、5位、6位的取代基種類和數量,可將嘧啶衍生物分為單取代嘧啶、二取代嘧啶、多取代嘧啶、吡啶并嘧啶衍生物、嘧啶并嘧啶衍生物[11]等.嘧啶類氮雜環化合物可作為強配位能力的多N配位點配體而構成結構新穎的配合物:如Yang等[12]選擇腺嘌呤為主配體與金屬銅配位,合成了除氨基之外嘧啶和吡啶環的4個氮原子全部參與配位的二維網狀結構配合物;Domínguez-martín等[13]選擇4-氨基吡唑并[3,4-d]嘧啶為主配體與金屬銅配位,合成了2個新穎的配合物,并研究了這種配體的分子識別模式,為進一步了解在生物系統內嘌呤與金屬的結合行為提供了新見解.另外,嘧啶類氮雜環化合物還可以作為氫鍵的供體或受體,產生結構新奇、功能奇特的配合物,應用于分子識別[14]、藥物合成[15]、Watson-Crick和Hoogsteen氫鍵研究[16]等.羧酸配體與中心原子之間不僅可以實現多種多樣的配位模式,還可以與中心原子形成次級結構單元[17-19].溶劑極性、溶液pH值、體系穩定性、合成方法等都會影響羧基的去質子化程度,進而影響選擇的契合配位模式和配合物結構的構筑.
為了進一步研究嘧啶衍生物的金屬配合物以及氫鍵在自組裝過程中的作用,選用4,6-二氨基-5-醛基嘧啶和間苯二甲酸作為混合配體,與金屬鎘(Ⅱ)離子進行自組裝反應,在水熱條件下合成了首例基于4,6-二氨基-5-醛基嘧啶的鎘(Ⅱ)配合物,并對其合成方法、晶體結構和熱穩定性進行了詳細研究.
1 實驗
1.1 儀器與試劑
儀器:Apex-ⅡCCD X-線單晶衍射儀,德國Bruker公司;CE-440元素分析儀,美國Leeman-Labs公司;IR-200傅里葉紅外光譜儀,美國Nicolet公司;Q50熱重分析儀,美國TA公司.
試劑:4,6-二氨基-5-醛基嘧啶,北京百靈威科技有限公司;間苯二甲酸,天津市福晨化學試劑廠;四水合硝酸鎘,北京化工廠.所有試劑均為分析純級.
1.2 配合物的合成
4,6-二氨基-5-醛基嘧啶和間苯二甲酸的結構式如圖1所示.
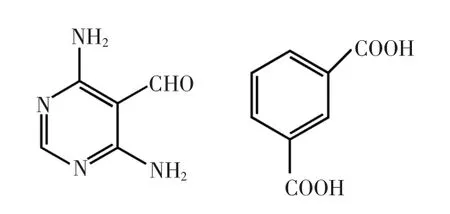
圖1 4,6-二氨基-5-醛基嘧啶和間苯二甲酸的結構式Fig.1 Structural formula of 4,6-diamino-5-carbaldehydepyrimidine and isophthalic acid
取 4,6-二氨基-5-醛基嘧啶(7.3 mg,0.05 mmol)、間苯二甲酸(8.3 mg,0.05 mmol)、硝酸鎘(30.8 mg,0.1 mmol)溶解到10.0 mL的二次去離子水中,用三乙胺調節上述混合溶液的酸堿度(pH=7.0),置于內襯有聚四氟乙烯的23.0 mL的高壓水熱反應釜中,140℃下加熱96 h,然后以2℃/h的速率緩慢降至室溫,得到適合于X-線單晶衍射分析的無色塊狀晶體.用乙醇洗滌,干燥,產率約為73%(以4,6-二氨基-5-醛基嘧啶計算).C13H16CdN4O8的元素分析計算值(%):C,33.31;H,3.41;N,11.95.實驗值(%):C,33.29;H,3.45;N,11.90.
FT-IR 數據(KBr壓片法,cm-1):3 457(bs),2 976(w),2 363(w),1 610(m),1 551(m),1 478(vw),1 441(vw),1 383(m),1 162(w),1 081(w),1 046(w),722(w),674(w),516(w),461(w).
1.3 配合物的晶體結構測定
選擇尺寸為0.22 mm×0.21 mm×0.18 mm的配合物單晶,溫度為293 K的條件下,在Apex-ⅡCCD X-線單晶衍射儀上用Mo Kα射線(λ=0.071 073 nm)收集數據,收集過程中未出現晶體變質.用SADABS方法進行半經驗吸收校正[20],使用SAINT程序對衍射數據進行還原,使用SHELXTL-97程序直接對所有結構進行解析和精修[21].用全矩陣最小二乘法對所有非氫原子進行各向異性精修.配合物的CCDC編號為1574702,晶體學數據和精修參數如表1所示.

表1 目標配合物的晶體學數據和精修參數Tab.1 Structural and refinement parameters of the complex
2 結果與分析
2.1 配合物的晶體結構
由表1可知,配合物結晶于三斜的Pī空間群,由間苯二甲酸陰離子橋聯相鄰的Cd(Ⅱ)離子形成一維鏈狀結構.配合物的不對稱單元中含有1個晶體學獨立的鎘(Ⅱ)離子、2個端基配位的水分子、1個中性的4,6-二氨基-5-醛基嘧啶配體和1個雙去質子的間苯二甲酸二價陰離子.晶體學獨立的鎘(Ⅱ)離子采用NO5的配位模式,呈現扭曲的八面體配位構型.配合物中鎘(Ⅱ)離子的配位環境如圖2所示,主要鍵長數據如表2所示.
由圖2可以看出,八面體的赤道平面被間苯二甲酸二價陰離子中的3個羧基氧原子和4,6-二氨基-5-醛基嘧啶配體中的1個氮原子占據,2個軸向位置被2個配位水分子中的氧原子占據.配合物的主要鍵角數據如表3所示.
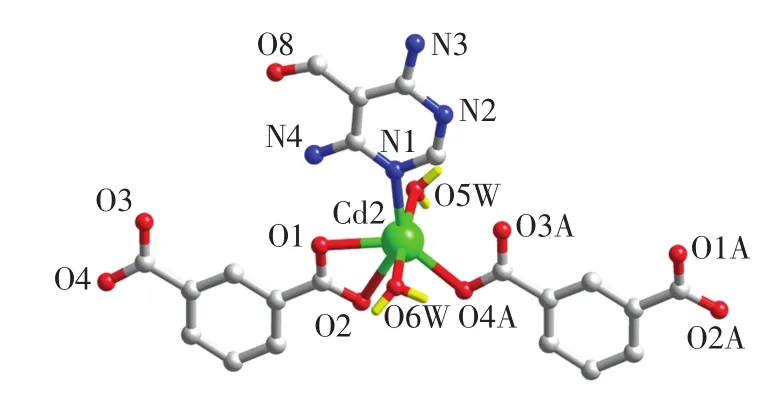
圖2 配合物中鎘(Ⅱ)離子的配位環境圖Fig.2 Local coordination environment of Cd(Ⅱ)ion in complex

表2 配合物的主要鍵長aTab.2 Selected bond lengths for the complex
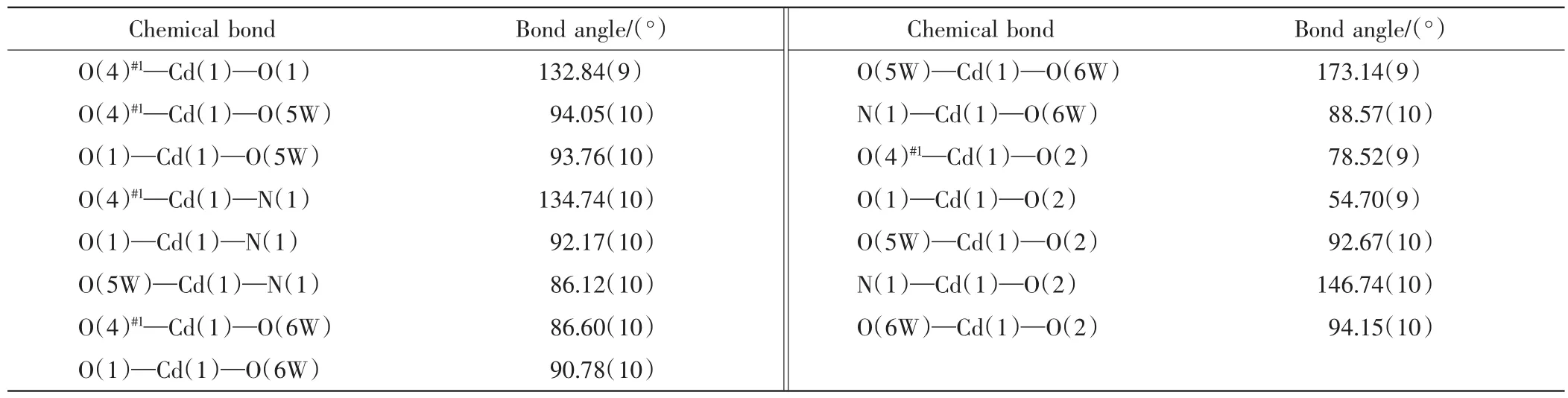
表3 配合物的主要鍵角aTab.3 Selected bond angles for the complex
間苯二甲酸配體在配合物中以雙去質子的二價陰離子形式存在,以單齒和螯合雙齒配位模式與金屬離子鍵合,如圖3所示.中性的4,6-二氨基-5-醛基嘧啶配體提供氮原子,以端基配位形式與鎘(Ⅱ)離子鍵聯.相鄰的鎘(Ⅱ)中心通過處于對位的2個間苯二甲酸二價陰離子,采取μ3-模式橋聯,沿著b軸方向形成一維鏈狀結構.
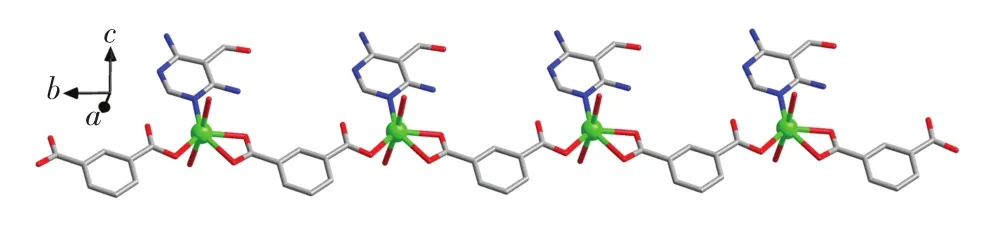
圖3 配合物的一維鏈狀結構Fig.3 Polymeric one-dimensional chain of the complex
4,6-二氨基-5-醛基嘧啶配體的嘧啶六元環上,氮原子和醛基氧原子作為氫鍵受體與其中一個配位水分子形成O(6W)—H(6A)…O(8)和O(6W)—H(6B)…N(2)氫鍵,另一個配位水分子作為氫鍵供體與第一個配位水中的氧原子和間苯二甲酸的羧基氧形成O(5W)—H(5B)…O(6W)和 O(5W)—H(5A)…O(3)氫鍵,使一維鏈狀結構延伸成為二維結構,如圖4所示,氫鍵參數如表4所示.

圖4 配合物通過氫鍵作用拓展的二維結構Fig.4 2D suparmolecular layers of the complex generated by hydrogen bonding interaction
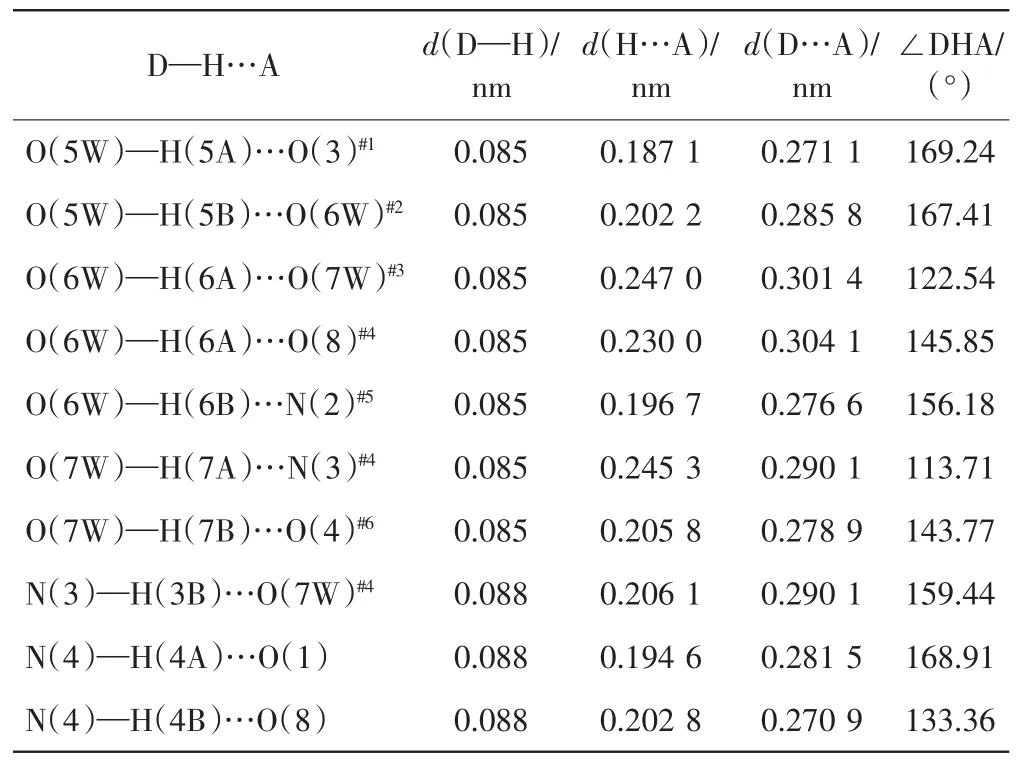
表4 配合物的氫鍵參數aTab.4 Selected hydrogen-bond parameters for the complex
配合物的三維超分子結構如圖5所示.由圖5可以看出,配合物中,1個游離水同時作為氫鍵的供體和受體,形成了4重氫鍵.嘧啶六元環4位氨基的氮原子、間苯二甲酸的羧基氧分別與游離水上的2個氫原子形成 O(7W)—H(7A)…N(3)、N(3)—H(3A)…O(7W)和O(7W)—H(7B)…O(4)氫鍵,將二維網狀結構拓展為三維超分子結構.配位水分子的氫原子和嘧啶環4位氨基上的氫原子與游離水分子的氧原子形成O(6W)—H(6A)…O(7W)和 N(3)—H(3B)…O(7W)氫鍵,進一步加固了三維超分子結構的穩定性.
2.2 配合物的紅外光譜分析
配合物的紅外光譜結果顯示:3 459 cm-1處的吸收峰為水分子中的O—H伸縮振動吸收峰,1 610 cm-1處的強峰表明配合物中的羧基是完全去質子化的[22].去質子羧基的不對稱和對稱伸縮振動吸收峰分別在1 551、1 478、1 441、1 383 cm-1處.配合物的紅外光譜測定結果與X-線單晶衍射結構的測定結果一致.

圖5 配合物通過氫鍵作用形成的三維超分子結構Fig.5 3D suparmolecular structure of the complex generated by hydrogen bonding interaction
2.3 熱重分析
配合物的熱重分析結果如圖6所示.
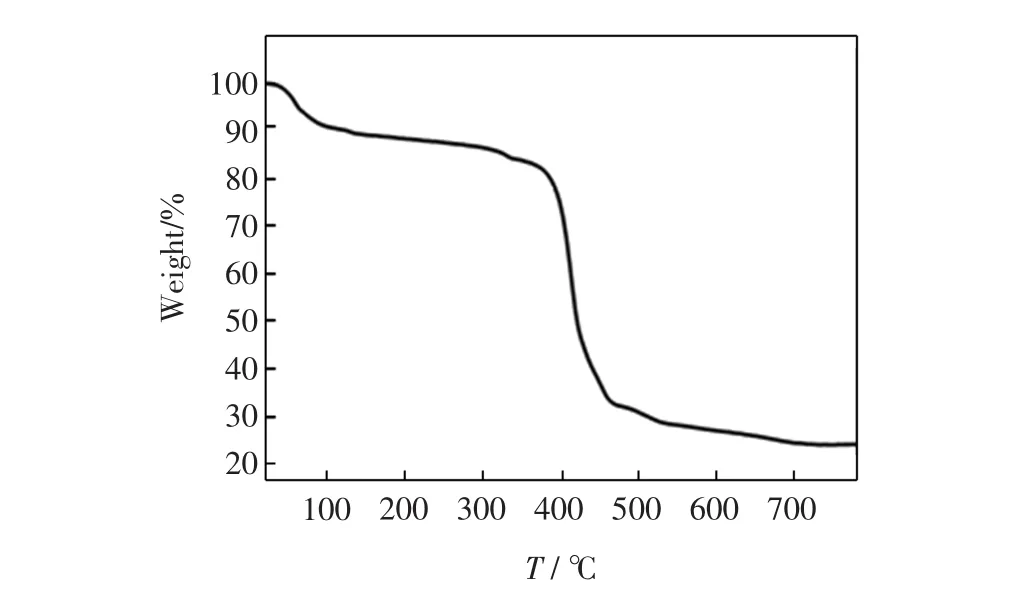
圖6 配合物的熱重分析圖Fig.6 TG curve for the complex
由圖6可以看出,配合物有2個失重過程:第一步失重過程在56~100℃范圍內,伴隨著游離水分子的失去(實驗值為3.84%,計算值為3.89%);第二步失重過程在350~536℃范圍內,歸屬為配位水分子、4,6-二氨基-5-醛基嘧啶配體和間苯二甲酸陰離子的分解(實驗值為72.69%,計算值為73.31%).CdO為最后的剩余產物,加熱到690℃時質量不再損失.
3 結論
本研究選用輔助配體間苯二甲酸和六水合硝酸鎘,采用水熱合成法合成了首個基于4,6-二氨基-5-醛基嘧啶的混配金屬配合物.X-線單晶衍射結果表明,配合物中心鎘原子以六配位的模式呈現扭曲的八面體構型,相鄰的鎘(Ⅱ)中心通過2個間苯二甲酸二價陰離子采取μ3-模式橋聯形成一維鏈狀結構.通過8種分子間氫鍵,配合物從一維鏈狀結構拓展為三維超分子結構.熱重分析表明,配合物具有較好的熱穩定性.

