OPN-siRNA對膠原誘導性關節炎小鼠的治療作用①
王 慧 楊國安 駱康凱 竇晶莉 王永福
(包頭醫學院第一附屬醫院風濕免疫科,包頭醫學院風濕免疫研究所,包頭014010)
類風濕關節炎(Rheumatoid arthritis,RA)是一種慢性全身性自身免疫性疾病。以侵犯關節為主,引起關節滑膜炎、軟骨和骨的破壞,最后導致關節畸形、功能障礙,甚至殘疾,嚴重影響患者的生活質量。另外此病可出現系統受累,最終危及生命。骨橋蛋白(Osteopontin,OPN)也稱為分泌磷蛋白1(SPP1)或早期T淋巴細胞活化因子1(Tta1),是一種糖基化的磷酸蛋白,在多種組織和細胞合成,并分泌到體液。最初OPN被鑒定為骨基質蛋白,隨后被確定為多種細胞分泌的一種細胞因子,如骨細胞、軟骨細胞、滑膜細胞、巨噬細胞、淋巴細胞、上皮細胞及血管平滑肌細胞等。研究表明,OPN在RA滑膜襯里層、襯里下層、軟骨表面及侵蝕的滑膜中過表達[1]。RA患者關節局部產生的OPN也是升高的[2]。免疫組化法發現了高水平的OPN,尤以RA滑膜襯里細胞為著。RA患者滑膜CD4+T細胞OPN mRNA表達水平顯著升高,與滑液中OPN濃度升高相關[3]。OPN過表達僅限于RA滑膜,與滑膜T細胞選擇性OPN受體共表達相關,包括整合素αV、β1 及 CD443。關節炎復發期血清OPN水平顯著升高,而在進展期血清中持續出現更高水平OPN[4]。因此,OPN在RA發病過程中可能起著至關重要的作用。
siRNA是一種特定基因沉默技術,廣泛用于腫瘤、自身免疫性疾病和肝炎等疾病的治療[5-7],而且小鼠體內研究發現,口服siRNA制劑對小鼠不會造成任何的不良反應[8]。因此,本研究采用siRNA技術沉默CIA小鼠中OPN基因的表達,探討OPN基因的siRNA對CIA小鼠的治療作用。
1 材料與方法
1.1試劑與儀器 載體pGFP-V-RS 購自美國Origene公司,AxyPrep質粒DNA大量抽提試劑盒購自美國Axygen公司,TRIzol購自日本TaKaRa公司,M-MLV逆轉錄酶和脂質體LipofectamineTM2000購自美國Invotrigen公司。
1.2方法
1.2.1siRNA的設計 本實驗針對OPN基因的cDNA序列設計2段siRNA。第1段序列為:5′-CCAAGTCTGGAAACACACA-3′,第2段序列為:5′-GTTCCAAAGCCAGCCTGGA′-3。將上述序列的模板插入質粒載體pGFP-V-RS中,構建其真核表達載體。
1.2.2CIA模型小鼠的建立 4~6周齡DBAⅠ雌性小鼠30只,購自南京大學動物模式研究所。隨機抽取3只小鼠為空白組;其余的小鼠用于CIA模型的建立,每只小鼠尾根部皮內注射100 μlⅡ型膠原和完全弗氏佐劑乳化液。第21天尾根部皮內注射同等劑量Ⅱ型膠原和不完全弗氏佐劑乳化液。
1.2.3實驗小鼠分組及給藥 27只用于造模的小鼠,出模15只,分別分配到模型組、空載體組及OPN-siRNA1和OPN-siRNA2,每組3只,余3只不夠分組未用于實驗,即本實驗共分為5組,分別為空白組、模型組、空載體組、OPN-siRNA1組和OPN-siRNA2組,每組3只小鼠。將構建好的OPN siRNA 60 μg和脂質體LipofectamineTM2000的混合物200 μl[DNA(μg):LipofectamineTM2000(μl)為1∶2]分別自尾靜脈注射CIA小鼠,對照組CIA小鼠注射等劑量、等比例的磷酸鹽緩沖液(PBS)和LipofectamineTM2000的混合物。每周注射1次,每次注射100 μl,共注射8次。
1.2.4指標的檢測及組織病理學 注射后28 d處死所有組別CIA小鼠,心臟取血,分離血清,在-80℃下保存,檢測血清IL-17、IL-10及IFN-γ水平;取小鼠肺組織,TRIzol提RNA,實時熒光定量PCR檢測小鼠肺臟中OPN mRNA的表達水平,根據ct值計算2-ΔΔct。引物由上海生工生物工程技術服務有限公司合成,OPN上游引物:5′-CACTCCAATCG-TCCCTAC-3′,下游引物:5′-AGACTCACCGCTC-TTCAT-3′,擴增的產物長度為157 bp,內參β-actin上游引物:5′-CTGTCCCTGTATGCCTCTG-3′,下游引物:5′-ATGTCACGCACGATTTCC-3′,擴增的產物長度為218 bp;另外取肺組織和踝關節,4%甲醛固定,石蠟包埋,切2張片,分別作HE染色和熒光免疫組織化學染色,熒光免疫組織化學染色的圖片采用IPP6軟件分析平均A值;取小鼠脾臟,檢測脾細胞Th17及Treg水平。另外檢測注射后小鼠血清中細胞因子IL-17、IL-10、IFN-γ水平。
2 結果
2.1OPN siRNA注射后小鼠肺組織OPN mRNA的表達水平 注射后28 d處死小鼠OPN-siRNA1組和OPN-siRNA2組小鼠肺組織中OPN mRNA的表達水平明顯低于模型組和空載體組,差異有統計學意義(P<0.05),模型組和空載體組比較差異無統計學意義(P>0.05),OPN-siRNA1組和OPN-siRNA2組比較差異有統計學意義(P<0.05)。見表1。
2.2OPN siRNA注射后小鼠踝關節和肺組織中OPN蛋白的表達水平 注射后28 d處死小鼠,檢測小鼠踝關節和肺組織中OPN蛋白的表達水平,結果顯示:模型組和空載體組有很強的紅色熒光,而OPN-siRNA1組和OPN-siRNA2組的紅色熒光量明顯減弱,即OPN-siRNA1組和OPN-siRNA2組OPN的表達明顯低于模型組和空載體組,模型組和空載體組比較無明顯差異,siRNA1組和siRNA2組比較也無明顯差異。見圖1和圖2 (上述應用的為熒光免疫組化,無需染色,放大倍數為10倍)。
2.3OPN siRNA注射后小鼠的踝關節和肺組織病理改變 光鏡下觀察踝關節的HE染色病理切片,結果發現:與空載體組和模型組比較,OPN-siRNA1組和OPN-siRNA2組中的小鼠踝關節病理顯示:關節的炎性細胞浸潤減少,關節腫脹程度減輕。見圖3。光鏡下觀察小鼠肺組織的HE染色病理切片,結果發現:與模型組及空載體組比較,OPN-siRNA1組和OPN-siRNA2組肺組織炎細胞浸潤減輕,間質性肺病改善。見圖4。
2.4OPN siRNA注射后小鼠血清中細胞因子的變化 與模型組和空載體組相比,OPN-siRNA1組和OPN-siRNA2組中IL-17的表達水平下降,但差異無統計學意義(P>0.05),模型組和空載體組比較差異無統計學意義(P>0.05),OPN-siRNA1組和OPN-siRNA2組比較差異無統計學意義(P>0.05)。見表2。
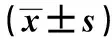

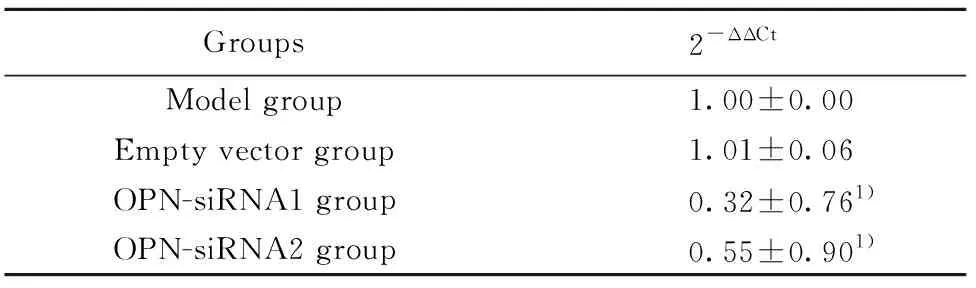
Groups2-ΔΔCtModel group1.00±0.00Empty vector group1.01±0.06OPN-siRNA1 group0.32±0.761)OPN-siRNA2 group0.55±0.901)
Note:Compared with model group and empty vector group,1)P<0.05.
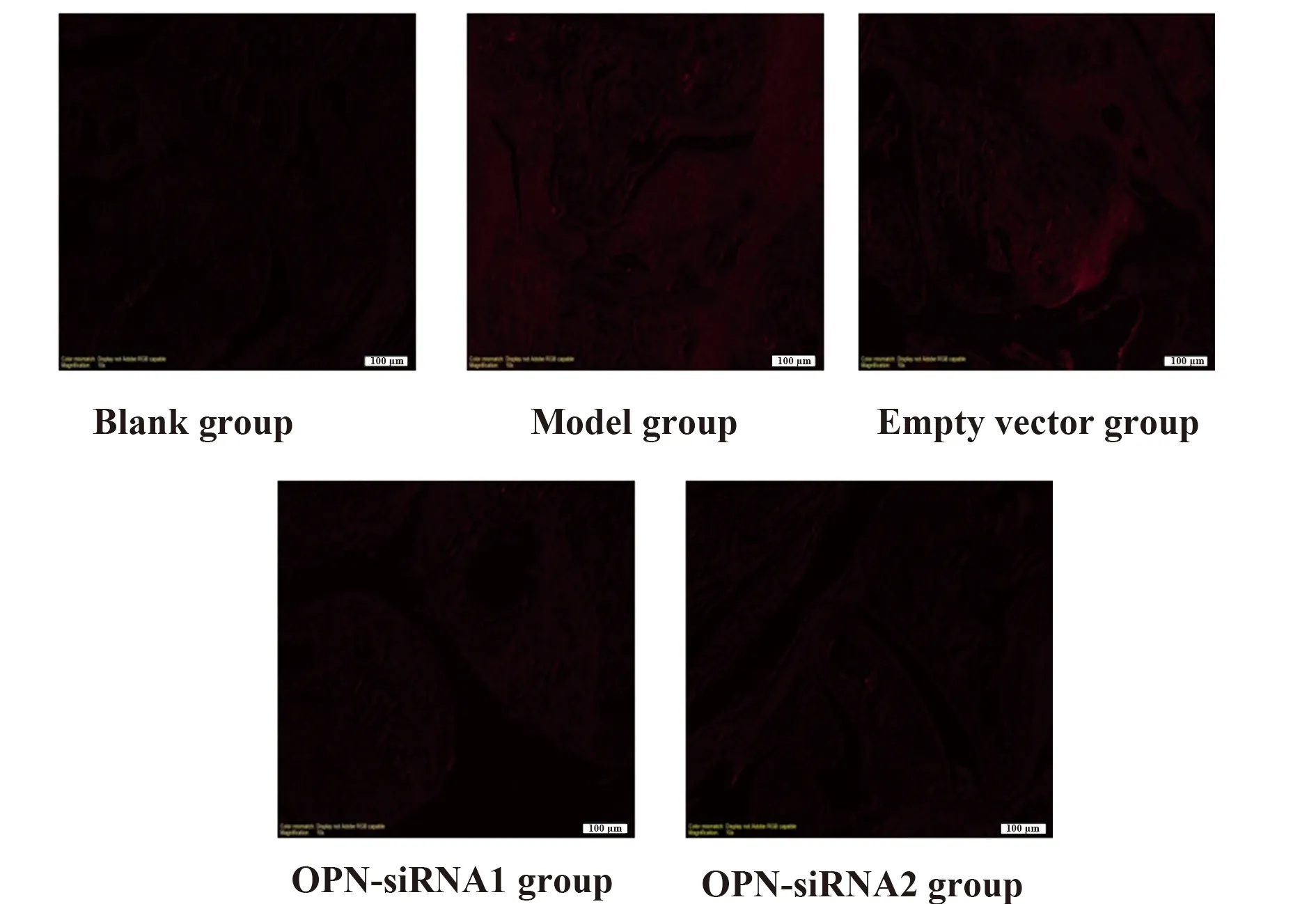
圖1 小鼠踝關節中OPN蛋白的表達水平Fig.1 Expression levels of OPN protein in ankle from CIA mice
OPN-siRNA1組和OPN-siRNA2組IL-10的表達水平明顯高于模型組和空載體組,差異有統計學意義(P<0.05),模型組低于空白對照組,差異有統計學意義(P<0.05),空載體組低于空白對照組,差異無統計學意義(P>0.05)。模型組和空載體組比較差異無統計學意義(P>0.05),OPN-siRNA1組和OPN-siRNA2組比較差異無統計學意義(P>0.05)。見表3。
OPN-siRNA1組和OPN-siRNA2組IFN-γ的表達低于模型組和空載體組,差異有統計學意義(P<0.05),模型組和空載體組高于空白對照組,差異有統計學意義(P<0.05)。模型組和空載體組比較差異無統計學意義(P>0.05),OPN-siRNA1組和OPN-siRNA2組比較差異無統計學意義(P>0.05)。見表4。
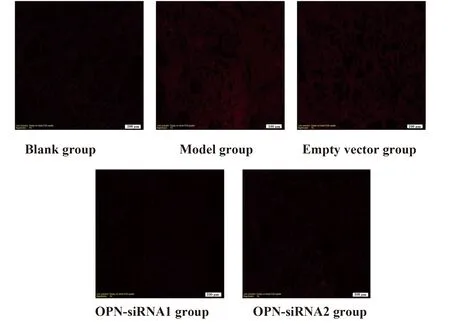
圖2 小鼠肺組織中OPN蛋白的表達水平Fig.2 Expression levels of OPN protein in lung from CIA mice
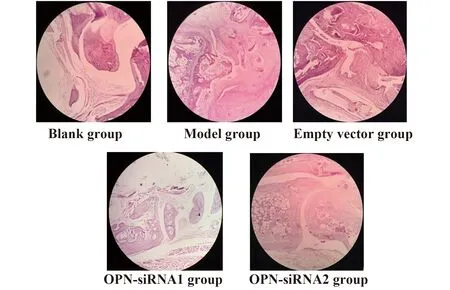
圖3 小鼠踝關節病理改變Fig.3 Pathology of ankle joint in mice

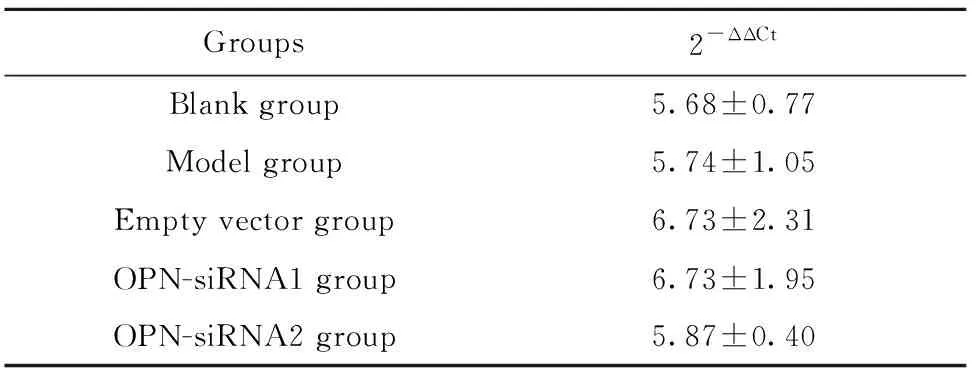
Groups2-ΔΔCtBlank group5.68±0.77Model group5.74±1.05Empty vector group6.73±2.31OPN-siRNA1 group6.73±1.95OPN-siRNA2 group5.87±0.40
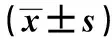

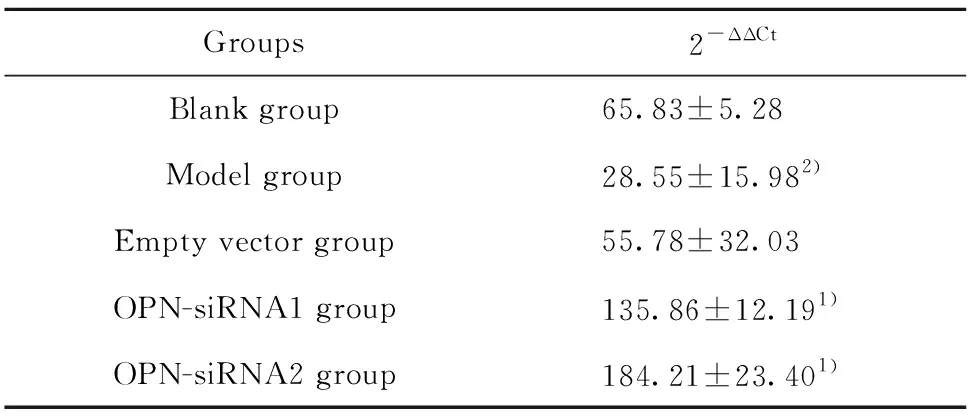
Groups2-ΔΔCtBlank group65.83±5.28Model group28.55±15.982)Empty vector group55.78±32.03OPN-siRNA1 group135.86±12.191)OPN-siRNA2 group184.21±23.401)
Note:Compared with model group and empty vector group,1)P<0.05;compared with blank group,2)P<0.05.
2.5OPN siRNA注射后小鼠脾細胞中Th17和Treg的變化 OPN siRNA作用小鼠后,脾細胞中Th17細胞的比例低于模型組和空載體組,差異有統計學意義(P<0.05),模型組和空載體組比較差異無統計學意義(P>0.05),模型組和空載體組高于空白對照組,差異有統計學意義(P<0.05),OPN-siRNA1組和OPN-siRNA2組比較差異無統計學意義(P>0.05),見表5。
OPN siRNA作用小鼠后,脾細胞中Treg細胞的比例高于模型組和空載體組,差異有統計學意義(P<0.05),模型組和空載體組比較差異無統計學意義(P>0.05)。OPN-siRNA1組與OPN-siRNA2組比較差異無統計學意義(P>0.05)。模型組、空載體組與空白對照組比較差異無統計學意義(P>0.05)。見表6。
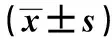


Groups2-ΔΔCtBlank group4.46±0.94Model group15.52±1.902)Empty vector group13.66±3.802)OPN-siRNA1 group5.28±1.411)OPN-siRNA2 group5.54±1.551)
Note:Compared with model group and empty vector group,1)P<0.05;compared with blank group,2)P<0.05.
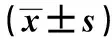


Groups The proportion of Th17 cellBlank group2.63±0.67Model group6.23±1.102)Empty vector group4.70±1.102)OPN-siRNA1 group2.33±0.851)OPN-siRNA2 group2.90±0.801)
Note:Compared with model group and empty vector group,1)P<0.05;compared with blank group,2)P<0.05.
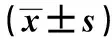


GroupsThe proportion of Treg cellBlank group3.23±0.40Model group1.87±0.25Empty vector group1.40±0.22OPN-siRNA1 group7.67±1.071)OPN-siRNA2 group6.63±0.751)
Note:Compared with model group and empty vector group,1)P<0.05.
3 討論
RA是一種慢性、以侵犯關節為主要特征、原因未明的自身免疫性疾病。全世界RA的患病率是0.5%~1%,女性高于男性[9]。至今RA尚不能根治,治療的總原則是達標治療。
OPN是RA的一種自身抗原,臨床上,抗OPN抗體可能與RA疾病嚴重程度相關[10]。在DBA/1J小鼠,抗OPN單克隆抗體23C3可有效抑制CIA疾病的發展甚至逆轉病情。單克隆抗體23C3降低血清Ⅱ型膠原特異性自身抗體和炎性細胞因子的水平,并抑制T細胞針對Ⅱ型膠原的免疫應答[11]。之前的研究結果有力地提示OPN參與RA的發展,并表明OPN siRNA、OPN表位的中和性抗體以及整合素抗體有望成為RA治療的工具。本研究針對OPN基因的cDNA序列設計2段siRNA,將上述序列的模板插入質粒載體pGFP-V-RS中,構建其真核表達載體。分別自尾靜脈注射CIA小鼠。肺組織OPN mRNA的表達水平明顯降低;小鼠踝關節和肺組織中OPN蛋白的表達結果顯示:模型組和空載體組有很強的紅色熒光,而OPN-siRNA1組和OPN-siRNA2組的紅色熒光量明顯減弱。以上結果說明:OPN siRNA可抑制CIA小鼠肺臟中OPN mRNA的表達;另外可以抑制肺組織和踝關節OPN蛋白水平的表達。因此,OPN-siRNA可以抑制OPN mRNA及OPN蛋白的表達,有望成為RA治療的新武器。
OPN是一種具有多效性的細胞外基質蛋白[3]。滑膜T細胞的OPN過表達與局部炎癥相關,且OPN是RA發病過程中重要的介質。在滑膜襯里層和軟骨浸潤部位的成纖維細胞產生的OPN不僅可以介導這些細胞附著于軟骨,而且通過刺激關節軟骨膠原酶1的分泌促進RA基質降解[1]。本研究結果顯示:與模型組和空載體組比較,踝關節病理顯示:OPN-siRNA1組和OPN-siRNA2組關節的炎性細胞浸潤減少,關節腫脹程度減輕。另外肺組織病理顯示炎細胞浸潤減輕,間質性肺病改善。OPN-siRNA可以明顯抑制關節及肺組織炎細胞浸潤,從而控制疾病的進展。RA滑液刺激T細胞OPN的表達,這是由于滑液中IL-10的出現及其被IL-10抗體中和所引起[3]。OPN選擇性誘導促炎因子和趨化因子(如IL-1和IL-8)的表達,從而促進炎癥細胞的遷移和募集。此外,在單核細胞中OPN可以激活轉錄因子NF-κB[3]。OPN通過與其受體αvβ3整合素連接,可以介導破骨細胞參與的關節炎骨吸收過程[4]。OPN mRNA主要存在于關節破壞的骨侵蝕部位,該部位有活化的破骨細胞存在;同時骨侵蝕部位也檢測到OPN蛋白。RA滑液中內源性OPN的產生是由于T細胞內IL-17和單核細胞內MCP-1或 MIP-1β生成增加所引起,這種作用可以被OPN抗體阻斷[12,13]。OPN對Th17分化的影響是通過一個獨立的IL-6/STAT-3通路或其他細胞因子,具體涉及OPN受體CD44和CD29及轉錄因子維甲酸相關孤核受體(Retinoic acid-related orphan receptor,ROR)。此外,OPN可以誘導IL17A基因啟動子的H3乙酰化作用,主要是通過在CD4+T細胞的CD44結合域,IL17A基因位點與ROR的相互作用來實現[13]。本研究結果顯示:OPN siRNA作用小鼠后,脾細胞中Th17細胞的比例低于模型組和空載體組,而脾細胞中Treg細胞的比例較模型組和空載體組增高。OPN siRNA可以抑制致病性Th17水平;OPN siRNA治療后Treg水平升高,進一步誘導免疫耐受,促進關節炎癥的控制。另外:OPN siRNA作用后,小鼠血清中細胞因子水平發生了明顯的變化:引起促炎因子IL-17及IFN-γ下降,而抑炎因子IL-10升高。從而達到抑制關節炎癥的目的。
本研究采用siRNA技術沉默CIA小鼠中OPN基因的表達,探討OPN基因的siRNA對小鼠CIA的治療作用。結果顯示,OPN-siRNA抑制RA模型鼠體內OPN表達及炎癥介質的水平,因此可能成為RA治療新的潛在靶點,本研究樣本量較小,有待進一步擴大樣本進行證實。

