高血壓心衰合并高尿酸血癥患者hURAT1(T6092C)基因多態性對氯沙坦降尿酸療效的影響
余廣煒 劉青 吳文偉


[摘要] 目的 探討hURAT1(T6092C)基因多態性對高血壓心衰合并高尿酸血癥患者服用氯沙坦療效的影響。方法 方便選取2014年1月—2018年8月該院急診科收治的高血壓性心臟病、心功能不全合并高尿酸血癥患者146例為研究對象,應用多聚酶鏈-限制性片段長度多態性(PCR-RFLP)方法檢測146例患者的hURAT1(T6092C)基因多態性,同時觀察不同基因組服用氯沙坦后尿酸值下降幅度的差異。結果 患者TT、TC、CC 3組基因型服用氯沙坦后尿酸值下降幅度差異有統計學意義(P<0.05),TT基因型個體血尿酸下降幅度為(132.3±62.7)μmol/L,高于TC(7.3±12.4)μmol/L和CC基因型個體(2.0±13.9)μmol/L。結論 氯沙坦對hURAT1(T6092C)基因突變的高血壓性心臟病、心功能不全合并高尿酸血癥患者療效降低,應該注意聯合用藥提高療效。
[關鍵詞] hURAT1;氯沙坦;療效;高血壓;高尿酸血癥;基因多態性
[中圖分類號] R589? ? ? ? ? [文獻標識碼] A? ? ? ? ? [文章編號] 1674-0742(2019)11(b)-0004-04
[Abstract] Objective To investigate the effect of hURAT1 (T6092C) gene polymorphism on the efficacy of losartan in patients with hypertensive heart failure complicated with hyperuricemia. Methods Convenient selected a total of 146 patients with hypertensive heart disease, cardiac insufficiency and hyperuricemia admitted to the hospital from January 2014 to August 2018 were enrolled in the study. Polymerase-restriction fragment length polymorphism was used. The (PCR-RFLP) method was used to detect the hURAT1 (T6092C) gene polymorphism in 146 patients, and to observe the difference in the decrease in uric acid value after taking losartan in different genomes. Results There was a statistically significant difference in the decrease of uric acid value between patients with TT, TC and CC genotypes after taking losartan (P<0.05), the decrease of blood uric acid in TT genotype was (132.3±62.7)μmol/L, higher than TC (7.3±12.4)μmol/L and CC genotype (2.0±13.9)μmol/L. Conclusion Losartan is effective in the treatment of hypertensive heart disease, cardiac insufficiency and hyperuricemia with hURAT1 (T6092C) gene mutation. It should be noted that the combination therapy can improve the curative effect.
[Key words] hURAT1; Losartan; Efficacy; Hypertension; Hyperuricemia; Genetic polymorphism
近年來,較多研究顯示,血尿酸水平的升高是引發心血管疾病的一個重要危險因素,且其與血脂異常、肥胖癥、高血壓的發生有關。高血壓所致高血壓性心臟病及最終發展至心功能衰竭是許多高血壓患者致死率的主要原因。該文研究了高血壓心衰合并高尿酸患者在基因多態性層面對氯沙坦降尿酸療效的影響,指導臨床進一步在藥物基因組層面進行該類患者尿酸水平的控制。該院方便選取2014年1月—2018年8月該院急診科收治的高血壓性心臟病、心功能不全合并高尿酸血癥患者146例為研究對象展開研究,現報道如下。
1? 對象與方法
1.1? 研究對象
該研究對象為方便選取該院收的高血壓心臟病、心功能不全合并高尿酸血癥患者,共146例。高血壓心臟病、心功能不全入選標準為根據中國高血壓指南及中國心衰指南要求,高血壓診斷標準:成人:舒張壓≥95 mmHg,收縮壓≥160 mmHg,臨界高血壓:90 mmHg<舒張壓<95 mmHg,或140 mmHg<收縮壓<160 mmHg,同時符合心功能不全診斷標準(每例患者均行心臟彩超檢查,(LVEF<40%,NT-proBNP>125 ng/L),并符合高尿酸血癥入選標準。該研究所選病例均經倫理委員會批準,患者均曾經口服或間斷口服過該藥物,均知情同意。
1.2? 實驗試劑與儀器
①利用PCR-RFLP方法建立hURAT1(T6092C)基因分型體系。hurat1 T6092C基因引物根據Jean-Sebastien Hulot等文獻設計上游引物:3-CCAGAACGAAAGTCGGTA-5,由上海英駿生物技術有限公司合成下游引物:5-ACAGCATCCCAACCACAATC-3。酶切位點應用Restrictin Enzyme Site Mapper version 3 軟件查找。酶切后酶切產物在3%瓊脂糖凝膠電泳后,紫外光下觀察結果:PCR擴增片段總長度為539 bp,含CC等位基因的突變型純合子凝膠電泳僅539 bp一條帶;含TT等位基因的野生型凝膠電泳顯示357 bp和182 bp兩條帶;而含TC等位基因的突變型雜合子則顯示539 bp、357 bp和182 bp 3條帶。
②測序驗證。選取所分型的PCR擴增產物樣本50 μL送至英駿生物公司(中國上海)進行測序驗證。
③分組治療。各基因型患者均口服氯沙坦片(50 mg,H20130409)10~14 d(50 mg/d)。
1.3? 統計方法
采用SPSS 13.0統計學軟件進行數據分析,正態性檢驗方法采用K-S檢驗法(Kolmogorov-Smirnov Test),并行方差齊性Levene檢驗,計量資料以均數±標準差(x±s)表示,組間比較采用t檢驗;計數資料以[n(%)]表示,組間比較采用χ2檢驗,若四格表有格子1≤T<5,則應用Fisher精確檢驗進行分析。P<0.05為差異有統計學意義。
2? 結果
2.1? Hardy Weinberg遺傳平衡檢驗
146例高尿酸血癥合并高血壓患者中,SLC22A12 T6092C分別經Hardy Weinberg遺傳平衡檢驗軟件檢驗基因型分布頻率觀測值與預計值之間差異無統計學意義(P>0.05),與Hardy-Weinberg遺傳平衡相符合,說明樣本具有一定的代表性,均來自一個處于隨機婚配、較大的平衡狀態的群體。
2.2? 高尿酸血癥合并高血壓患者組用藥前不同基因型臨床資料的比較
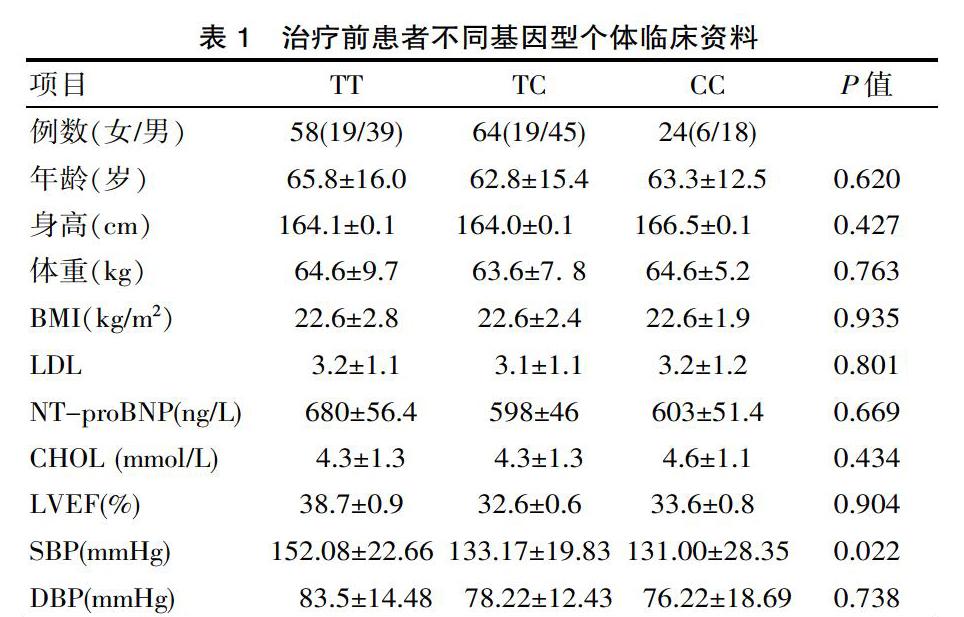
參與實驗的146例高尿酸血癥合并高血壓性心臟病、心功能不全患者治療前的基因分型、一般情況及實驗分組見表1。
2.3? 高尿酸血癥合并原發性高血壓組服用氯沙坦前后3組基因型間尿酸測定值比較
氯沙坦治療前及10~14 d后尿酸測定值比較,在SLC22A12 TT野生型個體治療前后差異有統計學意義(P<0.01),在SLC22A12? TC突變型雜合子個體治療前后差異有統計學意義(P<0.05),在SLC22A12? CC突變型純合子個體治療前后差異無統計學意義(P>0.05)。見表2。
2.4? 服用氯沙坦后3組基因型間尿酸測定值下降幅度比較
氯沙坦治療10~14 d后尿酸測定值下降幅度比較,TT、TC、CC 3組基因型個體尿酸下降幅度分別為(132.3±62.7)μmol/L、(7.3±12.4)μmol/L、(2.0±13.9)μmol/L,3組之間方差分析比較差異有統計學意義(P<0.001),兩兩比較顯示,在SLC22A12? TT野生型個體下降幅度較SLC22A12? TC突變型純合子個體明顯(P<0.01),在SLC22A12 TC突變型雜合子個體較SLC22A12? CC突變型純合子個體明顯,差異有統計學意義(P<0.05)。見表3。
3? 討論
人尿酸鹽陰離子交換器(hURAT1)是由SLC22A12基因所編碼的,SLC22A12基因主要定位在11q13,其cDNA編碼區長1 659 bp,全長2 642 bp,含有9個內含子和10個外顯子,由其編碼的氨基酸共555個[1]。hURAT1通過與少數無極陰離子和多種單價的有機陰離子交換來完成對尿酸的少量分泌及重吸收,其主要是重吸收在腎近端小管的尿酸,進而對血清中尿酸濃度發揮調節作用,是血清中尿酸水平達到動態平衡[2]。
尿酸在人類血清中的濃度主要是經過近端腎小管的重吸收來平衡的[3]。因此hURAT1對于調節人體血尿酸水平發揮著重要作用。hURAT1基因突變或者多態與高尿酸血癥的發生存在相關性,Hamada 等[4]研究發現在高血壓患者中hURAT1 的一些功能性突變比如G269A/C1429A/ G774A 會消除氯沙坦的降尿酸作用,其中TT基因型個體血尿酸下降幅度為(130.3±65.3)μmol/L, TC(6.8±11.5)μmol/L和CC基因型個體(2.0±12.8)μmol/L而hURAT1 未突變患者仍能降低血尿酸水平,因此該方面已經成為國內外學者研究的熱點。與該次研究TT基因型個體血尿酸下降幅度為(132.3±62.7)μmol/L,高于TC(7.3±12.4)μmol/L和CC基因型個體(2.0±13.9)μmol/L相似,患者TT、TC、CC 3組基因型服用氯沙坦后尿酸值下降幅度差異有統計學意義(P<0.05),單核苷酸多態性(single nucleotide polymorphism, SNP)的檢測方法多種多樣,如等位特異性雜交,等位特異性PCR,PCR-單鏈構象多態性(PCR-SSCP),PCR-限制性片段長度多態性(PCR-RFLP)和直接測序等[5]。該研究采用PCR-RFLP方法進行基因分型,每一個樣本兩次的PCR-RFLP分析結果均相同,并且與測序的結果相吻合,說明所有方法均有很好的可重復性和準確性。
藥物基因組學主要是通過應用已知的基因組學理論,來分析遺傳因素與藥物反應的相關性,或者可以說是以藥物安全性和藥物效應作為主要研究目標,來分析藥物學差異和藥物動力學的基因特征,以及因基因變異而對不同個體對藥物所作出的不同反應,其主要包括基因組學(genemics)與遺傳藥理學(phanacogenetics)[6-7]。藥物基因組學的研究內容和基礎是基因多態性。藥物代謝酶多態性主要是因在同一個基因位點上存在多個等位基因所引發的,其多態性決定藥物代謝酶活性和表型多態性,并呈現基因劑量-藥效的關系,導致不同的個體發生不同的藥物代謝反應,是喪失或降低藥效及產生藥物不良反應的主要原因之一。大多數藥物能與其特異性蛋白發生相互作用而產生藥物效應,藥物作用靶點的基因多態性導致靶蛋白對特定藥物存在不同的親和力,這是產生藥物產生不同療效的原因之一[8-10]。該研究通過高血壓心衰合并高尿酸患者在基因多態性層面對氯沙坦降尿酸療效的影響進行分析,結果顯示,治療后,高尿酸血癥合并原發性高血壓組服用氯沙坦前后3組基因型間尿酸測定值均較治療前降低,且治療后SLC22A12? CC突變型純合子個體的尿酸測定值明顯高于SLC22A12? TC突變型雜合子個體、SLC22A12 TT野生型個體,SLC22A12 TT野生型個體尿酸水平下降幅度明顯高于SLC22A12? CC突變型純合子個體、SLC22A12? TC突變型雜合子個體,說明不同基因型患者發熱療效不同,與文獻報道相符[11],氯沙坦對基因型為SLC22A12 TT野生型個體效果更顯著。國內有利用患者及健康志愿者進行的臨床研究表明,服用氯沙坦后,突變基因型患者(TC/CC)的Ur和Cr的降低水平均明顯低于TT基因型患者(P<0.05),并且TC和CC型患者的Ur降低幅度也明顯低于TT基因型患者(P <0.05),URAT1基因6092T/C遺傳變異影響氯沙坦的降尿酸療效,并且可能是氯沙坦降尿酸潛在的遺傳靶點[12]。藥物基因組學主要是研究基因突變與藥物安全性和療效之間的關系,及其在基因水平的影響。研究藥物反應多態性與等位基因多藥性之間的相關性,主要是為了探討如何預測個體的藥物反應及如何降低研發成本、提高藥物研發的特異性[13]。因此,藥物基因組是以藥物安全性和藥物效應為目標,來研究個體間藥物效應的差異,在分子水平上對藥物作用靶位、藥物療效、毒副作用、作用模式進一步證明和闡述。
綜上所述,氯沙坦對hURAT1(T6092C)基因突變的高血壓性心臟病、心功能不全合并高尿酸血癥患者療效降低,應該注意聯合用藥提高療效。
[參考文獻]
[1]? 耿春梅,郭瑞臣.藥物基因組學在新藥臨床試驗及個體化用藥中的應用[J].藥學進展,2015,39(1I):803-809.
[2]? 王曉躍,鄧運明.hURAT1基因多態性與急性痛風性關節炎濕熱證型的相關性研究[J].江西中醫學院學報,2014(1):38-41.
[3]? 劉正奇,鐘琴.苗藥痛風停湯對人腎小管上皮細胞hURAT、 hURAT1基因表達的影響[J].湖南中醫雜志,2016,32(2):167-169.
[4]? Hamada T,Ichida K,Hosoyamada M,et al. Uricosuric action of losartan via the inhibition of urate transporter1(URAT 1) in hypertensive patients[J].Am J Hypertens,2008,21(10):1157-1162.
[5]? 黃旭慧,孫紅,蔡加琴,等.高尿酸合并高血壓患者URAT1 6092(T/C)基因多態性對氯沙坦降尿酸療效的影響[J].中國臨床藥理學與治療學雜志,2015, 20(4):435-440.
[6]? 黃亞威,楊昂.雙退火溫度PCR擴增DNA[J].微生物學報2017, 57(8)1262-1269.
[7]? Shima Y,Teruya K,Ohta H. Association between intronic SNP in urate-anion exchanger gene,SLC22A12,and serum uric acid levels in Japanese[J].Life Sci,2006,79(23) :2234-2237.
[8]? 謝潘潘,胡欣,史愛欣.藥物基因組學應用于藥物I期臨床試驗的研究進展[J].中國臨床藥理學雜志,2014,30(3):235-237.
[9]? 時晉麗.藥物基因組學在臨床應用的影響因素及思考[J].中國保健營養,2017, 27(32):330-331
[10]? 孫雪林,陳重建,施紅.藥物基因組學網絡資源[J].中華老年醫學雜志,2017,36(12):1370-1374.
[11]? 倪偉建,方焱,張善堂.基于藥物基因組學與血藥濃度監測指導的個體化用藥研究[J].中國醫院藥學雜志,2018, 38(17):1863-1868.
[12]? 劉博武.心力衰竭藥物基因組學的研究進展[J].西南軍醫,2018,20(5):529-533.
[13]? ?Hamada T,Hisatome I,Kinugasa Y,et al.Effect of the angiotensin II receptor antagonist losartan on uric acid and oxypurine metabolism in healthy subjects[J].Intern Med,2002,41(10) : 793-797.
(收稿日期:2019-08-15)

