全自動發光免疫分析儀性能評價技術研究
王 軍, 代蕾穎, 楊 忠, 趙丙鋒, 李 正, 王會如
(北京市醫療器械檢驗所體外診斷檢驗室, 北京 101111)
1 引 言
自動化的發光免疫分析儀越來越廣泛地應用于醫學檢驗[1-3]。全自動發光免疫分析儀研發制造技術門檻高,涉及光、機、電、軟、液路、溫控、免疫分析等多方面的綜合技術,系統結構復雜、控制時序要求嚴格、運行可靠性和精度要求高[4-5]。由于儀器結構復雜,相應地對其進行性能評價和質量檢測也有相當的難度,主要體現在:不同廠家的儀器,原理、結構不一樣,很難建立統一的評價標準;儀器全封閉、自動化,從工程學上進行操作和干預比較困難;核心評價技術,例如標準光源、發光劑等,被少數國外大企業掌握。基于以上原因,目前企業、監管部門、使用單位基本采用儀器配套用發光免疫試劑盒來評價檢測系統(儀器+試劑盒)的整體性能[6-10]。這種評價方法過度依賴配套試劑盒,不能準確反映儀器本身的性能,并且各個儀器所配試劑不同(激素、血藥、腫瘤標志物、病原體……),得出的指標也缺乏可比性。
全自動發光免疫分析儀的關鍵模塊包括加樣系統、孵育系統、清洗系統和檢測系統,本研究對各個模塊分別建立了可行的、標準化的評價方法。本研究建立的評價方法適用于化學發光、電化學發光、熒光等不同發光原理的儀器,也適用于酶促發光和非酶促發光不同反應類型的儀器。
2 材 料
2.1 主要儀器
全自動發光免疫分析儀:西門子Centaur XP、Centaur XPT、Centaur CP、Centaur Atellica、IMMULITE1000、IMMULITE2000、Dimension EXL;雅培ARCHITECT i2000sr;羅氏cobas e411、cobas e601、cobas e801;貝克曼庫爾特 DxI、Access 2;希森美康 HISCL-800、HISCL-5000;賽默飛世爾Phadia 250;生物梅里埃 VIDAS 3;邁克IS 1200、i3000;利德曼CI1000;邁瑞CL-1000i、CL-2000i;迪瑞CM-180;博奧ChemLiteTM 1200;新產業Maglumi 800、Maglumi 4000;安圖AUTOLUMO A2000、AUTOLUMO A2000 Plus;科美LiCA 500、CHEMCLIN 1500。
福祿克f50d或其他分辨率不低于0.1 ℃的溫度測量儀。
梅特勒bs210s或其他分度值為0.01 mg的電子天平。
日立U-3010型紫外分光光度計。
MilliQ Advantage超純水機。
2.2 參考光源
參考光源為發光二級管(LED),通過調節LED驅動電流的DA值,可獲得不同光強的光。
2.3 試劑
橙黃G(Orange G):CAS號1936-15-8。
發光劑:分為酶促和非酶促兩種,酶促發光劑由游離酶液和底物液組成,非酶促發光劑主要成分為發光標記物和緩沖液。
空白樣品:待測物為零濃度的樣品液。
人絨毛膜促性腺激素(β-HCG)試劑盒及配套校準品。
高濃度β-HCG臨床樣品:濃度超過105mIU/mL。
3 測試方法
3.1 反應區溫度控制的正確度和波動度
將全自動發光免疫分析儀反應區溫度設置為37 ℃,待穩定后,使用溫度測量儀進行測量,每隔30 s測定一次溫度值,測定時間為10 min。計算溫度測量值的算術平均值,算術平均值與設定值之差為測量偏倚,測量最大值與最小值之差的一半為溫度波動度。
3.2 加樣正確度與精密度
準備可防水分揮發的適當容器,在電子天平上調零后放到合適位置,控制全自動發光免疫分析儀的試劑針或樣品針,向該容器中加入規定量除氣超純水,再在電子天平上稱量其增加質量,以該質量除以當時溫度下純水的密度得到實際加入的體積。每種規定加入量重復測量20次,超純水需提前置于恒溫、恒濕的實驗室內平衡數小時。以加樣體積的變異系數表征加樣精密度,以加樣體積的相對偏倚表征加樣正確度。
3.3 光檢測裝置部分
3.3.1 儀器噪聲
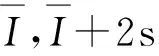
3.3.2 發光值的線性
測試發光值的線性有下列兩種方法:
(1)發光劑法。將光源檢測專用高值發光劑用稀釋液按比例稀釋成至少5個樣品,混合均勻后用分析儀檢測發光值,每個樣品重復測定3次。計算各樣品3次測量值的算術平均值,以稀釋比例為自變量,以測定結果均值為因變量進行線性擬合,并計算線性回歸的相關系數(r)。
(2)參考光源法。在分析儀上測試參考光源,通過調節LED驅動電流的DA值,可獲得不同光強的光,以標定值為自變量,以分析儀實際測量所得的發光值為因變量進行線性擬合,并計算線性回歸的相關系數。
3.3.3 發光值的精密度
可選用發光劑法或參考光源法進行試驗。用分析儀對在線性范圍內的高、低2個水平的參考光源或發光劑進行測試,連續測試10次,記錄發光值,計算發光值的變異系數,用變異系數表征發光值的精密度。
3.3.4 發光值的穩定性
可選用發光劑法或參考光源法進行試驗。待分析儀開機處于穩定工作狀態后,用在線性范圍內的高、低2個水平的參考光源或發光劑進行測試,重復測試3次,記錄發光值,計算測定結果的算術平均值I0。過4 h和8 h再分別上機重復測試3次,計算測定結果的算術平均值I1和I2,以I0作為基準值,計算4 h和8 h的相對偏倚(a,%),用相對偏倚表征發光值的穩定性。
3.4 攜帶污染

4 結 果
4.1 反應區溫度控制的正確度和波動度
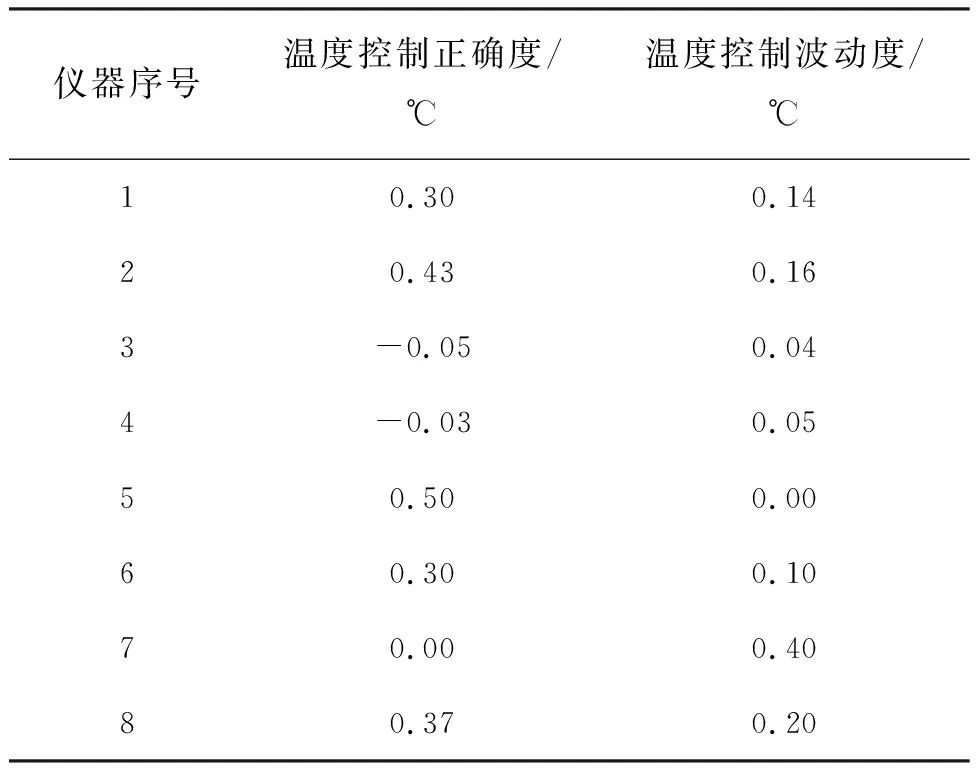
免疫反應的完成需要在一定溫度下進行,因此儀器要對反應區溫度進行精密控制,該項考察的是儀器孵育系統的性能。使用溫度測量儀對8個型號的儀器進行了溫度采集,溫度控制準確度和波動度結果見表1。可以看出,溫度控制正確度均在(37±0.5) ℃,波動度均不超過0.5 ℃。參考全自動生化分析儀行業標準[11],全自動生化分析儀溫度控制正確度要求不超過0.3 ℃,波動度不超過0.2 ℃。免疫反應對溫度要求沒有生化反應嚴苛,溫度控制正確度不超過0.5 ℃、波動度不超過0.5 ℃應能滿足臨床要求,因此初步判定這8款全自動發光免疫分析儀溫度控制合格。
表1全自動發光免疫分析儀反應區溫度控制結果
Tab.1 Testing result of temperature control of automatic luminescence immunoassay analyzers
儀器序號溫度控制正確度/℃溫度控制波動度/℃10.300.1420.430.163-0.050.044-0.030.0550.500.0060.300.1070.000.4080.370.20
注:表中儀器序號與條款2.1不對應,也與下面各表不對應。下表同。
4.2 加樣正確度與精密度
全自動儀器的樣本處理、試劑處理均為批量化操作,加樣模塊的精確設計和加工制造對于提高操作效率、加強實驗精度非常關鍵。經調查,由于市面上各型號儀器的試劑針、樣品針的加樣量程差別很大,無法設定統一的加樣考核點,因此本研究對儀器標稱的樣品最小加注量和最大加注量、試劑最小加注量和最大加注量都進行了測試。
采用稱量法對27個型號的加樣模塊進行了測試,結果見表2。表2可印證,各型號儀器的樣品針和試劑針加樣量程差別大,樣品針最小加注量從5 μL到40 μL,最大加注量從20 μL到300 μL,試劑針最小加注量從5 μL到50 μL,最大加注量從47 μL到450 μL。無論是樣品針還是試劑針,當加注量>10 μL時,大部分儀器能滿足偏倚不超過10%,CV不超過3%;當加注量>50 μL時,大部分儀器能滿足偏倚不超過5%,CV不超過2%。從表2可看出,加樣量越小,偏倚和CV越大,這是因為加樣量越小,對儀器要求越高,技術實現難度越大。綜合起來,建議7號、15號、22號、27號儀器應對加注裝置進一步改進,以達到其聲稱的加樣量要求。
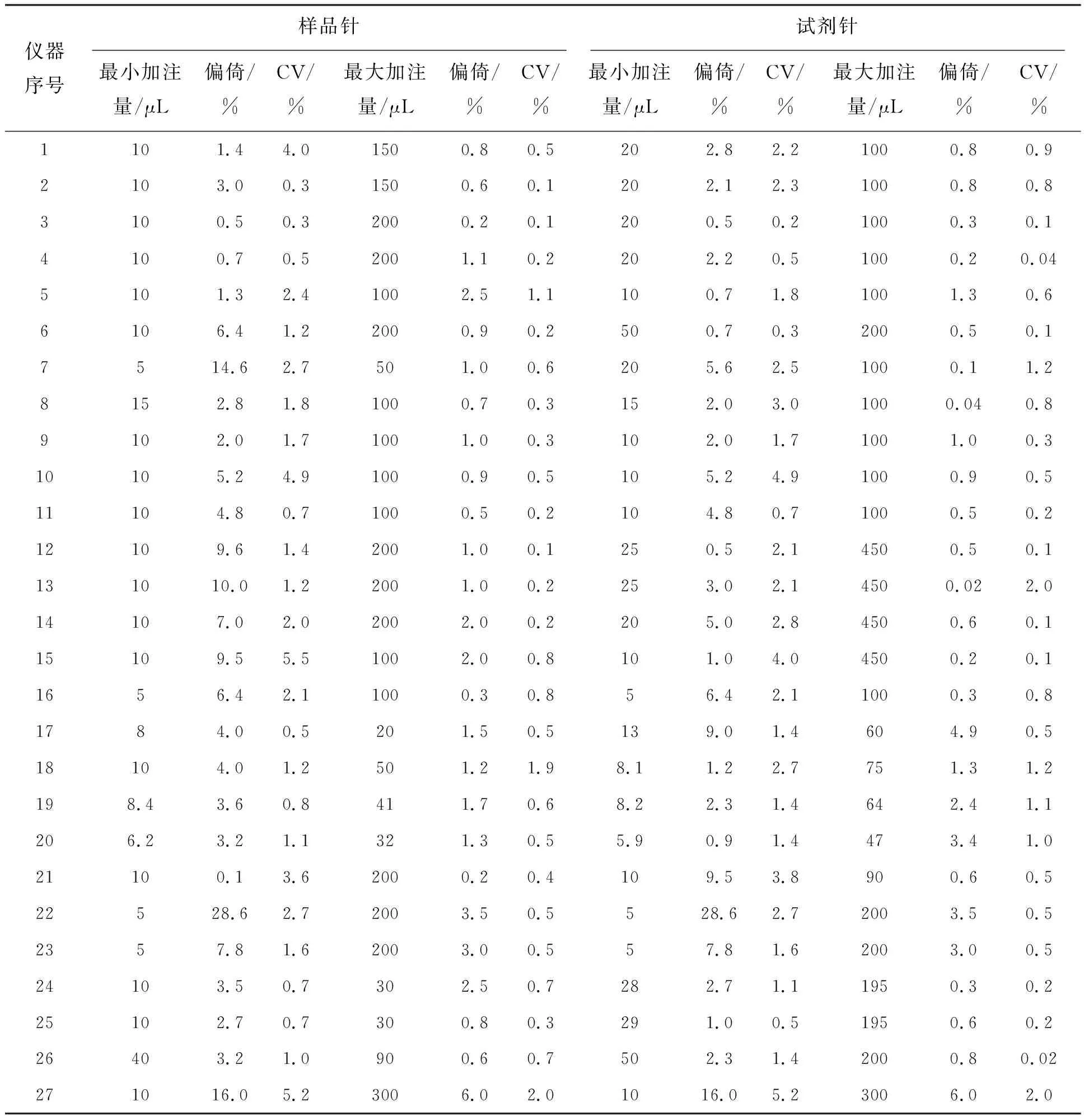
表2 全自動發光免疫分析儀加樣模塊測試結果
由于全自動發光免疫分析儀為全封閉儀器,在采用稱量法測試加樣模塊精度時,有的儀器不能實現儀器開蓋、加純水作為待測樣品或試劑、中斷加樣操作等干預步驟,實施稱量法較為困難。在此情況下,本研究開發了第二種方法即比色法。比色法的原理是色素溶液的稀釋比例與吸光度成線性關系。本研究采用橙黃G色素液,將其作為樣品或試劑,控制儀器按設置的加注量加注到反應杯中,然后將杯中橙黃G全部回收,在分光光度計波長478 nm下測試其吸光度,與理論吸光度進行比較,通過計算,得出儀器加樣的精度。與稱量法相比,色素法操作相對繁瑣,但其具有受環境影響小的優點,尤其適用于加注量小的情況。
4.3 光檢測裝置部分
4.3.1 儀器噪聲
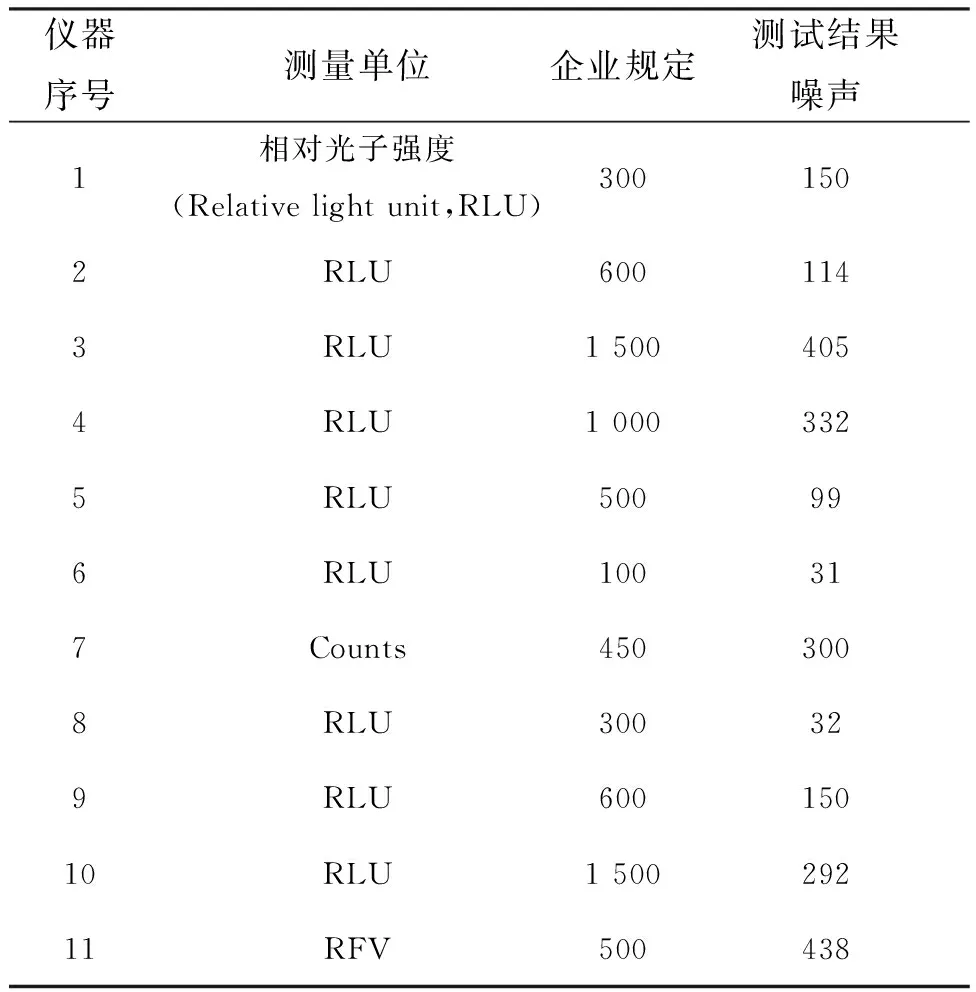
儀器噪聲大小直接關系到儀器的檢測靈敏度,噪聲越大,檢測的靈敏度就越低。免疫檢測為超微量分析,因此要求儀器的噪聲越小越好。表3為檢測器噪聲檢測結果,結果顯示,化學發光儀、電化學發光儀、熒光免疫儀檢測的發光信號是不同的,并且發光強度是一個相對值,儀器可以進行調整。各個廠家對儀器噪聲規定值不同,實際測試值也不同,但均能滿足各自規定。
表3全自動發光免疫分析儀噪聲測試結果
Tab.3 Testing result of noise of automatic luminescence immunoassay analyzers
儀器序號測量單位企業規定測試結果噪聲1相對光子強度(Relative light unit,RLU)3001502RLU6001143RLU1 5004054RLU1 0003325RLU500996RLU100317Counts4503008RLU300329RLU60015010RLU1 50029211RFV500438
4.3.2 發光值的線性
發光值的線性大小直接反映儀器的測量范圍。由于儀器原理、結構、操作可行性等因素,本研究對發光值線性的測試采用了2種方法,參考光源法和發光劑法。
目前,發光儀所使用的參考光源大多采用發光二級管(LED),通過調節LED驅動電流的DA值,可獲得不同光強的光。參考光源在制作、標定上有一定技術難度,所以采用參考光源進行發光儀光學系統檢測的廠家還較少[12]。大多數廠家采用發光劑法[13]。發光劑分為酶促和非酶促兩種,酶促發光劑由游離酶液(如堿性磷酸酶)和底物液組成,不同體積量的游離酶液與固定體積量的底物液充分混合后,將會發出不同強度的光強。非酶促發光劑主要成分為發光標記物(如異魯米諾)和緩沖液。使用時,用稀釋液將酶液或標記物稀釋成不同濃度梯度,再與底物液混合,發出不同強度的光強,用來測試發光儀的性能。
發光值線性測試,共測試了11個不同型號的儀器,其中1個型號的儀器采用參考光源進行測試,8個型號的儀器采用發光劑進行測試,還有2個型號的儀器同時采用兩種方法進行測試,結果見表4。從表中可以看出,儀器的線性范圍均不小于3個發光值數量級,有的甚至達到6個數量級,線性相關系數都達到0.99以上。2個型號的儀器同時采用兩種方法進行測試,結果接近,基本說明兩者方法是等效的。
表4全自動發光免疫分析儀發光值線性結果
Tab.4 Testing result of luminescence linear of automatic luminescence immunoassay analyzers
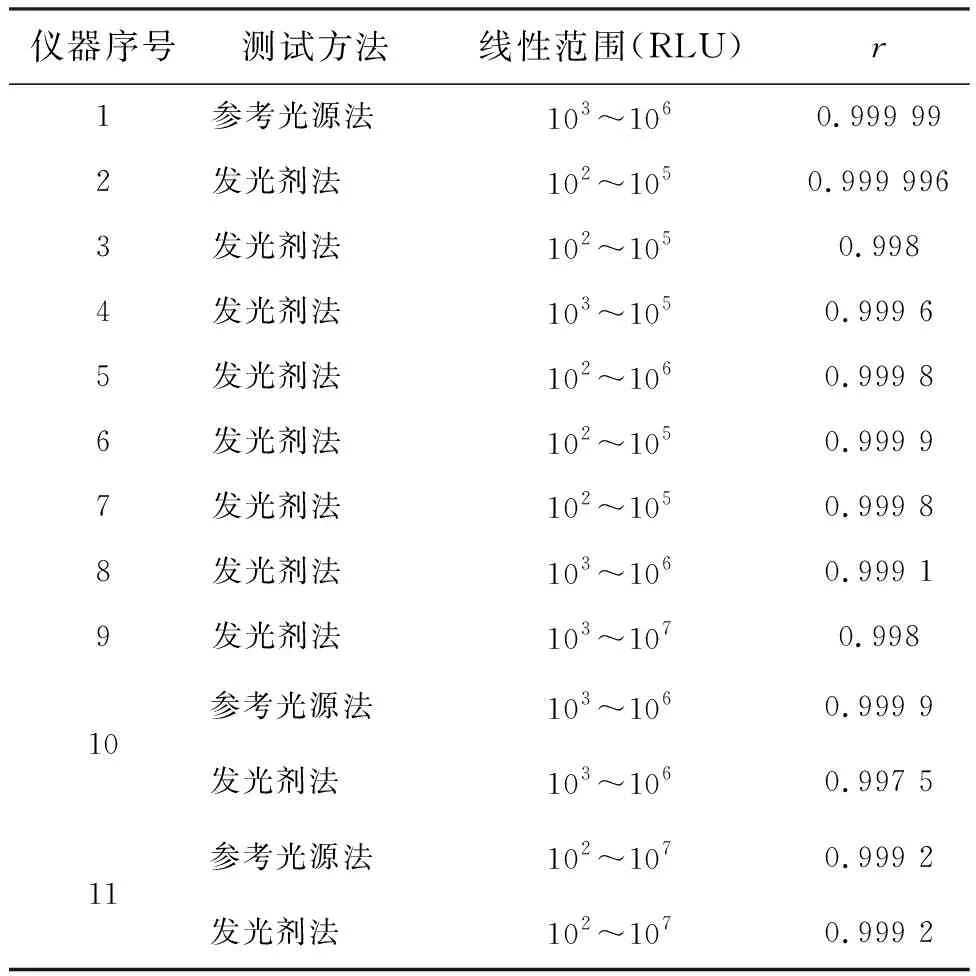
儀器序號測試方法線性范圍(RLU)r1參考光源法103~1060.999 992發光劑法102~1050.999 9963發光劑法102~1050.9984發光劑法103~1050.999 65發光劑法102~1060.999 86發光劑法102~1050.999 97發光劑法102~1050.999 88發光劑法103~1060.999 19發光劑法103~1070.99810參考光源法103~1060.999 9發光劑法103~1060.997 511參考光源法102~1070.999 2發光劑法102~1070.999 2
4.3.3 發光值的精密度
對發光值的精密度測試,選取了接近廠家標稱的測量范圍的上限和下限兩個點,具體結果見表5。測量范圍下限點的CV要高于測量范圍上限點的精密度,最大值達到3.8%。目前行業內對發光儀檢測模塊的精密度要求是CV不超過3%,因此建議1號、3號儀器要進一步改進。
表5全自動發光免疫分析儀發光值精密度結果
Tab.5 Testing result of luminescence precision of automatic luminescence immunoassay analyzers
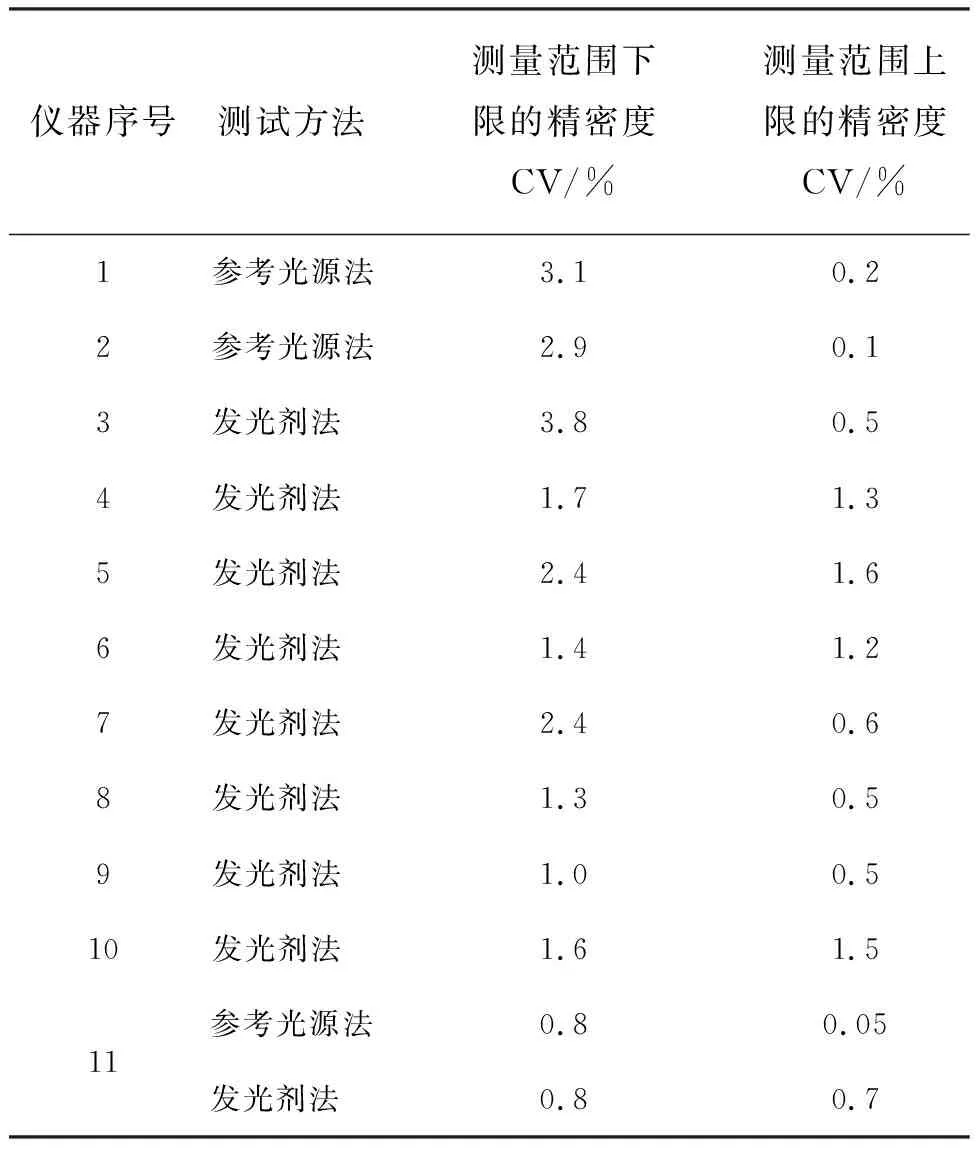
儀器序號測試方法測量范圍下限的精密度CV/%測量范圍上限的精密度CV/%1參考光源法3.10.22參考光源法2.90.13發光劑法3.80.54發光劑法1.71.35發光劑法2.41.66發光劑法1.41.27發光劑法2.40.68發光劑法1.30.59發光劑法1.00.510發光劑法1.61.511參考光源法0.80.05發光劑法0.80.7
4.3.4 發光值的穩定性
對發光值的穩定性測試,同樣選取了接近廠家標稱的測量范圍上限和下限兩個點,具體結果見表6。測量范圍下限點的偏倚要高于測量范圍上限點的偏倚,最大值達到8.0%。目前行業內對發光儀檢測模塊的穩定性要求是偏倚不超過5%,因此建議1號、5號儀器要進一步改進。
4.4 攜帶污染
攜帶污染主要表現為不同濃度樣品間連續測試的相互影響,特別是含量高的樣品對含量低的樣品所產生的影響,考察的是儀器清洗系統的性能。本研究對6個不同型號的儀器進行了攜帶污染測試,結果見表7。攜帶污染率差別較大,從0.8×10-6~54×10-6。對于部分線性范圍不太寬的項目,攜帶污染對檢測系統引入的總誤差貢獻很小,但是對于乙肝表面抗原(HBsAg)、HCG這類測量范圍較寬的項目,如果攜帶污染大,就很容易對低值的陰性樣品造成干擾,可能造成樣品檢測成假陽性[14]。本研究中將攜帶污染率設置為10×10-6,10×10-6可認為是一個門檻,滿足該要求后95%的臨床檢測項目都可滿足臨床要求。按照該要求,建議5號、6號儀器要進行進一步改進。
表6全自動發光免疫分析儀發光值穩定性結果
Tab.6 Testing result of luminescence stability of automatic luminescence immunoassay analyzers
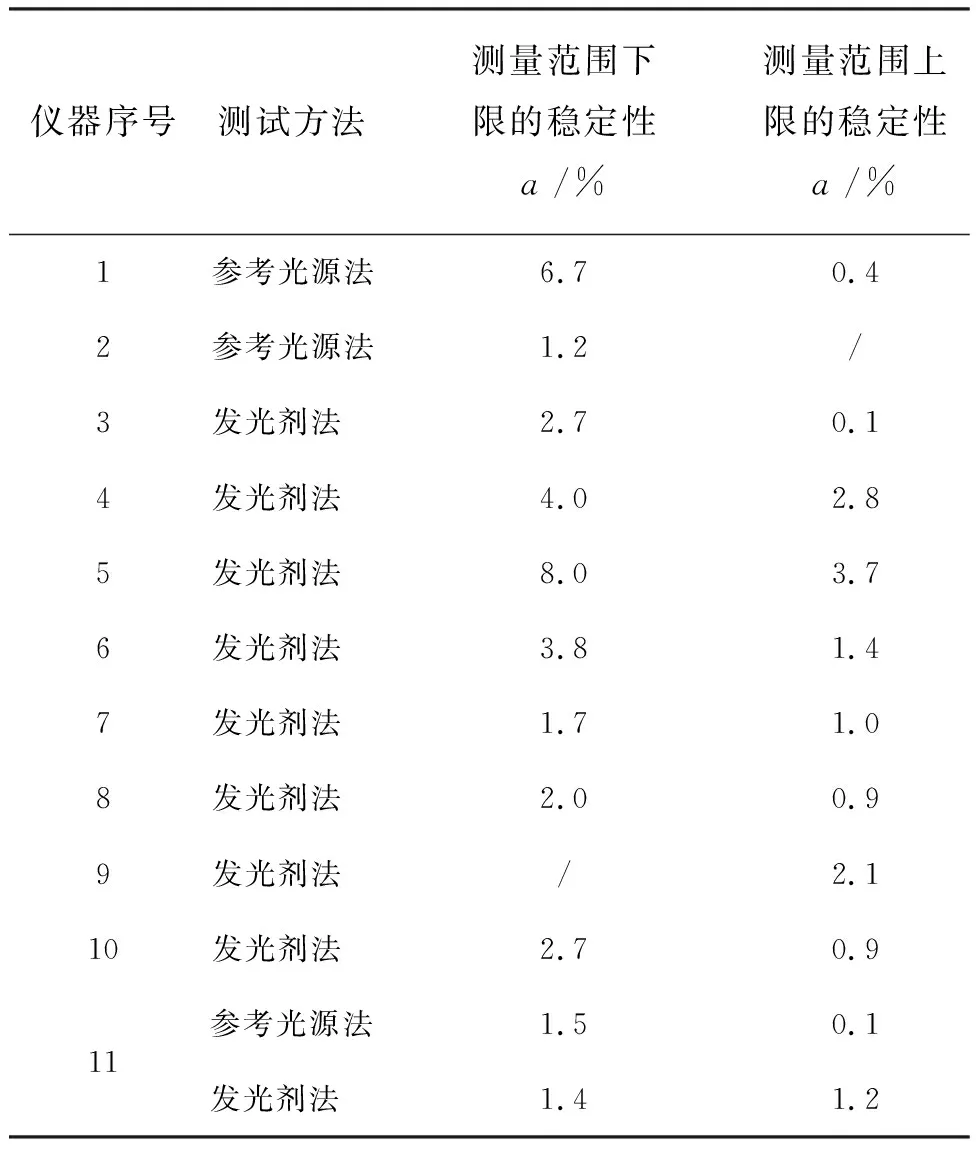
儀器序號測試方法測量范圍下限的穩定性a/%測量范圍上限的穩定性a/%1參考光源法6.70.42參考光源法1.2/3發光劑法 2.70.14發光劑法4.02.85發光劑法8.03.76發光劑法3.81.47發光劑法1.71.08發光劑法2.00.99發光劑法 /2.110發光劑法 2.70.911參考光源法1.50.1發光劑法1.41.2
表7全自動發光免疫分析儀攜帶污染結果
Tab.7 Testing result of carry-over of automatic luminescence immunoassay analyzers
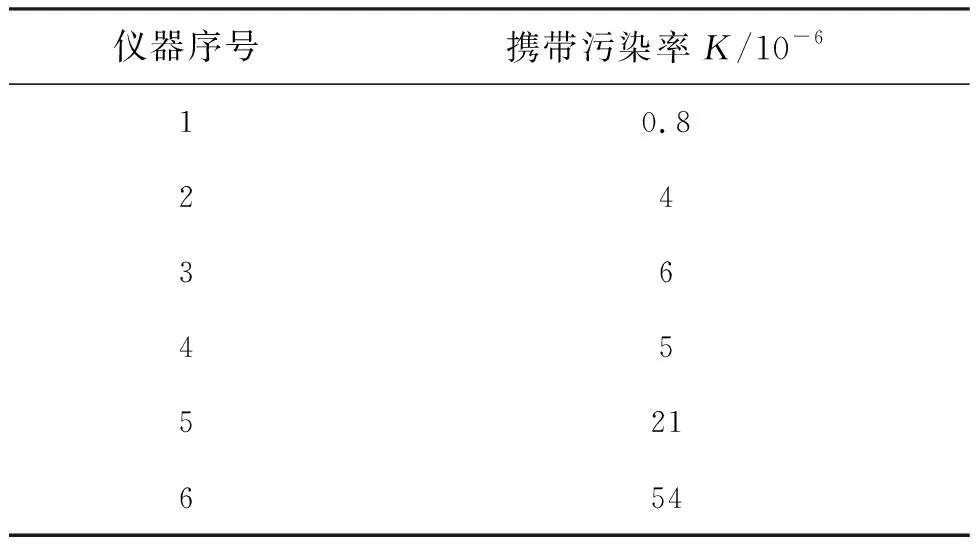
儀器序號攜帶污染率K/10-610.8243645521654
5 討 論
全自動發光免疫分析儀的關鍵模塊包括加樣系統、孵育系統、清洗系統和檢測系統,本研究從全自動發光免疫分析儀的結構和特點出發,建立了統一的評價方法。采用本研究建立的方法,完成了對市面上主流的15家生產企業生產的30個不同型號的全自動發光免疫分析儀的性能評價,基本證明了該方法的適用性和可操作性。本研究主要貢獻體現在:
(1)建立了全自動發光免疫分析儀可行的、統一的、標準化的評價方法。
本研究對加樣系統、孵育系統、清洗系統和檢測系統(噪聲、線性、精密度、穩定性)分別建立了檢測方法,結合全自動發光免疫分析儀的特點,對加樣系統同時建立了稱量法和比色法兩種方法,對檢測系統同時建立了參考光源法和發光劑法兩種方法。本研究建立的檢測技術適用性強,能適用于化學發光、電化學發光、熒光免疫等不同發光原理的儀器,也適用于酶促發光和非酶促發光不同反應類型的儀器。
(2)完成了對市面上主流的全自動發光免疫分析儀的摸底測試。
用本研究建立的方法,對市面上主流的15家生產企業生產的30個不同型號的全自動發光免疫分析儀進行了性能評價,基本結論為:孵育系統,所有儀器均能滿足要求;加樣系統,少數儀器不能達到其聲稱的最小加注量;檢測系統,所有儀器均能滿足噪聲和線性要求,少數儀器不能達到精密度和穩定性要求;清洗系統,某些儀器的攜帶污染率不能達到要求。數據顯示,全自動發光免疫分析儀還有一定的質量提升空間。
(3)促進企業開發參考光源、發光劑等檢測工裝。
本研究開展前,只有少數企業具備參考光源或發光劑。在建立全自動發光免疫分析儀檢測方法過程中,國內外企業積極參與。通過對方法的反復討論和驗證,拓寬了思路,促使企業去開發檢測設備和工裝,特別是參考光源、發光劑等重要工裝的開發,解決了全自動發光免疫分析儀評價的核心技術障礙,從而也促進了產品的質量提升。
目前各廠家用參考光源和發光劑尚不能實現標定和計量學溯源,因此本研究后續工作設想是與計量部門合作,開發參考光源和發光劑的標準物質,從而進一步完善發光免疫分析儀的檢測方法,促進免疫診斷結果的溯源和量值準確傳遞。

