藜蘆莖葉的質量標準研究
邢瀟 張航 徐彤彤 劉治民 楊建龍 曲艷麗
摘?要:
目的:通過對藜蘆莖葉常規檢驗及特征檢驗方法的研究,為其質量標準的制定與開發利用提供依據。方法:采用性狀鑒定、顯微特征及TLC法對其進行定性鑒別;通過水分、總灰分、酸不溶性灰分等常規檢查方法對其進行藥材質量考察;通過HPLC法測定其活性成分白藜蘆醇含量,進一步考察其藥材質量。結果:10批樣品TLC斑點清晰,分離度好;水分測定值在6.4%~10.6%之間;總灰分測定值在8.5%~13.4%之間;酸不溶性灰分測定值在1.0%~2%之間;白藜蘆醇含量在0.007%~0.030%之間。討論:所選性狀、顯微及TLC方法可有效鑒別藥材真偽;所選水分等常規檢查方法可在一定程度反映藥材質量;所選HPLC方法專屬性強,分離度好,方法穩定可靠。
關鍵詞:
藜蘆莖葉;質量標準;試驗研究
中圖分類號:S-3
文獻標識碼:A
DOI:10.19754/j.nyyjs.20191230006
藜蘆莖葉為百合科植物藜蘆(Veratrum nigrum L.)的干燥莖葉,主產于東北、華北、西北、內蒙古等地。藜蘆具有吐風痰、定癲癇等作用,用于痰涎涌盛,癲癇喉痹;外用治療小兒消化不良性腹瀉,腸炎等;還有祛痰,催吐,殺蟲之效[1,2]。中醫用于治療中風失語及痰壅、黃疸、久拒、喉癖、鼻息、泄痢、頭痛、濟癬等。現代藥理研究表明,藜蘆具有抗氧化、降血壓作用[3];藜蘆中某些成分還具有抗血栓以及增強心肌細胞的收縮功能以改善高血壓時的心臟超負荷狀態等作用[4]。藜蘆化學成分主要為甾體生物堿類化合物、茋類化合物、二肽類、黃酮類及其它類化合物。其中茋類化合物白藜蘆醇(C14H12O3)為藜蘆中的主要藥理活性成分之一。藜蘆始載于《神農本草經》,古本草及各省標準中常選用根及根莖作為其藥用部位,但考慮其根及根莖中的有毒生物堿成分較多,故部分省市也應用其地上部分作為藥用部位[1,5-9]。目前藜蘆莖葉尚無國家飲片炮制標準,而其各省標準也較為落后,不能有效地控制藜蘆莖葉的藥材質量,其質量標準迫切需要提高。
1?儀器與試劑試藥
生物顯微鏡BX51(OLYMPUS);1260高效液相色譜儀(Agilent); GR-202電子天平(日本A\\D公司);KQ-500VDE型雙頻數控超聲波清洗器(昆山市超聲儀器有限公司);DK-98-11A電熱恒溫水浴鍋(天津泰斯特儀器有限公司);101-1A型電熱鼓風干燥箱(天津市泰斯特儀器有限公司);SX2-4-10型高溫箱式電爐(上海博迅實業有限公司)等;中藥手工切片刀(深圳眾達)。
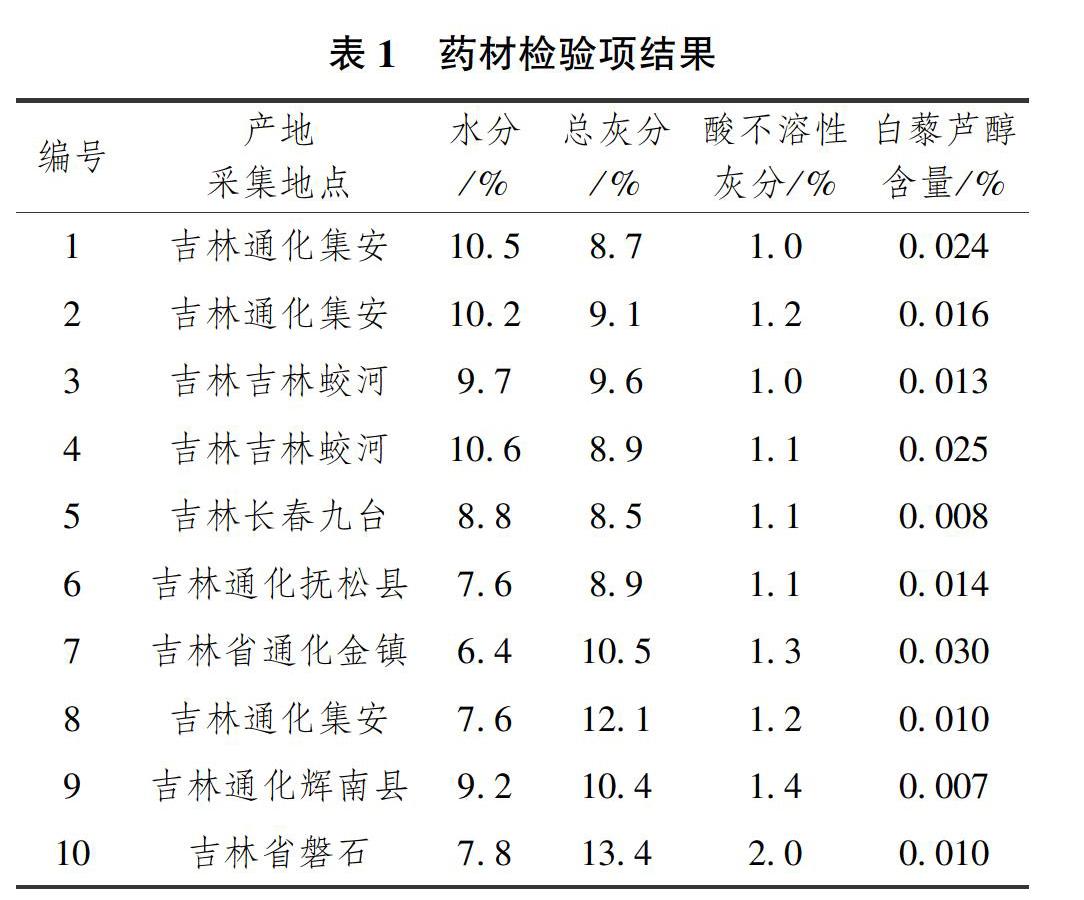
藜蘆莖葉對照藥材(長春市食品藥品檢驗中心自制并經專家鑒定,批號:201607);白藜蘆醇對照品(中檢院,批號:111535-201703);色譜甲醇(Fisher Chemical);乙醇(北京化工廠)等。共選擇10批樣品為2015年5月—2016年10月之間采集,均為野生樣品,并經過吉林中醫藥大學教授鑒定為百合科植物藜蘆的干燥莖葉,見表1。
2?方法與結果
2.1?性狀
根據收集到的樣品進行性狀研究,其性狀特征大致如下:本品全長約30~100cm,莖圓柱狀,中空,表面灰綠色或棕褐色,莖基部常殘留黑褐色網狀纖維;葉片橢圓形,基部抱莖,全緣,兩面無毛,具數條明顯的平行脈;體輕質脆,氣微。
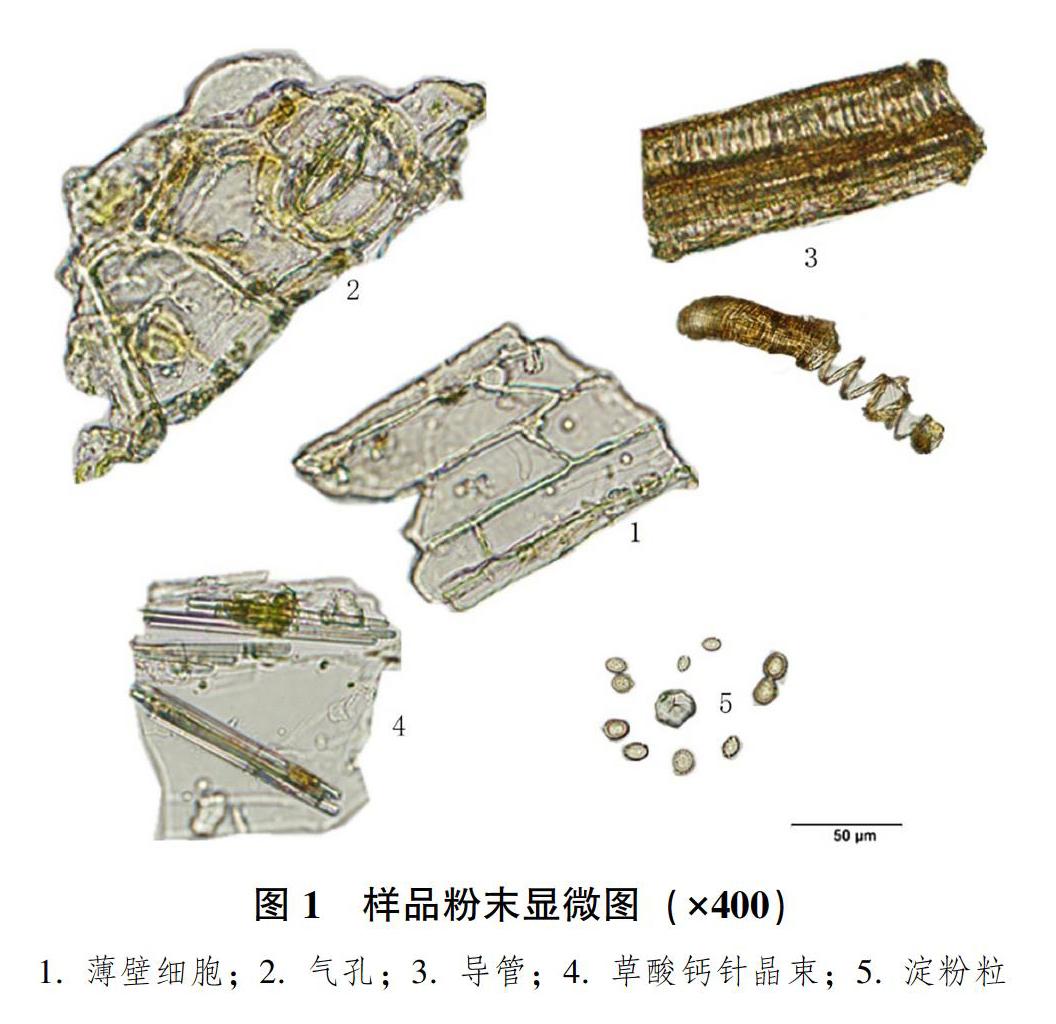
2.2?顯微特征
植物可以通過具有專屬性的顯微特征而進行真偽的鑒別。通過顯微鏡下觀察各樣品的粉末,發現其有以下顯微特征:本品粉末呈黃綠色或棕褐色,淀粉粒較多,呈圓形或橢圓形,直徑4~20μm,多為單粒,臍點點狀或呈人字狀;草酸鈣針晶成束或散列于薄壁細胞中,長約40~150μm;導管多為螺紋導管,亦有網紋導管及梯紋導管,直徑12~80μm;葉表皮細胞中可見氣孔,大小不一。
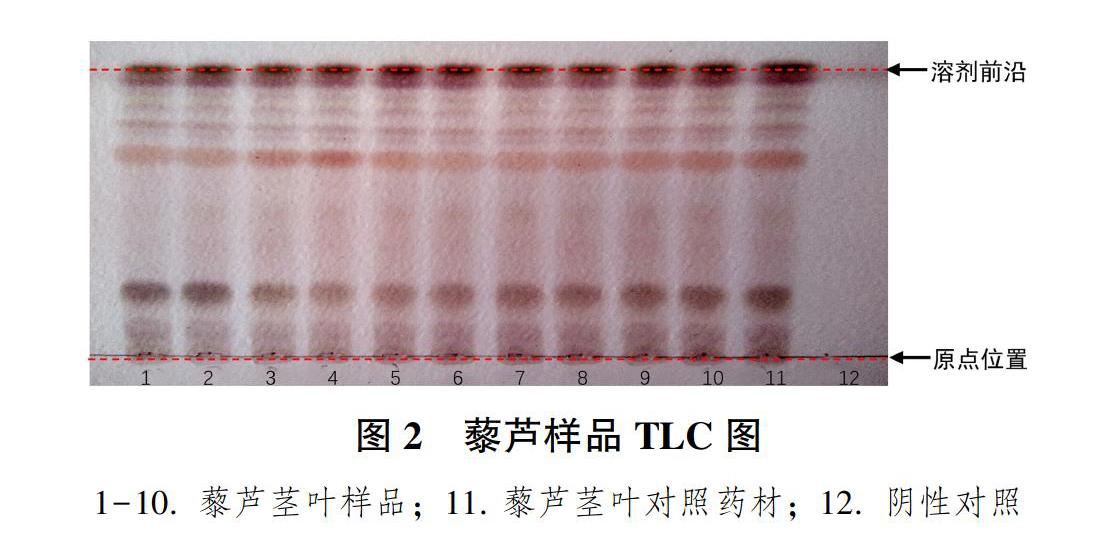
2.3TLC鑒別
經對不同展開條件進行選擇,結果顯示,取本品粉末2g,加甲醇30mL,超聲處理20min,過濾,濾液蒸干,殘渣加甲醇2mL溶解,作為供試品溶液。另取藜蘆對照藥材同法制成對照藥材,作為對照藥材溶液。照薄層色譜法(中國藥典2015年版 通則0502[10])試驗,吸取上述2種溶液各10μL,分別點于同一硅膠G薄層板上,以三氯甲烷-甲醇-水(15∶5∶0.5)為展開劑,展開,取出,晾干,噴以10%硫酸乙醇溶液,在105℃加熱至斑點顯色清晰。供試品色譜在與對照藥材色譜相應的位置上,顯相同顏色的斑點。該方法省時、簡便、直觀,并可以有效對藥材真偽進行鑒別。
2.4檢查
對藥材的常規檢查可以有效地評價藥材的優劣,主要按《中國藥典》2015年版四部通則對藥材的檢查要求進行水分、總灰分、酸不溶性灰分的檢查,其結果見表1。結果顯示:10批樣品的水分測定值在6.4%~10.6%之間;總灰分測定值在8.5%~13.4%之間;酸不溶性灰分測定值在1.0%~2%之間。
2.5?含量測定
為確保藜蘆莖葉藥材質量的穩定性、專屬性及可控性,采用高效液相色譜法測定藜蘆中有效成分—白藜蘆醇,按照高效液相色譜法(《中國藥典》2015年版四部通則0512)進行測定。
2.5.1?色譜條件
試驗結果表明: 白藜蘆醇經DAD光譜掃描,在306nm處有最大吸收,考慮其基線平穩程度,并根據參考文獻中白藜蘆醇的檢測波長[11],確定306nm為其測定波長。
以十八烷基硅烷鍵合硅膠為填充劑,分別以乙腈-水、甲醇-水為流動相,不同流動相比例,不同柱溫、不同流速下進行比較,結果顯示,乙腈-水(20∶80)可以將白藜蘆醇成分有效分析,且分離度不受柱溫及流速的影響。
根據實驗結果最終確定色譜條件:以十八烷基硅烷鍵合硅膠為填充劑;乙腈-水(20∶80)為流動相;檢測波長為306nm。進樣量10μL,柱溫25℃,流速1.0mL/min。理論板數按白藜蘆醇峰計算應不低于1500。
2.5.2?提取方法
取同一批次樣品粉末約0.5g,加不同溶劑,采用不同處理方法,以十八烷基硅烷鍵合硅膠為填充劑;乙腈-水(20∶80)為流動相;檢測波長為306nm。進樣量10μL,柱溫25℃,流速1.0mL/min進行樣品提取方法學考察,結果顯示最佳提取方法為:取本品粉末約0.5g,精密稱定,加甲醇50mL,超聲處理(功率400W,頻率45kHz)40min,過濾,濾液為供試品溶液。10批樣品中白藜蘆醇的含量測定結果見表1,色譜圖見圖3。
2.5.3?方法學驗證與結果
2.5.3.1?線性及范圍
取白藜蘆醇對照品適量,精密稱定,加甲醇制成每1mL中含4.864μg(1)及0.0206mg(2)的溶液,搖勻,作為對照品溶液。精密吸(1)1μL,(2)1μL、2μL、5μL、10μL、16μL、18μL,注入液相色譜儀,測定,計算。以對照品峰面積為縱坐標,進樣量為橫坐標,繪制白藜蘆醇對照品的標準曲線。結果表明,白藜蘆醇在2.904~13.794μg范圍內,峰面積與白藜蘆醇呈良好的線性關系,回歸方程為Y = 29944X +22.626,相關系數r = 0.9993。
2.5.3.2?耐用性
分別試驗3個不同品牌的C18色譜柱進樣,測定。考查不同品牌的色譜柱對待測成分色譜峰的分離效果。
色譜柱a:Agilent ZORBAX SB-C18(4.6×250mm,5μm)柱
色譜柱b:Agilent C18 (4.6mm×250mm,5μm)柱
色譜柱c:Diamonsil C18(4.6×250mm,5μm)柱
白藜蘆醇平均含量為0.024%、n=3、RSD=3.4%。結果顯示;各品牌的色譜柱均能將白藜蘆醇色譜峰達到基線分離,樣品中各色譜峰峰型及分離度均較好。
2.5.3.3?重復性
取同一批次藜蘆莖葉藥材,按上文確定的提取方法制備供試品溶液6份,測定白藜蘆醇的含量,結果白藜蘆醇的平均含量為0.0240%、n=6、RSD=2.9%;說明本方法的重復性良好。
2.5.3.4?儀器精密度
取重現性項下的一份供試品溶液,按上述色譜條件,精密吸取供試品溶液10μL重復進樣6次,測定白藜蘆醇的峰面積,結果白藜蘆醇的平均峰面積為460.001282、n=6、RSD=0.2%。說明儀器精密度良好。
2.5.3.5?準確度
取重現性試驗同批次樣品(白藜蘆醇含量:0.0240%)9份,每份取約0.5g,精密稱定,再分別加入3種比例白藜蘆醇對照品適量,按標準正文含量測定項下方法制備供試品,進樣,測定其中白藜蘆醇的含量,計算回收率。結果3種比例白藜蘆醇的平均回收率分別為105.07%、n=9、RSD=3.1%。說明本方法回收率良好。
2.5.3.6?穩定性
精密吸取同一供試品溶液10 μL,分別在0h,6h,12h,24h進樣,計算峰面積的RSD值。結果白藜蘆醇的平均峰面積為741.4033625、n=6、RSD=1.7%。結果表明供試品溶液在24h內穩定。
2.5.4?樣品含量測定結果
該方法簡單易操作,重復性與分離度均較好。結果顯示樣品中白藜蘆醇含量在0.007%~0.030%之間。考慮原料藥產地、加工及生產等因素以及采收時間的影響,發現各地區白藜蘆醇含量差異較大。
3?討論
各省份關于藜蘆地上部分的藥材標準相對落后,已不能有效地評價藜蘆莖葉藥材的質量。本研究參照了中國藥典2015版藥材標準制定技術的相關要求,通過性狀特征可有效將其與不同來源及易混淆品種的藜蘆如毛穗藜蘆、尖被藜蘆、狹葉藜蘆等進行區別[12,13];顯微特征、TLC等項可以進一步有效鑒別藥材真偽,TLC方法斑點清晰、分離度好;水分、灰分、總灰分及酸不溶性灰分檢查等項可以有效評價藥材的質量;通過多條件篩選后的HPLC法可有效測定藜蘆莖葉中活性成分白藜蘆醇的含量。該方法簡單易操作,可重復性及準確度良好,有利于其標準限度的制定及合理用藥。
綜上,本文的實驗結果及方法可以作為藜蘆莖葉藥材質量標準制定的參考,并為藜蘆莖葉藥材的質量控制提供理論依據。
參考文獻
[1] 吉林省衛生局. 吉林省藥品標準(1977年版)[M]. 長春:吉林科學技術出版社,1977:258-259.
[2]?國家中藥管理局編委會.中華本草:第八卷[M]. 上海:上海科學技術出版社,1999:183-188.
[3]?趙錄英,趙畫晨,吳博威.藜蘆混堿對離體心泵功能的效應及其與洋地黃類藥物的對比[J]. 山西醫科大學學報, 2002, 33(3): 231-232.
[4]?劉海燕,費洪新.順柏與白藜蘆醇聯合對胃癌細胞影響的研究[J]. 齊齊哈爾醫學院學報,2010,31 (1):11-12.
[5]?段維和,樊紹缽,鄧明魯,等. 吉林藥材圖志 [M]. 北京:中醫古籍出版社,1987:212-215.
[6]?吉林省衛生局.吉林省中藥飲片炮制規范(1986年版)[M]. 長春:吉林科學技術出版社,1986:57.
[7]?北京市藥品監督管理局.北京市中藥飲片炮制規范(2008年版)[M]. 北京:化學工業出版社,2008:192.
[8]?黑龍江省食品藥品監督管理局.黑龍江省中藥飲片炮制規范(2012年版)[M]. 哈爾濱:黑龍江科學技術出版社,2012:398.
[9]?天津市食品藥品監督管理局.天津市中藥飲片炮制規范(2012年版)[M]. 天津:天津市食品藥品監督管理局,2012:204.
[10]?國家藥典委員會. 中華人民共和國藥典2015年版四部[M]. 北京:中國醫藥科技出版社,2015:57.
[11]?叢悅,王金輝,李銑.HPLC 法測定藜蘆中虎杖苷和白藜蘆醇的含量[J]. 中藥研究與信息,2005,7(7):16-19.
[12]?林壽全,馮毓秀,陳紅.藜蘆屬中草藥的原植物與生藥鑒別[J].藥物分析雜志,1983,3(4):197-202.
[13]?尹子麗,楊仙雨,張潔. 民族民間藥狹葉藜蘆生藥學研究[J]. 云南中醫中藥雜志,2015,36(3):57-59.
作者簡介:
邢瀟(1983-),女,博士,副主任藥師。研究方向:中藥材及飲片的質量評價及質量標準研究。

