脂聯素基因單核苷酸多態性與高血壓易感性及血壓值關聯性研究
李 倩,劉夢微,劉 珊,楊魯平,張凱麗,張 倩,王 玥,劉萬洋
(中國醫科大學公共衛生學院營養與食品衛生學教研室,沈陽 110122)
高血壓是以體循環動脈血壓增高為特征,可伴有心、腦、腎等器官功能或器質性損害的全球性疾病,是心腦血管疾病的高危因素,其與肥胖、胰島素抵抗、葡萄糖不耐受以及高血脂并稱為代謝綜合征。脂聯素作為一種胰島素超敏化激素,與炎癥、氧化應激、血栓前狀態、心血管疾病和2型糖尿病的風險增高有關。脂聯素是脂肪組織中最豐富的肽類激素之一。其在葡萄糖和脂質代謝中起主要作用,并能阻止血管的變化,低脂聯素可能對代謝綜合征的發生具有某種作用。有研究表明,較低的血漿脂聯素水平與高血壓密切相關[1-2]。低脂聯素血癥患者有高血壓可能與多種機制有關,如胰島素抵抗、交感神經激活、脂肪酸水平升高、內皮依賴性血管舒張功能受損和血管炎癥等[3]。對于脂聯素(adiponectin,ADIPOQ)基因單核苷酸多態性(single nucleotide polymorphisms,SNP)與高血壓的關聯研究,國內外報道的結果不一致,本研究收集2017年遼寧省撫順市石文鎮和盤錦市興盛社區65歲及以上老年人體檢資料,從基因多態性的角度探討ADIPOQ基因rs182052、rs7627128和rs1501299三個多態位點與高血壓的關聯性,為進一步揭示高血壓的遺傳易感性機制提供依據。
1 對象與方法
1.1研究對象 選取2017年1—10月遼寧省撫順市石文鎮中心醫院和盤錦市興盛社區衛生服務中心65歲及以上老年體檢者為研究對象,均為漢族。其中444例高血壓患者作為病例組,均為正在接受降壓治療的患者或在靜息狀態下非同日3次血壓測量的平均收縮壓≥140 mmHg(1 mmHg=0.133 kPa)和(或)舒張壓≥90 mmHg的患者,排除嚴重的肝、腎疾病及急慢性感染性疾病、甲狀腺功能亢進或減退、全身大動脈疾病、各種腫瘤及糖尿病、肥胖、患有其他腦血管疾病和代謝性疾病的高血壓患者。選擇同期304例健康體檢者作為對照組。
1.2方法
1.2.1一般資料的收集 研究對象的基本情況由統一培訓的調查員進行問卷調查,包括年齡、性別、身高、體重、既往史和家族史等。受試者靜坐休息5 min 后采用國產魚躍臺式血壓計(水銀)測量3次血壓,每次測量間隔30 s,求其平均值。自動生化分析儀(邁瑞BS-820)統一檢測所有研究對象的各項血液指標。
1.2.2血樣收集以及基因組DNA的提取 抽取研究對象外周靜脈血10 mL,置于裝有乙二胺四乙酸四鈉鹽二水合物抗凝管中,采用基因組DNA提取試劑盒(北京康為世紀生物科技有限公司生產,批號:Lot.50308)提取基因組DNA,采用Nanodrop 2000核酸測定儀測定基因組DNA濃度及純度。當A260/280≈1.8時,可認為提取的DNA純度達到后續試驗要求,后置于-80 ℃冰箱長久保存。
1.2.3ADIPOQ基因rs182052、rs7627128和rs1501299的基因分型 采用Taqman基因分型技術對3種基因多態性進行基因分型(探針:Applied Biosystems,Foster City,USA)聚合酶鏈反應(polymerase chain reaction,PCR)反應體系為5 μL,其中含2.0 μL的DNA模板,TaqPathTMProAmpTMMaster Mixes(Applied Biosystems,Foster City,CA,USA)溶液2.5 μL,40×SNP基因分型探針0.1 μL,無酶水0.4 μL。PCR擴增條件:95 ℃預變性30 s,95 ℃變性5 s,60 ℃退火5 s,60 ℃延伸30 s,40個循環后60 ℃再延伸30 s。使用QuantTMstudio Flex 6 Real-Time PCR系統(Applied Biosystems,Foster City,USA)進行檢測。

2 結 果
2.1兩組受試者一般臨床指標比較 兩組性別、年齡、身高、空腹血糖、總膽固醇、三酰甘油比較差異無統計學意義(P>0.05),病例組體重、腰圍、體質指數、收縮壓和舒張壓均高于對照組(P<0.05)。見表1。

表1 兩組受試者一般臨床指標比較
1 mmHg=0.133 kPa;a為χ2值,余為t值
2.2兩組受試者ADIPOQ基因3個SNP位點等位基因和基因型的分布 ADIPOQ三個基因多態性rs182052、rs7627128和rs1501299在本研究兩個地區調查人群中滿足Hard-Weinberg 平衡比例。兩組rs182052、rs7627128和rs1501299位點的等位基因頻率、基因型頻率比較差異均無統計學意義(P>0.05)。見表2。
2.3ADIPOQ基因3個SNP位點在3種遺傳模式下Logistic回歸分析 在加性模型、顯性模型和隱性模型三種不同遺傳模式下,分別對病例組和對照組ADIPOQ基因rs182052、rs7627128和rs1501299進行Logistic回歸分析。單因素Logistic回歸分析結果顯示,ADIPOQ基因rs182052和rs7627128的多態性在加性模型、 顯性模型和隱性模型下均對高血壓的發生無影響(P>0.05),而rs1501299隱性模型下是高血壓發生的危險因素。進一步對年齡、性別、空腹血糖、體質指數等因素校正后進行多因素Logistic回歸分析,結果顯示,rs1501299在加性模型和隱性模型下仍對高血壓的發生具有危害作用,TT基因型攜帶者發生高血壓的危險性是GG基因型的1.881倍,是GT+GG基因型攜帶者的1.901倍(P<0.05)。見表3。
2.4ADIPOQ基因3個SNP位點的單體型的分布 應用SHEsis軟件計算ADIPOQ基因3個SNP位點rs182052、rs7627128和rs1501299的單體型頻率,兩組4種單體型頻率比較差異無統計學意義(P>0.05)。見表4。

表2 兩組受試者3個SNP位點等位基因和基因型的分布 [頻數(%)]
SNP:單核苷酸多態性
2.5ADIPOQ基因3個SNP位點在3種遺傳模式下血壓值差異分析 ADIPOQ基因多態性rs182052和rs7627128不同基因型間的收縮壓和舒張壓比較差異均無統計學意義(P>0.05);rs1501299的TT、GT和GG三個基因型的舒張壓比較差異無統計學意義(P>0.05),GT+TT和GG基因型的收縮壓和舒張壓均差異無統計學意義(P>0.05);而rs1501299的基因型TT的收縮壓高于GT和GG基因型(P<0.05),基因型TT的舒張壓高于GT+GG基因型(P<0.05)。見表5。
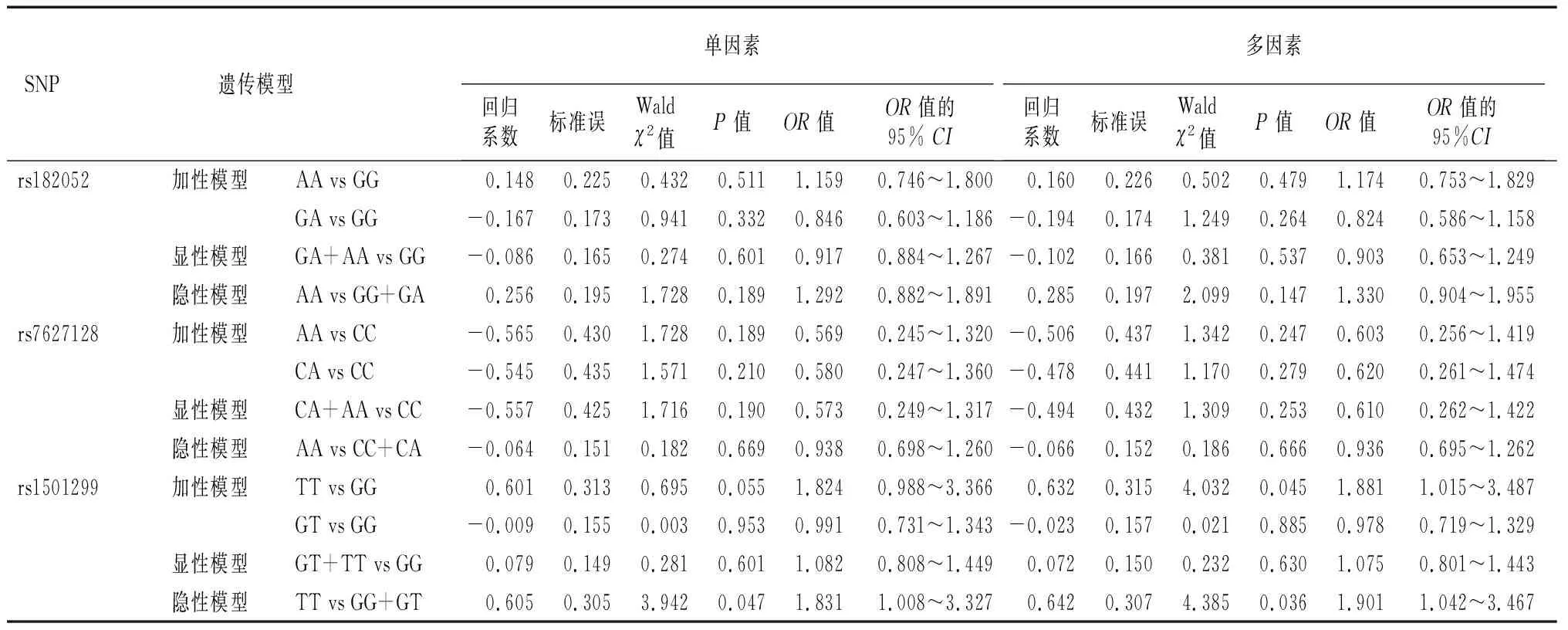
表3 脂聯素基因三種遺傳模式下Logistic回歸分析
SNP:單核苷酸多態性

表4 三個基因多態性單體型關聯分析 [頻數(%)]
3 討 論
全世界患有難治性高血壓的人數將近10億(約占世界人口的15%),預計到2025年,患病人數將增加到15.6億[6]。據估計,由高血壓引起的心腦血管疾病死亡人數占所有死亡人數的13%[7]。高血壓患病率升高的原因主要有人口老齡化、城市化、生活


SNP遺傳模型例數收縮壓F/t值P值舒張壓F/t值P值rs182052加性模型AA140140.6±19.286.1±10.5GA391140.2±18.00.129b0.87985.9±9.70.164b0.849GG217141.0±18.586.4±9.9顯性模型GA+AA531140.3±18.30.476c0.63486.0±9.90.535c0.593GG217141.0±18.586.4±9.9隱性模型AA140140.6±19.20.021c0.98386.1±10.50.031c0.975GG+GA608140.5±18.186.1±9.7rs7627128加性模型AA431140.4±18.986.0±9.8CA289140.1±17.51.926b0.14686.1±10.10.942b0.390CC28147.2±18.288.6±8.3顯性模型CA+AA720140.3±18.31.955c0.05186.0±9.91.363c0.173CC28147.2±18.288.6±8.3隱性模型AA431140.4±18.90.272c0.78686.0±9.80.482c0.630CC+CA317140.8±17.686.3±9.9rs1501299加性模型TT57146.7±20.088.8±11.8GT312139.8±18.7a3.572b0.02985.5±10.02.675b0.070GG379140.2±17.6a86.2±9.4顯性模型GT+TT369140.9±19.00.549c0.58386.0±10.30.158c0.875GG379140.2±17.686.2±9.4隱性模型TT57146.7±20.02.664c0.00888.8±11.82.161c0.031GG+GT691140.0±18.185.9±9.7
1 mmHg=0.133 kPa;SNP:單核苷酸多態性;a與rs1501299加性模型TT比較,P<0.05;b為F值;c為t值
方式和飲食習慣的改變,除此之外,高血壓的遺傳因素也不容忽視,雙胞胎和家族遺傳學研究表明,在血壓變化中遺傳因素的作用占20%~60%[8]。近年來,研究者對高血壓患者進行了廣泛的遺傳學研究,包括全基因組關聯性研究[9-14]。目前脂肪組織被認為是一個巨大的內分泌腺,參與調節多種生物功能。脂肪組織與其他生物系統之間的溝通是通過大量生物活性介質的表達來完成的,這些物質統稱為脂肪因子[15]。脂聯素是最重要的脂肪因子之一,其是一種來源于脂肪組織的細胞因子,具有抗炎和抗動脈粥樣硬化的特性,除有胰島素抵抗功能外,還與中樞性肥胖有關,在代謝性疾病的發生和發展中起重要作用[16]。編碼脂聯素的基因位于3q27染色體,其編碼的蛋白是一種含有244個氨基酸的多肽(蛋白),該蛋白由4個結構域組成:N端信號序列、可變區域、膠原型結構域和C端球狀結構域[17]。人血清脂聯素濃度約為瘦素的3倍,占所有血漿蛋白的0.01%[18]。研究表明,此基因的一些SNP參與調節脂聯素在血液中的濃度。目前,已有多項研究探討ADIPOQ基因SNP與高血壓風險的關系,其中包括rs2241766、rs1501299、rs266729和rs7649121等[19-26],Mousavinasab等[27]發現rs1501299的GT或GG基因型患者的舒張壓明顯低于TT基因型患者。由于以上研究結果不一致,本研究選取ADIPOQ基因3個位點(rs182052、rs7627128和rs1501299)來探討ADIPOQ基因與高血壓的關聯性及其對于血壓的影響。本研究結果顯示該基因rs182052、rs7627128和rs1501299與本研究調查地區的高血壓不存在關聯性。產生此結果的原因可能有以下幾點:①雖然之前有研究發現ADIPOQ與高血壓有關[24],但是由于研究人群具有種族差異性可能導致研究結果不一致;②本研究的樣本量較小,只是選擇了遼寧省兩個地區的體檢人群,缺乏覆蓋面更大的抽樣調查,故本研究結果有待進一步證實;③高血壓是環境因素和遺傳因素共同作用的結果,屬于多基因疾病,除遺傳因素外,高血壓還受多種環境因素的影響[28],如年齡、性別、生活習慣以及行為等,而本研究進行Logistic回歸分析時缺少一些未收集關鍵因素的資料;④本研究僅選了ADIPOQ的3種SNPs,故研究結果不能完全解釋脂聯素與高血壓的關聯性。
盡管本研究結果提示該基因rs182052和rs7627128與東北地區漢族人群的高血壓可能不存在關聯性,但rs1501299的基因型TT的收縮壓高于GT和GG基因型,基因型TT的舒張壓高于GT+GG基因型,提示高血壓的發生可能與ADIPOQ基因多態性rs1501299位點的基因突變有關,此位點可能參與血壓的調節,而高血壓患者更容易患有卒中等慢性疾病,因此rs1501299攜帶者更需要特別注意控制血壓,以防止腦血管疾病的發生。rs1501299多態性不同基因型之間血壓比較差異有統計學意義,其是否在高血壓發病機制中起關鍵作用還需進一步研究。在過去的幾十年中,越來越多的證據表明脂肪組織不僅具有能量儲存功能[16,29-30],脂聯素作為一種脂肪分泌的脂肪因子還可通過與其受體adipor1和adipor2結合,發揮調節多種心血管保護和抗糖尿病作用[31]。隨著對高血壓復雜機制的進一步了解,多項研究表明脂聯素可能是其發病的重要因素[2-3,26-27,32]。另有研究表明,即使在血壓正常的受試者中,不考慮胰島素抵抗,血壓也與血漿脂聯素水平呈負相關[11]。低脂素血癥通過損害血管內皮依賴性舒張作用而導致動脈血壓失調[33]。暗示脂聯素可以作為一種潛在的治療高血壓的方法。脂聯素作為脂肪組織的特異性細胞因子,在調節胰島素、維持血糖穩態和脂代謝中起重要作用[34]。血漿脂聯素下降與肥胖、糖尿病和冠狀動脈疾病有關[35],除此之外,高血壓患者脂聯素水平降低提示脂聯素在高血壓發病機制中起關鍵作用[36],ADIPOQ基因多態性是否通過調節脂聯素水平影響高血壓的形成尚不明確,因此需要進一步的遺傳學、其他水平的基礎實驗研究以及更大樣本量的流行病學研究;此外,基因多態性還可能通過胰島素抵抗或炎癥反應造成血管內皮損傷,從而引起高血壓疾病的產生;最后環境和基因的交互作用對疾病產生的影響也不容忽視。
綜上所述,進一步研究脂聯素的分子性質和作用途徑以及ADIPOQ基因與環境的交互作用,可以提高研究者對脂聯素相關代謝綜合征的認識,有助于制訂預防心血管疾病的策略。

