宮腔鏡冷刀技術在宮內疾病治療中的應用和優勢
周靜,陳靜,翁同芳,程芳,朱可安,潘瓊,徐大寶
(1.安徽省六安市金安區婦幼保健院 婦科,安徽 六安 237006;2.湖南省人民醫院 婦產科,湖南 長沙 410002;3.中南大學湘雅三醫院 婦產科,湖南 長沙 410013)
宮腔鏡技術是診治宮內疾病的重要手段,傳統的宮腔鏡手術以電切為主,而宮腔鏡冷刀技術是相對傳統使用電能并且產生熱能的宮腔鏡電極手術而言的。宮腔鏡冷刀技術采用非能量器械進行宮腔鏡手術,沒有電、熱損傷的風險;同時此技術采用生理鹽水膨宮,而非單極宮腔鏡電切手術所用的非電解質膨宮液(比如5%甘露醇膨宮液或者5%葡萄糖膨宮液)。因此,此技術更加安全,能夠更好地保護子宮內膜免受電、熱損傷。此技術的臨床應用,從理論上來說對女性生育力的保護有重要意義。六安市金安區婦幼保健院2016年6月引進法國HEOS宮腔鏡系統(hysteroscopy endo-operative system,HEOS),其強大的3 mm宮腔鏡非能量器械賦予了宮腔鏡冷刀技術更多的優勢。現回顧分析本院開展的HEOS宮腔鏡冷刀手術的病例資料,以評估其臨床應用效果和優勢。
1 資料與方法
1.1 一般資料
選擇2016年6月-2017年8月在本院診治的165例宮內疾病并且行HEOS宮腔鏡手術者為研究對象。患者年齡20~65歲,平均(34.86±9.28)歲。患者入院均經婦檢、實驗室檢查和B超檢查等,無手術禁忌證,無米索前列醇使用禁忌證。在患者知情同意后行HEOS宮腔鏡手術治療宮腔內病變。入組的165例患者中,40例為宮內膜息肉,7例為縱隔子宮,22例為宮腔粘連,13例為子宮黏膜下肌瘤,7例為剖宮產瘢痕部位妊娠(cesarean scar pregnancy,CSP),15例為稽留流產,50例為宮內妊娠物殘留,11例為宮內節育環嵌頓或殘留。
1.2 HEOS宮腔鏡手術
1.2.1 術前準備 每個患者術前常規行婦科彩超檢查,術前2或3 d陰道準備,軟化宮頸[術前1 d開始米索前列醇2片(0.4 mg)放入直腸內(2次/d),術前2 h米索前列醇2片放入直腸內]。
1.2.2 麻醉方法 一般采用靜脈麻醉,如果聯合腹腔鏡手術則采用氣管插管全身麻醉。
1.2.3 HEOS宮腔鏡手術方法 麻醉滿意后,患者取膀胱截石位,常規消毒鋪巾。膨宮液采用0.9%生理鹽水持續灌流,設定流速350~450 ml/min,膨宮壓力為100~150 mmHg(根據不同手術需要而調整膨宮壓力)。對于產后胎盤殘留的患者,手術開始前可宮頸注射20 u縮宮素或者10~30 ml高度稀釋垂體后葉素(30 ml生理鹽水+6 u垂體后葉素),加強子宮收縮減少出血且減少膨宮液吸收入患者體內。先用診斷性宮腔鏡檢查宮頸管及宮腔情況,以進一步明確診斷和評估HEOS宮腔鏡手術的可行性和安全性。然后探宮深,擴宮至10號;直視下置入HEOS宮腔鏡,觀察宮頸管及宮腔,并進行相應的宮腔鏡冷刀手術:①宮內膜息肉:由于HEOS宮腔鏡的3 mm雙關節彎鉗的夾持力很大,宮內膜息肉可以直接用雙關節鉗直接鉗夾摘除;②宮腔粘連:用3 mm單關節剪刀分離粘連,并參照文獻[1-2]行粘連瘢痕組織犁田分割和“撐開法”分離粘連的技術;③子宮縱隔:用HEOS 3 mm雙關節剪刀直接剪開縱隔,如果創面有明顯的動脈出血,可以用HEOS 3 mm雙極電凝電極準確電凝止血[3-4];④子宮黏膜下肌瘤(附圖):0型且直徑小于2 cm者,用3 mm雙關節剪刀直接剪斷蒂部后用卵圓鉗或者HEOS 3 mm抓鉗直接取出肌瘤,取出有困難時,可以在鏡下用3 mm剪刀把肌瘤剪成2塊后分別取出;0型且直徑大于2 cm者,先用HEOS單關節剪刀,根據肌瘤大小將之剪開為2~4塊后再分塊取出;非0型的肌瘤,則用HEOS單關節剪刀先充分打開肌瘤包膜后,適當分離肌瘤與假包膜之間的連接,再將肌瘤分塊為2~4塊,再分塊取出[5];⑤CSP:一般需要術前預處理(如用甲氨蝶呤等,因為本院沒有子宮動脈栓塞條件),對于沒有機化者,先用8號吸管在負壓0.05 mPa情況下吸除切口處的妊娠物,少量殘留的組織在宮腔鏡下直接用HEOS 3 mm雙關節鉗夾摘除;對于機化的陳舊的CSP,一般直接在HEOS宮腔鏡下用3 mm雙關節彎鉗摘除;對于妊娠物大部分深入切口內或者向宮腔外凸的CSP,一般不采用宮腔鏡手術治療;⑥稽留流產:明確妊娠物位置后,先用7-8號吸管,在負壓0.04~0.05 mPa情況下針對性的吸除妊娠物,如果有殘留,則不再反復吸宮,而是直接在宮腔鏡下用HEOS雙關節彎鉗直接摘除;⑦妊娠物殘留:對于宮腔大小適合宮腔鏡手術的妊娠物殘留者,一般直接在HEOS宮腔鏡下用雙關節彎鉗摘除妊娠物,取出妊娠物困難時,可以用HEOS抓鉗抓住妊娠機化組織取出,也可以配合卵圓鉗的鉗夾功能取出妊娠物[6];⑧宮內節育環嵌頓或殘留:由于HEOS宮腔鏡的3 mm雙關節彎鉗力量很大,一般可以直接在宮腔鏡下夾持殘留或者崁頓的節育器而取出。HEOS宮腔鏡是采用冷切割,沒有電切手術閉合創面血管的功能。因此,術中非常強調加強子宮的收縮,以減少出血并改善視野和減少膨宮液的吸收。
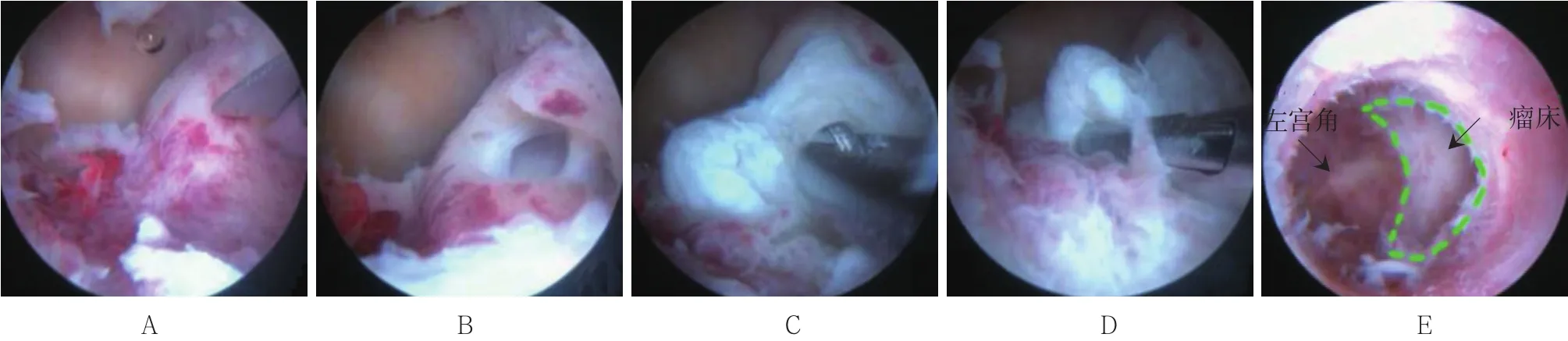
附圖 宮腔鏡黏膜下肌瘤切除術Attached fig. Submucosal myoma resection under hysteroscopic
1.3 術后處理
中度或重度宮腔粘連患者,術后予戊酸雌二醇片(補佳樂)3 mg(2次/d),促進子宮內膜生長修復[7-9];子宮內膜息肉患者,術后予月經周期后半期黃體酮治療3個周期;CSP患者,術后每周檢測血漿人絨毛膜促性腺激素(β-human chorionic gonadotropin,β-HCG),觀察陰道流血情況及術后3周超聲檢查判斷是否有妊娠物殘留;對于需要日后生育的稽留流產患者,術后常規給予雌激素治療促進子宮內膜生長;子宮縱隔患者,術后根據內膜情況個體化給予雌激素治療[3]。所有補充激素患者均簽署知情同意書,并排除禁忌證。
2 結果
本研究中,子宮黏膜下肌瘤0型7例,除了1例直徑為5 cm外,其他6例直徑均小于4 cm;另外6例子宮黏膜下肌瘤中,Ⅰ型5例,直徑均小于3 cm,Ⅱ型1例,直徑為2 cm;宮腔粘連22例,其中重度宮腔粘連9例在院外專家指導下完成,另外13例為中度宮腔粘連,分度采用美國生育協會評分系統[10];7例CSP均為妊娠物凸向宮腔且妊娠腫塊直徑小于3 cm;15例稽留流產者子宮大小均沒有大于孕2個月;50例妊娠物殘留者的子宮大小也沒有大于孕2個月;11例節育器崁頓或殘留者均沒有穿過子宮漿膜面。
宮腔鏡冷刀技術治療宮內膜息肉,平均手術時間為(19.37±9.08)min,無1例出現手術并發癥,2例術后出現月經量減少。治療縱隔子宮,平均手術時間為(19.42±6.80)min,無1例出現手術并發癥,所有患者術后月經正常來潮,無經量減少。治療宮腔粘連,平均手術時間為(25.77±11.09)min,無1例出現手術并發癥,所有患者術后月經較術前均有不同程度增多。治療子宮黏膜下肌瘤,平均手術時間為(26.85±9.15)min,無1例出現手術并發癥,1例術后出現月經量較其正常月經量減少。治療CSP,平均手術時間為(29.07±15.35)min,術中1例發生中度水中毒(經過積極治療后痊愈),所有患者術后月經正常來潮,無經量減少。治療稽留流產,平均手術時間為(21.06±7.07)min,無1例出現手術并發癥,所有患者術后月經正常來潮,無經量減少;治療宮內妊娠物殘留,平均手術時間為(24.72±10.72)min,術中1例發生子宮穿孔,2例術后出現月經量減少。治療宮內節育環嵌頓或殘留,平均手術時間為(19.18±8.31)min,無1例出現手術并發癥,1例術后出現月經量減少。所有患者中,除了1例子宮穿孔的病例(保守治療后未作特殊處理),164例HEOS宮腔鏡冷刀手術均成功實施。術者對22例宮腔粘連的患者進行了跟蹤隨訪,截止至本文投稿之日,除5例患者暫無生育要求外,余下17人中已有10名患者已成功妊娠,術后妊娠率為58.8%。
3 討論
20世紀70年代,宮腔鏡技術開始應用于婦科疾病的診治,隨著纖維光學、冷光技術、操作器械和技術設備的開發與利用以及手術技巧的日益成熟,使宮腔鏡的手術指征不斷拓寬,宮腔鏡手術作為婦科微創手術的重要組成部分,已廣泛應用于多種婦科疾病的診療中,成為診治宮內疾病的金標準。
在傳統的宮腔鏡手術治療中,電切占有舉足輕重的地位。子宮縱隔電切術、子宮內膜息肉電切術、子宮黏膜下肌瘤電切術和宮腔粘連電切術等都是極為經典的術式。宮腔鏡電切術在電切的同時也可電凝止血,術中可視下止血確切,其優勢顯而易見。但近年來,電切對子宮內膜和殘存干細胞的二次損傷以及對術后生育功能的影響,也受到越來越多的關注。電切所帶來的電損傷和熱損傷的風險是不能忽視的,電切時產生的熱量高,宮腔容積相對較小,長時間電切所產生的大量熱量如果無法及時導出,會導致宮腔內膨宮液溫度瞬時升高,對病變部位以外的正常子宮內膜造成熱損傷,增加術后宮腔粘連的風險。婦產科的特殊之處在于很多手術治療與生育息息相關,所以在治療疾病的同時必須考慮治療本身對于生育功能的影響。子宮最重要的功能就是孕育胚胎,子宮內膜就像土壤一樣,所以在治療過程中,需要盡可能地保護子宮內膜。也正是出于此種目的,近年來宮腔鏡冷刀手術得到越來越多婦科醫師的推崇和認可。
HEOS宮腔鏡是一種新型的硬型手術宮腔鏡,配有3 mm非能量硬性器械,包括硬式單關節和雙關節剪刀、抓鉗和分離鉗等。由于其3 mm器械遠比傳統的5Fr或者7Fr宮腔鏡器械粗大和強壯并且操作靈活,具有手術時間短、器械作用效率高、沒有電熱損傷風險、采用生理鹽水膨宮比非電解質膨宮液更加安全和具有拖拉的功能等。另外,HEOS宮腔鏡為一體鏡,且鏡體較粗而視野更大更清晰;加上其強大且容易操作的冷器械,使得宮腔鏡手術難度和風險降低。由于本院此次是首次引進宮腔鏡技術,術者為長期從事婦產科工作的臨床人員,經過短期的相關技術培訓后即開展了上述宮腔鏡手術。考慮到術者的宮腔鏡基礎和經驗有限,所以在開展宮腔鏡手術之初,沒有開展宮腔鏡電切手術;另外,為了減少宮腔鏡手術的難度和風險,在選擇病例時進行了考慮。本科應用HEOS宮腔鏡冷刀技術治療165例宮腔內病變病例,除了1例早期病例出現了子宮穿孔和1例CSP術中出現中度水中毒者,無重大手術并發癥,且一次性手術成功率高。從手術時間分析,HEOS宮腔鏡手術時間比較短。從術后月經量是否少于正常月經量間接分析,HEOS宮腔鏡手術對子宮內膜的損傷較小,本研究僅6例出現術后月經量較正常月經量減少。當然,術后子宮內膜的損傷情況評估的金標準是宮腔鏡檢查,但是考慮到宮腔鏡檢查的有創性,本研究采用了術后月經量與患者正常月經量比較的方法。從165例宮腔鏡手術的病種看,囊括了大部分傳統宮腔鏡電切手術的病種,間接說明HEOS宮腔鏡手術可以替代大部分傳統的宮腔鏡電切手術。值得一提的是,本研究的宮腔鏡術者是宮腔鏡技術相對不高的婦產科醫生,雖然使手術患者在適應證選擇上有了一定的限制,但是,從本研究中比較高的一次性手術成功率、較低的并發癥和較短的手術時間等分析說明,HEOS宮腔鏡冷刀技術可能降低了宮腔鏡手術的難度。
綜上所述,HEOS宮腔鏡冷刀技術在臨床上有重要的應用價值,值得日后大樣本多中心的隨機對照研究,進一步證實其臨床應用價值和優勢。

