血液病粒細胞缺乏患者合并產超廣譜β內酰胺酶腸桿菌血流感染的臨床特征分析▲
劉倍材 韋杰敏 孫起翔 石敏娟 李橋川
( 廣西醫科大學第一附屬醫院1 血液內科,2 呼吸內科,南寧市 530021,電子郵箱:735094092@qq.com;3 廣西醫科大學公共衛生學院,南寧市 530021)
粒細胞缺乏患者免疫力低下,容易發生細菌性血流感染[1]。國內研究結果顯示,腸桿菌所致血流感染占細菌性血流感染的34.66%[2]。腸桿菌中的產超廣譜β內酰胺酶(extended-spectrum beta-lactamases,ESBLs)菌株可水解β內酰胺環,從而使β內酰胺類抗菌藥物失去抗菌活性。國外研究表明,產ESBLs腸桿菌檢出率逐年增加[3],給臨床治療帶來嚴峻挑戰。本研究回顧性分析192例粒細胞缺乏合并腸桿菌血流感染患者的臨床資料及藥敏試驗結果,為臨床合理使用抗生素治療提供參考。
1 資料與方法
1.1 臨床資料 納入2012年6月至2018年12月在廣西醫科大學第一附屬醫院血液科確診為院內腸桿菌血流感染的192例患者。納入標準:抽血培養時患者處于粒細胞缺乏狀態,即外周血中性粒細胞絕對計數<0.5×109/L或預計48 h后中性粒細胞絕對計數<0.5×109/L;血流感染的診斷符合《醫院感染診斷標準(試行)》[4]中的相關標準。排除標準:未進行ESBLs檢測者;血培養結果陽性未經治療而放棄治療出院者。其中男性122例、女性70例,中位年齡33(1~67)歲;原發疾病包括急性髓細胞白血病75例,急性淋巴細胞白血病74例,淋巴瘤15例,再生障礙性貧血9例,地中海貧血6例,慢性粒細胞白血病5例,混合細胞白血病3例,嗜血細胞綜合征2例,多發性骨髓瘤2例,骨髓增生異常綜合征1例。根據ESBLs檢測結果,將患者分為產ESBLs組98例和非產ESBLs組94例。
1.2 菌株培養與鑒定方法 按《全國臨床檢驗操作規程》[5],在患者寒戰時或發熱初進行兩個不同部位靜脈采血各1~20 mL(成人15~20 mL,兒童根據年齡體重進行適量采血),進行細菌分離培養,采用法國生物梅里埃公司的ATB Expression細菌鑒定系統及配套的ID32GN鑒定試劑卡(批號:2410803203)確定菌株,通過表型確證試驗確定產ESBLs菌株,采用K-B紙片擴散法進行藥敏試驗。只取第1次血培養結果進行統計分析。
1.3 資料收集 包括性別、年齡、血流感染發生前1個月內第三代頭孢菌素及喹諾酮類藥物暴露情況、入院至血流感染發生的間隔時間、血流感染發生前2周使用免疫抑制劑、血流感染當天白蛋白水平、血流感染后30 d內因感染導致死亡情況。
1.4 統計學分析 采用SPSS 24.0軟件進行統計分析。非正態分布的計量資料以[M(P25,P75)]表示,組間比較采用秩和檢驗;計數資料以例數(百分比)表示,組間比較采用χ2檢驗。將單因素分析中P<0.1的指標納入多因素Logistic回歸模型進行危險因素分析。以P<0.05為差異有統計學意義。
2 結 果
2.1 192例血液病粒細胞缺乏患者合并血流感染病原體及藥敏試驗結果 192例患者中,檢出大腸埃希菌114株,其中產ESBLs大腸埃希菌68株(59.6%);檢出克雷伯菌屬78株,產ESBLs克雷伯菌屬30株(38.5%)。產ESBLs腸桿菌對哌拉西林他唑巴坦、美羅培南、亞胺培南、替加環素的耐藥率均較低,分別為5.1%、2.9%、1.0%和0,見表1。
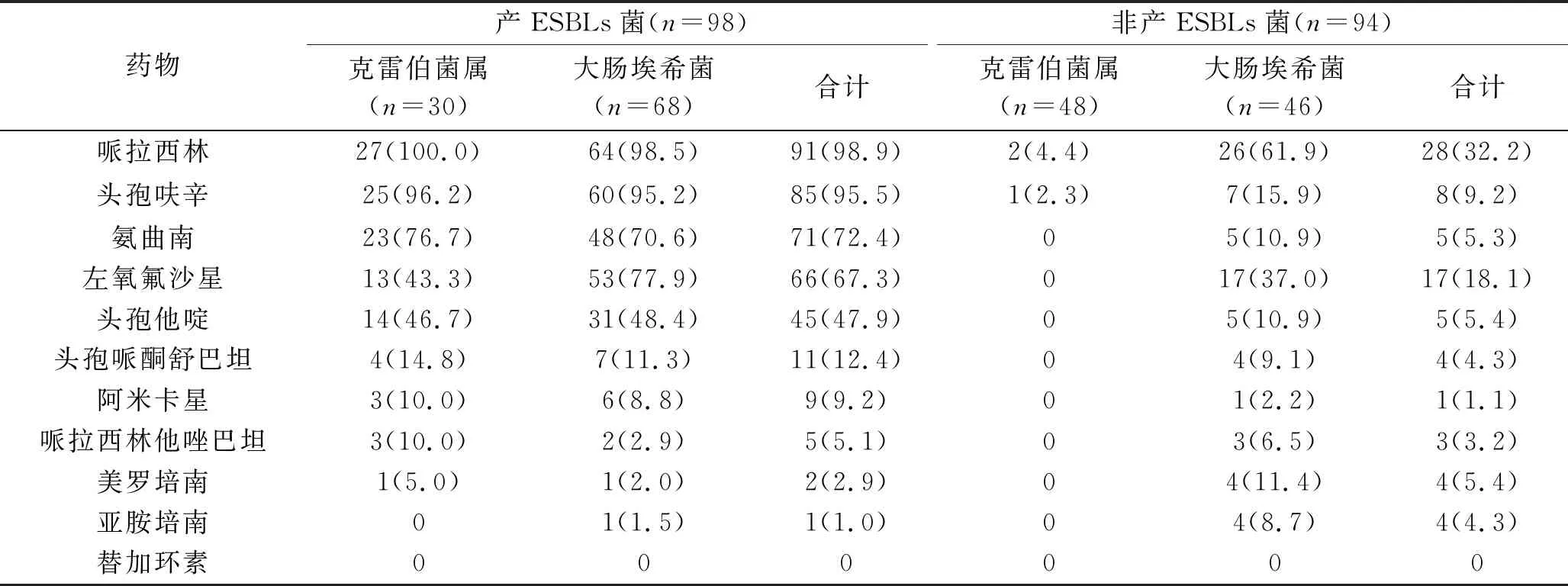
表1 產ESBLs腸桿菌與非產ESBLs腸桿菌對主要抗菌藥物的耐藥情況比較[n(%)]
注:產ESBLs菌中,行哌拉西林、頭孢呋辛、頭孢哌酮舒巴坦、美羅培南藥敏試驗的克雷伯菌屬分別有27株、26株、27株、20株;行哌拉西林、頭孢呋辛、頭孢他啶、頭孢哌酮舒巴坦、美羅培南敏試驗的大腸埃希菌分別有65株、63株、64株、62株、50株;行其他藥敏試驗的克雷伯菌屬均為30株、大腸埃希菌均為68株。非產ESBLs菌中,行哌拉西林、頭孢呋辛、美羅培南藥敏試驗的克雷伯菌屬分別有45株、43、39株;行哌拉西林、頭孢呋辛、頭孢哌酮舒巴坦、阿米卡星、美羅培南藥敏試驗的大腸埃希菌分別有42株、44株、44株、45株、35株;行其他藥敏試驗的克雷伯菌屬均為48株,大腸埃希菌均為46株。
2.2 192例血液病粒細胞缺乏合并腸桿菌血流感染患者30 d內病死率 192例患者中,30 d內死亡31例(16.1%),其中產ESBLs組23例(23.5%),非產ESBLs組8例(8.5%)。產ESBLs組30 d內病死率高于非產ESBLs組(χ2=7.930,P=0.005)。
2.3 血液病粒細胞缺乏患者合并產ESBLs腸桿菌血流感染的危險因素 單因素分析結果顯示,產ESBLs組1個月內第三代頭孢菌素及喹諾酮暴露、入院至血流感染發生的時間間隔大于15 d、近2周使用免疫抑制劑、白蛋白水平小于35 g/L的患者比例均高于非產ESBLs組(均P<0.05),見表2。以上述P<0.1的指標作為自變量,以病原菌是否為產ESBLs腸桿菌為因變量,進行多因素Logistic回歸分析(變量賦值情況見表3),結果顯示,1個月內第三代頭孢菌素暴露是血液病粒細胞缺乏患者合并產ESBLs腸桿菌血流感染的獨立危險因素(P<0.05)。
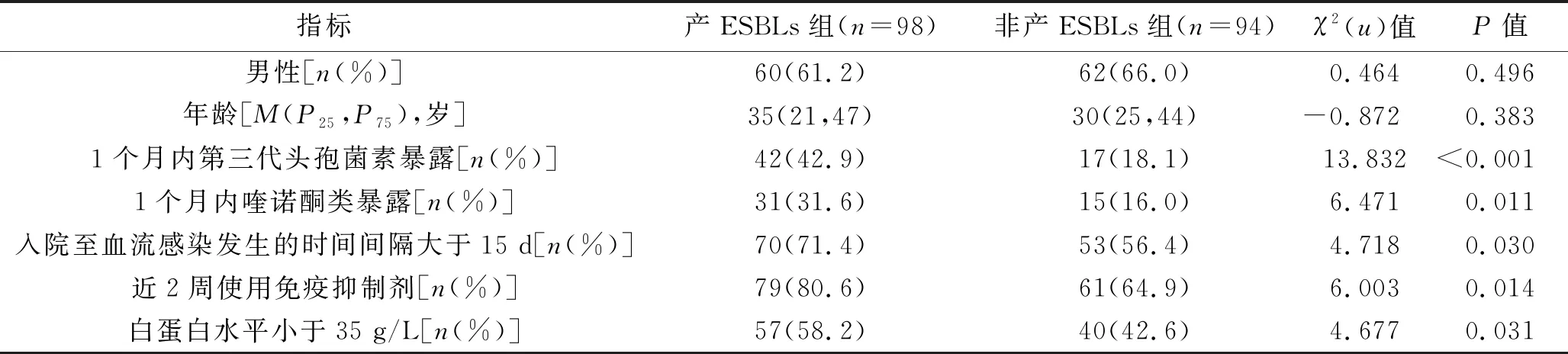
表2 產ESBLs組與非產ESBLs組的臨床特征比較

表3 變量賦值情況
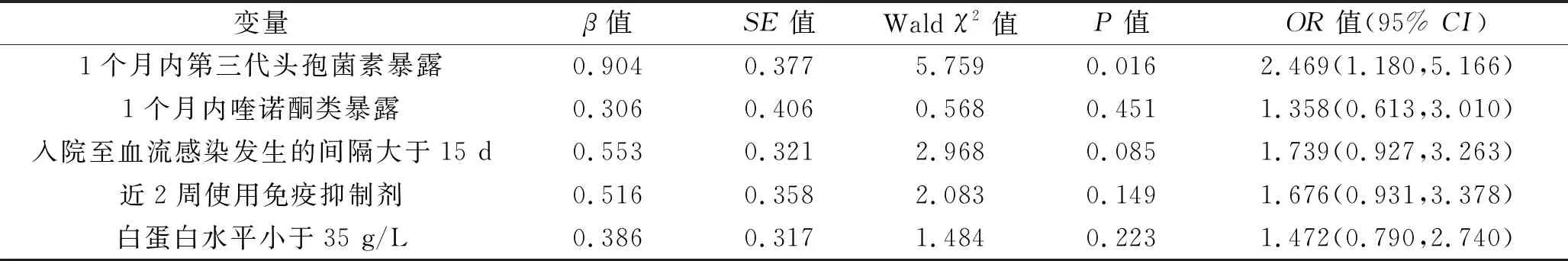
表4 多因素Logistic回歸分析結果
3 討 論
粒細胞缺乏患者易發生細菌性血流感染,危及生命[6]。2016年中國細菌耐藥監測網(China Antimicrobial Surveillance Network,CHINET)的監測數據顯示,大腸埃希菌及克雷伯菌屬是常見的產ESBLs腸桿菌,其ESBLs陽性檢出率分別為45.2% 和25.2%[7]。本研究中,大腸埃希菌及克雷伯菌屬ESBLs陽性檢出率分別為59.6%和38.5%,均高于2016年中國CHINET的監測結果,這可能與研究人群基礎疾病不同、臨床上血液病粒細胞缺乏患者預防性使用抗菌藥物率高等因素有關(本研究數據僅來源于三級醫院血液科病房粒細胞缺乏患者,而CHINET納入人群為入試醫院所有臨床感染患者)。此外,張曉琳等[8]通過薈萃分析發現,產EBSLs腸桿菌血流感染患者病死率較非產ESBLs腸桿菌血流感染患者病死率高近2倍。本研究結果也顯示,產ESBLs組患者30 d內病死率達23.5%,高于非產ESBLs組(P<0.05)。因此,對于粒細胞缺乏并發熱的患者,臨床醫師應警惕產ESBLs腸桿菌所致感染的發生并及時進行干預,以降低病死率。
相關研究結果顯示,發生血流感染的住院患者,致病菌為產ESBLs腸桿菌的獨立危險因素有長時間留置中心靜脈導管、留置胃管、近期抗菌素或頭孢菌素暴露、存在尿路感染等[9-10]。本研究結果顯示,1個月內第三代頭孢菌素暴露是血液病粒細胞缺乏患者合并產ESBLs腸桿菌血流感染的獨立危險因素(P<0.05)。第三代頭孢菌素的使用會誘導細菌產ESBLs[11]。因此,1個月內有第三代頭孢菌素暴露史的粒細胞缺乏伴發熱患者應考慮產ESBLs腸桿菌感染可能。
發熱往往是粒細胞缺乏伴感染患者的唯一臨床表現,臨床醫師對粒細胞缺乏伴發熱患者應盡早經驗性應用抗菌藥物治療[12]。本研究體外藥敏結果顯示,產ESBLs腸桿菌對哌拉西林他唑巴坦、美羅培南、亞胺培南及替加環素的耐藥率均較低,分別為5.1%、2.9%、1.0%和0,因此,對于產ESBLs腸桿菌所致血流感染的粒細胞缺乏患者,可以考慮使用上述抗菌藥物。美國感染病學會《2010年粒細胞缺乏腫瘤患者抗菌藥物使用指南》[13]指出,對于粒細胞缺乏伴發熱且預期粒細胞缺乏時間>7 d的患者,推薦盡早使用哌拉西林他唑巴坦或碳青霉烯類抗菌藥物治療。《中國中性粒細胞缺乏伴發熱患者抗菌臨床應用指南(2016年版)》[12]建議,對于存在感染產ESBLs菌危險因素(如先前存在ESBLs定植菌、近期第三代頭孢菌素暴露史等)或者高度懷疑感染了產ESBLs菌的患者,應盡早首選碳青霉烯類經驗性治療。但是,隨著碳青霉烯類抗菌藥物的廣泛使用,耐碳青霉烯類腸桿菌檢出率逐年升高[14],對于感染耐碳青霉烯類腸桿菌的患者,推薦使用替加環素治療[12]。
綜上所述,血液病粒細胞缺乏患者合并產ESBLs腸桿菌血流感染時病死率高;第三代頭孢菌素暴露會增加血液病粒細胞缺乏患者合并產ESBLs腸桿菌血流感染的風險,臨床醫師應對血液病粒細胞缺乏伴發熱患者盡早經驗性使用可覆蓋產ESBLs腸桿菌的抗菌素治療。

