土槿乙酸C-18醇酯衍生物的合成及其體外免疫抑制活性研究
曾憲杰,張 猜,陳守強,陳 虹
(1.天津醫科大學藥學院,天津300070;2.武警后勤學院軍事藥學教研室,天津300309)
土槿皮(pseudolarixkaempferi,PAB)是我國南方特有松科植物金錢松(Pseudolarixamabilis)的根皮或近根部樹皮,最早見于清代趙學敏所著《本草綱目拾遺》,性辛、溫、有毒;歸肺、脾經;功能殺蟲止癢,用于疥癬瘙癢[1-2]。土槿乙酸(pseudolaric acid B,PAB,圖1)為土槿皮的主要活性成分[3],其基本母核是特殊的薁類結構,并具有內酯環和共軛雙烯酸側鏈的結構,這類結構在天然產物中是很少見的。我們課題組研究顯示土槿乙酸能顯著改善遲發型超敏反應小鼠的耳腫脹并呈劑量依賴,其作用機制通過抑制與MAPK與PPAR信號通路相關的p38MAPK、ATF-2、MK2、HSP27 及 TNF-α 活性[4-5]。土槿乙酸還具有抗腫瘤[6]、抗白血病[7]、抗真菌[8]、抗血管生成等作用。PAB是很好的免疫抑制活性先導化合物。為尋找高效、低毒,具有良好水溶性的免疫抑制劑,對土槿乙酸進行進一步的結構改造。
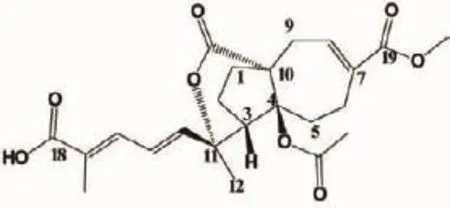
圖1 土槿乙酸結構Fig 1 Pseudolaric acid B
1 材料與方法
1.1 儀器和試劑 Varian Mercury Vx400核磁共振光譜儀;Agilent 6210 LC-TOF質譜測定儀;XT顯微熔點儀(溫度未校正);DHG-9000A電熱恒溫鼓風干燥箱;ZK-30BS真空干燥箱;BüCHI R-124旋轉蒸發儀。薄層色譜和柱色譜所用硅膠(青島海洋化工公司);土槿乙酸系實驗室自提取提純得到,純度大于95%;無水二氯甲烷用五氧化二磷回流4 h后蒸出備用;無水四氫呋喃以二苯甲酮做檢測試劑,用金屬鈉回流制得,當溶液變為深藍色后蒸出備用;無水甲醇用 CaO(250 g/L)回流 6 h,過夜,加至3A型分子篩中貯存備用。除特殊說明外,本實驗所用試劑均從北京百靈威試劑公司購得。
1.2 合成方法 土槿乙酸C18羧酸的還原:在25mL三頸瓶中依次加入土槿乙酸(PB,0.432g,1 mmol),10 mL無水二氯甲烷,移至冰浴,冷卻反應液溫度至0℃。在此溫度下,將過量草酰氯(0.94 mL,10 mmol)用恒壓滴液漏斗緩慢滴加至反應瓶中,滴加完畢,移至室溫攪拌反應2 h。減壓蒸餾除去過量草酰氯,得泡沫狀固體粗產物。將10 mL無水 四氫呋喃(THF)迅速加入反應瓶中,移至冷阱冷卻反應液溫度至-40℃,在N2保護下,分兩次緩慢加入LiAlH[OC(CH3)3]3(3.6 mL,4 mmol),滴加完畢,室溫攪拌反應。TLC檢測至反應完全。將反應移至冰浴,15 min后,加無水乙醇20mL淬滅還原劑。然后用10%HCl洗滌,20mL乙酸乙酯萃取3次,合并有機層,加入無水Na2SO4脫水,過濾,減壓蒸餾得到粗品,粗品經柱色譜(二氯甲烷:乙酸乙酯)純化得白色固體粉末0.338 g,收率81%。
土槿乙酸C18酯衍生物的合成:在15 mL干燥的反應瓶中依次加入土槿乙醇(PB-OH,0.062 g 0.15 mmol),10 mL干燥 DCM 和小分子酸類(0.15 mmol),冰浴下加入HOBt(0.18 mmol),EDCI(0.18 mmol),2滴三乙胺,15 min后移至室溫反應,TLC點板檢測。反應完畢,分別加入15 mL 10%HCI,飽和NaHCO3,蒸餾水,飽和NaCl洗滌,萃取,取二氯甲烷層,加入無水Na2SO4脫水,過濾,濾液回收,減壓蒸餾溶劑得到粗品,粗品以不同比例的二氯甲烷和乙酸乙酯為流動相,經柱色譜法純化得產品。以此路線共合成10個化合物,B1-B10。化合物B1-B10合成路線及所引入基團見圖2。
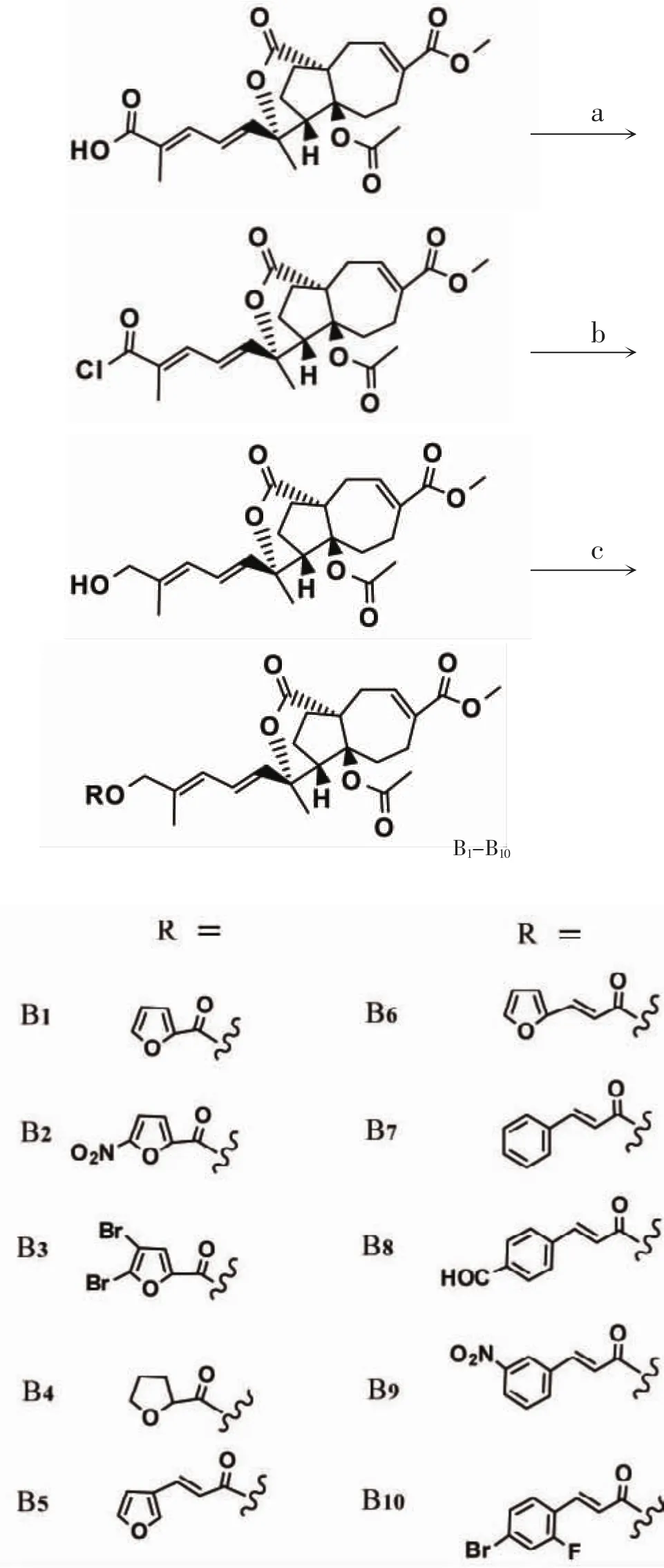
圖2 土槿乙酸衍生物B1-B10的合成路線Fig 2 The synthesis of pseudolaric acid B derivatives B1-B10 Conditions and reagents:(a)anhydrous DCM,oxalyl chloride,0℃-rt;(b)anhydrousTHF,LiAlH[OC(CH3)3]3,N2,-40℃;(c)anhydrousDCM,R-COOH,HOBt,EDCI,0℃-rt.
1.3 藥理實驗部分
1.3.1 MTT法檢測目標化合物對小鼠脾淋巴細胞的毒性作用[9]
(1)在超凈臺中取昆明小鼠脾臟,并按上述方法制備單細胞懸浮液。
(2)將土槿乙酸衍生物和陽性藥霉酚酸酯分別溶于 DMSO,用培養液稀釋至 10 μmol/L、1 μmol/L、0.1 μmol/L、0.01 μmol/L, 其中 DMSO 含量均低于0.1%,空白培養基同樣處理。
(3)于96孔板中以每孔 100 μL(約 1×105個細胞)進行培養,同時加入土槿乙酸衍生物和陽性藥霉酚酸酯,每種藥物設置4個濃度(10μmol/L、1μmol/L、0.1 μmol/L、0.01 μmol/L),每個濃度設置 3 個復孔,并以RPMI1640培養液為調零孔。向陰性對照組中加入與給藥組相同體積的溶劑。置于37℃,5%二氧化碳溫箱中。
(4)48 h后每孔加 20 μL 5mg/mL MTT 溶液(PBS配制)。37℃條件繼續孵育4 h,吸取上清液80 μL,每孔加入100 μL三聯液用于溶解甲簪顆粒,輕度振蕩充分溶解。
(5)在波長570 nm下,用酶標儀測定光密度值(OD),以溶劑處理的細胞為陰性對照組,用以下公式計算藥物對細胞的抑制率,并計算IC50:抑制率=(陰性對照組OD值-加藥組OD值)/(陰性對照組OD值-空白對照組OD值)×100%。
1.3.2 MTT法檢測目標化合物對小鼠T、B淋巴細胞增殖的抑制作用
(1)在超凈臺中取昆明小鼠脾臟,制備淋巴細胞懸液,調整細胞濃度為1×106-5×106/mL,加入ConA或LPS至終濃度為5 μg/mL。
(2)以每孔100 μL培養于96孔板中,同時加入土槿乙酸衍生物與陽性藥霉酚酸酯100 μL,每個藥物設置 4 個濃度(10 μmol/L、1 μmol/L、0.1 μmol/L、0.01μmol/L),每個濃度設置 3個復孔,并以RPMI1640培養液為調零孔。向陰性對照組中加入與給藥組相同體積的溶劑,置于37℃,5%CO2溫箱中。
(3)48 h后每孔加 20 μL 5 mg/mL MTT 溶液(PBS配制)。37℃繼續孵育4 h,吸取上清液80 μL,每孔加入三聯液100 μL溶解甲簪顆粒,輕度振蕩溶解。
(4)在波長570 nm下,用酶標儀測定光密度值(OD),以溶劑處理的細胞為陰性對照組,以RPMI1640培養液為空白對照組,用以下公式計算抑制率:抑制率=(陰性對照組OD值-加藥組OD值)/(陰性對照組OD值-空白對照組OD值)×100%。
2 結果
2.1本文共合成了10個目標化合物,均為未見文獻報道的新化合物,經1H-NMR、13C-NMR和HRESI-MS確證了這些化合物的結構。這些化合物的理化數據如下。
B1:乳白色粉末,66 mg,86%yield,1H NMR(400 MHz,CDCl3):δ 7.59(dd,J=1.7,0.8 Hz,1H,H-5’),7.24-7.16(m,2H,H-8,H-4’),6.52(dd,J=3.5,1.7 Hz,1H,H-6’),6.46(dd,J=15.1,11.0 Hz,1H,H-14),6.12(d,J=11.0 Hz,1H,H-15),5.57(d,J=15.1 Hz,1H,H-13),4.75 (s,2H,H-18),3.72 (s,3H,-OCH3),3.26(m,1H,H-3),3.07(dd,J=13.9,6.0 Hz,1H,H-5a),2.89(dd,J=15.6,6.3 Hz,1H,H-6a),2.75(dd,J=15.0,8.8 Hz,1H,H-9a),2.61 (ddd,J=15.1,3.9,1.7 Hz,1H,H-9b),2.13(s,3H,-OCOCH3),2.05(s,1H,H-6b),1.86(s,3H,CH3-17),1.81-1.66(m,5H,H-1,2,5),1.57(s,3H,CH3-12).
13C NMR (101 MHz,CDCl3):δ 173.1,169.4,168.1,158.5,146.5,144.5,141.8,137.8,134.4,133.1,126.9,121.7,118.1,111.9,90.3,83.8,69.7,55.2,52.0,49.5,33.3,30.7,28.8,27.8,24.3,21.8,20.2,14.7.
HR-ESI-MS m/z:535.1918(M+Na)+, 理論值:535.1944[M+Na]+
B2:乳白色粉末,74 mg,89%yield,1H NMR(400 MHz,CDCl3):δ 7.36(d,J=3.7 Hz,1H,H-4’),7.31(d,J=3.8 Hz,1H,H-3’),7.24-7.17(m,1H,H-8),6.45(dd,J=15.1,11.0 Hz,1H,H-14),6.14(d,J=11.0 Hz,1H,H-14),5.60 (d,J=15.1 Hz,1H,H-13),4.81(s,2H,H-18),3.72(s,3H,-OCH3),3.27(m,1H,H-3),3.07 (dd,J=14.1,6.1 Hz,1H,H-5a),2.89 (dd,J=15.5,6.3 Hz,1H,H-6a),2.75 (dd,J=15.0,8.8 Hz,1H,H-9a),2.61(dd,J=15.0,2.4 Hz,1H,H-9b),2.13(s,3H,-OCOCH3),2.05 (s,1H,H-6b),1.87 (s,3H,CH3-17),1.82-1.62(m,5H,H-1,2,5),1.58(s,3H,CH3-12).
13C NMR (101 MHz,CDCl3):δ 173.1,173.0,169.4,168.1,156.8,144.7,141.8,138.5,134.5,132.1,128.0,121.5,119.0,111.5,90.3,83.8,71.1,55.2,52.0,49.5,33.4,30.7,28.8,27.8,24.3,21.8,20.2,14.7.
HR-ESI-MS m/z:580.1801(M+Na)+,理論值:580.1795[M+Na]+
B3:乳白色粉末,87 mg,91%yield,1H NMR(400 MHz,CDCl3):δ 7.20(s,2H,H-8,3’),6.44(dd,J=15.1,11.0 Hz,1H,H-14),6.10 (d,J=10.9 Hz,1H,H-15),5.58(d,J=15.1 Hz,1H,H-13),4.74(s,2H,H-18),3.72 (s,3H,-OCH3),3.26 (d,J=5.8 Hz,1H,H-3),3.07 (dd,J=14.2,6.3 Hz,1H,H-5a),2.89 (dd,J=15.5,6.2 Hz,1H,H-6a),2.75 (dd,J=15.0,8.8 Hz,1H,H-9a),2.61(dd,J=15.1,3.4 Hz,1H,H-9b),2.12(s,3H,-OCOCH3),2.04 (s,1H,H-6b),1.84 (s,3H,CH3-17),1.80-1.68(m,5H),1.57(s,3H,CH3-12).
13C NMR (101 MHz,CDCl3):δ 173.1,169.4,168.1,156.7,145.9,141.8,138.2,134.5,132.6,128.6,127.4,122.0,121.6,103.8,90.3,83.8,70.3,55.2,52.0,49.6,33.4,30.7,28.8,27.8,24.3,21.8,20.2,14.7.
HR-ESI-MS m/z:669.1309(M+H)+,理論值:669.0257[M+H]+
B4:乳白色粉末,217 mg ,87%yield,1HNMR(400 MHz,CDCl3):δ 7.20(m,1H,H-8),6.43 (dd,J=15.1,11.0 Hz,1H,H-14),6.05(d,J=10.8 Hz,1H,H-15),5.54(d,J=15.1 Hz,1H,H-13),5.30(s,1H,H-2’),4.59(s,2H,H-5’),4.49(dd,J=8.3,5.1 Hz,1H,H-3a’),4.03(dd,J=14.4,7.2 Hz,1H,H-4a’),3.93(dd,J=13.8,7.3 Hz,1H,H-4b’),3.72 (s,3H,-OCH3),3.26 (d,J=5.8 Hz,1H,H-3),3.07 (dd,J=14.2,6.3 Hz,1H,H-5a),2.89 (dd,J=15.5,6.0 Hz,1H,H-6a),2.75(dd,J=15.0,8.8 Hz,1H,H-9a),2.61(dd,J=15.1,3.4 Hz,1H,H-9b),2.26(m,1H,H-3b’),2.12(s,3H,-OCOCH3),2.06-1.83(m,6H,H-6b,1,2,5),1.79(s,3H,CH3-17),1.57(s,3H,CH3-12).
13C NMR (101 MHz,CDCl3)δ 173.2,173.1,169.4,168.1,141.8,137.8,134.5,133.1,126.8,121.7,90.3,83.8,69.8,69.7,69.4,55.2,52.0,49.6,33.3,30.7,30.2,28.8,27.8,25.3,24.3,21.8,20.2,14.6.
HR-ESI-MSm/z:539.2263(M+H)+,理論值:539.2257[M+H]+
B5:乳白色粉末,67 mg,83%yield,1H NMR(400 MHz,CDCl3):δ 7.66(s,1H,H-5’),7.60(d,J=15.8Hz,1H,H-3’),7.44 (d,J=1.3 Hz,1H,H-7’),7.21(m,1H,H-8),6.59(d,J=1.9 Hz,1H,H-8’),6.45(dd,J=15.1,11.0 Hz,1H,H-14),6.19(d,J=15.6 Hz,1H,H-2’),6.08(d,J=11.0 Hz,1H,H-15),5.55(d,J=15.1 Hz,1H,H-13),4.64 (s,2H,H-18),3.72 (s,3H,-OCH3),3.25(m,1H,H-3),3.07(dd,J=14.3,5.6 Hz,1H,H-5a),2.89(dd,J=15.6,6.3 Hz,1H,H-6a),2.75(dd,J=15.0,8.8 Hz,1H,H-9a),2.60 (ddd,J=15.0,4.0,1.7 Hz,1H,H-9b),2.12(s,3H,-COCH3),1.88(m,1H,H-6),1.84(s,3H,CH3-17),1.81-1.68(m,5H,H-1,2,5),1.57(s,3H,CH3-12).
13C NMR (101 MHz,CDCl3):δ 173.2,169.4,168.1,166.7,144.6,144.5,141.8,137.6,135.1,134.4,133.7,126.3,122.6,121.8,117.6,107.4,90.3,83.9,69.3,55.2,52.0,49.6,33.3,30.7,28.8,27.8,24.3,21.8,20.2,14.7.
HR-ESI-MS m/z:561.2070(M+Na)+,理論值:561.2101[M+Na]+
B6:乳白色粉末,73 mg90%yield,1H NMR(400 MHz,CDCl3):δ 7.49(d,J=1.4 Hz,1H,H-6’),7.45(d,J=15.7 Hz,1H,H-3’),7.24-7.18(m,1H,H-8),6.62(d,J=3.4 Hz,1H,H-8’),6.49-6.46(dt,J=7.0,2.8 Hz,2H,H-14,H-7’),6.35(d,J=15.7 Hz,1H,H-2’),6.08(d,J=11.0 Hz,1H,H-15),5.55(d,J=15.1 Hz,1H,H-13),4.64(s,2H,H-18),3.72(s,3H,-OCH3),3.25(m,1H,H-3),3.07(dd,J=14.3,5.6 Hz,1H,H-5a),2.89(dd,J=15.6,6.3 Hz,1H,H-6a),2.75(dd,J=15.0,8.8 Hz,1H,H-9a),2.61 (ddd,J=15.0,4.0,1.7 Hz,1H,H-9b),2.12(s,3H,-COCH3),1.88(m,1H,H-6b),1.83(s,3H,CH3-17),1.80-1.68(m,5H,H-1,2,5),1.57(s,3H,CH3-12).
13C NMR (101 MHz,CDCl3):δ 173.2,169.4,168.10,166.8,150.9,144.9,141.9,137.5,134.4,133.7,131.4,126.2,121.8,115.5,115.0,112.3,90.3,83.9,69.3,55.2,52.0,49.6,33.3,30.7,28.8,27.8,24.3,21.8,20.2,14.7.
HR-ESI-MS m/z:561.2057(M+Na)+,理論值:561.2101[M+Na]+
B7:淡黃色粉末,72 mg,88%yield,1H NMR(400 MHz,CDCl3):δ 7.72(d,J=16.0 Hz,1H,H-3’),7.58-7.49(m,2H,H-5’,9’),7.45-7.35(m,3H,H-6’,7’,8’),7.24-7.17(m,1H,H-8),6.53-6.40(m,2H,H-14,2’),6.10(d,J=11.0 Hz,1H,H-15),5.56(d,J=15.1 Hz,1H,H-13),4.66 (s,2H,H-18),3.72 (s,3H,-OCH3),3.26(m,1H,H-3),3.07(dd,J=14.3,5.6 Hz,1H,H-5a),2.89 (dd,J=15.6,6.3 Hz,1H,6a),2.75(dd,J=15.0,8.8 Hz,1H,9a),2.61(ddd,J=15.1,3.9,1.7 Hz,1H,9b),2.12(s,3H,-OCOCH3),1.89(m,1H,6b),1.85(s,3H,CH3-17),1.82-1.59(m,5H),1.58(s,3H,CH3-12).
13C NMR (101 MHz,CDCl3):δ 173.1,169.4,168.1,166.7,145.2,141.8,137.6,134.4,134.3,133.7,130.4,128.9,128.1,126.4,121.8,117.8,90.3,83.9,69.4,55.2,52.0,49.6,33.3,30.7,29.7,28.8,27.8,24.3,21.8,20.2,14.8.
HR-ESI-MS m/z:571.2278(M+Na)+,理論值:571.2308[M+Na]+
B8:淡黃色粉末,67 mg,78%yield,1H NMR(400 MHz,CDCl3):δ 10.04(s,1H,CHO-7’),7.91(d,J=8.1 Hz,2H,H-6’,8’),7.74 (d,J=16.0 Hz,1H,H-3’),7.69 (d,J=8.1 Hz,2H,H-5’,9’),7.25-7.17(m,1H,H-8),6.59(d,J=16.0 Hz,1H,H-2’),6.47(dd,J=15.1,11.0 Hz,1H,H-14),6.11 (d,J=11.0 Hz,1H,H-15),5.57(d,J=15.1 Hz,1H,H-13),4.68(s,2H,H-18),3.72 (s,3H,-OCH3),3.26 (d,J=6.0 Hz,1H,H-3),3.07(dd,J=14.1,6.1 Hz,1H,H-5a),2.89(dd,J=15.5,6.2 Hz,1H,H-6a),2.75(dd,J=15.0,8.8 Hz,1H,H-9a),2.61(dd,J=15.0,2.5 Hz,1H,H-9b),2.13(s,3H,-OCOCH3),1.88 (s,1H,H-6b),1.86 (s,3H,CH3-17),1.82-1.67(m,5H,H-1,2,5),1.58(s,3H,CH3-12).
13C NMR (101 MHz,CDCl3):δ 191.4,173.1,169.4,168.1,166.1,143.4,141.8,140.0,137.8,137.3,134.5,133.4,130.2,128.6,126.7,121.8,121.1,90.3,83.8,69.8,55.2,52.0,49.6,33.4,30.7,28.8,27.8,24.3,21.8,20.2,14.7.
HR-ESI-MS m/z:599.2277(M+Na)+,理論值:599.2257[M+Na]+
B9:淡黃色粉末,75 mg,85%yield,1H NMR(400 MHz,CDCl3):δ 8.39 (t,J=1.8 Hz,1H,H-5’),8.30-8.19(m,1H,H-7’),7.84(d,J=7.8 Hz,1H,H-9’),7.74 (d,J=16.0 Hz,1H,H-3’),7.60 (t,J=8.0 Hz,1H,H-8’),7.22-7.20(m,1H,H-8),6.60(d,J=16.0 Hz,1H,H-2’),6.47(dd,J=15.1,11.0 Hz,1H,H-14),6.11(d,J=11.0 Hz,1H,H-15),5.58(d,J=15.1 Hz,1H,H-13),4.69(s,2H,H-18),3.72(s,3H,-OCH3),3.27 (d,J=5.9 Hz,1H,H-3),3.07 (dd,J=14.0,6.0 Hz,1H,H-5a),2.89(dd,J=15.5,6.3 Hz,1H,H-6a),2.75 (dd,J=15.0,8.7 Hz,2H,H-9a),2.61 ((dd,J=15.0,2.5 Hz,1H,H-9b),2.13(s,3H,-OCOCH3),2.05(s,1H,H-6b),1.86 (s,3H,CH3-17),1.82-1.62(m,5H,H-1,2,5),1.58(s,3H,CH3-12).
13C NMR (101 MHz,CDCl3):δ 173.1,169.4,168.1,165.8,148.7,142.2,141.8,137.9,136.1,134.5,133.7,133.3,130.0,126.7,124.6,122.4,121.7,121.1,90.3,83.8,69.9,55.2,52.0,49.6,33.3,30.7,28.8,27.8,24.3,21.8,20.2,14.7.
HR-ESI-MS m/z:616.2170(M+Na)+,理論值:616.2159[M+Na]+
B10:淡黃色粉末,86 mg,89%yield,1H NMR(400 MHz,CDCl3):δ 8.02 (d,J=15.9 Hz,1H,H-3’),7.61(dd,J=8.7,5.9 Hz,1H,H-6’),7.37(dd,J=8.1,2.2 Hz,1H,H-8’),7.21(m,1H,H-8),7.07(td,J=8.4,2.3 Hz,1H,H-9’),6.46 (dd,J=15.1,11.0 Hz,1H,H-14),6.36(d,J=15.9 Hz,1H,H-2’),6.10(d,J=11.0 Hz,1H,H-15),5.56 (d,J=15.1 Hz,1H,H-13),4.67(s,2H,H-18),3.72(s,3H,-OCH3),3.26(d,J=5.9 Hz,1H,H-3),3.07 (dd,J=14.2,6.3 Hz,1H,H-5a),2.89(dd,J=15.4,6.1 Hz,1H,H-6a),2.75(dd,J=15.0,8.8 Hz,1H,9a),2.60 (dd,J=15.1,3.5 Hz,1H,9b),2.12(s,3H,-OCOCH3),2.04(s,1H,H-6b),1.85(s,3H,CH3-17),1.81-1.68(m,5H,H-1,2,5),1.58(s,3H,CH3-12).
HR-ESI-MS m/z:667.1325(M+Na)+,理論值:667.1319[M+Na]+。
2.2本實驗采用MTT(噻唑藍)法測試了目標化合物對小鼠T、B淋巴細胞的增殖抑制活性和正常細胞的細胞毒作用。體外活性篩選實驗以霉酚酸酯(MMF)為陽性對照藥,實驗結果如表1所示。
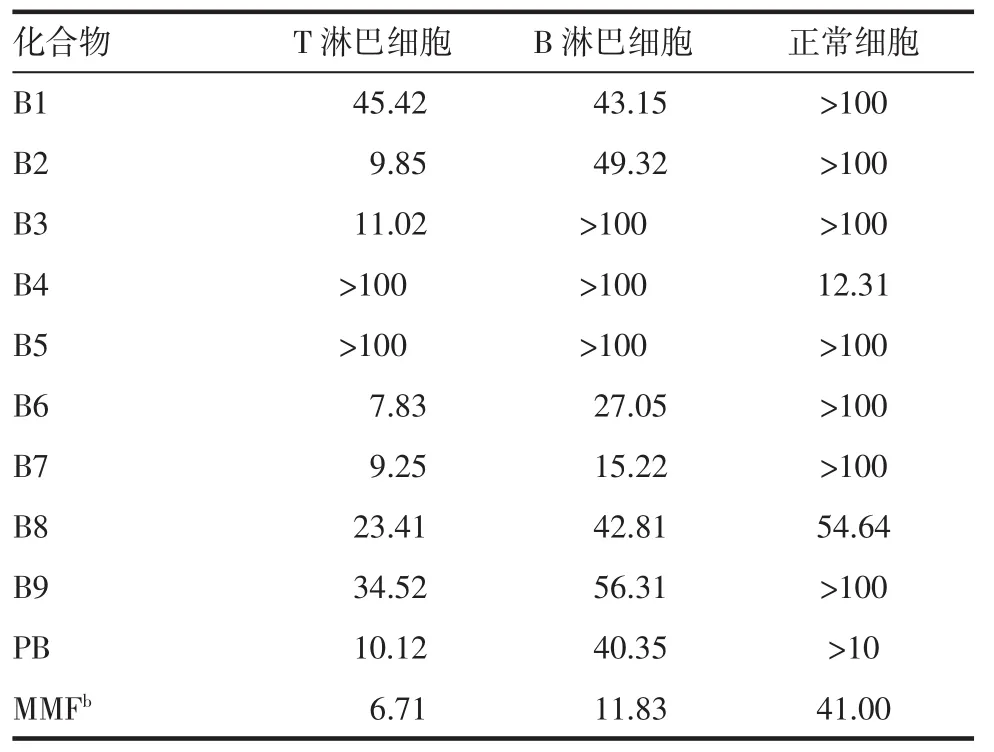
表1 新型土槿乙酸醇酯衍生物的體外抑制作用和細胞毒性[aIC50(10-6mol·L-1)]Tab 1 In vitro inhibitory effects and cytotoxicities of novel PB and indoles derivatives[aIC50(10-6mol·L-1)]
3 討論
結果顯示土槿乙酸C-18醇酯系列衍生物多數具有顯著的免疫抑制活性,其中衍生物B2,B6,B7對T淋巴細胞增殖抑制活性強于土槿乙酸,衍生物B3與土槿乙酸的抑制活性類似,尤其是B6抑制活性接近陽性對照藥霉酚酸酯。衍生物B6,B7對B淋巴細胞抑制活性明顯強于土槿乙酸,衍生物B1,B2,B8,B9對B淋巴細胞抑制活性與土槿乙酸活性接近。大多數化合物對正常細胞作用很弱,遠低于陽性對照藥,呈現高效低毒特性。
呋喃系列衍生物:對T淋巴細胞的增殖抑制活性,當引入呋喃環時其活性降低,當5-位有吸電子基硝基的存在時其活性明顯提高,引入鹵素溴原子時其活性較土槿乙酸雖有提高,但比硝基取代時活性低,引入四氫呋喃酸時其活性則完全喪失。由此而推測當引入有吸電子基取代呋喃環時,形成了邁克爾反應受體,這種呋喃環的電子共軛體系導致了藥理活性增加。B6化合物活性接近于陽性對照藥,而B5則完全失去活性,二者結構區別僅僅是-烯酸的取代位置不同,由此推測,引入呋喃丙烯酸有助于提高其藥理活性,且2位取代優于3位。
芳香共軛體系系列衍生物:對T淋巴細胞的增殖抑制活性,其化合物活性B7>B8>B9,而B10無活性。表明肉桂酸的引入有助于提高活性,當其芳環上有吸電子基取代時其活性降低,至于B10,F和Br原子的引入則導致完全喪失活性。據此而推測,吸電子基團不利于活性的提高,可能是通過吸電子基的引入降低了芳香環的電子云密度,進而影響與靶標的結合。
乙酸C-18醇成酯類化合物,引入呋喃環,抑制T、B淋巴細胞增殖活性明顯增加,引入具有共軛體系的呋喃環時活性更佳,并且毒性降低。對土槿乙酸構效關系的研究將促進新型免疫抑制劑的開發。

