食品乳液凝膠的制備及其應(yīng)用研究進(jìn)展
崔夢楠,鹿 瑤,高彥祥,毛立科*
(北京食品營養(yǎng)與人類健康高精尖創(chuàng)新中心,中國農(nóng)業(yè)大學(xué)食品科學(xué)與營養(yǎng)工程學(xué)院,北京 100083)
乳液凝膠是指一種被乳狀液液滴填充的具有凝膠網(wǎng)狀結(jié)構(gòu),且機(jī)械性能較強(qiáng)的凝膠[1]。因乳液凝膠獨特的結(jié)構(gòu)特性和功能特性,現(xiàn)已廣泛應(yīng)用于奶酪、酸奶、加工肉制品等領(lǐng)域中[2-3]。按照凝膠基質(zhì)的不同可分為蛋白質(zhì)乳液凝膠、多糖乳液凝膠、復(fù)合乳液凝膠等。乳液凝膠的結(jié)構(gòu)、功能特性取決于凝膠基質(zhì)和填充顆粒間的結(jié)合特性,根據(jù)顆粒與基質(zhì)之間的相互作用,填充顆粒可分為活性填充顆粒和非活性填充顆粒[4]。活性填充顆粒會與凝膠基質(zhì)相互作用,能夠影響乳液凝膠的微結(jié)構(gòu)和流變學(xué)性能;非活性填充顆粒不會與基質(zhì)結(jié)合,對乳液凝膠的強(qiáng)度無增強(qiáng)效應(yīng)。一般來說,乳液凝膠的制備過程可以分為以下兩步:一是乳狀液的制備,二是通過一系列的誘導(dǎo)方式使乳狀液的連續(xù)相凝膠,從而得到乳液凝膠。常用的誘導(dǎo)方式有熱誘導(dǎo)、酸誘導(dǎo)、鹽誘導(dǎo)、酶誘導(dǎo)、化學(xué)交聯(lián)劑誘導(dǎo)等[5-8]。乳液凝膠可作為脂肪替代物,有效降低飽和脂肪酸的含量,提高多不飽和脂肪酸、人體必需氨基酸、礦物質(zhì)等含量[9];還可作為傳遞體系,用來包埋水溶性較差的生物活性物質(zhì),并能顯著提高生物活性因子的穩(wěn)定性[3]。本文對近十多年來不同乳液凝膠的制備工藝及其應(yīng)用研究進(jìn)展進(jìn)行總結(jié),以期為乳液凝膠的制備工藝和其在食品、醫(yī)藥等領(lǐng)域的應(yīng)用發(fā)展提供一定的借鑒。
1 基于蛋白質(zhì)的乳液凝膠的制備
1.1 熱誘導(dǎo)
許多蛋白質(zhì)都有熱凝膠性,加熱時,未折疊的蛋白質(zhì)之間通過鏈間、鏈內(nèi)二硫鍵相互作用,從而形成凝膠的空間網(wǎng)狀結(jié)構(gòu)[10]。乳液凝膠的油滴表面粗糙并具有結(jié)構(gòu)性,能夠通過改變蛋白質(zhì)與油脂比例調(diào)整乳液凝膠的微結(jié)構(gòu)。當(dāng)?shù)鞍踪|(zhì)的濃度較高時,蛋白質(zhì)會發(fā)生自聚集[5]。乳液凝膠結(jié)構(gòu)還與熱誘導(dǎo)過程中pH值、加熱時間和離子強(qiáng)度有關(guān)。酸性條件下,蛋黃蛋白的熱凝膠速度較快[11]。在一定范圍內(nèi),加熱時間越長,越有利于蛋白質(zhì)分子間的疏水作用,形成的網(wǎng)狀結(jié)構(gòu)更加致密緊湊[12]。離子強(qiáng)度主要通過靜電屏蔽效應(yīng)影響乳液凝膠的結(jié)構(gòu)和性能,隨著鹽濃度的增加,乳液凝膠的持水性降低,有序的凝膠結(jié)構(gòu)變得無序[13]。酪蛋白乳狀液在熱作用下形成乳液凝膠的臨界溫度隨著酪蛋白濃度的增加而升高。乳化作用使液滴被膠束酪蛋白包裹,加熱時油滴會結(jié)合到酪蛋白的網(wǎng)狀結(jié)構(gòu)中,起著活性填充物的作用。用乳清分離蛋白代替部分酪蛋白,能夠增強(qiáng)蛋白質(zhì)的乳化性,使形成的乳液凝膠結(jié)構(gòu)均一,彈性、強(qiáng)度較大[14]。
雖然熱誘導(dǎo)這一方式簡便易于操作,但由于該過程需在較高的環(huán)境溫度條件下處理,不適合作為熱敏性生物活性物質(zhì)的輸送載體。當(dāng)包埋熱敏性生物活性物質(zhì)時,就需使用酶誘導(dǎo)、酸誘導(dǎo)、鹽誘導(dǎo)等制備乳液凝膠的方式。
1.2 酸誘導(dǎo)
酸誘導(dǎo)乳液成膠主要應(yīng)用于酸奶等發(fā)酵食品的制作中。酸誘導(dǎo)乳液凝膠的制備通常需在乳化作用之后對乳狀液或乳狀液同酸的混合液加熱一段時間[15],目的是保證葡萄糖酸內(nèi)酯充分水解為葡萄糖酸,降低體系的pH值,促進(jìn)蛋白質(zhì)包裹的油滴之間的相互作用,提高乳液凝膠的硬度[15]。酸誘導(dǎo)乳液凝膠的形成機(jī)理為蛋白質(zhì)分子吸附到液滴的表面使乳狀液液滴聚集并進(jìn)入到凝膠基質(zhì)中,該過程與氫鍵、疏水作用有關(guān)[16]。在酸誘導(dǎo)凝膠體系中,液滴和凝膠基質(zhì)的結(jié)構(gòu)有序化會使酸誘導(dǎo)的乳清分離蛋白聚集物乳液凝膠的模量增加[17]。酸誘導(dǎo)乳液凝膠的形成過程與酸化溫度、蛋白質(zhì)的濃度有關(guān)。酸化溫度的提高能顯著縮短膠凝化時間,但凝膠的硬度有所降低[6]。隨著蛋白質(zhì)濃度的增加,乳液凝膠的彈性增加,乳液凝膠的儲能模量與蛋白質(zhì)的濃度為指數(shù)函數(shù)關(guān)系[18]。酸誘導(dǎo)的乳液凝膠的微結(jié)構(gòu)與體系的pH值有關(guān),當(dāng)pH值接近于蛋白質(zhì)的等電點時,靜電排斥作用下降,有利于吸附在油滴表面的蛋白質(zhì)分子和凝膠基質(zhì)中的蛋白質(zhì)分子共價交聯(lián)[19]。此外,酸誘導(dǎo)的乳液凝膠的結(jié)構(gòu)與性能還與油相的組成有關(guān),含棕櫚硬脂的大豆分離蛋白穩(wěn)定的乳液凝膠,其硬度大于含葵花籽油或大豆油的乳液凝膠,且油脂吸附能力強(qiáng),穩(wěn)定性較好[20]。
1.3 鹽誘導(dǎo)
由于鹽誘導(dǎo)的乳液凝膠的形成過程中不涉及加熱或酸化,這種誘導(dǎo)方式更適合于熱敏感、酸敏感生物活性物質(zhì)的運載,像益生菌、維生素等。鹽誘導(dǎo)乳液凝膠形成的主要驅(qū)動力是蛋白質(zhì)包裹的油滴之間的“橋聯(lián)”作用。在制備過程中通常會對蛋白質(zhì)的分散液加熱,若未加熱,蛋白質(zhì)包裹的油滴易聚集成簇狀或絲狀,不利于網(wǎng)狀結(jié)構(gòu)的形成。加熱過程可以增強(qiáng)Ca2+和蛋白質(zhì)有效作用位點之間的相互作用,使更多的油滴進(jìn)入到三元網(wǎng)狀結(jié)構(gòu)中,增強(qiáng)乳液凝膠的強(qiáng)度[15]。
鹽誘導(dǎo)的乳液凝膠的結(jié)構(gòu)與性能與油的體積分?jǐn)?shù)、鹽離子濃度、蛋白質(zhì)的聚集程度和濃度有關(guān)。在β-乳球蛋白穩(wěn)定的乳液凝膠體系中,油滴是活性填充物,能夠與凝膠基質(zhì)相互作用,隨著油相的體積分?jǐn)?shù)的增加,乳液凝膠的網(wǎng)狀結(jié)構(gòu)變得致密且孔隙變小,彈性增加[7]。鹽濃度較低時,形成的乳液凝膠較柔軟,內(nèi)部結(jié)構(gòu)均一;隨著鹽濃度的增加,乳液凝膠的硬度增加,結(jié)構(gòu)更加致密緊湊[21],增加鹽離子的濃度也可以加速膠凝化過程。由于鹽誘導(dǎo)乳液凝膠的形成主要是通過Ca2+的“橋聯(lián)”作用,該過程不需要破壞界面上的蛋白質(zhì)薄層,便能形成致密的結(jié)構(gòu),能夠有效地避免液滴的聚集。在鹽誘導(dǎo)的大豆分離蛋白乳液凝膠中,隨著大豆分離蛋白的聚集,乳液凝膠的彈性增強(qiáng),增大鹽離子濃度,形成的乳液凝膠的油滴較小、結(jié)構(gòu)均一、持水性能增強(qiáng)[22]。
1.4 酶誘導(dǎo)
酶誘導(dǎo)是一種較溫和的、易受控制的制備乳液凝膠的方式,且不會產(chǎn)生副產(chǎn)物,制備成的乳液凝膠的結(jié)構(gòu)緊湊、質(zhì)地堅硬、彈性好[23]。與乳狀液相比,酶誘導(dǎo)的乳液凝膠具有較強(qiáng)的氧化穩(wěn)定性,該體系可用來抑制脂肪的氧化[24]。該方法中常用的酶是微生物谷氨酰胺轉(zhuǎn)氨酶,它是轉(zhuǎn)移酶的一種,能夠催化蛋白質(zhì)分子上的谷氨酰胺殘基和賴氨酸殘基之間的交聯(lián)反應(yīng),使蛋白質(zhì)發(fā)生分子內(nèi)交聯(lián)和分子間交聯(lián)以形成空間網(wǎng)狀結(jié)構(gòu)[25-26]。Tang Chuanhe等[15]用酶誘導(dǎo)法制備了大豆分離蛋白穩(wěn)定的乳液凝膠,實驗發(fā)現(xiàn),酶誘導(dǎo)的乳液凝膠具有均一的、較薄的、孔隙較小的網(wǎng)狀結(jié)構(gòu),機(jī)械強(qiáng)度較大。在乳化作用之前對大豆分離蛋白溶液加熱,能夠使更多的油滴進(jìn)入到網(wǎng)狀結(jié)構(gòu)中,未加熱的大豆分離蛋白穩(wěn)定的乳液凝膠在共聚焦顯微鏡下能夠觀察到裂口。但在乳化作用后對乳狀液加熱,不利于乳液凝膠的形成。
酶誘導(dǎo)的大豆分離蛋白穩(wěn)定的乳液凝膠的結(jié)構(gòu)與大豆蛋白的組成、濃度和油的體積分?jǐn)?shù)有關(guān),通過調(diào)整這些因素可以獲得具有特定結(jié)構(gòu)性能的乳液凝膠。Tang Chuanhe等[8]發(fā)現(xiàn),當(dāng)大豆分離蛋白中大豆球蛋白與β-伴球蛋白的比例較高時,制備成的乳液凝膠硬度較大,且凝膠硬度隨著蛋白質(zhì)濃度的增加而增加。油滴與油滴之間的作用除受到已吸附在油滴表面的蛋白質(zhì)影響,還受到未吸附在油滴表面的蛋白質(zhì)之間相互作用的影響[27]。當(dāng)大豆油的體積分?jǐn)?shù)較低時,凝膠網(wǎng)狀結(jié)構(gòu)的形成主要與未吸附在油滴表面的蛋白質(zhì)之間的共價交聯(lián)有關(guān)。隨著大豆油體積分?jǐn)?shù)的增加,越來越多的蛋白質(zhì)吸附在油滴表面,蛋白質(zhì)分子變得伸展甚至重排,有利于吸附在不同油滴表面的蛋白質(zhì)之間酶促交聯(lián)。因此,隨著油相體積分?jǐn)?shù)的逐漸增加,大豆分離蛋白穩(wěn)定的乳液凝膠的彈性和持水能力增強(qiáng)[28]。除此之外,在酶誘導(dǎo)過程中對乳狀液進(jìn)行攪拌能夠促進(jìn)網(wǎng)狀結(jié)構(gòu)的形成,增強(qiáng)乳液凝膠的硬度。與連續(xù)式攪拌相比,間歇式攪拌效果更佳[29]。有研究表明,將微波輻射同酶交聯(lián)協(xié)同應(yīng)用,可以將牛奶蛋白的聚合速率提高3 倍[30],這為酶誘導(dǎo)乳液凝膠的快速制備提供了新思路。
1.5 化學(xué)交聯(lián)

表1 不同誘導(dǎo)方式制備的蛋白質(zhì)乳液凝膠及其優(yōu)缺點比較Table1 Advantages and shortcomings of protein-stabilized emulsion gels induced by different treatments
將明膠穩(wěn)定的乳狀液放置于5 ℃的環(huán)境中,明膠即可完成溶膠-凝膠的轉(zhuǎn)化;但該方法制備的乳液凝膠中乳狀液液滴是非活性填充物,不能與基質(zhì)相互作用且會降低乳液凝膠的硬度[31-32]。通過使用京尼平這一毒性小的化學(xué)交聯(lián)劑可制備具有較強(qiáng)機(jī)械強(qiáng)度和熱力學(xué)特性的明膠乳液凝膠[33]。Thakur等[34]發(fā)現(xiàn),均質(zhì)時間影響京尼平交聯(lián)的明膠乳液凝膠的微結(jié)構(gòu)。當(dāng)均質(zhì)壓力為3.5 MPa時,均質(zhì)時間越長,乳狀液的顆粒越小且分布越集中,油滴能夠均勻地分散在明膠基質(zhì)中,當(dāng)均質(zhì)時間較短時,油滴會發(fā)生聚集。隨著均質(zhì)時間的延長,京尼平交聯(lián)的乳液凝膠的穩(wěn)定性和機(jī)械強(qiáng)度也增加。表1為不同誘導(dǎo)方式制備的蛋白質(zhì)乳液凝膠及其優(yōu)缺點比較。
2 基于多糖的乳液凝膠的制備
2.1 淀粉乳液凝膠
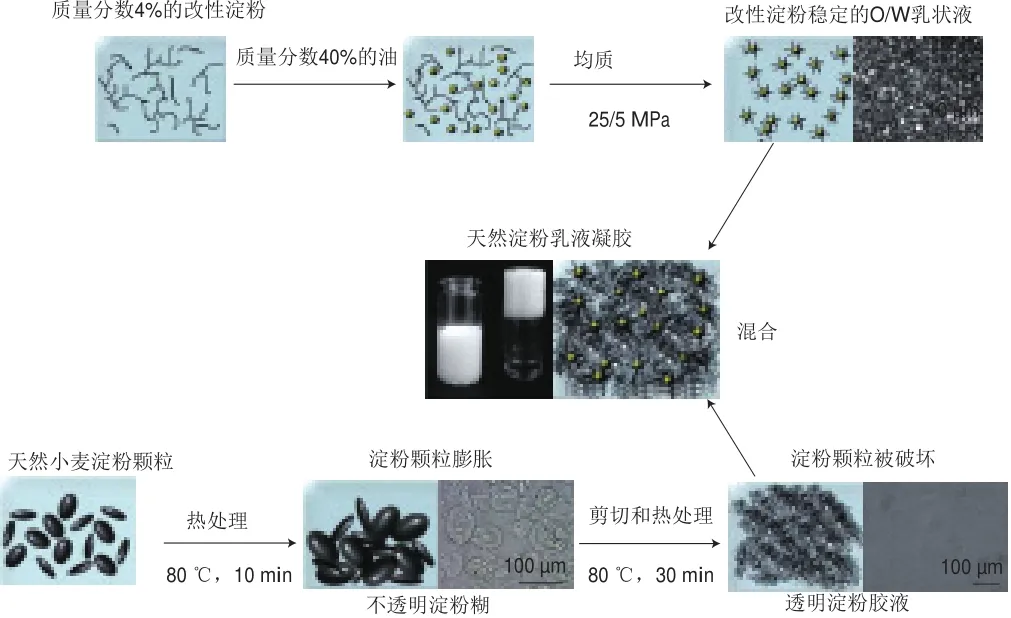
圖1 天然淀粉乳液凝膠的制備示意圖和相關(guān)顯微鏡照片[35]Fig.1 Schematic diagram for the formation of natural starch emulsion gel and micrographs[35]
Torres等[35]以改性淀粉、天然小麥淀粉為原料制備天然淀粉乳液凝膠,制備過程如圖1所示。吸附在油滴表面的改性淀粉中的疏水基團(tuán)定向排列,有利于吸附在不同油滴上的相鄰改性淀粉和連續(xù)相中的改性淀粉之間形成疏水網(wǎng)狀結(jié)構(gòu)[36];此外,相鄰的天然淀粉分子上的羥基也可通過氫鍵相互作用,增強(qiáng)顆粒與天然淀粉凝膠基質(zhì)之間的相互作用。在天然淀粉凝膠中,改性淀粉穩(wěn)定的乳狀液液滴是活性填充物,隨著葵花籽油添加量的增加,凝膠的彈性增加。
2.2 果膠乳液凝膠
低甲氧基果膠凝膠的形成主要是通過Ca2+與果膠主鏈上的羧基基團(tuán)之間的相互作用[37],高甲氧基果膠凝膠結(jié)構(gòu)的形成主要是通過未解離的羧基和仲醇基之間的氫鍵和甲基酯之間的疏水作用[38]。果膠乳液凝膠的流變學(xué)性能與甲基化程度有關(guān)。在低甲氧基果膠中,隨著甲基化程度的降低,果膠的膠凝能力增強(qiáng),形成的乳液凝膠抵抗形變的能力增強(qiáng)。當(dāng)甲基化程度為27.2%時,在較大的溫度范圍內(nèi),乳液凝膠的動態(tài)儲能模量幾乎保持不變[39]。
2.3 κ-卡拉膠乳液凝膠
κ-卡拉膠乳液凝膠的制備通常是將乳狀液和卡拉膠溶液在45 ℃的環(huán)境下加熱一段時間,然后冷卻到室溫并靜置使其成膠,加熱的目的是抑制液滴的消耗聚集[40]。在卡拉膠乳液凝膠體系中,油滴是非活性填充物,隨著中鏈甘油三酯濃度的增加,乳液凝膠的斷裂應(yīng)變幾乎不變,斷裂應(yīng)力和楊氏模量降低;但當(dāng)用溶菌酶穩(wěn)定乳狀液時,乳液凝膠的楊氏模量增加,這可能是由于卡拉膠與溶菌酶形成了纖維結(jié)構(gòu)[41]。
2.4 菊粉乳液凝膠
菊粉是一種益生元多糖,且具有抗細(xì)胞毒性和抗基因毒性[42]。菊粉凝膠網(wǎng)狀結(jié)構(gòu)是通過細(xì)小微晶相互交聯(lián)形成的,當(dāng)微晶聚集形成較大的簇狀物時,其網(wǎng)狀結(jié)構(gòu)能夠截留大量的水分[43]。菊粉形成的網(wǎng)狀結(jié)構(gòu)的性質(zhì)類似于脂肪結(jié)晶形成的網(wǎng)狀結(jié)構(gòu),已有研究表明,菊粉可作為膠凝劑應(yīng)用于乳液凝膠中[44]。菊粉乳液凝膠的制備需卵磷脂作為乳化劑,當(dāng)橄欖油含量較高時,形成的乳液凝膠含有豐富的纖維、不飽和脂肪酸和酚類抗氧化物。與機(jī)械剪切形成的乳液凝膠相比,超聲均質(zhì)后的乳液凝膠網(wǎng)狀結(jié)構(gòu)更均一、細(xì)膩[43]。
3 復(fù)合乳液凝膠
3.1 復(fù)合蛋白質(zhì)乳液凝膠
Qin Xinsheng等[45]制備了以大豆分離蛋白和小麥蛋白混合物穩(wěn)定的乳液凝膠,該乳液凝膠體系有效地改善了大豆分離蛋白的乳化性和小麥蛋白的溶解性[46]。超聲處理能夠促進(jìn)蛋白質(zhì)的巰基基團(tuán)和疏水基團(tuán)充分暴露,提高蛋白質(zhì)的起泡性和乳化性[47]。乳液凝膠的微結(jié)構(gòu)與大豆油的體積分?jǐn)?shù)有關(guān),隨著油相體積分?jǐn)?shù)的增加,油滴會發(fā)生聚集、絮凝,乳液凝膠的網(wǎng)狀結(jié)構(gòu)變得疏松不均一;但乳液凝膠的彈性增加,抵抗機(jī)械力的能力增強(qiáng),持水力增強(qiáng)[45]。油相體積分?jǐn)?shù)增加也會加快凝膠速率,縮短成膠時間。在較低體積分?jǐn)?shù)下,維系乳液凝膠內(nèi)部結(jié)構(gòu)的主要作用力是疏水作用和二硫鍵,當(dāng)體積分?jǐn)?shù)較高時,靜電相互作用占主導(dǎo)[46]。
3.2 蛋白質(zhì)-多糖乳液凝膠
固體脂質(zhì)微顆粒能夠?qū)⑾顸S油等熔點較高的脂肪酸耦合到乳液凝膠中,并能夠加強(qiáng)乳液凝膠的結(jié)構(gòu)和流變學(xué)性能[48]。Geremias-Andrade等[49]通過熱誘導(dǎo)方式制備了以乳清分離蛋白、黃原膠穩(wěn)定的具有高熔點油的乳液凝膠。改變固體脂質(zhì)微顆粒分散液的濃度,可獲得具有不同結(jié)構(gòu)和流變性能的乳液凝膠。當(dāng)分散液濃度較低時,油滴是非活性填充物,不影響乳液凝膠的機(jī)械性能;當(dāng)分散液的濃度較高時,油滴是活性填充物,均一地分散在凝膠基質(zhì)中,能夠增加乳液凝膠的硬度,這可能是由于蛋白質(zhì)的構(gòu)象發(fā)生了變化,其疏水殘基充分暴露[50],加強(qiáng)了蛋白質(zhì)與油滴之間的相互作用。
Hou Junjie等[51]通過酶誘導(dǎo)法制備了以大豆分離蛋白(soy isolate protein,SPI)、甜菜果膠(sugar beet pectin,SBP)或二者混合物穩(wěn)定的乳液凝膠,并探討了均質(zhì)作用對形成的乳液凝膠微結(jié)構(gòu)的影響。通過共聚焦顯微鏡可以觀察到,不經(jīng)過均質(zhì)作用形成的乳液凝膠均具有良好的網(wǎng)狀結(jié)構(gòu):以交聯(lián)的大豆分離蛋白為骨架,將甜菜果膠乳化的油滴或油滴、甜菜果膠包埋在其中(圖2)。經(jīng)均質(zhì)作用后,只有甜菜果膠穩(wěn)定的乳液凝膠中油滴均一地分布在大豆分離蛋白的網(wǎng)狀結(jié)構(gòu)中且粒徑小,其他體系中,油滴聚集成簇狀。較小的油滴具有較高的界面區(qū)域,可以為高聚物的吸附提供較多的位點,從而增強(qiáng)油滴與基質(zhì)的結(jié)合作用,提高乳液凝膠的斷裂力和張力[52]。

圖2 乳液凝膠的共聚焦顯微鏡圖[51]Fig.2 Confocal microscopic images of emulsion gels[51]
4 乳液凝膠的應(yīng)用
4.1 代替飽和脂肪酸
乳液凝膠是一種介于液體和固體之間的材料,常用來仿制飽和脂肪酸的質(zhì)構(gòu)特性,有利于設(shè)計低脂食品[53]。Poyato等[2]以卡拉膠、聚山梨酯80和葵花籽油為原料制備成的乳液凝膠可作為豬脂的替代物,能夠降低新鮮肉制品中的飽和脂肪酸含量,且最終產(chǎn)品的風(fēng)味能夠讓消費者滿意。將奇亞籽乳液凝膠或燕麥糠凝膠混合在鮮香腸中,能夠提高單不飽和脂肪酸、礦物質(zhì)、氨基酸的含量,降低飽和脂肪酸的含量[9]。

表2 乳液凝膠作為傳遞體系的應(yīng)用Table2 Applications of emulsion gels as delivery systems for some nutrients
乳液凝膠的微結(jié)構(gòu)、性能與油相組成和濃度有關(guān)。在酸誘導(dǎo)的乳清分離蛋白穩(wěn)定的乳液凝膠中,當(dāng)用中鏈脂肪酸代替部分葵花籽油時,膠凝時間有所延長,但乳液凝膠的硬度增加。隨著中鏈脂肪酸添加量的增加,其凝膠速度提高[54]。
4.2 作為功能因子的遞送體系
4.2.1 包埋益生菌
Pandey等[55]以黃原膠和瓜爾豆膠為載體、山梨醇酐單棕櫚酸酯為乳化劑制備了同時包埋益生菌和甲硝唑的乳液凝膠,該乳液凝膠能夠有效提高益生菌的存活率。由于黃原膠和瓜爾豆膠幾乎只在結(jié)腸中被消化利用,用這些天然膠作益生菌的載體,可實現(xiàn)定點釋放[56]。在黃原膠質(zhì)量分?jǐn)?shù)為40%、瓜爾豆膠質(zhì)量分?jǐn)?shù)為10%的乳液凝膠體系中,益生菌在深冷凍生產(chǎn)過程中存活穩(wěn)定性極高,存活率高達(dá)95%,且該體系及其穩(wěn)定,甲硝唑的釋放不受乳液凝膠貯藏溫度和時間的影響,能夠?qū)崿F(xiàn)甲硝唑的持久釋放。
4.2.2 包埋α-生育酚
Li Liang等[3]制備了Ca2+誘導(dǎo)的β-乳球蛋白穩(wěn)定的乳液凝膠,并用該體系包埋α-生育酚,實驗發(fā)現(xiàn),該體系大大提高了α-生育酚的釋放穩(wěn)定性及生物利用率,在模擬的胃液和腸液中,α-生育酚的釋放和基質(zhì)的降解均是完全的;而在模擬的胃腸道環(huán)境中,α-生育酚緩釋緩慢。將α-生育酚和VE同時包埋在乳液凝膠體系中,可進(jìn)一步提高α-生育酚的穩(wěn)定性[57]。
4.2.3 包埋風(fēng)味物質(zhì)
與乳狀液體系相比,乳液凝膠體系能更有效地抑制其在儲藏期間風(fēng)味物質(zhì)的釋放。風(fēng)味物質(zhì)的釋放速率與構(gòu)成凝膠的基質(zhì)有關(guān),與大豆分離蛋白乳液凝膠體系相比,酪蛋白酸鈉乳液凝膠體系能更有效地抑制己酸乙酯的釋放[58]。
Hou Junjie等[51]制備了以大豆分離蛋白和甜菜果膠的混合物穩(wěn)定的乳液凝膠,并用其包埋風(fēng)味物質(zhì)(己酸乙酯、己酸丁酯和辛酸乙酯),結(jié)果發(fā)現(xiàn),乳液凝膠體系能夠顯著抑制風(fēng)味物質(zhì)的釋放速率。風(fēng)味物質(zhì)的釋放速率主要由風(fēng)味物質(zhì)的擴(kuò)散速率和凝膠基質(zhì)的空間位阻效應(yīng)決定[54],由于辛酸乙酯的疏水性極高,對油脂的吸附能力極強(qiáng),幾乎不與蛋白質(zhì)或多糖相互作用,與其他兩種風(fēng)味物質(zhì)相比,它的空氣/乳液凝膠分配系數(shù)、初始釋放速率均非常低。風(fēng)味物質(zhì)的初始釋放速率還與油滴的粒徑有關(guān);油滴較小時,它能夠為蛋白質(zhì)/多糖的吸附提供較多的位點,有利于油滴與基質(zhì)之間的相互作用,使油水界面致密緊湊、結(jié)構(gòu)均一,能充分起到屏障保護(hù)作用[51]。表2為不同乳液凝膠作為傳遞體系的應(yīng)用。
5 結(jié) 語
通過一定的誘導(dǎo)方式使乳狀液中的連續(xù)相膠凝可制備乳液凝膠,乳液凝膠體系既具有乳狀液的特性,又具有凝膠的特性。乳液凝膠在作為脂肪替代物、提高生物活性因子穩(wěn)定性中已顯示出了巨大的優(yōu)勢。然而,乳液凝膠在材料的選擇、制備及其在更復(fù)雜的食品體系中的應(yīng)用等方面還需進(jìn)一步研究,即如何控制制備過程中的成本、乳液凝膠機(jī)械性能的合理性及其有效調(diào)控、作為脂肪替代物的感官評價、包埋的生物活性因子的負(fù)載率和穩(wěn)定性、生物活性因子的消化代謝與在普通食品中的消化代謝是否存在區(qū)別等。突破和解決上述問題,需要多學(xué)科交叉研究,以為拓展乳液凝膠在食品中的應(yīng)用提供依據(jù)。

