八珍湯聯合肺俞埋針對肺氣虛型慢性阻塞性肺疾病的療效研究
朱 靜
0 引言
慢性阻塞性肺疾病(Chronic obstructive pulmonary disease,COPD)是一種較為常見的呼吸系統疾病,該病的特點是病程長、病情極易反復等,嚴重影響患者的生活質量,給患者家庭及社會帶來了沉重的經濟負擔[1]。持續氣流受限是COPD的病理生理特征,且其氣流受限一般呈進行性發展,主要與有害顆粒及煙草、煙霧等有害氣體產生的慢性炎性反應有關,監測肺功能對評估患者的氣流受限程度具有十分重要的意義。研究顯示,COPD患者往往出現細胞免疫功能的變化,且大多患者的氣道中均存在一定的慢性炎癥反應[2]。以往關于COPD的治療以抗感染、抗凝、吸氧、解痙、平喘、止咳、化痰等常規治療為主,其雖能在一定程度上改善患者的肺功能,但并不能延緩病情的進展,因此,尋找一種更為有效的治療方案尤為重要[3]。中醫藥治療具有作用持久、毒副作用少等優勢,已被廣泛用于各類疾病的治療。慢阻肺屬于中醫 “喘證”、“咳嗽”、“肺脹”等范疇。肺氣虛是COPD的基本病機,肺失宣肅,氣不布津,累及脾而致脾失健運,或飲食不節,脾土受損,最終導致脾肺氣虛,累及五臟,從而導致疾病的發生。八珍湯具有健脾益肺、溫陽益氣之效,埋針治療可調節機體的經絡臟腑,從根本上治療疾病,從而達到防治COPD的作用[4]。本研究旨在探討八珍湯聯合肺俞埋針對肺氣虛型COPD的療效,觀察其對免疫系統的影響,以期為肺氣虛型COPD的臨床治療提供參考依據。
1 資料與方法
1.1 臨床資料 選擇2016年1月至2017年12月我院收治的120例肺氣虛型COPD患者,采用隨機數字表法將120例患者隨機分為觀察組(60例)和對照組(60例),觀察組男32例,女28例;年齡35~80歲,平均(51.94±3.31)歲;病程5~20年,平均(11.98±2.34)年。對照組男33例,女27例;年齡35~80歲,平均(51.95±3.69)歲;病程5~20年,平均(11.84±2.63)年。觀察組及對照組患者的性別、年齡、病程等基線資料比較,差異無統計學意義(P>0.05)。
1.2 西醫診斷標準 根據中華醫學會呼吸病學分會慢性阻塞性肺疾病學組2013 年制定的《慢性阻塞性肺疾病診治指南》[1]中關于COPD的診斷標準擬定:(1)吸入支氣管擴張劑后FEV1/FVC<70%即明確存在持續的氣流受限,可確診為 COPD;(2)排除閉塞性細支氣管炎、彌漫性泛細支氣管炎、肺結核、支氣管擴張癥等已知病因或具有特征性病理表現的氣流受限疾病。COPD 穩定期是指患者氣短、咳嗽、咳痰等癥狀輕微或穩定。
1.3 中醫辨證標準 參考《中藥臨床研究指導原則(試行)》制定[5]。肺氣虛型辨證標準:(1)主癥:神疲,乏力,氣短,喘息,動則加重,易感冒,腰膝酸軟,舌苔白,舌質淡,脈細;(2)次癥:食少,腹脹,胃脘痞滿,自汗,便溏,脈沉、細、緩、弱。
1.4 病例納入及排除標準 納入標準:(1)符合西醫關于COPD的診斷標準及中醫關于肺氣虛的辨證標準;(2)COPD 穩定期;(3)肺功能為Ⅱ~Ⅲ級;(4)年齡35~80歲;(5)血尿常規檢查及肝腎功能檢查結果均在正常值范圍內;(6)患者知情同意并且簽署知情同意書。排除標準:(1)合并嚴重腎病、肝病、代謝性疾病、心功能不全、腦部疾病、造血系統及其他重要臟器原發性疾病者;(2)合并有肺結核、肺大皰、肺癌等其他肺部疾病者;(3)意識障礙或合并有精神病患者;(4)有明顯除外肺氣虛證的中醫兼夾證者;(5)無法按照治療方案治療者。
1.5 方法 對照組患者予以化痰、吸氧、抗感染、解痙、平喘、糾正水電質紊亂等常規西醫治療,根據患者的病情予以糖皮質激素、支氣管擴張劑、祛痰藥、免疫調節劑、抗氧化劑等藥物治療,并結合氧療、肌肉訓練、呼吸生理治療、健康教育等常規治療。連續30 d為1 個療程,共治療2個療程。觀察組患者在對照組治療基礎上加以八珍湯聯合肺俞埋針治療,八珍湯藥物組成:茯苓 15 g,人參 10 g,炙甘草10 g,白術 15 g,白芍30 g,當歸 15 g,川芎15 g,熟地黃15 g,大棗 5 枚,生姜3 片。水煎服,1劑/d,分早晚2次服用。肺俞埋針治療:于肺俞穴皮下埋針,每2周埋針1次,連續4周為 1 個療程,共治療2個療程。
1.6 觀察指標 對比治療前后兩組患者的肺功能指標(FEV1、FVC和FEV1/FVC)和免疫功能指標(CD3+、CD4+、CD8+、CD4+/CD8+、TNF-α、VEGF、IL-8、IL-17) 變化情況,采用圣·喬治呼吸問卷評分(SGRQ)、BODE 指數評價治療前后兩組患者的生活質量變化情況,同時比較兩組患者的臨床療效。采用德國 MasterScreen 肺功能儀測定治療前后患者的肺功能指標。采用美國 Coulter Epics 流式細胞儀測定治療前后兩組患者的CD3+、CD4+、CD8+、CD4+/CD8+水平;采用 ELISA 法檢測治療前后患者血清炎癥因子 IL-8、IL-17、TNF-α 水平及血管內皮生長因子(VEGF)水平。
1.7 生活質量評價 采用SGRQ、BODE 指數評價治療前后兩組患者的生活質量變化情況。SGRQ問卷有疾病影響、呼吸癥狀及活動能力3個維度,共50 個條目,分值為 0~100 分,分值越高表示患者的生活質量越差[6]。BODE 指數評分標準:(1)氣流阻塞程度:FEV1/FEV1%≥65%計為0分,50%≤FEV1/FEV1%<65%計為1分,35%≤FEV1/FEV1%<50%計為2分,FEV1/FEV1%<35%計為3分;(2)體重指數(Body mass index,BMI):≤21 kg/m2計為1分,>21 kg/m2計為0分;(3)運動能力:通過6分鐘步行距離(6-min walk distance,6MWD)(m)進行評價:6MWD≥350計為0分,250≤6MWD<350計為1分,150≤6MWD<250計為2分,6MWD<150計為3分;(4)呼吸困難程度:采用英國醫學研究委員會制定的呼吸困難量表(Modified medical research council scale,MMRC)對患者的呼吸困難程度進行評價:0~1級計為0分,2級計為1分,3級計為2分,4級計為3分。將上述4項單項評分相加,計算總分,分值越高,表示患者的生活質量越差[7]。
1.8 臨床療效判斷 比較兩組患者的臨床療效。臨床療效判斷標準參考《中藥臨床研究指導原則(試行)》制定[6]。(1)無效:臨床癥狀積分無任何改善或者加重,肺功能指標無任何改善或者降低,生活質量評分無任何改善或者降低;(2)有效:30%≤臨床癥狀積分減少<60%,10%≤肺功能提高<20%,10%≤生活質量評分提高<20%;(3)顯效:臨床癥狀積分減少≥60%,肺功能指標提高≥20%,生活質量評分提高≥20%。總有效率=(有效+顯效)/各組總例數×100%。

2 結果
2.1 治療前后兩組患者的肺功能指標變化情況比較 治療前,觀察組及對照組的FEV1、FVC和FEV1/FVC比較,差異無統計學意義(P>0.05);治療后,觀察組及對照組的FEV1、FVC和FEV1/FVC均明顯升高(P<0.05),且觀察組明顯高于對照組(P<0.05),見表1。

表1 兩組患者的肺功能指標變化情況比較
注:*與治療前比較,P<0.05;#與對照組比較,P<0.05
2.2 治療前后兩組患者的免疫功能指標變化情況比較 治療前,觀察組及對照組的CD3+、CD4+、CD8+、CD4+/CD8+比較,差異無統計學意義(P>0.05)。治療后,觀察組及對照組的CD3+、CD4+、CD4+/CD8+均明顯升高(P<0.05),且觀察組明顯高于對照組(P<0.05)。治療前后兩組患者的CD8+比較,差異無統計學意義(P>0.05),見表2。
2.3 治療前后兩組患者的炎癥因子和VEGF 水平變化情況比較 治療前,觀察組及對照組的IL-8、IL-17、TNF-α、VEGF水平比較,差異無統計學意義(P>0.05)。治療后,觀察組及對照組的IL-8、IL-17、TNF-α、VEGF水平均明顯降低(P<0.05),且觀察組明顯低于對照組(P<0.05),見表3。

表2 治療前后兩組患者的免疫功能指標變化情況比較
注:*與治療前比較,P<0.05;#與對照組比較,P<0.05
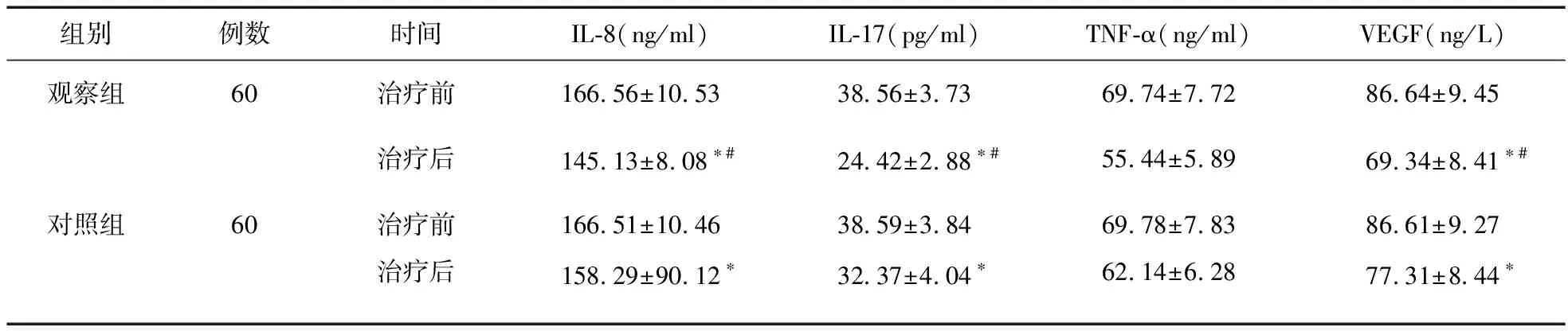
表3 治療前后兩組患者的炎癥因子和VEGF水平變化情況比較
注:*與治療前比較,P<0.05;#與對照組比較,P<0.05
2.4 治療前后兩組患者的生活質量評分變化情況比較 治療前,觀察組及對照組的SGRQ評分、BODE 指數比較,差異無統計學意義(P>0.05)。治療后,觀察組及對照組的SGRQ評分、BODE 指數均明顯降低(P<0.05),且觀察組明顯低于對照組(P<0.05)。見表4。

表4 治療前后兩組患者的生活質量評分比較
注:*與治療前比較,P<0.05;#與對照組比較,P<0.05
2.5 兩組患者臨床療效比較 觀察組總有效率為90.00%,對照組總有效率為70.00%,兩組比較差異有統計學意義(P<0.05)。見表5。

表5 兩組患者的臨床療效比較(例)
注:#與對照組比較,P<0.05
3 討論
COPD是一種較為常見的慢性肺部疾病,氣流受限是該病的主要特征。隨著病情的進展,機體胸廓及肺的順應性下降,最終誘發心肺功能損害,嚴重影響患者的生活質量。近年來,隨著我國社會老齡化現象的加劇,COPD的發病率呈現逐年遞增的趨勢,已經成為危害我國公共衛生問題的重要疾病[8]。
COPD屬于中醫“喘證”、“咳嗽”、“肺脹”等范疇。有學者認為,虛、痰、瘀是慢阻肺的重要病機,以脾肺虛最為常見[9]。肺主氣,脾為肺之母,脾氣運化是肺氣生成的基礎,肺氣源于脾,脾氣運化功能與肺氣盛衰密切相關。脾氣運化失常可致脾氣不足,肺氣虛衰。脾氣不足則致水濕運化無力,肺氣不固則致宣發肅降無力,水濕痰濁瘀滯于肺,最終導致COPD的發生。因此,臨床對于COPD的治療應以補脾益肺、化痰活血為主[10]。
研究發現,氣道炎癥反應是導致COPD發病的一個重要原因。當機體呼吸道受到外邪侵襲時,肺泡巨噬細胞可產生大量的TNF-α、IL-8等炎癥因子,這些炎癥因子又會進一步誘發肺部病變,大大增加了COPD的發病風險。老年人群為COPD的高發人群,老年人群由于免疫功能的下降,極易導致 T 細胞亞群平衡失調,造成呼吸道防御功能的下降,導致肺功能損害,促進COPD的發生發展[11]。本研究結果顯示,治療后,觀察組的炎性細胞因子水平明顯低于對照組,結果表明,八珍湯聯合肺俞埋針治療可有效抑制COPD機體的炎癥反應。VEGF 又稱為血管通透分子,體外試驗研究顯示,VEGF 主要以多種形式參與氣道重塑及血管重塑[12],COPD患者的VEGF水平明顯高于健康人群,提示 VEGF水平的升高可能與COPD患者肺泡破壞和氣流受限有關。本研究結果顯示,治療后,觀察組的VEGF水平明顯低于對照組,結果提示,八珍湯聯合肺俞埋針治療可有效改善COPD患者的氣流受限表現。BODE 指數綜合了COPD患者的氣流阻塞程度、生理因素、運動能力及呼吸困難程度,是COPD患者健康相關生存質量嚴重程度的一個重要預測因子,可作為評估COPD患者生活質量的一個重要指標[13]。本研究結果顯示,治療后,觀察組的SGRQ評分、BODE 指數均明顯低于對照組,結果表明,八珍湯聯合肺俞埋針治療可有效改善COPD患者的生活質量。
八珍湯來源于《正體類要》,是補血方四物湯和補氣方四君子湯的合方,由川芎、當歸、熟地黃、白芍、白術、人參、炙甘草、茯苓8 味中藥組成,常用于氣血皆虛諸證的治療[14]。方中熟地黃、人參為君藥,熟地黃具有益精填髓、補血滋陰之效;人參具有生津、安神、補脾益肺、大補元氣之效。熟地黃、人參為君藥,補益氣血,氣旺則精血能固而不外溢,氣足則精血化生有源,血足則可養氣,不致氣隨血脫。茯苓具有健脾安神、利水滲濕之效;白術具有燥濕利水、補氣健脾之效。當歸具有調經止痛、補血活血之效,是治療心肝血虛的要藥。川芎具有祛風止痛、活血行氣之效。諸藥合用,互相取長補短,具有健脾益肺、補氣養血之功[15]。現代藥理學研究顯示,人參所含人參皂苷可有效增強機體的免疫功能,并能抑制血小板的聚集[16-18]。當歸對特異性和非特異性免疫功能均具有增強作用。白芍提取物芍藥苷可抑制血小板聚集,并能起到抗炎、免疫調節的作用;白芍總苷可顯著增強吞噬細胞的吞噬功能,且對免疫活性物質的產生可產生雙向調節的作用。茯苓可有效提高巨噬細胞的識別功能,并能特異性增強小鼠的體液免疫反應。川芎嗪可增強單核巨噬細胞的吞噬功能,并能有效提高機體的免疫功能。
埋針療法又稱為皮內針療法,是一種較為常用的針刺療法,該療法主要是通過將特制的小型針具長時間埋藏固定在患者的皮下或皮內,從而達到調整經絡臟腑的功能[19]。肺腧穴屬于足太陽膀胱經,是一個重要的背俞穴。從西醫解剖角度解釋,肺俞穴位于皮膚皮下組織中的菱形肌、斜方肌、豎脊肌、上后鋸肌上。該區域深層分布有第三肋間動靜脈的分支和第三胸神經后支的肌支,淺層分布有靜脈背側支的內側皮支、第四胸神經后支的內側皮支。肺俞穴系肺臟的對應穴位,肺俞埋針是治療肺系疾患的常用針灸手段,具有止咳、平喘之效,因此,聯合肺俞埋針治療,可有效改善患者的臨床癥狀[20]。
綜上所述,在肺氣虛COPD患者中施以八珍湯聯合肺俞埋針治療,可有效改善患者的肺功能及生活質量,可能與其對機體的免疫系統調控作用有關。

