手術刮除聯合真空封閉引流治療巨大痛風石并骨破壞軟組織壞死16例
費志軍,謝寧靈,伍敬文,趙曉亮,謝俊鋒,林淮,辛鵬
(廣州總醫院157分院 骨科,廣東 廣州 510510)
痛風石是痛風的特征性損害,為尿酸鹽反復沉積使局部組織反復發生慢性異物樣反應[1]。該病輕者影響美觀,重者延及關節肢體的正常功能,遷延失治的痛風石逐漸增大增多,導致皮膚潰破、軟組織壞死及骨關節破壞,難以覆蓋的創面及骨缺損往往使患者選擇截趾(肢)手術根治,給其帶來極大的痛苦及傷害。本科2011年1月-2017 年12月先后采用痛風石刮除聯合真空封閉引流(vacuum sealing drainage, VSD)治療16例巨大痛風石合并骨破壞、軟組織壞死缺損患者,取得滿意療效,成功保趾(肢)率達93.8%,現報道如下。
1 資料與方法
1.1 一般資料
2011年1月-2017年12月采用痛風石手術刮除聯合VSD負壓吸引術治療巨大痛風石并骨破壞、軟組織壞死患者共16例。其中男13 例,女3例;發生于足部第1跖趾關節處11例,足部其他位置5例;年齡41~86歲,平均58歲。
臨床表現及診斷標準均采用美國風濕協會制定標準[2]擬定:①有典型痛風病史;②高尿酸血癥;③痛風石形成;④累計第1跖趾關節;⑤X線顯示骨皮質下囊腫、骨關節破壞;⑥痛風石穿破皮膚,形成竇道及皮膚軟組織壞死缺損;⑦功能障礙。
1.2 方法
本組所有患者術前均積極予以綜合的內科治療[3],使血尿酸保持在相對低的水平狀態,因為在術中隨著痛風石、尿酸鹽結晶的清除,勢必有部分尿酸鹽結晶溶解并吸收入血,易造成術后早期痛風急性發作,故所有手術時期選擇在靜息期[4]。
痛風急性期的藥物治療:口服秋水仙堿、雙氯芬酸鈉腸溶膠囊、潑尼松及碳酸氫鈉控制急性痛風癥狀,定期復查血尿酸、C反應蛋白(C-reactive protein, CRP)、血沉、血象及肝腎功等,根據血尿酸變化情況逐漸調整用藥,待血尿酸控制相對較低后,安排手術治療。手術均采取連續硬脊膜外阻滯麻醉,按痛風石具體位置設計手術切口,以充分暴露痛風石病灶為宜,其皮膚破潰處以缺損區為中心行擴創切口。切除壞死皮膚、筋膜及肌腱等失去活性軟組織;刮除創面內痛風石組織,咬除壞死骨組織,沖洗創面,修整破壞跖(趾)骨斷面至整齊,對合骨斷面稍短縮跖(趾)骨行簡單內固定(克氏針或縫合周圍軟組織固定),均未行一期植骨。創面閉合時予以稍游離創緣皮瓣,拉攏后全層縫合縮小創面。術后抬高患肢,每日換藥1、2次,早期仍有少量殘存痛風石組織滲出,其后逐漸減少至完全清除,時間約1周左右。術后1周行遺留創面VSD負壓吸引術,根據創面大小深淺及肉芽組織生長情況,通常需VSD負壓吸引1~3次,每次維持5~7 d。吸引術后,根據創面愈合情況行直接拉攏縫合至愈合,或行二期植皮處理覆蓋創面。術后無急性疼痛癥狀后,予苯溴馬隆、丙磺舒口服,繼續予以加強營養、預防感染及改善微循環等對癥治療。
1.3 療效評定
優:痛風癥狀控制,痛風石清除,創面自行閉合或延期縫合愈合,患足外形基本恢復正常,可負重行走,活動感覺保存。良:痛風癥狀控制,痛風石清除,創面需二期植皮愈合,患足短縮,外形接近正常,恢復部分活動,可部分負重。差:創面經久不愈,痛風石反復存在,患足骨外露,混合感染、需截趾(肢)處理。
1.4 典型病例
患者徐XX,男,65歲,北京人。因左足腫物4年,加重并潰破滲出、活動受限1周入院,既往有糖尿病史。入院查:雙手雙足多發性皮下白色圓形結節樣腫物,大小不等。左足重度腫脹,第1 跖趾關節前內側見直徑約8 cm圓形腫物,皮溫升高、透亮質軟,有3個破潰裂口,擠壓可見白色石灰粉狀物并黃色壞死組織滲液(見圖1)。X線示左足軟組織腫脹影,第1趾骨、1跖骨破壞,蟲嗜狀改變,左足2~5趾多發性骨破壞(見圖 2)。血尿酸:836 μmol/ L,CRP:210.3 mg/ L,血沉:98 mm/ h,WBC:12.33×109/ L,血糖:10.6 mol/ L。診斷:①痛風急性發作;②左足痛風石形成并骨破壞軟組織壞死;③糖尿病。入院后予以左足創面清創換藥,口服秋水仙堿、雙氯芬酸鈉,控制痛風癥狀及控制血糖等對癥治療,1周后血尿酸:542 μmol/L,在連續硬脊膜外阻滯麻醉下行左足痛風石刮除清創術,以左足拇趾痛風石為中心作L型手術切口,長約10 cm,見左足第1跖趾關節處大量白色石灰粉膏狀組織粘連成團,直徑約8 cm,清除后見左足第1跖骨、近節趾骨部分骨破壞,病理性骨折,關節軟骨面已蠶食,骨髓腔間隙含大量痛風石組織(見圖3),咬通髓腔,以刮匙徹底刮除殘存痛風石,清除壞死肌肉及筋膜、皮膚,沖洗槍沖洗創面,稀碘伏浸泡,將跖趾骨斷端修整,拉攏縫合周邊軟組織穩定骨折,將創周皮緣稍松解后拉攏縫合,遺留直徑約4 cm軟組織缺損區域(見圖4),予以碘伏紗布疏松填塞后包扎,石膏托外固定患肢足踝部。術后頭孢他啶靜脈滴注2 d預防感染,創面換藥:1、2 次/日,早期仍有少量痛風石滲出,至術后1周,創面新鮮,無滲出,部分趾、跖骨外露,復查血尿酸及CRP值已顯著降低,即行左足創面VSD負壓吸引術治療(見圖5)。1周后患足腫脹明顯減輕,外露骨面已有少量肉芽組織生長。予以更換VSD負壓吸引,持續1周后拆除,見創面縮小,肉芽組織生長滿意(見圖6),予蝶形膠布拉攏創面,繼續換藥觀察。術后40 d,患者創面完全閉合,患足外形基本恢復正常(見圖7、8),可部分負重行走,無疼痛不適感,復查CPR:2.3 mg/ L,血尿酸:426 μmol/L,血沉:6.4 mm/ h,血象及肝腎功正常,予出院繼續康復鍛煉。
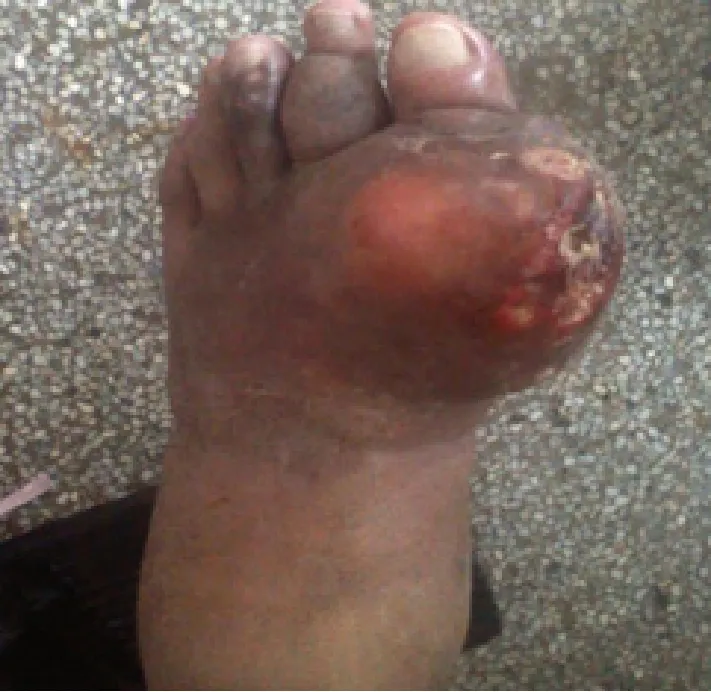
圖1 入院左足痛風石
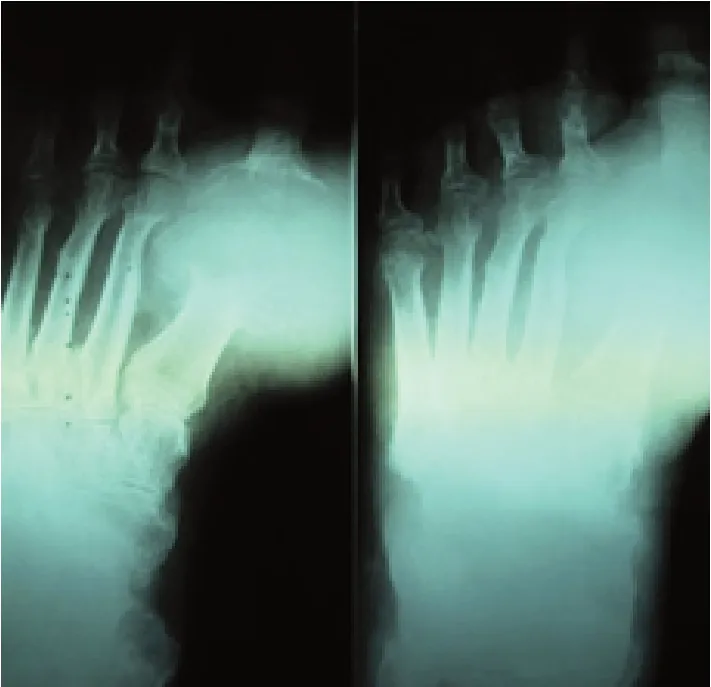
圖2 入院左足X線
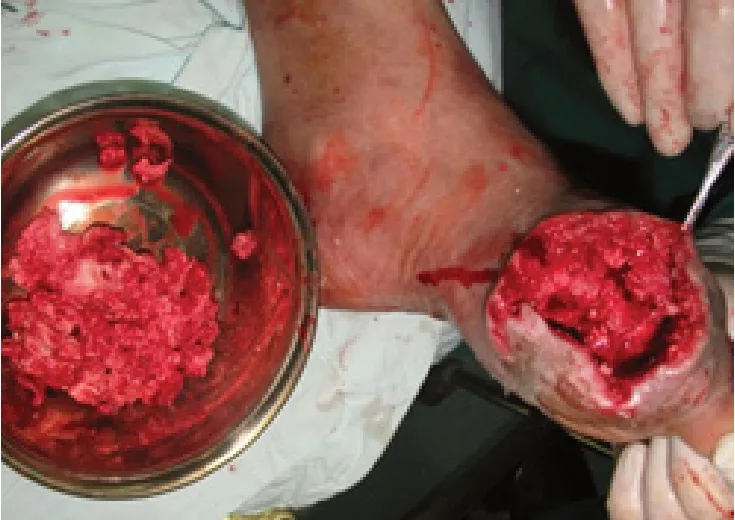
圖3 中刮除痛風石后第1跖、趾骨部分缺
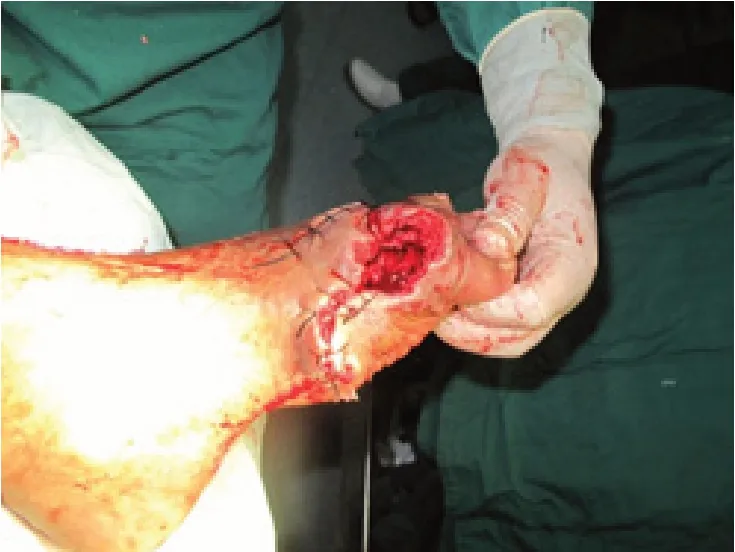
圖4 減張縫合后,遺留直徑4 cm無軟組織覆蓋創面
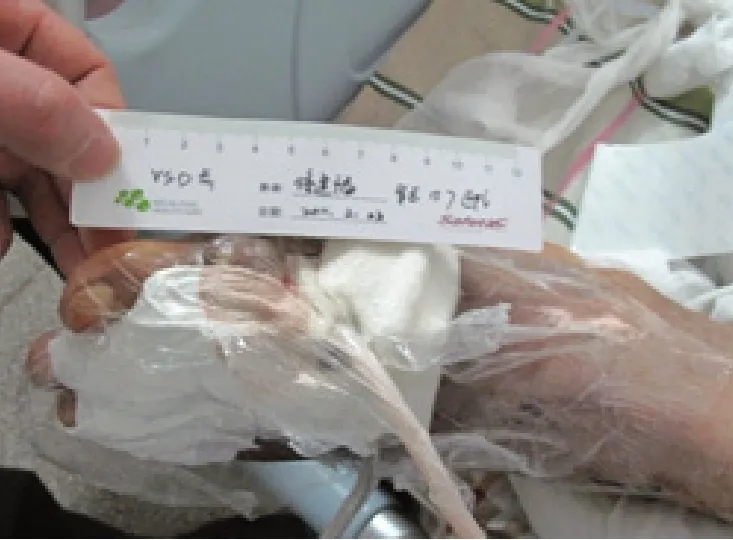
圖5 第1次VSD負壓吸引
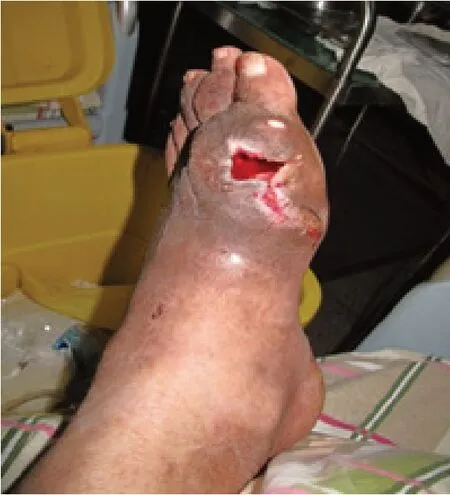
圖6 第1次負壓吸引后創面情況
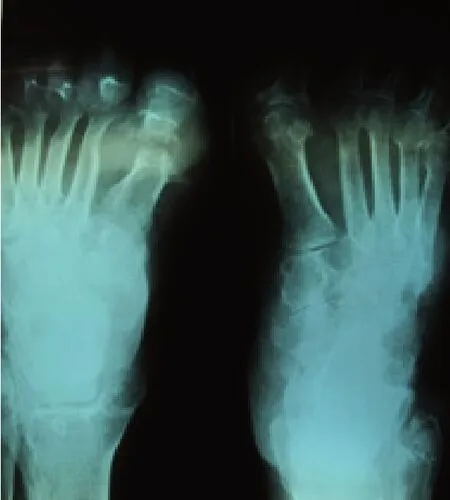
圖7 術后3周X線

圖8 術后40 d左足創面完全閉合
2 結果
采用痛風石手術刮除聯合VSD負壓吸引術治療巨大痛風石并骨破壞、軟組織壞死缺損患者16 例。其中優10例,良:5例,優良率:93.8%。差1例,該名患者合并糖尿病、腦梗死后遺癥、患肢偏癱、胃潰瘍及低蛋白血癥,營養狀況極差,雖經積極處理,創面愈合緩慢,最終患者及家屬選擇截趾處理。
3 討論
痛風是嘌呤代謝障礙和/或血尿酸升高引起的代謝性疾病,當尿酸濃度過高和(或)酸性環境下,尿酸可析出結晶,沉積在骨關節、腎臟及皮下組織等,造成組織病理性改變,導致痛風性關節炎、腎結石和痛風石等。病程長者發作期長而緩解期短,甚至有的患者遷延不愈,表現為痛風石性痛風[5]。痛風石體積逐漸增大,皮膚受損而破潰,可流出白色尿酸鹽結晶,對骨及關節產生腐蝕性破壞,手術對于痛風石以至破壞骨、軟骨及軟組織患者是必要的治療方法[6]。本組所治療16例患者均為巨大型痛風石形成并骨破壞、軟組織壞死缺損病例,主要表現在第1跖趾關節骨破壞、骨及軟組織缺損,治療體會如下。
3.1 擴創及爭取I期清除創內痛風石病變組織
痛風石系尿酸沉積,具有一定腐蝕性,不斷擴大的痛風石向外造成皮膚軟組織潰破壞死,向內侵蝕骨關節,所以治療重點是痛風石病變組織的徹底清除[7]。本組病例采用擴創切口,盡可能暴露病變組織,切除全部壞死軟組織,同時以刮勺配合沖洗槍徹底清除創內痛風石組織,尤其注意的是骨髓腔蟲嗜狀改變的骨破壞區,需配合咬骨鉗咬除髓腔病變骨質,打通髓腔,才能將可視下痛風石組織徹底沖洗干凈。
3.2 骨破壞及骨缺損處理
本組16例患者均出現不同程度骨破壞及骨缺損,徹底清除骨破壞區域修整斷面后,均直接將骨斷面對端連接,縫合周圍軟組織或克氏針固定穩定骨折,所有患者均未行I期植骨,主要考慮術后創面難以I期閉合,創面開放、骨外露無軟組織覆蓋,易導致植骨失敗,故僅以簡單內固定結合術后石膏托外固定維持患足骨缺損斷端的穩定。
3.3 術后引流
巨大痛風石破壞創面均未行I期閉合切口,這是因為痛風癥狀仍需進一步控制,不排除尿酸鹽結晶繼續滲出可能;二是敞開傷口,能徹底引流壞死組織及滲液。三是軟組織缺損較多,不能I期縫合關閉切口及創面,但擴創術后應根據局部皮瓣情況盡可能縮小創面,為二期閉合創面創造有利條件。
3.4 延期VSD負壓吸引
VSD負壓吸引技術的優點在于高效引流,去除了創面細菌培養基和受損組織產生的毒性產物,使毒性產物不進入機體造成重吸收,將開放變為閉合性創面,有效防止院內交叉感染的發生。同時促進創面血管新生、肉芽的生長,促進多種相關因子和酶類的基因表達、增殖和釋放,促進創面愈合[8-9]。本組16例患者均使用VSD負壓吸引,但在使用時間上是延期至術后1周,這是考慮術后創面仍有極少量尿酸鹽結晶滲出,VSD封閉創面后不易吸出,容易造成堵管,導致失敗(曾有1例患者經術中徹底清創已無肉眼痛風石,即行VSD負壓吸引,次日即出現堵管,予沖管灌洗及更換吸引管后仍引流不暢,拆除VSD后見少量尿酸鹽結晶梗阻管腔,改敞開換藥,1周后創面新鮮,無滲出后予以VSD負壓吸引直至痊愈)。所以筆者的治療經驗是術后縮小創面后持續敞開換藥5~7 d,待創面無尿酸鹽結晶滲出后,才予以VSD負壓吸引。通過1~3個療程的VSD負壓吸引術后,患者創面縮小,肉芽組織生長滿意,創面寬度少于2 cm者采用創緣皮瓣減張后拉攏縫合或碟形膠布固定直至愈合,寬度大于2 cm者,行游離植皮覆蓋創面,直至愈合。
3.5 綜合治療
手術治療僅為治療痛風性關節炎的措施之一,降低血尿酸的其他措施也是必需的[10]。本組16例患者在外科手術結合VSD治療同時,均積極予以抗痛風藥物治療痛風癥狀,根據血尿酸變化情況,逐漸調整用藥,同時調節患者飲食、改善微循環、控制血糖、加強營養及指導功能鍛煉等對癥支持治療,從而使患者內外結合,綜合治療,提高治愈率,預防復發。
綜上所述,痛風石刮除聯合VSD負壓吸引術療效顯著,能徹底清除病灶、及早關閉創面,提高治愈率,是治療巨大痛風石并骨破壞軟組織壞死的有效方法。

