低頻重復經顱磁刺激聯合鏡像療法對腦梗死患者上肢運動功能恢復的臨床研究
李菁,黃華垚,陳清法,陳振強
腦梗死是具有高致殘率的常見病,約2/3腦梗死患者遺留不同程度的肢體功能障礙,對患者的生存質量造成嚴重影響[1]。本研究將低頻重復經顱磁刺激(repetitive transcranial magnetic stimulation,rTMS)聯合鏡像療法(mirror therapy,MT)應用于腦梗死患者,旨在探討其對腦梗死患者上肢運動功能恢復的影響,為患者康復的優化策略提供依據。
1 資料與方法
1.1 一般資料 選取2017年2月~2018年1月在福建醫科大學附屬協和醫院康復醫學科住院治療的腦梗死患者60例。入選標準:符合1995年全國第四屆腦血管學術會議制定的診斷標準[2],經顱腦CT或MRI證實腦梗死;年齡35~70歲,首次發病,病程2周~6個月;病情平穩,意識清楚,無視覺障礙,無嚴重失語,可接受治療性指令;單側肢體癱瘓,患側上肢Brunnstrom分期II~IV期,肌張力改良Asworth分級≤Ⅱ級;坐位平衡至少達到1級;患側腦區運動誘發電位可測出;治療前患者本人或家屬簽署知情同意書。排除標準:病情不穩定,進展性卒中或出現繼發性腦出血;嚴重視聽障礙,言語或認知功能障礙,不能理解并配合指令;合并嚴重的心、肝、肺、腎等其他臟器疾病;既往有癲癇病史或正在服用抗癲癇藥物;有起搏器、體內有金屬植入物或顱骨缺損者;妊娠期婦女。剔除及脫落標準:不符合納入標準而誤入者;未按規定完成治療者;無法判斷療效或資料不全等影響療效判斷者。終止觀察標準:出現病情加重的應立即終止觀察;患者自行退出研究。將60例患者隨機分為觀察組和對照組各30例,所有患者均完成此次研究,治療期間未出現明顯不適而終止治療。2組患者一般資料比較差異無統計學意義。見表1。

表1 2組患者一般資料比較
1.2 方法 2組患者均接受常規的臨床藥物治療及規范的運動療法和物理因子治療。2組患者每天先進行rTMS治療,觀察組再進行MT治療,對照組進行常規作業治療。上述治療每日1次,每周6次,連續治療4周。 rTMS治療:采用武漢依瑞德公司出產的YRD CCY-I型經顱磁刺激儀,最大磁場強度為3T,磁刺激頻率為0~100Hz。治療前首先確定刺激位點,即在健側大腦初級運動皮質(M1區)尋找可引發健側拇短展肌最大運動誘發電位(motor envoked-potential,MEP)波幅的位點,即“運動熱點”[3],并在體表定位帽上標記好位置。另所有患者均測量靜息運動閾值(resting motor threshold,RMT),囑患者放松肌肉,用TMS刺激健側皮質相應的M1區標記處,給予較大強度單次刺激,后逐漸減少刺激強度,直至刺激10次最少引出5次運動誘發電位的幅度超過50uV的最小輸出量即為靜息運動閾值。治療時患者取仰臥位,8字線圈中點對準健側M1上肢區運動熱點并與顱骨相切,線圈柄朝后外側45°。磁刺激頻率1 Hz,以90%RMT的刺激強度連續刺激健側初級運動皮質(M1區)上肢投射區,刺激時間為20min,總刺激個數1200個,每日1次,每周6次,連續4周。觀察組患者在完成rTMS治療后即進行MT治療:患者坐于桌前,雙上肢之間的桌面上垂直放置一面鏡子(直徑60cm×60cm),鏡子鏡面朝向健側上肢,鏡子背面朝向患側上肢。囑患者觀察健側上肢運動成像,并想象成患側肢體在運動,同時要求患側上肢盡可能獨立執行與健側肢體一致的動作,包括上肢粗大及精細基本動作如取球、握球、持物、喝水、搭積木等功能性動作訓練,治療師提供必要的語言及運動輔助。每次訓練30min,每日1次,每周6 次,連續4周。對照組患者在完成rTMS治療后即進行常規作業治療:包括上肢關節活動度維持、肌力訓練、分離動作引導、手功能促通、深淺感覺訓練及進食、穿衣等ADL訓練。每次訓練30min,每日1次,每周6 次,連續4周。
1.3 評定標準 所有入選患者分別在治療前及治療4周后由專人對偏癱上肢運動功能和受累腦區的神經電生理指標進行評定。①簡化Fugl-Meyer上肢運動功能評分(Fugl-Meyer motor assessment,FMA):總分66分,受試者上肢運動功能越好則分值越高[4]。②上肢運動力指數(Motricity Index,MI):根據肩外展、屈肘和手指抓捏3個動作完成的肌力的情況進行評測,功能正常為100分,受試者上肢運動功能越好則分值越高[5]。③MEP潛伏期:刺激運動皮質開始至對側靶肌MEP出現的時間。首先確定刺激位點,然后將80%最大輸出強度的TMS刺激作用于患側大腦M1區刺激位點,并于患肢拇短展肌記錄動作誘發電位,取重復性好、波幅較大的5條波形,記錄其潛伏期值,其平均值即患肢拇短展肌記錄的MEP潛伏期。腦梗死患者受損半球MEP潛伏期延長。④中樞運動傳導時間(Central Motor Conduction time, CMCT):指從腦皮質到脊髓α前角運動神經元的傳導時間。將70%最大輸出強度的TMS刺激作用于患肢同側第7頸椎棘突旁,并于患肢拇短展肌記錄MEP,取重復性好、波幅較大的5條波形,記錄其潛伏期值,其平均值即患肢拇短展肌記錄的刺激C7神經根所得MEP潛伏期。刺激初級運動皮質引起的動作誘發電位潛伏期與刺激頸神經根引起的復合動作電位潛伏期之差即為CMCT[6]。腦梗死患者受損半球CMCT延長。
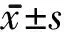
2 結果
2.1 2組患者治療前后FMA和MI評分比較 治療前2組患者FMA和MI評分差異無統計學意義。治療4周后,2組患者FMA和MI評分較治療前均明顯提高(均P<0.05),且觀察組2項評分均明顯高于對照組(均P<0.05),見表2。
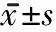
表2 2組患者治療前后FMA和MI評分比較分,
與治療前比較,aP<0.05;與對照組比較,bP<0.05
2.2 2組患者治療前后MEP潛伏期及CMCT比較 治療前2組患者MEP潛伏期和CMCT差異無統計學意義。治療4周后,2組患者MEP潛伏期和CMCT均較治療前縮短(均P<0.05),且觀察組MEP潛伏期和CMCT均較對照組更短(均P<0.05),見表3。

表3 2組患者治療前后MEP潛伏期及CMCT比較
與治療前比較,aP<0.05;與對照組比較,bP<0.05
3 討論
腦梗死造成的上肢功能障礙嚴重影響患者的自理能力和生活質量。如何更好地促進偏癱上肢運動功能的恢復也一直是康復研究的焦點之一。
重復經顱磁刺激作為一種非侵入性腦刺激技術,通過調節大腦皮質興奮性,恢復雙側大腦半球的平衡以促進腦梗死后運動功能恢復[7]。腦梗死發生后,雙側大腦半球間的抑制性平衡被打破,患側皮質對健側皮質抑制減弱,健側皮質對患側皮質抑制增強,因此患側運動皮質功能處于過度抑制狀態[8]。以低頻rTMS刺激腦梗死患者健側M1區,既降低健側運動皮質興奮性,又提高患側半球皮質興奮性,恢復雙側半球平衡,從而促進偏癱肢體運動功能恢復[9]。但有研究表明,單純rTMS若不聯合功能相關的行為學訓練,對偏癱患者肢體功能恢復的影響有限[10]。目前認為健側大腦半球低頻rTMS結合其他治療方法可以改善腦卒中后患者上肢功能,如肌力、耐力、協調性、靈敏性的提高[11]。陸操等[12]將低頻重復經顱磁刺激結合小組模式康復訓練,能有效改善腦卒中偏癱患者上肢及手功能,提高患者ADL能力。鏡像療法又稱鏡像視覺反饋療法,最初應用于幻肢痛的治療,現廣泛應用于腦卒中后運動功能障礙患者[13]。大量的臨床研究證實鏡像治療能提高腦卒中偏癱患者上肢的運動功能,而且對于急性期或慢性期患者,均有積極作用[14]。在進行鏡像療法時,患者持續觀察鏡中健側肢體的活動,想象成患側肢體活動,并模仿再學習,這樣持續的視覺反饋可以提高運動皮質興奮性,促進腦的功能重組[15]。Stefan等[16]報道實際執行動作和動作觀察均可激活頂額鏡像神經元系統從而促進大腦重塑。鏡像療法要求雙側肢體進行對稱性動作,這樣廣泛激活運動皮質區,促進肢體功能恢復[17]。此外,有研究證實,鏡像運動療法能減弱胼胝體的抑制作用,調節雙側大腦的平衡性,提高病灶側運動皮質的興奮性,有利于偏癱肢體運動功能的恢復[18]。
本研究將低頻重復經顱磁刺激聯合鏡像療法與低頻重復經顱磁刺激聯合常規作業療法對腦梗死患者偏癱上肢康復療效做了比較。研究結果表明2種治療方案均能改善梗死患者上肢功能,而且低頻rTMS聯合MT治療方案的療效優于低頻rTMS聯合常規作業療法方案。在神經電生理評價中,低頻rTMS聯合MT組的MEP潛伏期、CMCT縮短也更為顯著。MEP反映中樞運動傳導通路的功能,可反映運動神經元損害程度;CMCT則常用來評價皮質脊髓束的傳導性。腦梗死患者受損半球MEP潛伏期和CMCT均延長,且二者與神經功能缺損的嚴重性正相關[19],為腦梗死患者運動功能的預后提供重要臨床信息。從神經生理學角度看,運動功能的恢復通常顯示為錐體束功能的恢復。因此,低頻rTMS聯合MT治療較低頻rTMS聯合常規作業療法更能加快下行沖動傳導,從而增加α運動神經元或最終總通路在時間和空間上的總和,加快其興奮,從而促進患側肢體運動功能恢復。其可能的機制為:rTMS和MT均具有調節大腦皮質興奮性、恢復雙側大腦半球間的平衡以促進腦梗死后運動功能恢復;并且MT較常規作業療法相比,還能通過激活鏡像神經元系統、強化多種感覺反饋等方式以促進大腦功能重組,有助于上肢功能恢復;而且,先進行低頻rTMS治療后再予以MT治療,低頻rTMS抑制健側半球皮質,間接激活患側半球皮質,使患側運動皮質、鏡像神經元系統及相關聯腦區興奮性增高,提高MT激活鏡像神經元、重塑神經網絡的效率。
本研究表明,低頻重復經顱磁刺激聯合鏡像療法治療能提高腦梗死患者偏癱上肢運動功能,且療效優于低頻重復經顱磁刺激聯合常規作業療法治療。但如何尋找最佳的刺激參數從而取得更好的治療效果以及該研究的中、長期療效,需進一步臨床觀察和探索。

