SBHFRT和CFRT技術對NSCLC組織中淋巴細胞和細胞因子的影響*
岳宏程,熊良庚,張建文,林盛,傅少志,劉偉,彭紅菊
(1.西南醫科大學附屬醫院 腫瘤科,四川 瀘州 646000;2.重慶市巴南區人民醫院 腫瘤科,重慶401320;3.西南醫科大學附屬醫院 核醫學與分子影像四川省重點實驗室,四川 瀘州 646000)
肺癌是我國發病率和死亡率最高的腫瘤,其中非小細胞肺癌(non-small cell lung cancer, NSCLC)≥80%[1]。放療是NSCLC主要治療措施之一,合適的放療模式可增加腫瘤組織中抗腫瘤淋巴細胞表達和細胞因子含量,增強抗腫瘤作用[2-3]。而單次近距離大分割放療(single brachytherapy hypofractionated radiotherapy, SBHFRT)是否增強腫瘤組織中抗腫瘤淋巴細胞表達和細胞因子含量,目前少有報道。本研究探討SBHFRT和常規放療(conventional fractionation radiotherapy, CFRT)對NSCLC腫瘤組織中淋巴細胞表達和細胞因子含量的影響,為NSCLC放療方案的制定和聯合免疫治療提供依據。
1 材料與方法
1.1 材料
1.1.1 荷瘤小鼠模型復制 取對數生長的Lewis細胞株(西南醫科大學附屬醫院腫瘤科)接種于4、5周齡,體重16~22 g健康C57BL/16雌性小鼠(重慶騰鑫華阜生物科技公司,合格證編號:11401300024918,SPF級飼養)右后肢根部皮下。觀察記錄小鼠一般狀態、體重、成瘤情況及瘤體積變化。待移植瘤直徑達8~10 mm時,分成對照組、CFRT組、SBHFRT組進行實驗,每組12只小鼠。其中6只用于觀察腫瘤體積和代謝情況,其余6只用于淋巴細胞和細胞因子的檢測。
1.1.2 主要實驗儀器與設備 直線加速器(瑞典Elekta有限公司),石蠟切片機(德國萊卡儀器有限公司),新型BGZ系列Ⅱ型高精度烤箱(上海博訊實業有限公司),移液器(德國艾本德公司),倒置相差顯微鏡(日本奧林巴斯公司),Oncentra brachy TPS近距離治療計劃系統、Ir192三維后裝近距離治療機購自荷蘭Nucletron Netherlands公司。
1.2 方法
1.2.1 主要實驗試劑 DMEM高糖培養液(美國HyClone公司),胎牛血清(美國Gibco公司),抗小鼠CD4、CD8、Foxp3單克隆抗體(美國Bio-world公司),白細胞介素10(Interleukin-10, IL-10)、白細胞介素12(Interleukin-12, IL-12)及γ干擾素(Interferon-γ,INF-γ)檢測試劑盒購自北京安迪華泰生物科技有限公司。
1.2.2 實驗分組 ①CFRT組:Dt=20 Gy/10 d,放射源為6 MV X射線,源皮距100 cm,從接種后第19天開始放療,連續放療5 d后間隔2 d再連續放療5 d,接種后第30天放療結束;②SBHFRT組:于接種后第30天開始放療,沿腫瘤長軸方向植入施源器(依腫瘤大小植入1或2根),行模擬定位CT掃描,在Oncentra brachy TPS勾畫大體腫瘤靶區,設計和實施放療計劃(Dt=11.3 Gy/1F,D95%≥10 Gy),只放療1 d。按L-Q模型計算生物等效劑量(biological equralent dose, BED)( 腫 瘤 α/β=10),CFRT組 BED=24 Gy,SBHFRT組BED=24.07 Gy,兩者BED基本相同。
1.2.3 CD4+、CD8+及Foxp3+T淋巴細胞表達檢測放療結束后第14天,每組處死6只小鼠,完整剝離腫瘤,切取部分腫瘤用于酶聯免疫吸附(ELISA)檢測,其余腫瘤組織采用免疫組織化學SP法檢測腫瘤組織中CD4+、CD8+及Foxp3+T淋巴細胞表達,由2位經驗豐富的病理科醫生分別獨立對實驗結果進行雙盲法評估。CD4+、CD8+及Foxp3+T淋巴細胞表達判斷標準:CD4+、CD8+T淋巴細胞染色為細胞質或細胞膜呈棕黃色或褐色,Foxp3+T淋巴細胞染色為細胞核呈棕黃色或褐色。CD4+、CD8+及Foxp3+T淋巴細胞數計算方法:每張切片選5個視野,顯微鏡(400倍)下計數每個視野陽性淋巴細胞數,計算5個視野陽性淋巴細胞數平均值即為該切片陽性淋巴細胞數。
1.2.4 IL-10、IL-12及INF-γ含量檢測 采用ELISA法檢測腫瘤組織中IL-10、IL-12及INF-γ含量。具體操作:將腫瘤組織磨碎取上清液,用洗液清洗酶孔板,每孔加樣本稀釋液和檢測緩沖液,加等量樣本,加檢測抗體(1∶100),封板震蕩,室溫孵育2 h,洗板,加HRP標記的鏈霉親和素(1∶100),封板震蕩,室溫孵育45 min,洗板,TMB顯色,避光室溫孵育30 min,加終止液。調節酶標儀波長為450 nm測定吸光度值。依據標準曲線計算各樣本IL-10、IL-12及INF-γ的含量。
1.2.5 腫瘤體積的測量和生長抑制率(tumor growth inhibition rate, TGIR)的計算 各組從腫瘤接種后第12天開始,每隔2 d測量各組移植瘤最大直徑(a)與最小直徑(b),腫瘤體積(V):V=a×b2/2。放療后第14天計算各治療組TGIR。TGIR=(V對照組-V實驗組)/V對照組×100%。
1.2.6 腫瘤代謝活性檢測 放療結束后第14天,每組選6只小鼠分別行18F-FDG micro PET/CT掃描。18F-FDG micro PET-CT掃描參數:80 kV;500μA;層距1.5 mm。掃描圖像由2位經驗豐富的核醫學科醫師對18F-FDG PET/CT圖像進行分析,計算腫瘤組織SUV。SUV值高低反映腫瘤代謝活性,即腫瘤SUV值越小表示腫瘤代謝活性越低。
1.3 統計學方法
數據分析采用SPSS 17.0統計軟件。計量資料以均數±標準差(±s)表示,多組比較用單因素方差分析,兩兩比較用LSD-t檢驗;計數資料以率(%)表示,比較用t檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 3組CD4+、CD8+及Foxp3+ T淋巴細胞表達水平比較
3組CD4+、CD8+及Foxp3+T淋巴細胞表達水平比較,經單因素方差分析,差異有統計學意義(P<0.05)。進一步兩兩比較,SBHFRT組CD4+、CD8+T淋巴細胞表達高于CFRT組和對照組,而Foxp3+T淋巴細胞表達低于CFRT組和對照組(P<0.05)。見表1和圖1。
表1 3組CD4+、CD8+及Foxp3+ T淋巴細胞表達水平比較 (n =6,個,±s)
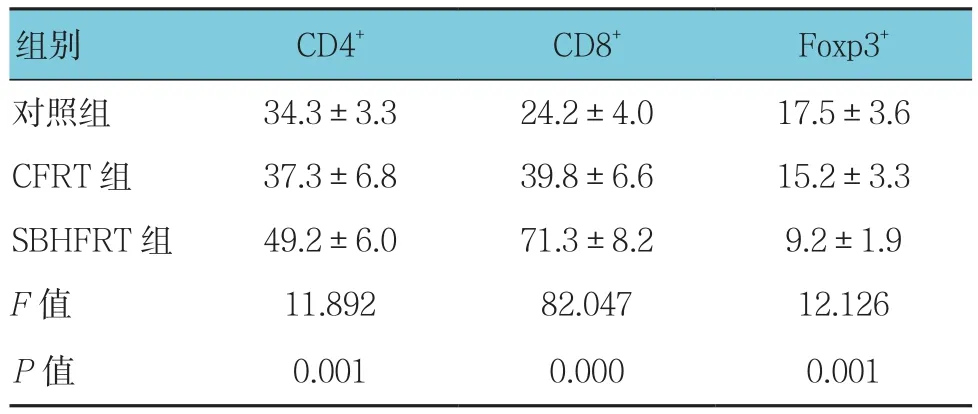
表1 3組CD4+、CD8+及Foxp3+ T淋巴細胞表達水平比較 (n =6,個,±s)
組別 CD4+ CD8+ Foxp3+對照組 34.3±3.3 24.2±4.0 17.5±3.6 CFRT 組 37.3±6.8 39.8±6.6 15.2±3.3 SBHFRT 組 49.2±6.0 71.3±8.2 9.2±1.9 F值 11.892 82.047 12.126 P值 0.001 0.000 0.001
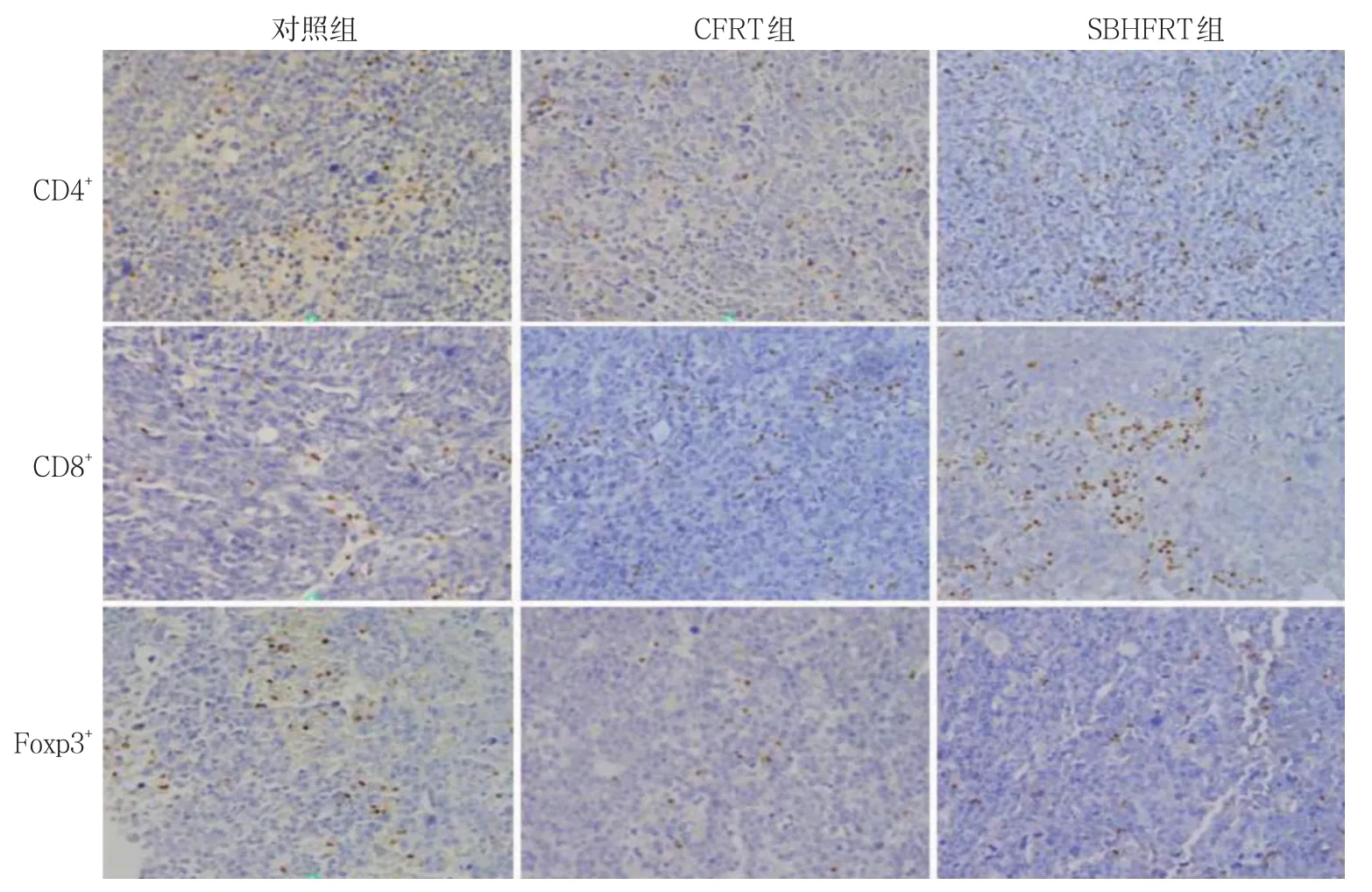
圖1 3組CD4+、CD8+及Foxp3+ T淋巴細胞的表達 (SP×400)
2.2 3組IL-10、IL-12及INF-γ含量比較
3組IL-10、IL-12及INF-γ含量比較,經單因素方差分析,差異有統計學意義(P<0.05)。進一步兩兩比較,SBHFRT組IL-12和INF-γ含量高于CFRT組和對照組(P<0.05);而IL-10含量低于CFRT組和對照組(P<0.05)。見表2。
2.3 3組腫瘤體積、腫瘤SUV值比較
3組腫瘤體積、腫瘤SUV值比較,經單因素方差分析,差異有統計學意義(P<0.05)。進一步兩兩比較,SBHFRT組腫瘤體積、腫瘤SUV值低于CFRT組和對照組(P<0.05)。見表3和圖2。
2.4 SBHFRT組和CFRT組TGIR比較
SBHFRT組、CFRT組TGIR分別為(37.0±2.5)%和(19.2±3.2)%。兩組TGIR比較,經t檢驗,差異有統計學意義(t=10.701,P=0.000);SBHFRT組TGIR高于CFRT組。
表2 3組IL-10、IL-12及INF-γ含量比較(n =6,pg/ml,±s)
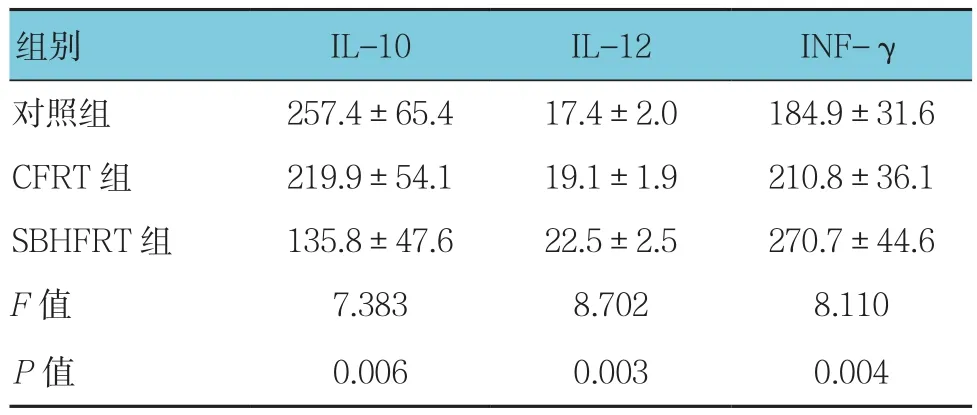
表2 3組IL-10、IL-12及INF-γ含量比較(n =6,pg/ml,±s)
組別 IL-10 IL-12 INF-γ對照組 257.4±65.4 17.4±2.0 184.9±31.6 CFRT 組 219.9±54.1 19.1±1.9 210.8±36.1 SBHFRT 組 135.8±47.6 22.5±2.5 270.7±44.6 F值 7.383 8.702 8.110 P值 0.006 0.003 0.004
表3 3組腫瘤體積、腫瘤SUV值比較 (n =6,±s)
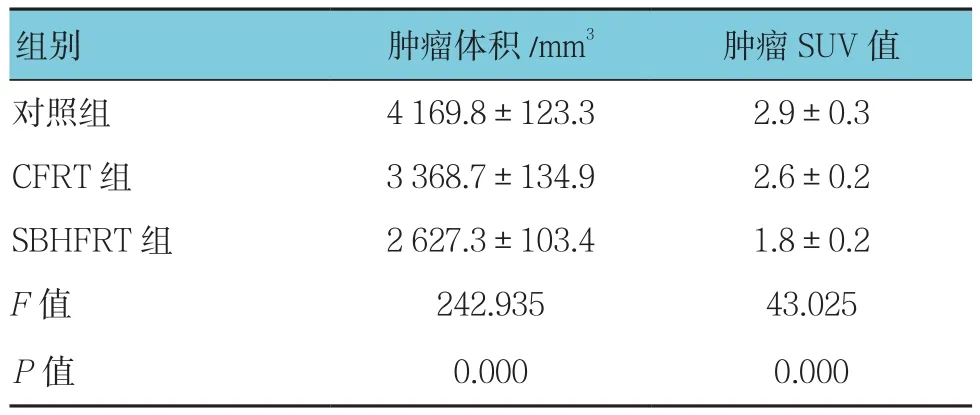
表3 3組腫瘤體積、腫瘤SUV值比較 (n =6,±s)
組別 腫瘤體積/mm3 腫瘤SUV值對照組 4 169.8±123.3 2.9±0.3 CFRT 組 3 368.7±134.9 2.6±0.2 SBHFRT組 2 627.3±103.4 1.8±0.2 F值 242.935 43.025 P值 0.000 0.000
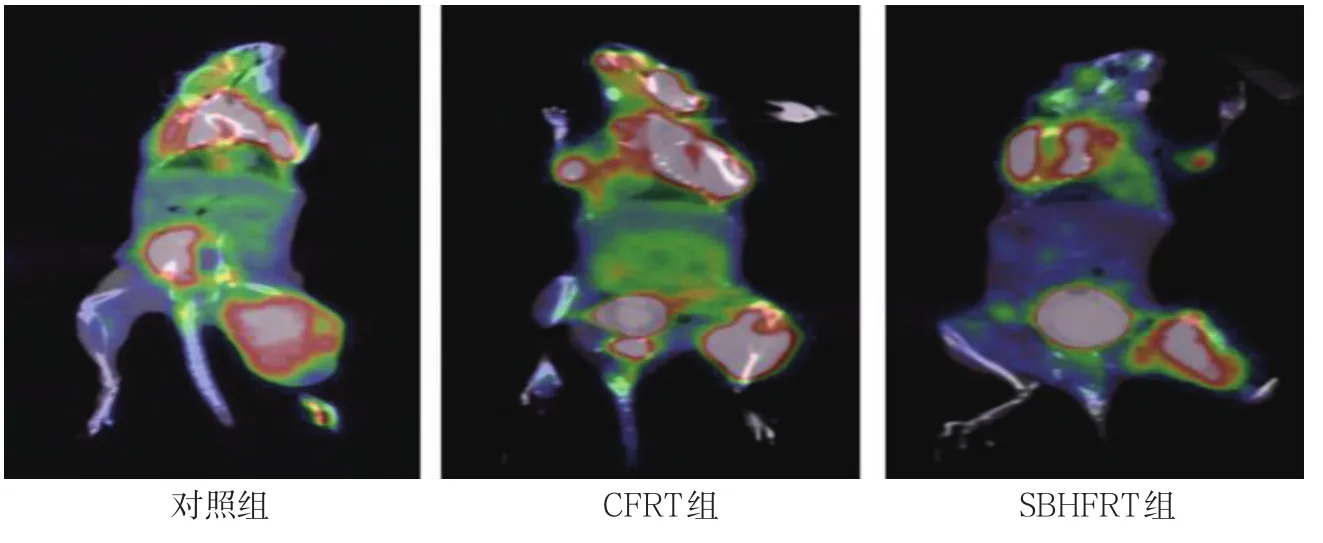
圖2 3組18F-FDG micro PET-CT掃描圖
3 討論
以立體定向放療(stereotactic body radiotherapy,SBRT)為代表的大分割放療能提高cT3和cT4N0M0期NSCLC患者的2年總生存率(overall survival, OS)和局部控制率[4]。NSCLC行SBHFRT放療研究較少,缺乏基礎性研究。對臨床NSCLC原發灶行SBHFRT聯合縱隔轉移淋巴結調強放療研究發現,其有效率、2年OS分別為92.3%和67%,中位生存期22.5個月[5]。上述結果表明,SBHFRT與SBRT能有效提高NSCLC治療的有效率和患者生存期。
腫瘤微環境的組成和作用十分復雜[6-7],對抗腫瘤免疫有抑制作用[8-10]。研究表明,放療可改變腫瘤微環境中淋巴細胞和細胞因子的組成,增強抗腫瘤免疫反應[11-13]。NSCLC腫瘤組織中CD4+、CD8+及Foxp3+T淋巴細胞表達與放療生存期密切相關,腫瘤組織中CD4+、CD8+T淋巴細胞高表達,中位生存期和3年生存率均高于低表達和無表達;而Foxp3+T淋巴細胞低表達中位生存期和3年生存率均高于高表達[14-15]。上述研究表明,增加腫瘤組織中CD4+、CD8+T淋巴細胞表達,降低Foxp3+T淋巴細胞表達,可提高腫瘤患者生存期和生存率。本研究結果提示,NSCLC行SBHFRT治療相對于CFRT治療,能有效聚集抗腫瘤淋巴細胞的能力,和其他學者報道類似[15-17]。
細胞因子在抗腫瘤免疫反應中發揮重要的作用,IL-12能誘導IFN-γ的產生,后者可刺激CD8+T淋巴細胞增值和活化,在抗腫瘤免疫反應中發揮正向調節作用[18]。IL-10由腫瘤細胞分泌的一種免疫抑制因子,其不僅可抑制腫瘤細胞凋亡,還有對抗FIN-γ作用,抑制抗腫瘤免疫反應[19]。本研究表明,SBHFRT較CFRT可增加腫瘤組織中IL-12和INF-γ含量,降低IL-10含量,更利于促進淋巴細胞增殖和腫瘤細胞凋亡,增強放射線作用。
腫瘤SUV值對腫瘤代謝情況及預后評估具有重要指導意義[20]。本研究通過PET-CT檢測各組腫瘤SUV值顯示,放療后SBHFRT組腫瘤代謝低于CFRT組和對照組;同時本研究顯示,SBHFRT在控制腫瘤體積和TGIR方面優于CFRT組,其機制可能與SBHFRT增加腫瘤組織中CD4+、CD8+T淋巴細胞浸潤和IL-12、INF-γ含量,從而增強抗腫瘤作用有關。
綜上所述,SBHFRT比CFRT更能促進肺癌腫瘤組織中抗腫瘤淋巴細胞浸潤,以及增加具有腫瘤殺傷作用的細胞因子IL-12和INF-γ含量,更有利于增強放療效應。但SBHFRT促進腫瘤組織中上述物質增加的最佳放療分割劑量,有待進一步研究。

