地西他濱方案治療骨髓增生異常綜合征及急性髓系白血病療效分析*
石 林,楊懿春,潘 暉,肖 青,陳建斌,唐曉瓊,張紅賓,劉 林,王 利
(重慶醫(yī)科大學附屬第一醫(yī)院血液科,重慶 400016)
骨髓增生異常綜合征(MDS)是一種克隆性造血干細胞疾病,特點是髓系細胞分化及發(fā)育異常,表現(xiàn)為病態(tài)造血及無效造血,難治性血細胞減少,造血功能衰竭,高風險向急性髓系白血病(AML)轉化[1-2]。AML是一種以骨髓和外周血中原始及幼稚性髓系細胞異常增生為特點的惡性腫瘤[3]。地西他濱是一種2′-脫氧胞苷類似物,特異性DNA甲基轉移酶抑制劑,低劑量能誘導DNA去甲基化,激活沉默失活的抑癌基因和造血細胞分化,高劑量則有細胞毒作用[4-5]。本研究中回顧性分析了使用含地西他濱方案治療血液系統(tǒng)腫瘤,包括各型骨髓增生異常綜合征(MDS)和AML的療效和不良反應。現(xiàn)報道如下。
1 資料與方法
1.1 一般資料
納入標準:根據(jù)骨髓和外周血涂片細胞分類計數(shù)、骨髓流式免疫表型分析、染色體核型分析、骨髓活檢等實驗室檢查,符合《骨髓增生異常綜合征診斷與治療中國專家共識(2014)》[6]和《成人急性髓系白血病(非急性早幼粒細胞白血病)中國診療指南(2017年版)》[7]診斷標準;臨床資料完整;本研究已獲得醫(yī)院醫(yī)學倫理委員會批準,患者均簽署知情同意書。
排除標準:未規(guī)律化學治療(簡稱化療);治療過程中資料不完整。
病例選擇與分組:選取我院2016年1月至2017年6月收治的MDS患者21例和 AML患者63例。21例MDS患者中,15例行MDS預后基因和融合基因檢測,其中4例存在基因突變;19例行染色體檢查,其中1例存在染色體核型異常,4例存在FISH檢測異常(檢查5q,7q,20q,+8)。63例 AML 患者中,41例行 AML 預后基因和融合基因檢測,其中22例存在基因突變;29例行染色體檢查,其中10例存在染色體核型異常,2例存在 FISH 檢測異常(檢查 5q,7q,20q,+8)。根據(jù)隨機原則,將 MDS患者分為 A組(10例)和 B組(11例),將AML患者分為C組(20例)和D組(43例)。患者一般資料比較,差異無統(tǒng)計學意義(P>0.05),具有可比性。詳見表1和表2。

表1 MDS患者一般資料比較(n=21)

表2 AML患者一般資料比較(n=63)
1.2 方法
A組和C組均為單藥治療,方案為注射用地西他濱(正大天晴藥業(yè)集團股份有限公司,國藥準字H20120066,規(guī)格為每支 50 mg)20 mg /(m2·d),靜脈滴注,第1~5天。化療周期A組為2.5個,C組為2.6個。B組和D組均為聯(lián)合化療,方案為D-CAG,包括地西他濱 20 mg/(m2·d),靜脈滴注,第 1~5 天;阿柔比星10 mg,靜脈滴注,第3~10天;阿糖胞苷15 mg,靜脈滴注,每 12 h 1次,第 3~16天;粒細胞集落刺激因子(G -CSF)300 μg,皮下注射 ,第 3~16 天 [白細胞(WBC)>20×109/L時停用]。化療周期 B 組為 2.5個,D組為2.4個。血小板低于20×109/L者給予輸入機采血小板,血紅蛋白低于60 g/L者給予輸注紅細胞懸液。如果出現(xiàn)發(fā)熱等感染征象,經(jīng)驗性使用廣譜抗生素,同時積極查找病原菌。根據(jù)血培養(yǎng)、痰培養(yǎng)、G試驗、GM試驗、病毒篩查及胸部CT等檢查結果及時調整抗生素。若治療3~5 d后體溫仍未得到控制,應結合真菌感染的證據(jù)加用抗真菌藥物治療。治療3個療程,每個療程結束后2周復查,評價療效。
1.3 療效判定標準[8]
治療結束2周復查骨髓穿刺,判定療效。完全緩解(CR):癥狀、體征全部消失,中性粒細胞計數(shù)、血小板計數(shù)恢復正常,骨髓原始粒細胞所占比例在5%以下;部分緩解(PR):癥狀、體征已顯著改善,中性粒細胞計數(shù)、血小板計數(shù)基本恢復正常,骨髓原始粒細胞所占比例為5% ~20%;未緩解(NR):癥狀、體征及骨髓均無改善。總緩解=CR+PR。不良反應按世界衛(wèi)生組織(WHO)化療藥物不良反應分析標準判定。
1.4 統(tǒng)計學處理
采用SPSS 19.0統(tǒng)計軟件進行分析。臨床特征及療效采用中位數(shù)(范圍)、百分率表示,比較行 χ2檢驗,指標評分行Fisher精確概率法檢驗;生存曲線比較經(jīng)Log Rank檢驗。P<0.05為差異有統(tǒng)計學意義。
2 結果
2.1 臨床療效
84例 MDS/AML 患者中,完全緩解(CR)59例(70.23%),部分緩解(PR)11 例(13.10%),總有效率為 83.33%(70/84)。不同方案對 MDS和 AML的療效結果見表3。可見,A組和B組、C組和D組相比,差異均無統(tǒng)計學意義(P=1.000>0.05)。對可能存在影響療效的因素進行Fisher精確概率法檢驗,結果見表4和表5。

表3 不同方案對MDS和AML的臨床療效比較[例(%)]

表4 不同臨床特征對MDS治療效果的影響
隨訪21例MDS及63例AML患者的生存情況,繪制生存曲線(圖1),并對兩組數(shù)據(jù)進行時序檢驗,可見,MDS患者使用地西他濱方案化療后隨訪總生存率高于AML患者,但差異無統(tǒng)計學意義(P=0.208)。
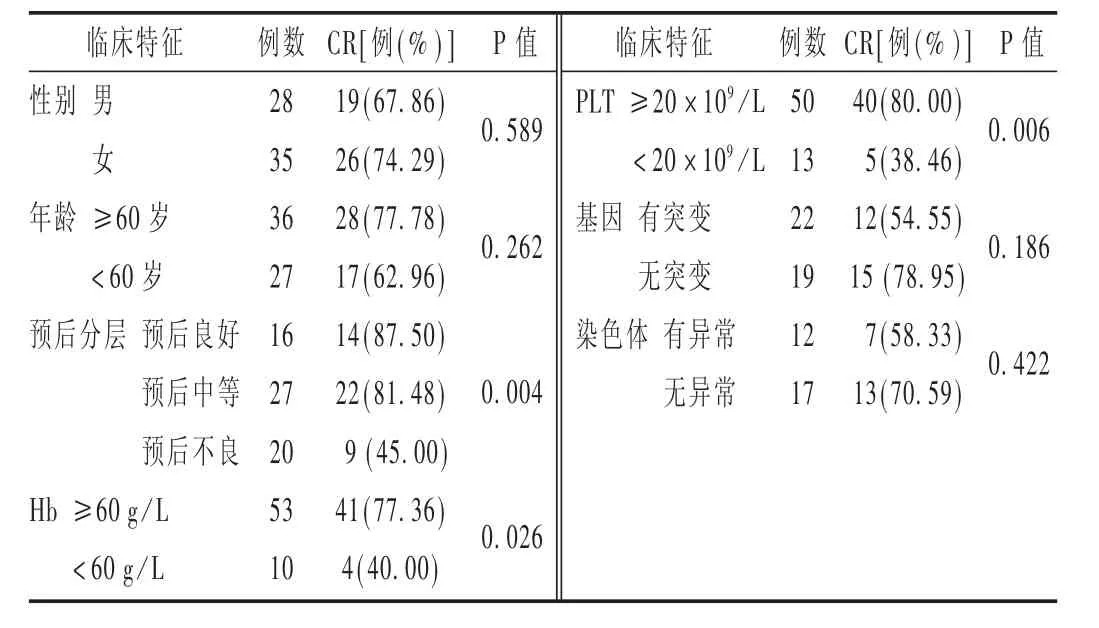
表5 不同臨床特征對AML患者治療效果的影響

圖1 MDS/AML患者生存曲線
2.2 不良反應
骨髓抑制:中性粒細胞計數(shù) <0.5×109/L發(fā)生率為 85.71%(72 /84),中位持續(xù)時間為 14(0 ~ 23)d。血小板計數(shù) < 20×109/L 發(fā)生率為 82.14%(69/84),中位持續(xù)時間為16(0~23)d。其中,Ⅳ級骨髓抑制的發(fā)生率為78.57%(66/84),余18例骨髓抑制較輕。
感染:化療期間感染發(fā)生率為 52.38%(44 /84),其中肺部感染發(fā)生率為50.00%(42/84),肺部細菌合并真菌感染率為26.19%(22/84),上呼吸道感染和敗血癥各4例,消化道感染和尿路感染各1例,且部分患者合并多部位感染。肝、腎功能及凝血功能受損少見。絕大多數(shù)患者經(jīng)積極抗感染可控制,但仍有4例(4.76%)患者發(fā)生嚴重感染,最終死亡。
3 討論
地西他濱能抑制DNA甲基化轉移酶的活性,使抑癌基因得以重新表達,是MDS/AML患者的治療新選擇[9]。WU等[10]發(fā)現(xiàn),地西他濱與阿糖胞苷在殺傷髓系原始細胞上有協(xié)同作用,故地西他濱聯(lián)合CAG方案可能比單藥能取得更好的療效。L譈BBERT等[11]分別用地西他濱單藥和支持治療的方法治療233例高危老年MDS患者,結果顯示,地西他濱組明顯延長MDS向AML的轉化時間,改善了患者的生活質量。GARCIAMANERO等[12]在分析856例MDS患者后得出IPSS評分、年齡不小于60歲、血小板小于50×109/L、原始細胞計數(shù)不低于4%等具有明顯的預后意義。本研究中21例MDS患者中,多數(shù)老年、預后評估較差、不良基因突變和一般情況較差的患者選用單藥方案化療,但對上訴因素進行多變量分析未得出類似結論,可能與樣本量不足和化療方案的選擇偏移有關。SCANDURA等[13]研究30例AML患者標準DA方案前予以地西他濱,完全緩解57%,部分緩解33%,不良反應與單用DA方案相似。本研究中,地西他濱方案對AML的治療,緩解率高于上述研究,提示使用含地西他濱的化療方案療效高于DA方案,但仍需進一步擴大樣本量進行驗證。
GHANEM等[14]研究分析了122例使用地西他濱方案治療MDS患者的數(shù)據(jù),結果發(fā)現(xiàn),地西他濱治療有血液學毒性反應,且聯(lián)合方案更易出現(xiàn)嚴重的骨髓抑制和繼發(fā)感染。本研究中不良反應與其相關研究類似。感染以肺部感染多見,細菌感染為主,細菌合并真菌感染也較為常見,少數(shù)患者合并敗血癥、消化道感染、尿路感染,甚至合并多部位感染,但經(jīng)積極預防和抗感染治療均有效。故在使用地西他濱方案治療MDS/AML過程中,應警惕感染相關并發(fā)癥的出現(xiàn),并積極預防感染及有效抗感染治療。
此外,L譈BBERT等[15]對復雜核型AML的治療中,地西他濱10 d方案可使患者獲得75%的總反應率(在16例患者中,CR 8例,PR 4例);而在7號染色單體或del(7q)的AML患者中反應率高達91%。提示含染色體異常的患者對地西他濱化療方案敏感。本研究中,染色體異常AML患者12例,化療后,CR 7例,與同類研究結果一致。但與無染色體異常組比較,差異無統(tǒng)計學意義(P=0.422)。該結果可能與基因或染色體異常的患者樣本量不足有關,需進一步擴大樣本量研究。
有研究發(fā)現(xiàn),隨著地西他濱使用的療程數(shù)增加,血液學毒性將逐漸下降[16]。本研究中觀察結果與之相符,部分患者隨療程增加后骨髓抑制期逐漸縮短,甚至無明顯骨髓抑制出現(xiàn),且感染發(fā)生也較之前減少,耐受程度逐漸升高。可見,首程緩解后的鞏固和維持治療時骨髓抑制程度較輕,時間縮短,出現(xiàn)嚴重并發(fā)癥的概率減少。
綜上所述,地西他濱單藥或聯(lián)合化療治療MDS/AML,療效確切,緩解率高,不良反應少,相對安全。隨療程的增加,其療效及不良反應均有一定提高,需增強患者對該藥的耐受性。

