新劑型藥物血漿中游離藥物濃度研究方法概述
摘 要 新劑型藥物改善了血漿中游離藥物濃度比率,從而降低毒性提高藥效,因而檢測血漿中游離藥物濃度具有重要意義。新劑型藥物游離濃度測定和藥物血漿蛋白結合率測定有一定差別,主要在于新劑型藥物引入的新的外源性蛋白(或其他影響藥物游離率的輔料),存在血漿中蛋白特異性差異大、蛋白濃度變化大和游離藥物濃度較低三方面問題。因而一般血漿蛋白結合率試驗的方法不一定都適用于新劑型藥物游離濃度測定。本文就常見的游離藥物濃度測定方法(超速離心法、超濾法、平衡透析法和快速平衡透析法)及其優缺點和適用范圍做一個概要介紹,為新劑型藥物的研發提供幫助。
關鍵詞 游離藥物濃度 超速離心 超濾 平衡透析
中圖分類號:R969.1 文獻標志碼:A 文章編號:1006-1533(2019)07-0074-04
Summary of research methods for free concentration of new dosage forms drug in plasma
MA Zhiyu*
(Shanghai Pharmaceuticals Holding Co., Ltd., Shanghai 201203, China)
ABSTRACT New dosage forms such as albumin binding and micelles can improve the solubility and targeting of drugs, reduce the adverse drug reactions drugs and increase the dose tolerance. These are all achieved by improving the ratio of free drug concentration in plasma, so it is important to determinate the concentration of free drug in plasma. In this paper, the common methods such as ultracentrifugation, ultrafiltration, equilibrium dialysis and rapid equilibrium dialysis for the determination of free drug concentration and their advantages and disadvantages and the scope of application are briefly introduced so as to provide assistance for the development of new dosage forms.
KEY WORDS free drug concentration; ultracentrifugation; ultrafiltration; equilibrium dialysis
近年來,隨著藥物新劑型的不斷發展創新,許多如紫杉醇一類的溶解度差的、毒性大的藥物越來越多被制成了白蛋白結合型、膠束等新劑型。這些新劑型增加了藥物的溶解性和靶向性,從而降低藥物本身及其助溶劑帶來的不良反應,提高給藥耐受劑量從而增加療效,并通過緩釋延長藥物半衰期以延長給藥間隔,提高患者的用藥依從性。而以上這些優勢,都是因為新劑型改變了藥物在血漿中游離比才實現的[1-3]。
眾所周知,藥物進入體循環發揮藥效,需在體內溶解和吸收。藥物吸收進入血液后,存在兩種狀態,一種是血漿蛋白結合型,一種是血漿蛋白未結合型(即游離型)。而藥物在體內的組織分布方式,主要是由血漿中游離藥物完成的。因此,研究游離藥物濃度,對評價新劑型藥物的藥效和毒性都具有重要意義[4-6]。
雖然研究新劑型藥物的游離藥物濃度和研究藥物血漿蛋白結合率有一定相似之處,但也有明顯差別:①新劑型藥物中往往含有外源性白蛋白之類助溶或靶向作用輔料,與人體內源性血漿蛋白會有一點差異;②新劑型藥物在體內的血漿蛋白結合率往往隨著給藥后時間而變化,這是由于外源性白蛋白逐漸被降解,藥物釋放改變或藥物周邊蛋白濃度改變造成的;③游離藥物濃度往往比較低,常常小于1 ng/ml。故許多適用于蛋白結合率測定的方法,諸如毛細管電泳、圓二色譜法等,由于蛋白特異性差異大、蛋白濃度變化大和游離藥物濃度較低的問題,并不適用測定游離濃度[7-9]。
目前用于測定血漿中游離藥物濃度的處理方法主要有以下四種:超速離心法、超濾法、平衡透析法和快速平衡透析法。本文將對這四種常見方法進行詳細概述,為游離藥物濃度的測定提供幫助,從而為新劑型藥物的研究和毒性評價提供幫助。
1 超速離心法
即含藥物的血漿樣品放專用的離心管中,用超速離心機于100 000 g、37 ℃離心15 h。離心后取上清液測定。
此方法優點為:①操作步驟簡單,直接取樣離心即可;②由于樣品不經過任何膜,僅在離心管中,故不存在樣品吸附問題。其缺點也較為明顯:①由于樣品需要在37 ℃下離心15 h,故血漿應在37 ℃、15 h內穩定;②需要借助昂貴的專用的超速離心機,且每次只能離心10~24個左右樣品,每次離心需要15 h,對于擁有大量樣品的藥動學和等效性試驗不適用;③由于新劑型中存在白蛋白之類非血漿內源性蛋白,離心后的血漿樣品存在一個濃度梯度,即最下層為結合蛋白的藥物,最上層為游離藥物,而中間層則兩種狀態藥物都存在。故在最終取樣測定時,取樣位置會顯著影響測定結果。
此方法適用于血漿穩定性好、樣品數量少、用其他方法會存在吸附藥物的游離濃度測定。r(游離藥物)=最上層游離藥物濃度[10-11]。
2 超濾法
即在超濾膜樣品側加入含藥物的血漿,用離心力之類外力使血漿部分通過超濾膜(于37 ℃離心),超濾膜有特定的分子質量截止值(如30 kDa),最終游離的藥物進入超濾膜的另一側,而蛋白結合型的藥物則留在樣品側。
此方法的優點如下:①超濾膜裝置相對于超速離心機易于獲得,且價格相對便宜;②樣品制備時間短,通常一次約20 min左右,適用于大量樣品測試;③由于制備時間短,適合血漿穩定性較差的藥物。其缺點如下:①不適用于吸附性藥物,即藥物若在超濾膜上吸附,則該方法不適用;②超濾膜使用前需活化,相對比較麻煩;③不同廠家和材料的超濾膜重現性相對較差。
此方法應用的前提是藥物在超濾膜上不被吸附。若樣品吸附性驗證通過,且對藥物血漿穩定性的要求較低,可用于大量樣品的測試。r(游離藥物)=濾過層的藥物濃度[9-15]。
3 平衡透析法
即用平衡透析膜分開等體積的含藥物血漿和緩沖液,由于平衡透析膜有特定的分子質量截止值(如30 kDa)。通過24 h(37 ℃)平衡孵化,蛋白結合型藥物無法通過透析膜,而游離型藥物側分布到了緩沖液一側。
此方法的優點如下:①平衡透析法為游離藥物測定最基本的方法,因此測定結果最能體現游離藥物濃度。②平衡裝置相對經濟便宜,平衡透析膜也比較常見。缺點如下:①孵化時間長,需24 h,不適合血漿穩定性差的藥物;②因時間長,且每次孵化樣品量少,故不適合大量樣品的測試;③由于樣品要接觸透析膜,故不適合吸附性強的藥物;④透析膜廠家和材質較多,不同透析膜對試驗結果有影響;⑤透析膜使用前需活化。
此方法需化合物血漿穩定性好,樣品在透析膜上不吸附,且只適用于少量樣品。r(游離藥物)=緩沖液層的藥物濃度[7-11, 16-19]。
4 快速平衡透析儀法
即用快速平衡透析儀進行游離藥物的測定。是平衡透析法的改進版,由于渦旋力存在和透析面積的擴大,平衡透析時間從24 h縮短至4 h。透析膜兩側,即血漿樣品側和緩沖液側的試驗加入體積不同,目的在于扣除藥物吸附的問題。
此方法的優點如下:①此裝置一次可以制備48個樣品,且孵化時間僅為4 h,適用于大量樣品測試;②該儀器兩側(血漿和緩沖液)體積不同,已排除吸附干擾,故適合吸附性強藥物;③孵化時間相對短,且最終計算方式為測定兩側濃度,已扣除穩定性干擾,故適合血漿穩定性差的藥物;④該透析膜已經批量生產,試驗溫度和CO2濃度固定,故其重現性較好;⑤該透析膜可同時測定已知結果的陽性藥物作為對照,保證試驗過程的可靠性。缺點如下:①快速平衡透析膜為消耗品,單個膜價格相對較高;②需要使用專門的孵化設備和快速平衡透析儀。
此方法適合大多數藥物游離濃度測定,但需要專門的儀器設備。r(游離藥物)=藥物血漿總濃度×(緩沖液層的藥物濃度/血漿層藥物濃度×100%)[20-24]。
5 結語
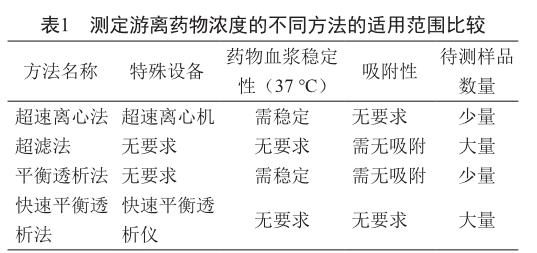
目前常用的測定游離藥物濃度的方法的優缺點如上所述,可根據不同藥物的特點和試驗條件進行選擇。在進行選擇之前,我們應了解是否有特殊設備、藥物本身的血漿穩定性(37 ℃)、吸附性和待測樣品的數量。每種方法的適用范圍見表1。
游離藥物濃度的檢測對于新劑型藥物的臨床用藥、藥效評價、安全性監測等都有重要意義,而更準確實用的游離藥物濃度測定方法也將對新劑型藥物的研發提供重要依據。
致謝:對中科院上海藥物研究所藥物代謝研究中心的全體領導、同事和學生對此綜述的完稿所提供的幫助表示衷心感謝!
參考文獻
[1] Gardner ER, Dahut W, Figg WD. Quantitative determination of total and unbound paclitaxel in human plasma following abraxane treatment[J]. J Chromatogr B Analyt Technol Biomed Life Sci, 2008, 862(1-2): 213-218.
[2] Sun J, Dai WB, Liang Z, et al. Advances in the formulation and delivery technology of paclitaxel for injection [J]. J Chin Pharm Sci, 2015, 24(8): 487-500.
[3] 毋海蘭, 馬智宇, 張淑秋, 等. 紫杉醇不同劑型對大鼠血漿中游離藥物濃度的影響[J]. 中國醫藥工業雜志, 2016, 47(11): 1430-1435.
[4] Trainor GL. The importance of plasma protein binding in drug discovery[J]. J Expert Opin Drug Discov, 2007, 2(1): 51-64.
[5] Howard ML, Hill JJ, Galluppi GR, et al. Plasma protein binding in drug discovery and development[J]. J Comb Chem High Throughput Screen, 2010, 13(2): 170-187.
[6] 陳冰, 蔡衛民. 游離藥物濃度監測及其應用研究進展[J].中國臨床藥理學雜志, 2008, 24(3): 255-259.
[7] Nevídalová H, Michalcová L, Glatz Z. In-depth insight into the methods of plasma protein-drug interaction studies: Comparison of capillary electrophoresis-frontal analysis, isothermal titration calorimetry, circular dichroism and equilibrium dialysis[J]. J Electrophoresis, 2018, 39(4): 581-589.
[8] Nilsson LB. The bioanalytical challenge of determining unbound concentration and protein binding for drugs[J]. J Bioanalysis, 2013, 5(24): 3033-3050.
[9] Sebille B. Methods of drug protein binding determinations[J]. Fundam Clin Pharmacol, 1990, 4(Suppl 2): 151s-161s.
[10] Kurz H, Trunk H, Weitz B. Evaluation of methods to determine protein-binding of drugs. Equilibrium dialysis, ultrafiltration, ultracentrifugation, gel filtration[J]. J Arzneimittelforschung, 1977, 27(7): 1373-1380.
[11] Barré J, Chamouard JM, Houin G, et al. Equilibrium dialysis, ultrafiltration,and ultracentrifugation compared for determining the plasma-protein-binding characteristics of valproic acid[J]. J Clin Chem, 1985, 31(1): 60-64.
[12] Eisenried A, Wehrfritz A, Ihmsen H, et al. Determination of total and unbound propofol in patients during intensive care sedation by ultrafiltration and LC-MS/MS [J]. J Pharm Biomed Anal, 2016, 126: 148-155.
[13] Saari TI, Fechner J, Ihmsen H, et al. Determination of total and unbound sufentanil in human plasma by ultrafiltration and LC-MS/MS: application to clinical pharmacokinetic study[J]. J Pharm Biomed Anal, 2012, 66: 306-313.
[14] Mortier KA, Lambert WE. Determination of unbound docetaxel and paclitaxel in plasma by ultrafiltration and liquid chromatography-tandem mass spectrometry[J]. J Chromatogr A, 2006, 1108(2): 195-201.
[15] Du P, Han X, Li N, et al. Development and validation of an ultrafiltration-UPLC-MS/MS method for rapid quantification of unbound docetaxel in human plasma[J]. J Chromatogr B Analyt Technol Biomed Life Sci, 2014, 967: 28-35.
[16] Metsu D, Lanot T, Fraissinet F, et al. Determination of dolutegravirs unbound fraction in human plasma using validated equilibrium dialysis and LC-MS/MS methods[J]. J Clin Chim Acta, 2018, 479: 56-65.
[17] Ray JA, Kushnir MM, Rockwood AL, et al. Direct measurement of free estradiol in human serum and plasma by equilibrium dialysis-liquid chromatography-tandem mass spectrometry[J]. J Methods Mol Biol, 2016, 1378: 99-108.
[18] 李瑞光, 陳歷俊, 姜鐵民, 等. 應用平衡透析法分析藥物小分子與蛋白質相互作用[J]. 生物技術通報, 2010(6): 80-84.
[19] 楊海艷, 王公軻, 陳得軍, 等. 平衡透析法用于有機小分子和蛋白質相互作用研究進展[J]. 河南師范大學學報(自然科學版), 2008, 36(4): 93-97.
[20] Thermo Scientific, Instructions of Red Device Inserts[EB/ OL]. [2018-06-31]. https://www.thermofisher.com/order/ catalog/product/89810?SID=srch-srp-89810.
[21] Ye Z, Zetterberg C, Gao H. Automation of plasma protein binding assay using rapid equilibrium dialysis device and Tecan workstation[J]. J Pharm Biomed Anal, 2017, 140: 210-214.
[22] Waters NJ, Jones R, Williams G, et al. Validation of a rapid equilibrium dialysis approach for the measurement of plasma protein binding [J]. J Pharm Sci, 2008, 97(10): 4586-4595.
[23] Vanstraelen K, Wauters J, De Loor H, et al. Proteinbinding characteristics of voriconazole determined by highthroughput equilibrium dialysis [J]. J Pharm Sci, 2014, 103(8): 2565-2570.
[24] Garcia-Martínez S, Rico E, Casal E, et al. Bioanalytical validation study for the determination of unbound ambrisentan in human plasma using rapid equilibrium dialysis followed by ultra performance liquid chromatography coupled to mass spectrometry [J]. J Pharm Biomed Anal. harm Biomed Anal, 2018, 150: 427-435.

