Mn2+對DNS法測定右旋糖酐發酵液中果糖含量的影響
慕 娟,問清江,孫曉宇,丁 浩
( 陜西省微生物研究所, 陜西 西安 710043)
右旋糖酐(Dextran)是一種由若干葡萄糖聚合而成的高分子聚合物,也稱葡聚糖,是一種非常重要的多糖,可用于醫藥、食品、輕工等多領域,例如血漿代用品,乳化劑和增稠劑,高黏度膠水,炸藥,鉆井添加劑,土壤改良劑等[1~2]。目前右旋糖酐主要是微生物發酵生產,腸膜狀明串珠菌(Leuconstoc mesenteriodes)以蔗糖為原料,產生右旋糖酐蔗糖酶(Dextransucrase, EC2.4.5.1),該酶以蔗糖為底物,切斷D-葡萄糖基與果糖基的糖苷鍵,形成D-葡萄糖基與酶的復合物,釋放出果糖,最后將葡糖糖基單元主要以α-1,6糖苷鍵連接形成右旋糖酐,產生果糖[3~6]。因此,右旋糖酐發酵液中的主要代謝產物有右旋糖酐、果糖和右旋糖酐蔗糖酶。在右旋糖酐發酵檢測中,由于右旋糖酐是高黏度的多糖,必須通過乙醇沉淀,烘干得出其含量,而果糖是一種還原糖,易于檢測,再者右旋糖酐蔗糖酶酶活檢測也是通過酶作用所產生的果糖來衡量的,因此果糖作為右旋糖酐發酵的主要檢測指標。3,5-二硝基水楊酸(DNS)分光光度法測定還原糖,操作簡便快速、試劑消耗少、重現性好、準確度易達到檢測要求,因此果糖的測定采用3,5-二硝基水楊酸試劑法(DNS)[7~8]。
在研究金屬離子對右旋糖酐發酵影響中發現,按照常規DNS 測定還原糖法檢測,Mn2+對發酵液中的果糖和右旋糖酐兩種代謝產物的影響結果不同,前者隨發酵液中Mn2+濃度的增加一直增加,而后者則相反,出現異常現象。隨后在研究金屬離子對右旋糖酐蔗糖酶作用的影響時,不同Mn2+濃度的酶反應體系作用結果檢測時,偶然發現,對照管的光吸收值隨Mn2+濃度的增加而增加,說明Mn2+也在檢測過程中發生反應。本文主要通過Mn2+對右旋糖酐發酵過程中果糖和右旋糖酐蔗糖酶的檢測的影響及Mn2+和DNS的定量發應等進行探索研究,改進DNS法測定右旋糖酐發酵液中果糖含量,為還原糖測定樣品中含有氧化還原性其他物質時的檢測提供參考,如果檢測樣品中含有待測還原糖外的其它具有還原性的物質時,在DNS測定還原糖時,一定要考慮其產生的氧化還原反應,消除其對檢測結果的影響。
1 實驗部分
1.1 試劑、材料與儀器
1.1.1 試劑與材料 果糖(D -(-)- fructose)(Sigma 公司);3,5-二硝基水楊酸(DNS)(化學純,上海科豐化學試劑有限公司);苯酚(重蒸酚,北京鼎國生物技術有限責任公司);蔗糖、磷酸氫二鈉、磷酸二氫鉀、氫氧化鈉、酒石酸鉀鈉、無水亞硫酸鈉、氯化錳、乙酸鈉、冰醋酸、(分析純,廣東光華科技股份有限公司);蛋白胨(北京奧博星生物技術有限責任公司);白砂糖(市售一級);菌株:Leuconstoc mesenteriodes -1226(Lm-1226)(中國藥品生物制品檢定所)。
1.1.2 儀器 722分光光度計(上海精密科學儀器有限公司);SPX-150BIII生化培養、GH-500型隔水式培養箱、101型電熱鼓風干燥箱、HH-4A電熱恒溫水浴鍋(北京科偉永興儀器有限公司)。
1.1.3 DNS試劑 稱取10.0 g DNS于600 mL蒸餾水中,逐漸加入10.0 g氫氧化鈉,加熱(50℃水浴)攪拌至溶解,依次加入200 g酒石酸鉀鈉,2.0 g苯酚和5.0 g無水亞硫酸鈉,待全部溶解并澄清后,冷卻至室溫,用水定容至1 000 mL,過濾,貯存于棕色試劑瓶中,于暗處放置7 d后使用。
1.1.4 1 mg·mL-1果糖標準溶液 準確稱取0.1000 g Sigma果糖(105 ℃干燥衡重),用蒸餾水溶解并定容至100 mL。
1.1.5 1 mg·mL-1Mn2+標準溶液 準確稱取0.3076 g 分析純硫酸錳(105 ℃干燥衡重),用蒸餾水溶解并定容至100 mL。
1.1.6培養基(g·L-1) 白砂糖120 g,蛋白胨 1.7 g ,磷酸氫二鈉1.4 g,pH7.0。
1.2 實驗方法
1.2.1 Lm-1226產右旋糖酐的發酵 以不同Mn2+將硫酸錳分別加入到培養基中,腸膜狀明串珠菌Lm-1226種子液以10%的接種量接入到培養基中,25 ℃,靜止培養28 h;取樣檢測果糖、右旋糖酐蔗糖酶,并將75%乙醇按135 mL·100 mL-1加入到發酵液中,充分攪拌均勻,放置,收集沉淀,沉淀用75%乙醇洗滌3次,烘干稱重測出右旋糖酐量。
1.2.2 Mn2+對右旋糖酐蔗糖酶作用的影響 右旋糖酐發酵液進行一定的稀釋,10 000 r·min-1離心15 min,收集上清液為提取液為右旋糖酐蔗糖酶酶液,在適當稀釋的酶液中加入不同濃度的Mn2+,以蔗糖為底物,右旋糖酐蔗糖酶在Mn2+濃度不同反應體系中作用,測定酶活力,以確定Mn2+對右旋糖酐蔗糖酶作用的影響。
1.2.3 果糖、右旋糖酐蔗糖酶活力的測定
1.2.3.1 果糖標準曲線制作
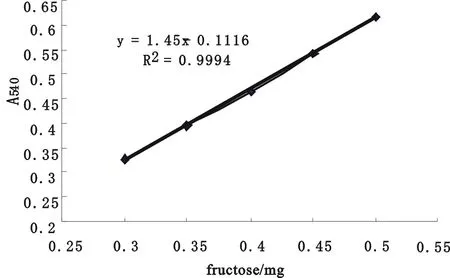
圖1 果糖標準曲線
采用DNS法測定還原糖方法,分別量取0.3、0.35、0.4、0.45、0.5 mL果糖標準溶液(1 mg·mL-1),用蒸餾水補齊1 mL,再加入2 mL DNS,沸水浴2 min,流水冷卻后加蒸餾水至10 mL,在540 nm測定光吸收值,繪制果糖標準曲線,得出回歸方程用于果糖和酶活測定。
1.2.3.2 果糖測定 發酵液等樣品稀釋一定倍數,取樣品1 mL加入2 mL DNS煮沸2 min顯色,然后冷水浴冷卻至室溫,定容至10 mL;蒸餾水為對照,取蒸餾水1 mL ,其余同樣品;540 nm測定吸光值,根據回歸方程得出樣品中的果糖含量果糖含量計算公式:
果糖(mg·mL-1)=[(Ae-A0) +0.1014]/1.302×Df
式中:Ae——樣品的吸光值
A0—蒸餾水空白的吸光值
Df—樣品的稀釋倍數
1.2.3.3 改進的果糖測定
發酵液等樣品稀釋一定倍數,取樣品1 mL加入2 mL DNS煮沸2 min顯色,然后冷水浴冷卻至室溫,定容至10 mL;發酵液相對應的發酵培養基為對照,發酵培養基與相對應的發酵液稀釋相同倍數,取樣品1 mL ,其余同樣發酵液樣品;540 nm測定吸光值,根據回歸方程得出發酵液樣品中的果糖含量。
果糖含量計算公式:
果糖(mg·mL-1)=[(Ae-A0) +0.1014]/1.302×Df
式中:Ae——樣品的吸光值
A0—培養基空白的吸光值
Df—樣品的稀釋倍數
1.2.3.4 右旋糖酐蔗糖酶活力測定
將酶液用pH5.4的0.2 M醋酸緩沖液適當稀釋后,取0.5 mL的酶液加入到0.5 mL10%的蔗糖溶液中,30℃準確反應1 h,加入2 mLDNS終止反應,沸水浴2 min顯色,然后流水冷卻至室溫,定容至10 mL;空白對照的酶液和DNS加入順序顛倒,其余同樣品測定。以蒸餾水為對照測定540 nm的吸光值,樣品和空白對照的吸光值之差根據回歸方程得出反應液中的果糖量,從而確定酶活。酶活力單位定義:在上述條件下,每分鐘催化蔗糖產生1 μmol果糖所需要的酶量定義為1個酶活力單位(IU)。
酶活力計算公式:
E={[(Ae-A0) +0.1014]/1.302×Df×1 000}/(WM×t×V)
式中:E——樣品酶活力(IU·mL-1)
Ae——酶液反應的吸光值
A0—滅活酶液空白的吸光值
Df—樣品酶液的稀釋倍數
WM——果糖分子量
t——酶反應時間(min)
V——發應的酶液體積(mL)
1.2.4 Mn2+與DNS試劑的作用 分別量取0.3、0.35、0.4、0.45、0.5 mL Mn2+標準溶液(1 mg·mL-1),用蒸餾水補齊1 mL,再加入2 mL DNS,沸水浴2 min,流水冷卻后加蒸餾水至10 mL,在540 nm測定光吸收值。
2 結果與討論
2.1 Mn2+對右旋糖酐發酵液中果糖檢測的影響
DNS法測定樣品中的還原糖一般是按照1.2.3.1和1.2.3.2的方法進行的,如此對含有不同Mn2+濃度的培養基經Lm-1226培養發酵后的右旋糖酐發酵液進行了果糖測定,同時用乙醇沉淀法提取了發酵液中的右旋糖酐進行了定量檢測(見表1)。結果表明:果糖含量隨Mn2+濃度的增加而增加,而右旋糖酐則相反。Leuconstoc mesenteriodes -1226發酵產右旋糖酐的機理是,蔗糖中的葡萄糖基以α-1,6糖苷鍵連接形成右旋糖酐,釋放果糖,因此二者隨Mn2+濃度變化的趨勢應該一致,但結果出現異常,需要進一步研究。
2.2 Mn2+對右旋糖酐蔗糖酶活力檢測的影響
右旋糖酐蔗糖酶在不同Mn2+濃度的發應體系中作用結果見表2,在1.25~7.5 mmol·L Mn2+濃度范圍內,右旋糖酐蔗糖酶作用開始隨著Mn2+濃度的增加而增強,5.0 mmol·L-1時作用最強,隨后增強作用逐漸降低,說明Mn2+對右旋糖酐蔗糖酶具有較強地激活作用,最適Mn2+濃度為5.0 mmol·L-1。但是還可以看出,滅活酶液空白的吸光值A0隨著Mn2+濃度的增加一直在增大,那么就有可能是Mn2+與DNS試劑發生反應而造成這一結果。2.1中果糖與右旋糖酐隨Mn2+濃度變化而變化的異常現象也可能由于Mn2+與DNS試劑產生發應而影響了果糖的測定結果。
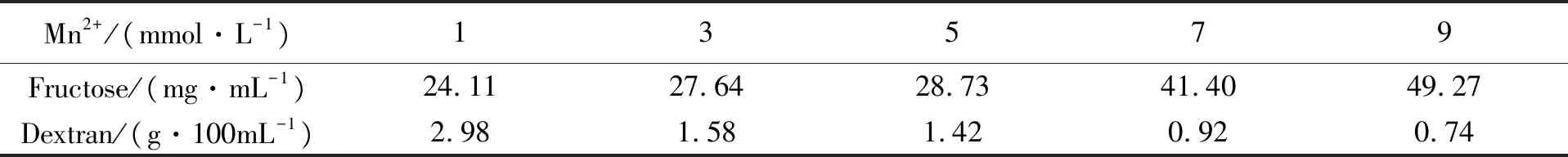
表1 Mn2+對右旋糖酐發酵液檢測的影響
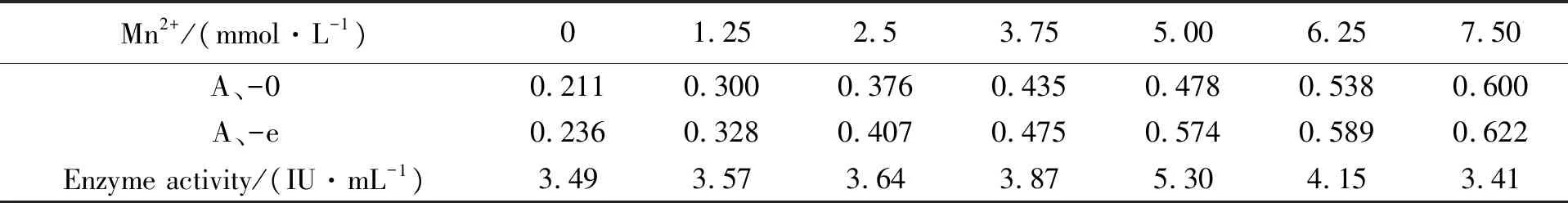
表2 Mn2+對右旋糖酐蔗糖酶活力檢測的影響
注:檢測樣品稀釋200倍。
2.3 Mn2+與DNS試劑的反應
按照DNS測定還原糖的方法對不同濃度的Mn2+進行反應并測定結果(見表3),隨著Mn2+濃度的增加吸收值A540也在增加,和果糖與DNS發應的變化趨勢一致,說明Mn2+的確與DNS發生發應。原因在于,Mn2+在堿性介質中很容易被氧化,DNS試劑,除了具有氧化性外,還含有氫氧化鈉而呈堿性。雖然相同量相對應吸光值有差,Mn2+的均低于果糖,原因可能在于Mn2+的還原性弱于果糖或者與DNS的反應弱于果糖的反應。因此在使用DNS測定果糖等還原糖樣品時,需要考慮其是否含有類似于Mn2+等的還原性其他物質存在,若有就必須改進方法消除影響。

表3 Mn2+、果糖與DNS試劑的反應
2.4 改進方法對右旋糖酐發酵液檢測
從2.1中可看出Mn2+對Lm-1226發酵產右旋糖酐無促進作用,且隨Mn2+的增加,抑制作用增強,因此將Mn2+濃度降低進行其對Lm-1226發酵產右旋糖酐影響實驗,按照1.2.1、1.2.3.1、1.2.3.3及1.2.3.4對發酵液中的右旋糖酐、果糖和右旋糖酐蔗糖酶進行檢測,Mn2+對Lm-1226發酵產右旋糖酐的影響見表4。果糖和右旋糖酐均隨著培養基中Mn2+濃度的增加而降低,說明Mn2+對Lm-1226發酵產右旋糖酐具有抑制作用,且濃度越大抑制性越強。發酵液中右旋糖酐蔗糖酶的活力隨Mn2+濃度的增加,開始上升,隨后降低。考慮到Mn2+本身和DNS發生應,因此將未經Lm-1226培養基作為相應Mn2+濃度發酵液檢測的空白對照,從而消除了Mn2+對果糖檢測結果的影響,使得果糖和右旋糖酐的變化顯示應有的一致性。但是從檢測數據的絕對值來看,果糖和右旋糖酐的含量對應性存在問題。1 kg蔗糖完全被轉化后產生0.526 kg果糖和0.474右旋糖酐,因此發酵液中果糖的含量應大于右旋糖酐。但是表4數據倒掛,果糖含量低于右旋糖酐,說明原因可能還在于果糖的檢測。根本原因仍在于Mn2+的性質所致,在Mn2+的鹽溶液中加堿時,可以析出膠狀白色Mn(OH)2沉淀,在空氣中不穩定,易被氧化成棕色的Mn(OH)4或MnO(OH)2。
MnSO4+ 2NaHO = Mn(OH)2↓ + Na2SO4
2Mn(OH)2+ O2= 2MnO(OH)2↓
DNS試劑含有氫氧化鈉和氧化劑,Mn2+和DNS一定發生氧化還原反應,但是到底是什么樣的反應,僅僅通過540 nm的光吸收值是難以清楚的,因此還需要進一步的工作,繼續探索Mn2+對DNS測定還原糖的影響。
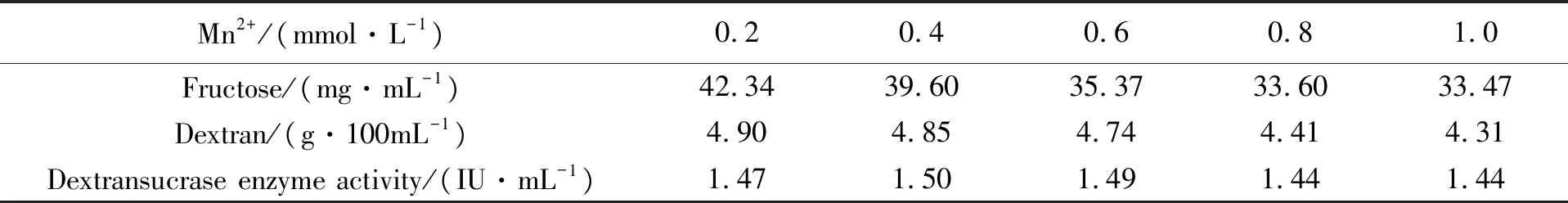
表4 Mn2+對Lm-1226發酵產右旋糖酐的影響液
3 結論
在Mn2+對腸膜狀明串珠菌發酵產右旋糖酐的影響研究中出現的果糖和右旋糖酐兩種代謝產物隨Mn2+濃度變化的不一致性而發現問題;隨后通過Mn2+對右旋糖酐蔗糖酶作用的影響研究中找處了DNS測定果糖是產生問題的原因;然后通過Mn2+與DNS的發應進一步證實,Mn2+本身的氧化還原型性導致其與DNS試劑產生反應,在測定果糖時要考慮到Mn2+對檢測結果的影響;最后通過檢測時以含有Mn2+的培養基作為相對應發酵液的空白對照,檢測結果表明,克服了果糖和右旋糖酐兩種代謝產物隨Mn2+濃度變化的不一致性的問題,但是從Mn2m-1226發酵產右旋糖酐的轉化機理的角度來看,檢測結果中的果糖含量和右旋糖酐產出量出現了倒掛現象,說明僅僅通過改變檢測空白來消除Mn2+對果糖檢測的影響還遠遠不夠,畢竟沒有搞清楚在發酵液中的果糖與DNS發應的同時Mn2y與DNS到底發生了什么樣的發應,還需要進一步的工作。總之,Mn2+對DNS法測定右旋糖酐發酵液中的果糖含量有影響,需要在利用DNS法測定樣品中的還原糖時,一定要考慮是否含有具有氧化還原性的其他成分,若有就需要改進方法,消除其對檢測結果的影響。

