酶促酯化制備DAG過(guò)程中的酰基轉(zhuǎn)移研究
宋志華,魯 珊,黃健花,金青哲,王興國(guó)
(江南大學(xué) 食品學(xué)院,江蘇 無(wú)錫 214122)
甘二酯,又稱甘油二酯、脂肪酸甘油二酯(DAG),按空間異構(gòu)分為1,3-甘二酯(1,3-DAG)和1,2-甘二酯(1,2-DAG)兩類,兩類DAG的功能差異較大,前者可抑制脂肪積累、預(yù)防肥胖及肥胖引發(fā)的相關(guān)疾病[1],后者具有細(xì)胞信號(hào)分子、促進(jìn)傷口愈合、改善糖尿病大鼠心肌功能紊亂[2-3]等作用。
酶促催化制備DAG工藝途徑主要包括酯交換法和直接酯化法。充分利用不同酶促催化位點(diǎn)的不同,制取獲得特定構(gòu)型或特定脂肪酸DAG已成為當(dāng)前研究的熱點(diǎn)。祝雨筱等[3]利用Lipozyme 435催化酯交換合成1,2-DAG,劉四磊等[4]利用Lipozyme RM IM催化酯化制取富含花生四烯酸的1,3-DAG。然而,不管是酯交換法還是直接酯化法,都會(huì)伴隨酰基轉(zhuǎn)移產(chǎn)生一些副產(chǎn)物,如單甘酯(MAG)、甘三酯(TAG);同時(shí),現(xiàn)有關(guān)于酶促催化制備DAG的研究,主要集中于酶篩選、催化參數(shù)優(yōu)化方面[3-5]。有關(guān)酰基轉(zhuǎn)移的研究報(bào)道也主要針對(duì)酶促催化的酯交換反應(yīng)體系,如:Laszlo等[6]研究酶促催化高油酸葵花籽油-乙醇酯交換體系酰基遷移動(dòng)力學(xué);李人望[7]研究了酶促催化單甘酯-甲醇酯交換體系中溶劑對(duì)脂肪酶位置選擇性和酰基轉(zhuǎn)移的影響;Pacheco等[8]研究了酶促催化大豆油-完全氫化大豆油酯交換體系的酰基轉(zhuǎn)移情況。鮮有關(guān)于酶促催化酯化反應(yīng)體系酰基轉(zhuǎn)移規(guī)律的研究和報(bào)道。因此,研究探討酶促催化酯化制備DAG反應(yīng)體系下的酰基轉(zhuǎn)移規(guī)律,對(duì)于豐富和完善酶促催化基礎(chǔ)理論體系,指導(dǎo)DAG合成、獲得特定高純DAG產(chǎn)物具有重要意義。本文采用Sn-1,3特異性脂肪酶Lipozyme RM IM為催化劑,以油酸和甘油的酶促酯化反應(yīng)體系為模型,初步探討酶促酯化制備DAG過(guò)程中的酰基轉(zhuǎn)移規(guī)律,以期為酶促催化酯化制備DAG過(guò)程中的酰基轉(zhuǎn)移調(diào)控提供理論指導(dǎo)。
1 材料與方法
1.1 試驗(yàn)材料
Lipozyme RM IM,諾維信生物技術(shù)有限公司;甘油、油酸、乙酸均為分析純,國(guó)藥化學(xué)試劑有限公司;異丙醇、正己烷均為色譜純,北京百靈威科技有限公司。
Re-501型旋轉(zhuǎn)蒸發(fā)器,Waters1525高效液相色譜儀,Alltech3300蒸發(fā)光散射檢測(cè)器, Waters Spherisorb Silica 色譜柱(2.0 mm×250 mm,5 μm),AR2140精密電子天平。
1.2 試驗(yàn)方法
1.2.1 酯化合成DAG
按一定摩爾比稱取適量的油酸與甘油置于50 mL圓底燒瓶,添加一定量脂肪酶,在一定溫度的水浴下真空旋轉(zhuǎn)反應(yīng)(80 r/min,0.1 MPa),反應(yīng)過(guò)程中按一定時(shí)間間隔取樣, 分析產(chǎn)物的甘油酯組成。所有試驗(yàn)因素水平均同時(shí)進(jìn)行3次重復(fù)試驗(yàn)。
1.2.2 酯化產(chǎn)物甘油酯組成分析
取酯化產(chǎn)物0.5 mL,加入0.5 mL高純水和5 mL正己烷,旋渦振蕩萃取1 min,離心收集有機(jī)相,氮吹揮干溶劑后定容至10 mL進(jìn)行HPLC分析。
檢測(cè)條件[9]:Spherisorb Silica 色譜柱(2.0 mm×250 mm,5 μm);柱溫35℃;流動(dòng)相A為正己烷-異丙醇(體積比99∶1),流動(dòng)相B為正己烷-異丙醇-乙酸(體積比1∶1∶0.01);采用梯度洗脫,0~10 min A由100%降至80%,10~14 min A由80%降至70%,14~15 min A由70%升至100%并保持5 min;流動(dòng)相流速0.5 mL/min;進(jìn)樣量10 μL;蒸發(fā)光散射檢測(cè)器漂移管溫度75℃。采用面積歸一化法進(jìn)行定量。
1.2.3 酯化反應(yīng)酰基轉(zhuǎn)移表征
Lipozyme RM IM為1,3-特異性脂肪酶,故反應(yīng)體系的酰基轉(zhuǎn)移產(chǎn)物主要為1,2-DAG、2-MAG和TAG,檢測(cè)酰基轉(zhuǎn)移產(chǎn)物組成發(fā)現(xiàn)2-MAG未檢出,故本文采用酰基轉(zhuǎn)移產(chǎn)物中1,2-DAG在DAG的占比直觀反映體系中DAG的酰基轉(zhuǎn)移情況,同時(shí),對(duì)體系的DAG含量變化情況進(jìn)行監(jiān)測(cè)。1,2-DAG在DAG的占比以酰基轉(zhuǎn)移率表示,計(jì)算公式如下。
酰基轉(zhuǎn)移率=1,2-DAG含量/(1,2-DAG含量+1,3-DAG含量)×100%
2 結(jié)果與討論
2.1 酯化時(shí)間對(duì)酰基轉(zhuǎn)移的影響
在底物(油酸與甘油)摩爾比2∶1、酯化溫度65℃、Lipozyme RM IM添加量6%(以底物總質(zhì)量計(jì),下同)的條件下,探討酯化時(shí)間對(duì)酶促酯化合成DAG過(guò)程中酰基轉(zhuǎn)移的影響,結(jié)果如圖1所示。

圖1 酯化時(shí)間對(duì)酶促酯化合成DAG過(guò)程中 酰基轉(zhuǎn)移的影響
由圖1可知,酰基轉(zhuǎn)移率隨酯化時(shí)間的延長(zhǎng)不斷增加,10 h時(shí)的酰基轉(zhuǎn)移率達(dá)26.1%。同時(shí)發(fā)現(xiàn),隨著酯化時(shí)間的延長(zhǎng),體系中DAG的含量先增加后下降,在2 h時(shí)DAG含量最高,之后隨酯化時(shí)間延長(zhǎng)DAG含量下降。這是由于隨著反應(yīng)進(jìn)行DAG進(jìn)一步反應(yīng)生成TAG,而Lipozyme RM IM催化生成TAG過(guò)程中,1,2-DAG較1,3-DAG更易發(fā)生反應(yīng),故隨著反應(yīng)的進(jìn)行,1,3-DAG不斷發(fā)生酰基轉(zhuǎn)移形成1,2-DAG,導(dǎo)致酰基轉(zhuǎn)移率隨之不斷增加[10]。因此,反應(yīng)時(shí)間控制在1 h以內(nèi)可以盡可能減少酰基轉(zhuǎn)移發(fā)生,保證體系產(chǎn)物具有較高的1,3-DAG含量。
2.2 底物摩爾比對(duì)酰基轉(zhuǎn)移的影響
根據(jù)甘油與脂肪酸酯化反應(yīng)的理論方程,綜合考慮反應(yīng)效率和成本,酶促酯化制備DAG過(guò)程中,脂肪酸與甘油的理論最佳摩爾比為2∶1。改變底物組成會(huì)影響體系的擴(kuò)散傳質(zhì),進(jìn)而影響反應(yīng),脂肪酸含量過(guò)高,利于反應(yīng)過(guò)程中1,3-DAG酰基轉(zhuǎn)移形成1,2-DAG和生成TAG;甘油含量增加則體系黏度加大、極性增強(qiáng),不利于其與脂肪酸的有效接觸,進(jìn)而影響反應(yīng)速率[11]。在酯化溫度65℃、酯化時(shí)間2 h、Lipozyme RM IM 添加量6%的條件下,探討底物(油酸與甘油)摩爾比對(duì)酶促酯化合成DAG過(guò)程中酰基轉(zhuǎn)移的影響,結(jié)果如圖2所示。
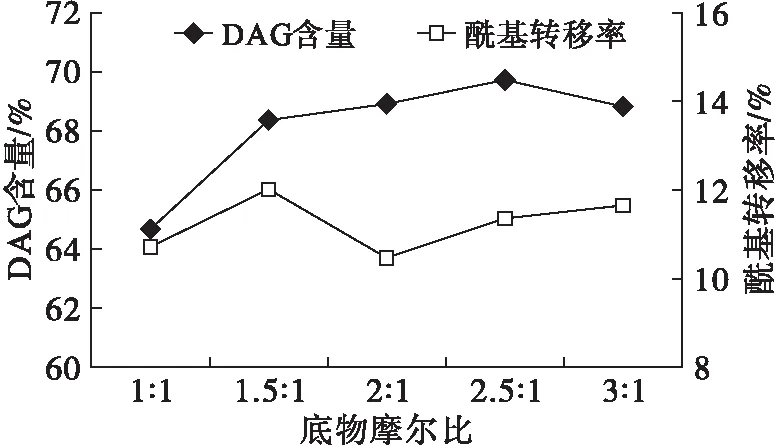
圖2 底物摩爾比對(duì)酶促酯化合成DAG過(guò)程中 酰基轉(zhuǎn)移的影響
由圖2可知,底物摩爾比對(duì)反應(yīng)體系的酰基轉(zhuǎn)移影響不大,不同底物摩爾比反應(yīng)時(shí)的酰基轉(zhuǎn)移率變化不大,基本在11%左右,在底物摩爾比為2∶1時(shí)酰基轉(zhuǎn)移率相對(duì)略低,符合理論最佳值。不同底物摩爾比反應(yīng)產(chǎn)物的DAG含量也無(wú)明顯差異。這可能是由于脂肪酶具有活性位點(diǎn),其通常被α-螺旋“蓋子”遮蓋,只有當(dāng)吸附于油-水界面時(shí)才會(huì)在油相疏水作用下,打開(kāi)“蓋子”,暴露活性位點(diǎn),發(fā)生催化作用[12]。而本實(shí)驗(yàn)條件下底物摩爾比的改變對(duì)酶在油水界面發(fā)揮催化作用的影響不大。底物摩爾比過(guò)小,甘油反應(yīng)不充分,DAG含量略低;底物摩爾比過(guò)大,脂肪酸過(guò)量導(dǎo)致TAG含量增加、DAG含量下降。綜合評(píng)估,當(dāng)?shù)孜锬柋瓤刂圃?∶1時(shí),體系的酰基轉(zhuǎn)移率最低,產(chǎn)物中1,3-DAG含量最高。
2.3 酶添加量對(duì)酰基轉(zhuǎn)移的影響
在底物(油酸與甘油)摩爾比2∶1、酯化溫度65℃、酯化時(shí)間2 h的條件下,探討酶添加量對(duì)酶促酯化合成DAG過(guò)程中酰基轉(zhuǎn)移的影響,結(jié)果如圖3所示。

圖3 酶添加量對(duì)酶促酯化合成DAG過(guò)程中 酰基轉(zhuǎn)移的影響
由圖3可知,當(dāng)酶添加量分別為2%、4%和6%時(shí),對(duì)應(yīng)的酰基轉(zhuǎn)移率分別為9.8%、10.6%和10.5%,酰基轉(zhuǎn)移率變化不大,相應(yīng)的DAG含量則從48%上升到68%。這是由于一開(kāi)始酶添加量較低時(shí),酶在油-水反應(yīng)界面的濃度隨酶添加量的增加而逐漸增大,從而有效提高了反應(yīng)速率[13],導(dǎo)致DAG含量的增加。當(dāng)進(jìn)一步增大酶用量時(shí),酰基轉(zhuǎn)移率與DAG含量的變化趨勢(shì)相反,即DAG含量呈現(xiàn)降低趨勢(shì),酰基轉(zhuǎn)移率則明顯增加,酰基轉(zhuǎn)移率由10.5%(酶添加量6%)增加至15.2%(酶添加量10%)。說(shuō)明當(dāng)酶添加量達(dá)到6%時(shí),酶基本在油-水反應(yīng)界面達(dá)到飽和,此時(shí)進(jìn)一步增加酶用量,導(dǎo)致副反應(yīng)增加[14],形成更多的副產(chǎn)物TAG,進(jìn)而推動(dòng)1,3-DAG的酰基轉(zhuǎn)移,導(dǎo)致酰基轉(zhuǎn)移率的增加。因此,在現(xiàn)有反應(yīng)條件下,6%的酶添加量可以保證產(chǎn)物具有較高的1,3-DAG含量。
2.4 酯化溫度對(duì)酰基轉(zhuǎn)移的影響
通常酶具有最適溫度,在最適溫度下表現(xiàn)出理想的催化活性。在底物(油酸與甘油)摩爾比2∶1、酯化時(shí)間2 h、Lipozyme RM IM 添加量6%的條件下,探討酯化溫度對(duì)酶促酯化合成DAG過(guò)程中酰基轉(zhuǎn)移的影響,結(jié)果如圖4所示。

圖4 酯化溫度對(duì)酶促酯化合成DAG過(guò)程中 酰基轉(zhuǎn)移的影響
升高酯化溫度,利于降低體系黏度,提高底物間相容性,加快傳質(zhì),提升反應(yīng)速率;同時(shí),本研究所采用的反應(yīng)裝置帶有真空脫水功能,在一定范圍內(nèi)升高酯化溫度,有利于反應(yīng)產(chǎn)物水的脫除,促進(jìn)反應(yīng)向正反應(yīng)方向進(jìn)行;然而,當(dāng)酯化溫度過(guò)高時(shí),會(huì)影響酶的空間結(jié)構(gòu)和構(gòu)象,降低酶的活性。由圖4可知,酯化溫度升高明顯促進(jìn)酰基轉(zhuǎn)移,45℃時(shí)的酰基轉(zhuǎn)移率僅為6.4%,而75℃時(shí)的酰基轉(zhuǎn)移率達(dá)15.1%。即使在75℃酶活降低的情況下,酰基轉(zhuǎn)移率仍較65℃反應(yīng)體系明顯增加,這是由于隨著酯化溫度的進(jìn)一步升高(高于65℃),熱力學(xué)平衡占據(jù)主導(dǎo)地位,酰基轉(zhuǎn)移急劇增加所致[15]。因此,酯化溫度應(yīng)控制在65℃為宜。
3 結(jié) 論
Sn-1,3特異性脂肪酶Lipozyme RM IM催化酯化油酸和甘油合成DAG的過(guò)程中,體系的酰基轉(zhuǎn)移情況呈現(xiàn)如下規(guī)律:酯化溫度和酯化時(shí)間與體系酰基轉(zhuǎn)移率呈現(xiàn)正相關(guān)性,酯化溫度的升高或酯化時(shí)間的延長(zhǎng),都會(huì)明顯促進(jìn)酰基轉(zhuǎn)移;底物(油酸與甘油)摩爾比對(duì)酰基轉(zhuǎn)移影響不大,但會(huì)影響DAG的得率;酶添加量在油-水反應(yīng)界面達(dá)到飽和之前,酶添加量的變化對(duì)酰基轉(zhuǎn)移的影響不大,當(dāng)酶添加量達(dá)到飽和之后,進(jìn)一步增加酶添加量,則會(huì)加劇體系的酰基轉(zhuǎn)移。

