髓系惡性腫瘤伴骨髓纖維化患者的預后研究
呂黎瑋 趙春亭* 崔渤莉 孫玲潔 費海榮 劉曉丹 吳少玲尹相叢 李田蘭 高珊珊 馮獻啟 王 偉 趙洪國 孟凡軍 高 燕
(青島大學附屬醫院血液內科,山東 青島 266000)
除原發性骨髓纖維化 (PMF) 外,骨髓增生異常綜合征 (MDS)[1]、白血病、淋巴瘤等[2]多種疾病可伴發骨髓纖維化。骨髓纖維化是疾病發生發展的關鍵環節,明確其對原發病的影響有利于為患者提供更精準的個體化治療。目前仍缺乏血液病伴骨髓纖維化的特定預后系統,陳猛等[3]應用PMF國際預后積分系統(PMF-IPSS)、動態國際預后積分系統(DIPSS),針對我國患者的改良IPSS(IPSS-Chinese)和DIPSS(DIPSS-Chinese)以及真紅細胞增多癥/原發性血小板增多癥后骨髓纖維化(post-PV/ET MF)預后模型(MYSEC-PM)對55例postPV/ET-MF患者進行分組,發現上述5種積分系統均不能對我國post PV/ET-MF患者進行準確預后。

表1 AML伴骨髓纖維化患者根據不同預后積分系統分組情況

圖1 MDS相關預后積分系統各組患者生存曲線
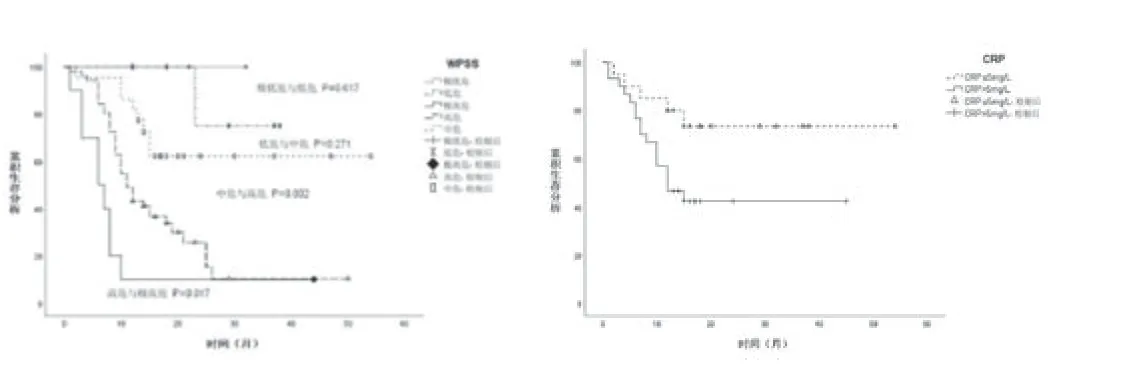
圖2 CRP水平對血液病伴骨髓纖維化患者生存的影響
受上述研究啟發,我們回顧性分析了我院134例急性髓系白血病(AML)及MDS伴骨髓纖維化患者資料,對PMF相關預后積分系統是否適用于我國AML/MDS伴骨髓纖維化患者進行分析,評估MDS常用預后積分系統對MDS伴骨髓纖維化的預后效力,并對AML/MDS合并骨髓纖維化預后影響因素進行了初步探討。
1 材料與方法
1.1 患者資料:收集2014年1月至2017年8月青島大學附屬醫院血液科確診的134例AML及MDS伴骨髓纖維化患者,男88例(65.7%),女46例(34.3%),中位年齡56.5(17~83)歲。其中AML 42例(31.3%),MDS 92例(68.7%)。所有患者診斷均符合WHO 2008標準[4],纖維化分級依照2005年歐洲纖維化分級共識標準[5]。
1.2 預后評估:使用PMF-IPSS、DIPSS、IPSS-Chinese、DIPSS-Chinese、MYSEC-PM對AML/MDS伴骨髓纖維化患者進行預后分組,使用MDS國際預后積分系統(MDS-IPSS)、修訂國際預后積分系統(IPSS-R)、WHO分型預后積分系統(WPSS)對MDS伴骨髓纖維化患者進行預后分組,評估各預后積分系統的預后效力。
1.3 其他研究參數:年齡、性別、血栓史、輸血依賴、肝脾腫大、外周血白細胞(WBC)計數、外周血血小板(PLT)計數、血紅蛋白(Hb)、血清乳酸脫氫酶(LDH)水平、血清堿性磷酸酶(ALP)水平、C-反應蛋白(CRP)水平、骨髓纖維化分級。
1.4 隨訪:所有患者隨訪至2018年8月31日。隨訪資料來源于患者門診、住院病歷資料、電話隨訪記錄。總體生存時間:確診骨髓纖維化至隨訪截止或死亡的時間。中位隨訪時間15(1~54)個月。
1.5 統計學處理:應用SPSS25.0統計軟件進行統計分析。計量資料用中位數表示;計數資料用例數和構成比表示;采用Kaplan-Meier和Cox多因素模型進行生存分析,繪制生存曲線,各組生存曲線比較應用Log-rank檢驗,P<0.05具有統計學差異。
2 結 果
2.1 骨髓纖維化相關預后積分系統對AML/MDS伴骨髓纖維化患者預后評估結果:IPSS、DIPSS、IPSS-Chinese、DIPSS-Chinese、MYSECPM均不能對AML、MDS伴骨髓纖維化的患者進行預后分組(表1)。
2.2 MDS相關預后積分系統對MDS伴骨髓纖維化患者預后評估結果:MDS-IPSS、IPSS-R、WPSS預后評分系統均無法準確對MDS伴骨髓纖維化患者進行預后分組(圖1)。
2.3 AML/MDS伴骨髓纖維化患者生存因素分析:單因素分析結果顯示,性別(P=0.045)、有脾腫大(P=0.002)、有輸血依賴(P=0.001)、纖維化≥2級(P<0.001)是影響AML/MDS伴骨髓纖維化患者的不良預后因素。將上述因素納入Cox多因素分析,結果顯示,有脾腫大(P=0.015)、有輸血依賴(P=0.008)、纖維化分級≥2級(P<0.001)是影響AML/MDS伴骨髓纖維化患者預后的獨立危險因素(表2)。
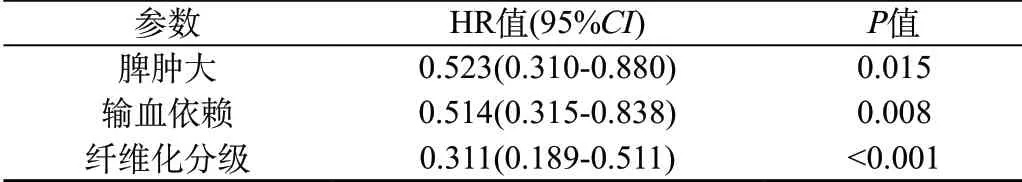
表2 AML及MDS伴骨髓纖維化患者Cox回歸多因素分析結果
對檢測CRP水平的50例AML及MDS伴骨髓纖維化患者進行單因素分析,結果顯示,CRP>5.0 mg/L是影響AML及MDS伴骨髓纖維化患者的不良預后因素(P=0.032)(圖2)。2.4 分別基于MDS-IPSS及WPSS預后積分系統增加骨髓纖維化分級預后指標,對患者進行預后評估。MDS-IPSS-MF:纖維化1級積0.5分,纖維化≥2級積1分,低危:0分,中危-1:0.5~1分,中危-2:1.5~2分,高危:≥2.5分。中危-1組與中危-2組(P<0.001),中危-2組與高危組(P=0.001)差異均有統計學意義,無低危組患者。WPSSMF:纖維化1級積1分,纖維化≥2級積2分,極低危:0分,低危:1~2分,中危:3~4分,高危:5~6分,極高危:7~8分。低危組與中危組(P=0.009)、中危組與高危組(P=0.006)、高危組與極高危組(P=0.009)差異均有統計學意義,無極低危組患者。
3 討 論
對于原發性骨髓纖維化,有多種包括臨床特征、實驗室指標及基因在內的預后積分系統,如IPSS[6]、DIPSS[7]、IPSS-Chinese和DIPSSChinese[8]。但目前國內外針對血液病伴骨髓纖維化的預后系統仍較少,僅有Passamonti等基于718例歐美post PV/ET-MF患者的研究制定的MYSEC-PM[9]。本研究分別采用上述5種預后積分系統對AML/MDS伴骨髓纖維化患者進行預后分組,結果顯示IPSS、DIPSS、IPSS-Chinese、DIPSS-Chinese均不能對其進行準確預后,可能的原因:①AML、MDS伴骨髓纖維化與原發性骨髓纖維化在發病機制、臨床特征方面存在差異,疾病進程及預后因素不盡相同;②AML、MDS伴骨髓纖維化患者的預后,是原發病與骨髓纖維化相互作用的結果;③本研究納入病例數有限且隨訪時間較短。本研究中MYSEC-PM亦不能對AML/MDS伴骨髓纖維化患者進行準確預后,可能的原因:①AML、MDS與PV、ET雖同屬于髓系惡性腫瘤,但在發病機制、病理生理等方面存在差異;②本研究隨訪時間較短,且無高危患者;③不同種族患者預后因素不全相同。因此,基于PMF患者及歐美MPN患者提出的預后系統,無法擴展至所有髓系惡性腫瘤伴骨髓纖維化患者的預后評估。
目前MDS-IPSS[10]、IPSS-R[11]及WPSS[12]廣泛應用于MDS的預后評估,本研究采用上述三種預后積分系統對MDS伴骨髓纖維化患者進行預后分組,結果顯示MDS-IPSS、IPSS-R、WPSS無法對MDS伴骨髓纖維化患者進行準確預后。可能的原因:骨髓纖維化影響了疾病的預后,而上訴預后積分系統未將骨髓纖維化及其相關指標如肝脾腫大等納入預后影響因素。多因素生存分析顯示,脾腫大、輸血依賴、纖維化分級≥2級是影響AML/MDS伴骨髓纖維化預后的獨立危險因素,為對患者進行更準確的預后提供了理論依據。本研究例數仍然偏少,骨髓纖維化是否對髓系惡性腫瘤均有不良影響仍需進一步擴大研究。
本研究將骨髓纖維化納入MDS-IPSS及WPSS預后積分系統,對MDS伴骨髓纖維化患者重新進行預后分組,結果顯示各組間均有統計學差異,進一步提示骨髓纖維化分級是MDS的危險因素,尤其對于傳統預后積分系統分組下的低危患者,納入骨髓纖維化分級可能會使得預后分組更加準確,有利于為患者提供更優化的個體化治療,提示臨床工作中應重視血細胞下降不明顯、染色體核型較好、原始細胞數無明顯增高但合并高等級骨髓纖維化的患者。
炎性反應在骨髓纖維化的發展中的有著突出作用。有學者認為骨髓纖維化病理生理的各個方面都是骨髓感染或暴露于化學、毒物后的反應性改變[13]。這使得急性期炎性蛋白如C反應蛋白(CRP)得到關注。一項包括PMF、post-PV/ET MF共184例患者的研究,發現纖維化患者高敏C反應蛋白(hs-CRP)水平要顯著高于對照組[14]。本研究對進行CRP檢測的50例AML/MDS伴骨髓纖維化患者進行單因素分析,首次發現CRP也是AML/MDS伴骨髓纖維化的預后因素。提示在繼發骨髓纖維化發生發展過程中,炎性反應發揮了一定作用。綜上所述,有脾腫大、有輸血依賴、纖維化分級≥2級是影響AML/MDS伴骨髓纖維化預后的獨立危險因素,目前國內外均缺乏適用于AML/MDS伴骨髓纖維化的預后系統,仍需多中心、大樣本的患者資料行進一步研究,且能否建立適用于所有髓系惡性腫瘤伴骨髓纖維化的預后系統將成為一項新的挑戰。本研究在國內首次發現CRP與AML/MDS伴骨髓纖維化預后相關,為骨髓纖維化發病機制的研究及治療提供了新的思路。

