光電催化氧化處理中各類活性物質的氧化機理
唐建偉,李 孟,李肇東
?
光電催化氧化處理中各類活性物質的氧化機理
唐建偉1,2,李 孟1*,李肇東1
(1.武漢理工大學市政工程系,湖北 武漢 430070;2.95338部隊,廣東 廣州 510405)
為了深入研究其中各類活性物質氧化機理,以難降解的3,4-二甲基苯胺(3,4-DMA)廢水作為研究對象,通過研究不同抑制劑條件下的動力學規律,并以貢獻度(k/)來量化各活性物質的作用效果,得出氯類活性物質的貢獻度為89.03%,羥基自由基(·OH)的貢獻度為6.24%,而空穴和陽極直接氧化貢獻度可以忽略.采用三聚氰胺法、二甲亞砜(DMSO)法和DPD法定性定量測定了空穴、·OH和自由氯的含量,結果表明:較高濃度的氯化鈉降低了空穴和·OH的貢獻度;·OH的產量符合零級動力學規律,其產生速率為0.106mg/(L·min);自由氯的累積濃度分為3個階段,第3階段累積速率為0.159mg/(L·min).自由氯僅占氯類活性物質氧化體系的一小部分,其他含氯氧化物質和氯類自由基的氧化占重要地位.通過GC-MS、UV-vis和TOC檢測,發現在反應10.0min前,主要通過氯類活性物質對側鏈的快速攻擊,使3,4-DMA轉化為苯甲醛等易分解的苯環類物質;10.0min后,主要通過·OH對苯環大π鍵的攻擊,使苯環類物質轉化為小分子物質,然后繼續被·OH氧化直到礦化.
光電耦合催化氧化;羥基自由基;自由氯;降解機理;3,4-二甲基苯胺
對于高鹽條件下的難降解有機廢水,單一的電催化技術和光催化技術容易產生副產物毒性強和效率低下等問題[1].而光電耦合催化由于其效率高、能耗低和副產物少的特點[2],近年來被廣泛關注和研究[3-5].但是由于光電耦合催化系統活性物質種類較多且相互關系復雜,單獨研究每一種活性物質的產生含量和降解機理較為困難,故此類研究相對較少.
在光電耦合體系,研究發現在降解雙酚A時主要活性物質為空穴和·OH[3];在氯化鈉電解質條件下主要活性物質為活性氯[6];而對于鈦基二氧化銥活性電極,·OH電化學吸附于陽極表面生成了高活性的過氧化銥,可以直接氧化有機物[7].因此本文擬通過電催化(ECO)、光催化(PCO)和光電耦合催化(HPECO)降解的對照試驗和結果分析,結合不同活性物質的檢測手段,定性化、定量化研究空穴、·OH、氯類活性物質和活性陽極等在降解過程中的作用方式和作用效果,并將活性物質的產生和累積量與有機物的降解規律有機聯系在一起,通過反應條件的優化,實現對活性物質產量或者累積量的調控,以取得最佳的有機物降解效果,進而用理論指導實踐.
1 材料與方法
1.1 材料與試劑
陽極和陰極分別選用鈦基二氧化銥(Ti/IrO2)電極和石墨極板(60.0mm×40.0mm×2.0mm),購自蘇州舒爾泰科技有限公司;德固賽納米二氧化鈦(Degussa P25),購自廣州合仟科技有限公司;直流電源,購自深圳市兆信電子科技有限公司.3,4-MDA、乙酰丙酮、叔丁醇(TBA)、二甲亞砜(DMSO)、NaCl、Na2SO4、EDTA-Na均為分析純,購自國藥集團化學試劑有限公司.
1.2 實驗裝置
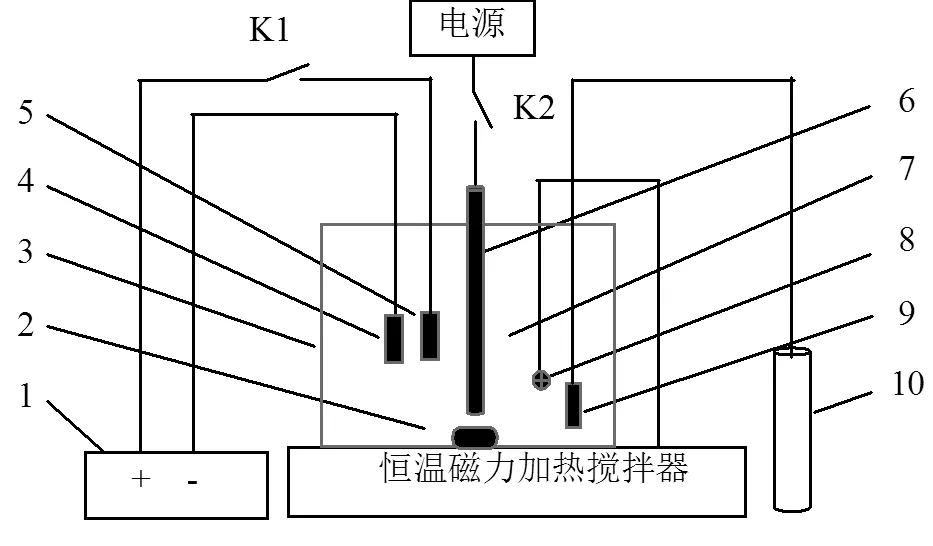
圖1 光電耦合催化氧化實驗裝置示意
1-直流穩壓電源, 2-磁力攪拌轉子, 3-反應容器,4-石墨板陰極, 5-鈦基二氧化銥陽極, 6-紫外燈,7-二氧化鈦光催化劑, 8-溫度探測器, 9-曝氣裝置,10-曝氣機或氮氣瓶
反應器由有機玻璃加工而成,外部用錫箔紙包裹.底部設置有恒溫磁力加熱攪拌器.中心設有半浸沒式石英套管紫外光燈,功率為6W,紫外光主波長為253.7nm.陽極極板(Ti/IrO2)和石墨陰極極板平行固定在反應器內,間距為5.0cm.直流電源可調節電壓范圍為0~30.0V.
1.3 實驗方法
通過稀釋儲備溶液準確配置6000mg/L NaCl、5.0mg/L 3,4-DMA的反應液1.0L,緩慢加入至反應器.經過預實驗得到最優反應條件.稱取300mg TiO2粉末加入反應器中,避光靜置30.0min.打開紫外光燈,調節直流電源,保持電流密度恒為2.5mA/cm2,此時反應開始.每隔2.0min取樣并用0.22μm聚醚礬膜過濾,然后檢測3,4-DMA的濃度和自由氯含量.在檢測·OH時反應液換為1.0L由蒸餾水配置的適量濃度DMSO和6000mg/L NaCl的混合液,每隔4.0min取樣并用0.22μm聚醚礬膜過濾,然后定量檢測·OH含量.所有實驗至少重復2次.
1.4 檢測方法
1.4.1 3,4-DMA的檢測 采用甲氧基苯酚分光光度法[9],于456.0nm處對水體中3,4-DMA進行測定.
1.4.2 ·OH的檢測 以二甲基亞砜為分子探針,于414.0nm波長處通過乙酰丙酮法測定生成的黃色化合物的分光光度值,從而定量表征·OH生成量[10-11].
1.4.3 自由氯的檢測 采用國標法《水質游離氯和總氯的測定 N,N-二乙基-1,4-苯二胺分光光度法》(HJ586-2010)[12]測定水中的自由氯濃度.
1.4.4 空穴檢測 以三聚氰胺為特異性捕獲劑,利用HPLC法測定相同降解時間內三聚氰胺的降解率來間接比較空穴氧化機理所占比重[13].
2 結果與討論
2.1 不同活性物質的降解貢獻度的確定
用TBA作為·OH的抑制劑[14],EDTA-Na作為空穴的抑制劑[15],Na2SO4電解質用來排除氯類活性物質的氧化作用[16],得到不同種類活性物質降解3,4- MDA變化規律(圖2).
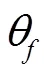

計算可得,陽極直接氧化貢獻度僅為0.42%(k/k),空穴直接氧化和陽極氧化的總貢獻度為0.69% (k/k),·OH的貢獻度為6.24%(k/k),氯類活性物質的貢獻度近似為89.03%(k/k).因此,該體系的降解機理為:氯類活性物質的氧化作用大于·OH的氧化作用,陽極直接氧化和空穴直接氧化可以忽略.

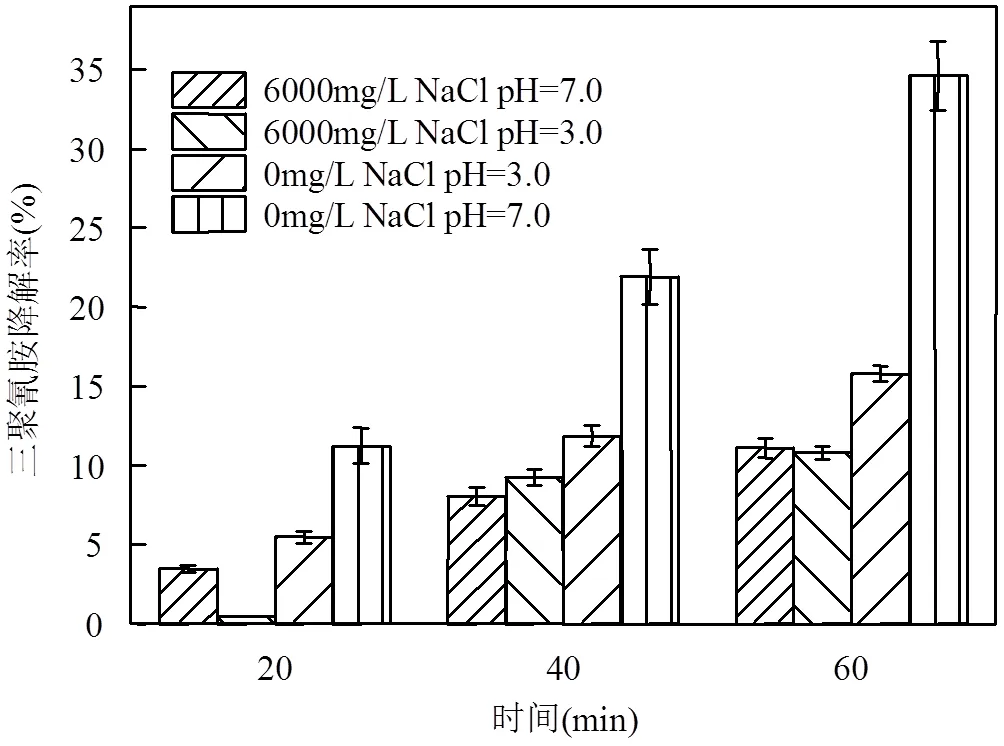
圖3 不同pH值和NaCl濃度條件對三聚氰胺降解率的影響
根據Maurino等[17]的研究,三聚氰胺只能被空穴降解.為研究HPECO體系空穴貢獻度低的原因,選用三聚氰胺作為反應物,測定不同條件下的光催化降解率.反應如圖3所示,可以發現在加入6000mg/L NaCl后,三聚氰胺的降解率受到明顯抑制,而且這種抑制效果在酸性條件下更強烈.這說明高濃度鹽分可以直接抑制有機物的空穴氧化.這是因為Cl-可以與有機物競爭空穴(式(2)),進而降低了空穴氧化在降解過程中的占比;在酸性條件由于靜電力作用(TiO2等電點為6.3[18]),更多的Cl-吸附于TiO2表面,從而更大程度抑制了有機物的空穴降解.
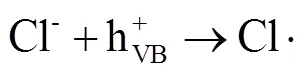
2.2 ·OH在降解過程中的作用機制
不同催化系統中·OH產量隨時間變化曲線(圖4)表明,PCO和HPECO體系分別選用20.0mL/L DMSO和70.0mL/L DMSO作為捕獲劑.無論PCO還是HPECO體系,·OH的產量均符合零級動力學規律.在ECO體系,DMSO捕獲的·OH的量幾乎為0,說明鈦基二氧化銥陽極上·OH沒有直接參與電催化系統中的降解反應,而是電化學吸附在二氧化銥表面形成強氧化性物質過氧化銥,進而氧化有機物.PCO體系和HPECO體系中·OH的產量基本相同,說明HPECO體系中的·OH均來自于其光催化子系統.
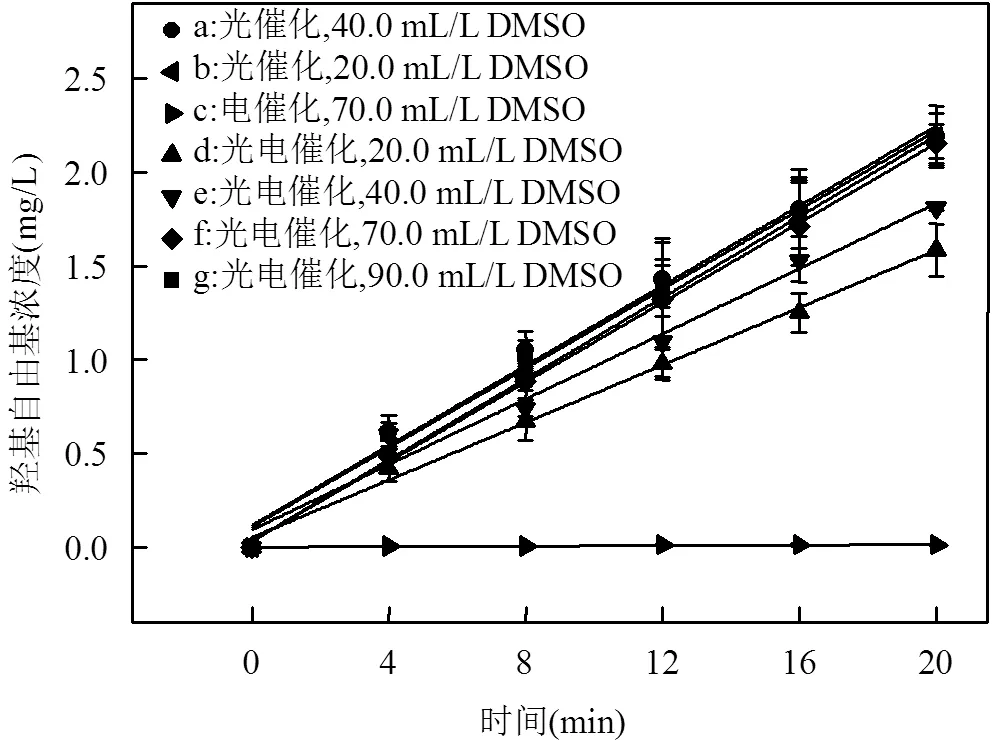
圖4 不同系統中×OH的產量
HPECO體系中,在6000mg/L NaCl條件下,·OH的產生速率如圖4中曲線f,為0.106mg/(L·min). 10.0min內·OH的理論電子轉移量為62.4μmol(式(3)).根據電量守恒(式(4)),氯類活性物質在10.0min內理論電子轉移量為310.6μmol,是·OH的4.9倍.但是在降解系統中,氯類活性物質的貢獻度約是·OH的14.1倍.這說明,產生的·OH只有部分用于降解3,4-DMA,其有效利用率較低.計算PCO體系不同NaCl濃度條件下反應半衰期內·OH理論轉移電子量和3,4-DMA降解量的比值(表1),發現transfer(e-)/deg(3,4-DMA)隨著NaCl濃度的增加而增加,且在沒有添加NaCl時比值最小,為12.8.加入29000mg/L NaCl后比值甚至增加到75.2.這說明NaCl的過量加入會嚴重阻礙3,4-DMA的表面吸附作用并與其競爭·OH(式(5)).因此,造成·OH利用率低的原因,其一是·OH存在時間極短并且容易淬滅[15](式(6)).其二是NaCl競爭·OH,減小了·OH的有效作用量.

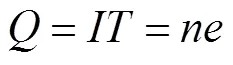


式中:、、分別表示電量、電流、時間;、分別表示元電荷數和元電荷的電荷量.
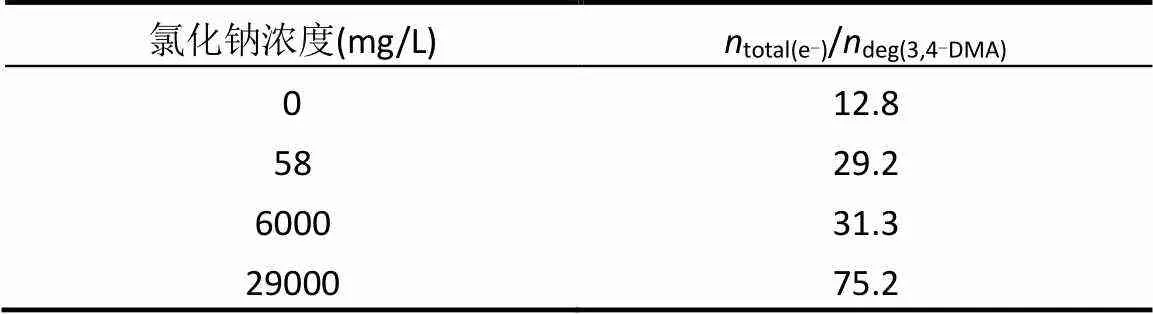
表1 半衰期內PCO體系總電子轉移量和總3,4-DMA降解量比值
2.3 氯類活性物質在降解過程中的作用機制
為了研究不同體系下自由氯濃度,根據DPD法測定自由氯濃度如圖5所示.
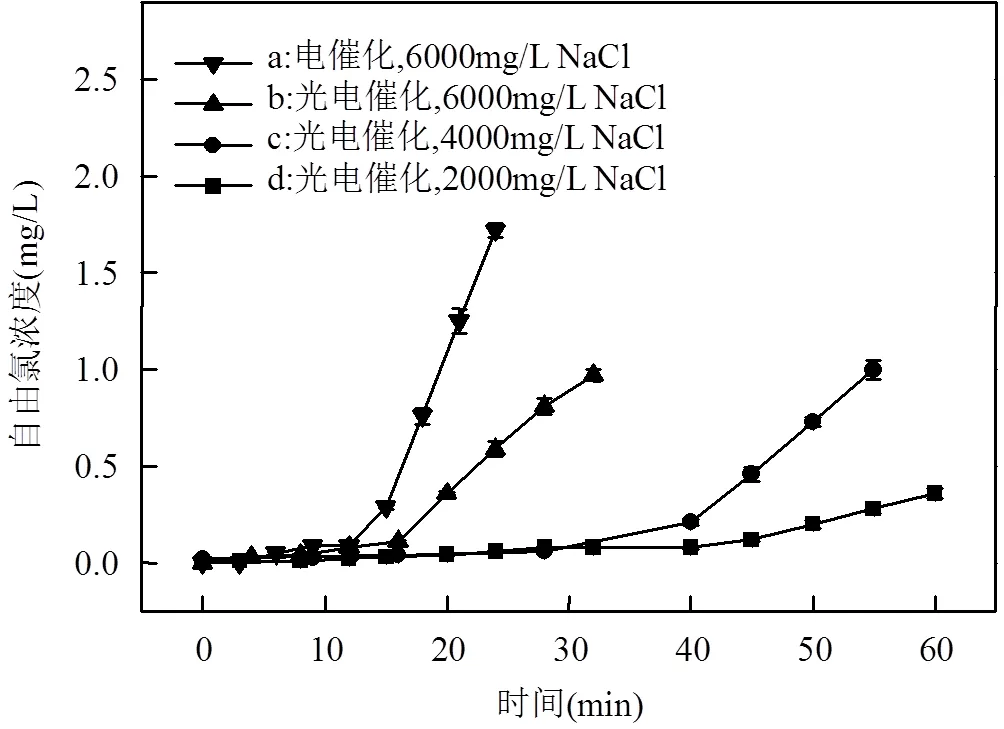
圖5 不同體系下自由氯累積濃度
為了有效分析自由氯變化規律,根據Comninellis等[19]的研究,發現其與有機物降解的變化規律有關,建立自由氯累積模型,如下:
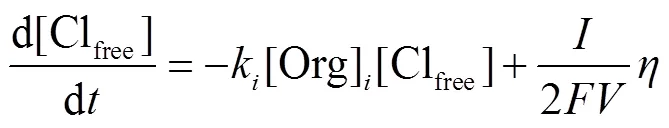
式中:[free]表示溶液中自由氯累積濃度;k表示自由氯降解3,4-DMA動力學常數;表示電流強度;是法拉第常數;為反應區域體積;表示電流轉換效率.根據公式可以將自由氯累積濃度分為如下3個階段:

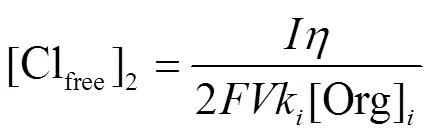

結合圖5可知,無論是ECO還是HPECO體系,自由氯累積濃度均符合建立的模型:反應初期,產生的自由氯大量作用于較高濃度的有機物,測得的累積濃度極低;隨著有機物的降解,自由氯開始緩慢累積,直到有機物降解基本完全,自由氯濃度線性增加.根據圖5進一步得出:隨著NaCl濃度的增加,HPECO自由氯第3階段的起始時間點不斷提前.在6000mg/L NaCl濃度條件下,自由氯第3階段的起始時間點為15.0min.這表明在15.0min 3,4-DMA的濃度極低,自由氯開始線性累積,累積速率為0.159mg/ (L·min).此結論與圖2(a)的3,4-DMA在12.0min全部降解基本吻合.
假設自由氯產生速率一定,且和第3階段的累積速率相近,可以發現自由氯和·OH產率基本接近,但是氯類活性物質的貢獻度卻遠遠高于·OH.這是由于:1)假設電源產生的電能全部用于產生自由氯,其理論產生速率為1.103mg/(L·min)(以Cl2計).由此計算,HPECO體系自由氯電流轉化效率值僅為14.45%.因此在氯類活性物質中自由氯的氧化僅占一小部分,電解產生的其他含氯氧化物質(式(11)~ (14))和自由基鏈式反應產生的氯類自由基[19]的氧化占重要地位.2)相比于·OH,自由氯、其他氯類氧化物質甚至氯類自由基的存活時間相對較長,可以有效作用于有機物,進而提高了氯類活性物質的有效利用率和貢獻度.


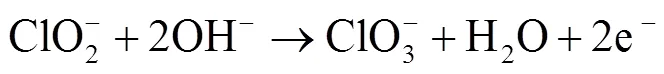

2.4 ·OH和氯類活性物質的降解方式與降解貢獻分析
GC-MS檢測結果(見圖6、圖7)發現,在保留時間為5.253、5.532、6.424、8.107, 10.989min分別發現了甲苯、鄰二甲苯、苯甲醛、3,4-二甲基苯酚和烷烴,于是推測3,4-DMA在HPECO體系下的降解路徑為3,4-DMA—3,4-二甲基苯酚—鄰二甲苯—甲苯—苯甲醛—烷烴類物質(圖8).并且此過程沒有發現氯代苯的生成.

圖6 降解反應7.0min時的GC-MS檢測圖
結合圖9的UV-vis檢測可以分析得出,0min時有機物最大吸收波長為1=233.0nm和2=280.0nm, 4.0min時最大吸收波長基本沒變,但是吸光度變大.這可能是因為生成的高助色團-OH增加了有機物的生色性.推測反應的前4.0min,由于氨基氮具有孤對電子,可以與苯環形成p-π共軛,具有比3、4位甲基與苯環形成的-π超共軛更強的吸電子效應,因此3,4-DMA的氨基被取代生成3,4-二甲基苯酚;4.0~10.0min, B帶最大吸收波長變為2=243.0nm,與苯甲醛吸收波長相同.推測此階段氯類活性物質和·OH繼續將酚類物質氧化,逐漸生成苯甲醛.根據不同體系3,4-DMA降解率深入分析(圖10),得出10.0min時HPECO、ECO和PCO體系3,4-DMA的降解率分別為94.58%、89.87%和12.72%.說明HPECO體系中3,4-DMA的迅速降解主要依靠電催化子系統中氯類活性物質的氧化,而光催化子系統中·OH的作用較弱.根據不同體系TOC的降解規律進一步分析(圖11),得出10.0min時不同系統TOC降解率都未達到4.00%,TOC降解緩慢.結合UV-vis,充分證明反應前10.0min,對于3,4-DMA的降解僅僅停留在對苯環側鏈的氧化,而并沒有真正將苯環開環,甚至達到礦化.綜上說明氯類活性物質可以有效攻擊3,4-DMA的側鏈,快速將其轉化為有利于開環的苯甲醛等物質.

圖7 二級質譜圖

圖8 3,4-DMA降解路徑示意
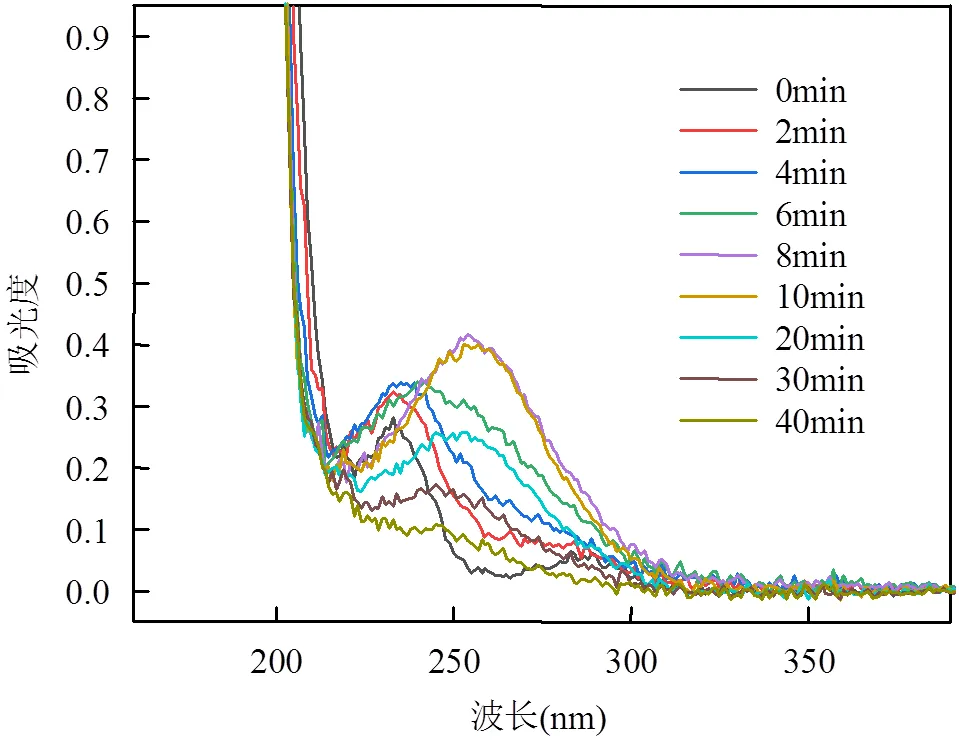
圖9 不同降解反應時間的UV-vis
10.0min后,UV-vis的吸收峰沒有發生移動,但是最大吸光度明顯隨著時間的增加而減小,并且未有新峰生成.10.0min后TOC降解率明顯增加,20.0min HPECO體系TOC降解率達到了15.12%.證明10.0min后苯甲醛等物質被不斷氧化開環,形成烷烴和小分子有機酸,直到被完全礦化.對于ECO體系,TOC降解率一直處于極低水平;反觀PCO體系,其TOC降解規律基本與HPECO體系一致.說明苯環的開環及礦化主要依靠·OH的氧化,氯類活性物質的開環和礦化速率較慢,效果較差.

圖10 不同反應體系3,4-DMA降解速率
因此,在反應前10.0min,HPECO體系充分發揮氯類活性物質快速攻擊3,4-DMA側鏈的優勢,迅速將其轉化為苯甲醛等易分解的有機物;在反應10.0min后,充分發揮·OH礦化效果好的優勢,將易分解的中間產物開環直到最終礦化,達到徹底降解的目的.
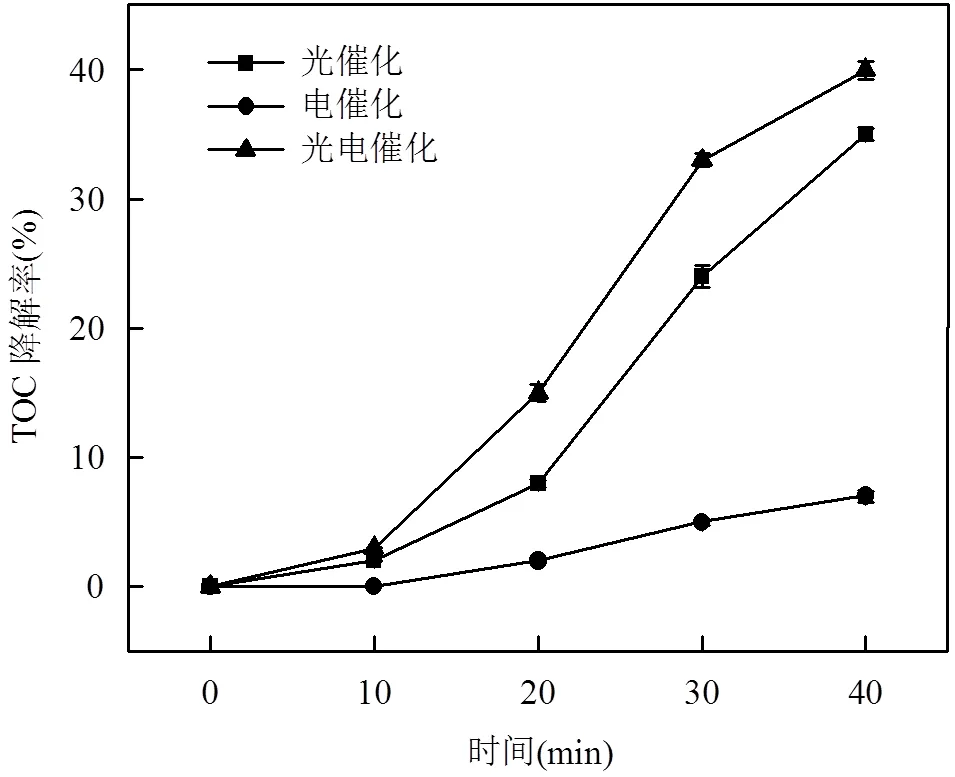
圖11 不同體系的TOC降解率
3 結論
3.1 HPECO體系中,在6000mg/L NaCl、2.5mA/ cm2電流密度、6W紫外光照條件下降解5.0mg/L 3,4- DMA,12.0min降解率達到100%,其降解滿足一級動力學規律.其中,·OH的貢獻度為6.24%,氯類活性物質的貢獻度為89.03%,而空穴和陽極直接氧化貢獻度極低,可以忽略.
3.2 HPECO體系中,·OH的產量符合零級動力學規律,產率為0.106mg/(L·min),其來源于光催化子系統.·OH降解3,4-DMA的速率較慢,利用率較低.
3.3 建立了自由氯累積濃度模型,解釋了自由氯隨時間和有機物濃度變化的規律,得出自由氯轉化效率為14.45%.說明自由氯的氧化僅占氯類活性物質氧化體系的一小部分,其他含氯氧化物質的氧化和氯類自由基的氧化占重要地位.
3.4 推測3,4-DMA在HPECO體系下的降解路徑為3,4-DMA—3,4-二甲基苯酚—鄰二甲苯—甲苯—苯甲醛—烷烴,此過程并無氯代苯生成.在反應前10.0min,主要發生苯環側鏈的轉化,通過氯類活性物質對側鏈的快速攻擊,使之轉化為苯甲醛等易分解的有機物;在反應10.0min后,主要發生苯環的開環和小分子的礦化,通過·OH對苯環大π鍵的攻擊,使之轉化為烷烴等小分子物質,最終完成礦化.
[1] Polcaro A M, Vacca A, Mascia M, et al. Product and by-product formation in electrolysis of dilute chloride solutions [J]. Journal of Applied Electrochemistry, 2008,38(7):979-984.
[2] Hurwitz G, Pornwongthong P, Mahendras, et al. Degradation of phenol by synergistic chlorine-enhanced photo- assisted electrochemical oxidation [J]. Chemical Engineering Journal, 2014,240(4):235-243.
[3] 沙 爽,周少奇,張小娜,等.Pr-N共摻雜TiO2光電催化降解孔雀石綠動力學 [J]. 環境科學, 2012,33(4):1267-1271. Sha S, Zhou S Q, Zhang X N, et al. Photoelectrocatalytic degradation kinetics of malachite green by Pr-N codoped TiO2photocatalyst [J], Environmental Science, 2012,33(4):1267-1271.
[4] 黨聰哲,李一兵,王彥斌,等.K2S2O8強化g-C3N4薄膜電極光電催化降解Cu(CN)32-并同步回收Cu [J]. 環境科學, 2018,39(1):145-151. Dang C Z, Li Y B, Wang Y B, et al. Enhanced photoelectrocatalytic oxidation of Cu(CN)32-and synchronous cathodic deposition of Cu by peroxydisulfate [J]. Environmental Science, 2018,39(1):145-151.
[5] 李 蔣,王 雁,張秀芳,等.Co3O4/BiVO4復合陽極活化過一硫酸鹽強化光電催化降解雙酚A [J]. 環境科學, 2018,39(8):3713-3718. Li J, Wang Y, Zhang X F et al Enhancement of photoelectrocatalytic degradation of bisphenol A with peroxymonosulfate activated by a Co3O4/BiVO4composite photoanode [J]. Environmental Science, 2018,39(8):3713-3718.
[6] Li G Y, An T C, Chen J X, et al. Photoelectrocatalytic degradation of oilfield wastewater with high content of chlorine [J]. Research of Environmental Sciences, 2006,19(1):30-34.
[7] Simond O, Comninellis C. Anodic oxidation of organics on Ti/IrO2, anodes using Nafion ?, as electrolyte [J]. Electrochimica Acta, 1997,42(13/14):2013-2018.
[8] Li A, Zhao X, Liu H, et al. Characteristic transformation of humic acid during photoelectrocatalysis process and its subsequent disinfection byproduct formation potential [J]. Water Research, 2011,45(18):6131- 6140.
[9] 楊曉芬,趙美萍,李元宗,等.水中苯胺類化合物的分光光度法測定 [J]. 分析化學, 2002,30(5):540-543. Yang X F, Zhao M P, Li Y Z, et al. Spectrophotometric methods for the determination of aniline in water [J]. Chinese Journal of Analytical Chemistry, 2002,30(5):540-543.
[10] 劉 婷,尤 宏,陳其偉,等.光助非均相芬頓體系中羥基自由基的熒光光譜法測定與影響因素研究 [J]. 環境科學, 2009,30(9):2560- 2564. Liu T, You H, Chen Q W, et al. Detection of hydroxyl radical in heterogeneous photo-fenton system using the fluorescence technique and influencing factor Study [J]. Environmental Science, 2009,30(9): 2560-2564.
[11] 邰 超,韓 丹,陰永光,等.二甲亞砜捕獲-高效液相色譜測定天然水體中羥基自由基的光化學生成 [J]. 環境化學, 2015,(2):212-218.Tai C, Han D, Yin Y G, et al. Determination of photogenerated hydroxyl radicals in natural water by high performance liquid chromatography after trapping with dimethyl sulfoxide [J]. Environmental Chemistry, 2015,34(2):212-218.
[12] HJ 586-2010 水質游離氯和總氯的測定[S]. HJ 586-2010 Determination of free chlorine and total chlorine-Spectrophotonetric method using N, N-diethyl-1, 4-phenylenediamine [S].
[13] 鄭銘華,陳前進.高效液相色譜法測定美耐皿餐具中三聚氰胺遷移量 [J]. 中國檢驗檢測, 2018,26(2):34-37. Zheng M H, Chen Q J. Determination of the migration quantity of melamine in melamine tableware by HPLC [J]. China Inspection &Laboratory, 2018,26(2):34-37.
[14] And T H, Nosaka Y. Properties of O2?-and OH? formed in TiO2aqueous suspensions by photocatalytic reaction and the influence of H2O2and some ions [J]. Langmuir, 2002,18(18):3247-3254.
[15] 楊世迎.TiO2光催化降解有機污染物的初始步驟機理研究 [D]. 杭州:浙江大學, 2005. Yang S Y. Initial processes in TiO2-assissted photodegradation of organic pollutants [D]. Hangzhou:Zhejiang university, 2005.
[16] Moreira F C, Boaventura R a R, Brillas E, et al. Electrochemical advanced oxidation processes: A review on their application to synthetic and real wastewaters [J]. Applied Catalysis B: Environmental, 2017,202:217-261.
[17] Maurino V, Minella M, Sordello F, et al. A proof of the direct hole transfer in photocatalysis: The case of melamine [J]. Applied Catalysis A General, 2016,521:57-67.
[18] Fujishima A. TiO2Photocatalysis and Related Surface Phenomena [C]// the 60th annual meeting of the international society of electrochemistry. 2009:515-582.
[19] Comninellis C, Nerini A. Anodic oxidation of phenol in the presence of NaCl for wastewater treatment [J]. Journal of Applied Electrochemistry, 1995,25(1):23-28.
[20] Yang Y, Pignatello J J, Ma J, et al. Comparison of halide impacts on the efficiency of contaminant degradation by sulfate and hydroxyl radical-based advanced oxidation processes (AOPs) [J]. Environmental Science & Technology, 2014,48(4):2344.
Oxidation mechanisms of all kinds of active substances by hybrid photoelectrocatalytic treatment.
TANG Jian-wei1,2, LI Meng1*, LI Zhao-dong1
(1.Department of Civil Engineering, Wuhan University of Science and Technology, Wuhan 430070, China;2.People's Liberation Army of China 95338, Guangzhou 510405, China).,2019,39(5):2048~2054
Refractory 3,4-dimethylaniline wastewater was studied for the oxidation mechanisms of various active substances generated in the HPECO process and the contribution degree (k/) based on kinetics was utilized to evaluate the oxidation effect of each active substance. The results showed that the contribution degrees of active chlorines and hydroxyl radicals were respectively 89.03% and 6.24% and the contribution of hole and anode direct oxidation was negligible. The holes, hydroxyl radicals and free chlorine were determined respectively by the ways of melamine, dimethylsulfoxide and DPD and the results showed that the contribution degrees of holes and ·OH were decreased due to high concentration of sodium chloride and ·OH yield followed the zero-order kinetic law with the rate of 0.106mg/(L·min). Moreover, the cumulative concentration regulation of free chlorine was divided into three stages with the rate of 0.159mg/(L·min) in the third stage. Free chlorine only accounted for a small portion in active chlorines, while the oxidation of other chlorinated oxides and chlorinated free radicals played important roles. By GC-MS, UV-vis and TOC determination, it showed that in the initial 10.0min, the active chlorines attacked the side chains rapidly, so that 3, 4-DMA could be converted into benzaldehyde and other benzene derivatives. After 10.0min, the benzene derivatives were attacked towards the π bonds by×OH and transformed into small molecules which could be finally mineralized.
hybrid photoelectrocatalytic oxidation;hydroxyl radicals;active chlorines;degradation mechanisms;3,4-dimethylaniline
X703.5
A
1000-6923(2019)05-2048-07
唐建偉(1982-),男,湖北谷城人,武漢理工大學土木工程與建筑學院市政工程系博士研究生,主要從事水污染控制研究.發表論文13篇.
2018-11-01
國家自然科學基金資助項目(20876122)
*責任作者, 教授, limeng189@163.com

