利拉魯肽對2型糖尿病合并冠心病病人血清免疫因子水平的影響
近年來,隨著人們生活方式及飲食習慣改變,糖尿病發病率呈上升趨勢。據研究,預計2020年糖尿病發病率高達4.4%[1]。2型糖尿病(T2DM)是以血糖水平升高為特征的代謝性疾病,涉及大部分大、小血管,引起多系統損傷,是冠心病和腦血管意外的高危因素之一[2]。有研究發現,T2DM病人心血管疾病風險是正常人群2~4倍,進而增加T2DM病人的死亡風險[3]。T2DM并發冠心病非典型臨床表現多、預后差,但其機制復雜,涉及糖基化終產物、蛋白酶激活、氧化應激、炎癥免疫等多個方面[4],T2DM合并冠心病的診治已成為目前心血管和內分泌領域的研究熱點。降糖藥在糖尿病合并冠心病臨床用藥頻次中位居第2位[5],種類較多,雖然為臨床提供了更高的治療概率,同時也可能給臨床合理用藥帶來更多誤區。本研究探討利拉魯肽對T2DM合并冠心病病人血清免疫因子水平的影響,旨在為此類疾病的臨床治療提供指導。
1 資料與方法
1.1 一般資料 選取2017年3月—2018年2月我院收治的T2DM合并冠心病病人92例。納入標準:符合《中國2型糖尿病防治指南(2013年版)》[6]擬定的T2DM診斷標準;經冠狀動脈造影確診為冠心病。排除標準: 1型糖尿病、妊娠期糖尿病或其他類型糖尿病;嚴重心律失常、中重度心臟瓣膜疾病、急性心力衰竭等疾病;急性或慢性感染性疾病、自身免疫性疾病、惡性腫瘤;嚴重肝、腎功能不全;嚴重糖尿病并發癥,如酮癥、酮癥酸中毒等;存在利拉魯肽用藥禁忌;未按規定治療,無法判斷療效或資料不全等。采用隨機數字表法將所有病人分為對照組與利拉魯肽組。對照組46例,男31例,女15例;年齡43~76(60.62±8.24)歲;糖尿病病程3~14(8.42±1.12)年;冠心病病程2~7(5.26±0.72)年;冠心病分型:心絞痛22例,陳舊性心肌梗死17例,缺血性心肌病7例。利拉魯肽組46例,男29例,女17例;年齡43~80(60.81±8.30)歲;糖尿病病程4~16(8.51±1.10)年;冠心病病程2~9(5.35±0.75)年;冠心病分型:心絞痛18例,陳舊性心肌梗死19例,缺血性心肌病9例。兩組一般資料比較,差異無統計學意義(P>0.05),具有可比性。所有病人均簽署醫院倫理委員會通過的試驗觀察告知書及知情同意書。
1.2 治療方法 所有病人均接受糖尿病常規治療,包括控制血糖、血脂水平。根據病人血糖情況合理選擇降糖藥物,包括二甲雙胍、阿卡波糖、磺脲類藥物與(或)胰島素等聯合治療。血糖控制標準:空腹血糖<7.0 mmol/L;根據高脂血癥類型選用他汀類藥物,如辛伐他汀10~20 mg口服;冠心病給予硝酸酯類、β-受體阻滯劑、阿司匹林等藥物。利拉魯肽組在上述常規治療基礎上每日早餐前皮下注射利拉魯肽注射液(丹麥諾和諾德公司,國藥準字J20110026)1.2 mg。兩組均治療12周,且治療期間監測病人一般情況。
1.3 觀察指標
1.3.1 免疫因子 采集治療前后空腹肘靜脈血5 mL,加入抗凝劑,25 ℃靜置分層,4 ℃條件下以3 000 r/min離心10 min,收集上層血清,凍存-70 ℃冰箱備用。采用酶聯免疫吸附法(ELISA)檢測血清超敏C反應蛋白(hs-CRP)、腫瘤壞死因子-α(TNF-α)、白介素-6(IL-6)水平。各項所有試劑盒均購自南京森貝伽生物科技有限公司。
1.3.2 血糖 采用日立7170A全自動生化分析儀及配套試劑檢測空腹血糖(FPG)、餐后2 h血糖(2 hPG)及糖化血紅蛋白(HbA1c)水平,各項操作嚴格參考說明書進行。
1.3.3 心功能 采用飛利浦HD15000彩色多普勒超聲儀檢測左室射血分數(LVEF)、舒張早期最大峰值速度(E峰)、舒張晚期最大峰值速度(A峰),計算E/A比值。
1.4 療效評定標準 顯效:冠心病癥狀顯著緩解,心絞痛發作次數、持續時間及嚴重程度減少≥80%;好轉:冠心病癥狀顯著緩解,心絞痛發作次數、持續時間及嚴重程度減少50%~80%;無效:未達上述標準[7]。

2 結 果
2.1 兩組血清hs-CRP、TNF-α和IL-6水平比較 治療前,兩組血清hs-CRP、TNF-α、IL-6水平比較,差異無統計學意義(P>0.05)。治療后,兩組血清hs-CRP、TNF-α、IL-6水平較治療前顯著降低(P<0.01);與對照組比較,利拉魯肽組血清hs-CRP、TNF-α、IL-6水平顯著降低(P<0.01)。詳見表1。
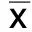
表1 兩組血清hs-CRP、TNF-α和IL-6水平比較(±s)
2.2 兩組FPG、2 hPG、HbA1c水平比較 治療前,兩組FPG、2 hPG、HbA1c水平比較,差異無統計學意義(P>0.05)。治療后,兩組FPG、2 hPG、HbA1c水平較治療前顯著降低(P<0.01);與對照組比較,利拉魯肽組FPG、2 hPG、HbA1c水平顯著降低(P<0.01)。詳見表2。
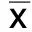
表2 兩組FPG、2 hPG、HbA1c水平比較(±s)
2.3 兩組心功能指標比較 治療前,兩組LVEF、E峰、A峰、E/A比值比較,差異無統計學意義(P>0.05)。治療后,兩組LVEF、E峰、E/A比值較治療前明顯升高(P<0.05),A峰明顯降低(P<0.05);與對照組比較,利拉魯肽組LVEF、E峰、E/A比值明顯升高(P<0.05),A峰明顯降低(P<0.05)。詳見表3。
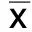
表3 兩組心功能指標比較(±s)
2.4 兩組臨床療效比較(見表4)

表4 兩組臨床療效比較 例(%)
注:兩組總有效率比較,P=0.028
3 討 論
世界衛生組織預測,2013年—2030年全球糖尿病患病人數將從3.71億增至5.52億,其中T2DM占90%~95%[7]。有研究顯示,糖尿病不但與冠心病相關,而且與冠狀動脈狹窄程度密切相關,亦是冠心病的重要危險因素[8]。Conaway等[9]研究發現,心血管疾病是T2DM病人常見的死亡原因,約占死亡率70%。糖代謝異常引起血管壁硬化,彈性減弱,致使各部位供血不足,從而導致冠狀動脈病變嚴重、復雜,多支病變及彌漫病變發生率高于糖代謝正常的冠心病病人。王婧文等[10]研究顯示,T2DM合并冠心病發病機制涉及氧化應激學說、糖基化終產物(AGEs)學說、脂質代謝紊亂等方面。因此治療T2DM合并冠心病時,可控制其發病機制,如積極保護血管內皮功能、抑制炎癥介質活性、降脂等。
隨著高血糖素樣肽1(GLP-1)深入研究發現,GLP-1類似物具有保護B細胞、血糖濃度依賴性降糖及降低多項心血管危險因素風險的作用[11],這些特點使GLP-1類似物成為T2DM治療的新方法。利拉魯肽作為GLP-1類似物,作用機制廣泛,具有保護胰島B細胞、降低血糖、抑制炎癥反應及保護心臟等作用[12]。該藥能促進葡萄糖濃度依賴的胰島素分泌,從而阻礙胰高血糖素分泌,強化胰島素敏感性及胰島細胞功能,并促進胰島細胞增殖[13]。利拉魯肽能促進受損胰島B細胞功能恢復,從而解決既往臨床降血糖藥物的缺陷。近年來,隨著GLP-1類似物及受體的深入研究,發現利拉魯肽對心血管系統具有良好的保護作用。Sokos等[14]針對嚴重心力衰竭病人(心功能Ⅲ~Ⅳ級),不論是否合并糖尿病,除給予標準抗心力衰竭治療外,采用GLP-1類似物治療5周后,均能顯著增加LVEF、心肌耗氧量、6 min耗氧量,證實其能改善心肌舒張功能,提高心肌最大耗氧量。冠心病主要生理病理變化是心肌缺血-再灌注損傷,利拉魯肽能激活促進存活信號通路,從而減輕機體氧化應激反應,減少心肌細胞死亡,提高室壁運動恢復,最終促進心肌缺血后左心室功能的恢復。本研究結果顯示,治療12周后,對照組治療有效率為78.26%,利拉魯肽組治療有效率為95.65%,兩組比較差異有統計學意義(P<0.05),說明利拉魯肽治療T2DM合并冠心病療效滿意,亦有研究表明利拉魯肽單次1.2 mg治療T2DM合并冠心病可獲得最佳效果[15]。
T2DM發生的病理生理基礎為胰島素抵抗和胰島B細胞功能障礙,后者引起胰島素分泌異常,并具有一定的進行性惡化特點。T2DM病人機體長期處于高血糖水平狀態,從而增加蛋白質氧化及糖基化過程,糖基化終末產物加快動脈粥樣硬化(AS)發展。高濃度血糖水平致使內皮損傷,減弱血管內皮舒縮功能,加上葡萄糖直接毒性作用抑制內皮細胞復制,使其自身修復能力下降,進而損傷內皮細胞,導致AS[16]。本研究結果顯示,治療后兩組FPG、2 hPG、HbA1c水平降低,且利拉魯肽組較對照組下降更顯著(P<0.01),表明利拉魯肽降糖的有效性。T2DM與冠心病病人均存在一定程度的全身炎癥狀態,大量炎癥介質釋放是導致T2DM、冠心病病情加重的根本原因之一[17-18]。hs-CRP作為肝合成急性反應時相蛋白之一,反映機體炎癥水平及心腦血管疾病進展,具有較高的敏感性和特異性。TNF-α、IL-6作為機體重要促炎細胞因子,二者促使炎癥細胞因子趨化、黏附,損傷冠狀動脈內皮細胞,加速糖尿病合并冠心病的病情發展[19]。本研究結果顯示,與對照組治療后比較,利拉魯肽組血清hs-CRP、TNF-α、IL-6水平降低(P<0.01),說明利拉魯肽能有效降低T2DM合并冠心病病人全身炎癥反應,可能是其治療作用機制之一。本研究結果同時顯示,與對照組治療后比較,利拉魯肽組LVEF、E峰、E/A比值明顯升高(P<0.05),A峰水平明顯降低(P<0.05),提示利拉魯肽能改善心功能,從而提高左心室射血功能,并改善心臟收縮和舒張功能,與劉英等[20]報道一致。
綜上所述,常規綜合治療同時給予利拉魯肽,可有效調節機體血糖代謝,同時降低全身炎癥反應,改善心功能,發揮心血管保護作用,具有肯定的臨床療效。

