BMSCs與VEGF 165-HUVEC局部皮下組織層共移植大鼠缺血皮瓣存活率觀察
明華偉,何蕓,付光新,李彪,甘升遠,邵學壘,夏德林
(1南充市中心醫(yī)院,四川南充 637000;2西南醫(yī)科大學口頜面修復重建和再生實驗室;3西南醫(yī)科大學附屬口腔醫(yī)院)
由于惡性腫瘤切除、創(chuàng)傷、嚴重感染及先天畸形等各種因素所致頜面部組織缺損,給患者身心帶來極大的負面影響,這使對創(chuàng)面進行修復以恢復患者的功能及外觀顯得尤為迫切。皮瓣移植應用于頜面部缺損的修復重建由來已久,其同時具有創(chuàng)面修復、功能重建等重要作用[1]。但有研究[2,3]報道,皮瓣移植術后部分壞死率達11.4%,完全壞死率為4.0%~6.3%;術后一旦出現(xiàn)皮瓣血運障礙、缺血壞死,臨床處理會非常棘手[4]。因此,如何提高缺血皮瓣的存活能力是修復重建外科一直以來研究的重點。血管生成是由血管內(nèi)皮祖細胞原位聚集、增殖分化、發(fā)育成血管系統(tǒng)的一個需要多種細胞因子參與的復雜過程[5]。血管內(nèi)皮生長因子(VEGF)及骨形態(tài)發(fā)生蛋白(BMP)在成骨及成血管方面發(fā)揮極為重要的生物學作用,骨髓基質(zhì)干細胞(BMSCs)及臍靜脈內(nèi)皮細胞(HUVEC)共培養(yǎng)后,兩者分泌的VEGF與BMP之間存在著相互促進、級聯(lián)放大的作用[6]。VEGF被認為是作用最直接、特異性最高的一種促血管化生長因子,其中VEGF 165在體內(nèi)含量最為豐富,促血管化作用最強[7~10]。但VEGF在體內(nèi)半衰期短,局部應用很快被周圍組織液稀釋。將VEGF 165基因?qū)際UVEC后再與BMSC共移植,在體內(nèi)是否能夠持續(xù)釋放VEGF促進缺血皮瓣的血管生成以往鮮有報道。本研究通過制備大鼠背部缺血皮瓣模型,并移植BMSCs、VEGF 165基因修飾的HUVEC(VEGF 165-HUVEC),觀察兩者共移植對缺血皮瓣存活能力的影響
1 材料與方法
1.1 實驗動物 6~8周齡雌性SD大鼠50只,體質(zhì)量180~200 g;4周齡雄性SD大鼠2只,體質(zhì)量250~300 g;均由西南醫(yī)科大學實驗動物中心提供。
1.2 HUVECs、pHBAd-MCMV-GFP-VEGF165及試劑、儀器 HUVECs(Sciencell公司);pHBAd-MCMV-GFP-VEGF165(由漢恒生物科技公司包裝、構建及鑒定);DMEM培養(yǎng)基、胎牛血清(HyClone公司)、EGM-2(Lonza公司)、血管內(nèi)皮生長因子抗原、ELISA檢測試劑盒、兔抗大鼠CD31抗體(一抗)、羊抗兔IgG(二抗,碧云天生物科技有限公司);倒置相差顯微鏡(奧林巴斯)。
1.3 BMSCs和HUVEC的培養(yǎng)、計數(shù)、定容 全骨髓貼壁培養(yǎng)法培養(yǎng)雄性SD大鼠股骨、脛骨骨髓。當細胞增殖達到90%融合時進行胰酶消化傳代,傳至第3代后制成單細胞懸液,離心后重懸細胞,計數(shù)、定容至1 mL培養(yǎng)液含1×106個BMSCs備用。從液氮容器中取出HUVECs,常規(guī)復蘇后將按比例接種、傳代。傳至第3代后制成單細胞懸液,離心后重懸細胞,同樣定容至1 mL培養(yǎng)液含1×106個HUVEC備用。
1.4 腺病毒介導VEGF-165基因轉(zhuǎn)染HUVEC第3代HUVEC 在前期體外實驗中[11],我們通過VEGF 165-HUVEC的MOI摸索時發(fā)現(xiàn),當MOI=30時為其最佳感染復數(shù),故在本實驗中采用MOI=30進行基因轉(zhuǎn)染。參照病毒轉(zhuǎn)染說明書步驟操作,將腺病毒介導攜帶VEGF 165基因重組pHBAd-MCMV-GFP-VEGF165質(zhì)粒轉(zhuǎn)染至HUVEC。
1.5 缺血皮瓣模型制備、分組及BMSCs和VEGF 165-HUVEC共移植 SD大鼠經(jīng)10%水合氯醛0.3 mL/100 g腹腔麻醉,備皮后在大鼠背部設計隨意皮瓣(4.0 cm×1.5 cm),并于皮瓣中軸線上等距離處標記三個注射點,銳性分離掀起皮瓣,再對位縫合,術后創(chuàng)口涂布紅霉素眼膏,無需敷料包扎。所有動物模型由同一組人員制備,大鼠術后分籠飼養(yǎng)。建模成功(缺血皮瓣制備手術過程順利,手術探查確認皮瓣無軸心血管,手術過程中及術后取材前未死亡,麻醉蘇醒后能正常活動)后所有大鼠隨機分為5組各10只,術后即刻在標記點(分別距離皮瓣遠蒂端1、2、3 cm處)皮下組織層移植等量細胞5×105個,A組移植BMSCs與VEGF 165-HUVEC(1∶1),B組移植VEGF 165-HUVEC,C組移植BMSCs與HUVEC(1∶1),D組移植HUVEC,E組注射等體積0.9%NaCl溶液。
1.6 皮瓣存活率測算 術后第11天,數(shù)碼相機對各組皮瓣拍照,采用 Image-Pro Plus 6.0軟件分析、計算各組皮瓣存活率(每組10只大鼠),皮瓣存活率(%)=皮瓣總面積(cm2)-皮瓣壞死面積(cm2)/皮瓣總面積(cm2)。
1.7 大鼠血清VEGF蛋白檢測 于術后第2、4、7、14天采用經(jīng)眼眶后靜脈叢采血法抽取大鼠外周血0.5~1.0 mL,離心取血清,采用ELISA法檢測血清中VEGF(第2、4、7天VEGF水平檢測時大鼠數(shù)為10只,第14天VEGF水平測定時大鼠數(shù)為5只)。
1.8 皮瓣微血管密度(MVD)測算 術后第11天,各組隨機抽取5只大鼠,麻醉過量處死后于皮瓣存活區(qū)域取材,行CD31免疫組化,檢測皮瓣MVD。在每組中隨機抽取10張切片,于200倍光鏡下每張隨機計算20個視野中的血管斷面數(shù)目,求均值計算各組皮瓣的MVD值[12]。皮瓣MVD(條/mm2)=第1個視野血管斷面數(shù)目(N1)+N2+、+N20/20。
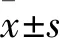
2 結果
2.1 各組術后第11 天皮瓣存活率比較 A、B、C、D、E組皮瓣存活率分別為84.3%±4.7%、61.2%±4.5%、50.1%±3.8%、43.8%±2.9%、30.7%±1.9%,兩兩比較,P均<0.05。
2.2 各組不同時點血清VEGF蛋白水平比較 血清VEGF蛋白水平比較見表1。


組別 VEGF蛋白 術后第2天術后第4天術后第7天術后第14天 A組486.3±7.5?583.7±13.4?682.5±12.6?274.2±7.1?B組352.3±4.8435.2±6.9550.2±9.7215.5±5.8C組34.8±2.935.6±3.229.1±2.826.9±1.9D組33.1±2.031.2±3.727.9±2.824.7±2.1E組33.2±3.630.7±2.833.2±2.725.7±1.8
注:與其余4組比較,*P<0.05。
2.3 各組皮瓣局部MVD計數(shù)比較 A、B、C、D、E組MVD計數(shù)分別為62.1±5.2、53.7±4.8、40.5±3.1、25.9±3.0、17.8±1.1,兩兩比較,P均<0.05。
3 討論
口腔頜面部常因手術切除良惡性腫瘤、頜面部創(chuàng)傷、間隙感染及發(fā)育性畸形等各種因素所致組織缺損,從而導致面部畸形,嚴重影響患者的吞咽、言語等生理功能及日常生活,不可避免的給這類患者的身心健康造成較大的影響。臨床選用何種方法對組織缺損來進行修復重建,才能盡可能恢復較為正常的生理功能及面部外形顯得尤為迫切。皮瓣移植自應用于口腔頜面部軟組織缺損的修復重建以來,取得了較為滿意的臨床效果,其兼具創(chuàng)面修復、功能重建等重要作用。但是皮瓣移植后由于局部壓迫、血栓形成等各種復雜的局部或全身因素造成其血流動力學發(fā)生變化,最終導致皮瓣因缺血而發(fā)生局部或全部壞死。皮瓣移植術后一旦出現(xiàn)血運障礙、缺血壞死,臨床處理較為棘手,往往需再次或多次手術,增加了患者的創(chuàng)傷及醫(yī)療費用,如何提高缺血皮瓣的存活能力一直以來是臨床研究的重點和難點。
BMSCs是一種存在于骨髓中的非造血干細胞,具有自我復制及多向分化的干細胞潛能,在體外特定的誘導環(huán)境中可以向成骨細胞、脂肪細胞、血管內(nèi)皮細胞等方向分化,經(jīng)體外培養(yǎng)后不影響其增殖、分化能力。HUVEC來源豐富,取材、操作方便,不像胚胎干細胞涉及安全性及倫理學問題,且具有干細胞的功能-能夠無限次(理論上)增殖傳代。VEGF已被公認為是在血管生成中發(fā)揮重要作用的促血管化生長因子,包括五種異構體,其中VEGF 121和VEGF 165兩種蛋白質(zhì)是主要的分泌成分和效應因子[13,14]。而VEGF 165在體內(nèi)含量最為豐富,促血管化作用最強[15]。國內(nèi)外學者利用VEGF促血管化研究的實施方案包括對其進行蛋白重組和基因轉(zhuǎn)染這兩種形式。但是經(jīng)過蛋白重組后的VEGF應用于體內(nèi)實驗研究時發(fā)現(xiàn),其半衰期非常短,很快就會溶解于周圍組織液當中并降解而失去生物學活性,無法持續(xù)、穩(wěn)定地發(fā)揮促血管生成的作用;通過血液循環(huán)途徑不能精準定位至損傷局部發(fā)揮作用,且需要多次給藥,不可避免地增加了經(jīng)濟負擔。近年來,大多數(shù)學者將目光投向基因轉(zhuǎn)染這個方式,通過將目的基因?qū)胨拗骷毎笞屪陨碓丛床粩嗟暮铣尚鞍祝瑥亩軌蛟隗w內(nèi)持續(xù)發(fā)揮促血管生成的生物學效應[16]。應用HUVEC與BMSCs共培養(yǎng)體系時,利用它們之間分泌的細胞因子在生物學功能方面產(chǎn)生偶聯(lián)協(xié)同效應,加速血管生成,相互促進,相互影響。本研究顯示,各組皮瓣存活率兩兩比較有差異,且A組皮瓣成活質(zhì)量明顯高于其他四組。
有研究發(fā)現(xiàn)[17],BMSCs與HUVEC在共培養(yǎng)條件下,除HUVEC自身能夠分泌VEGF 165外,還能增加BMSCs合成和分泌VEGF 165,兩者分泌的VEGF 165共同促進了HUVEC的分裂、增殖、遷移以及血管芽的形成。本研究顯示,A組VEGF蛋白表達水平并未明顯升高,C、D、E組各時間點的VEGF水平波動較小。我們分析,出現(xiàn)這種現(xiàn)象的原因可能是由于HUVEC和BMSCs自身能分泌多種促血管化生長因子,如VEGF、bFGF、PDGF等,這些促血管化因子通過一系列復雜的生物學效應發(fā)揮了血管生成的作用,一定程度上提高了皮瓣存活率,但是這些促血管化生長因子的量較少,在全身血液循環(huán)過程中被稀釋。而本實驗經(jīng)大鼠眼眶后靜脈叢采血離心后檢測VEGF水平,其局部產(chǎn)生的VEGF蛋白經(jīng)全身血液循環(huán)至眼眶后靜脈時已被大量稀釋,C、D組皮瓣局部實際的VEGF水平應該明顯高于實驗檢測的結果。比較B、D組的VEGF蛋白水平,我們發(fā)現(xiàn)轉(zhuǎn)染基因的HUVEC在體內(nèi)能持續(xù)高表達VEGF蛋白,結合兩組相應的皮瓣存活率及MVD表明,VEGF發(fā)揮了促血管生成的作用;A組皮瓣存活率高于B、C組,轉(zhuǎn)染基因的HUVEC與BMSCs共移植后VEGF表達水平明顯高于單獨共移植或單獨轉(zhuǎn)染基因,A、B、C組皮瓣MVD數(shù)據(jù)比較同樣印證該結果。有研究[18]發(fā)現(xiàn),在BMSCs與HUVEC共培養(yǎng)體系中,HUVEC分泌的尿激酶類纖容酶原激活劑(uPA)和VEGF受體增加,同時BMSCs中VEGF 165的表達也上調(diào),VEGF 165進而活化HUVEC中uPA,uPA與血管內(nèi)皮鈣粘蛋白可能一起啟動了共培養(yǎng)細胞的自組裝進網(wǎng)絡以及細胞的遷移、增殖、分化。Kaigler等[19]發(fā)現(xiàn),在BMSCs與血管內(nèi)皮細胞共培養(yǎng)體系中,BMSCs能分泌VEGF來促進內(nèi)皮細胞的分裂、增殖分化形成血管芽狀結構。還有研究發(fā)現(xiàn)[20~23],共培養(yǎng)的VECs可以釋放BMP-2,一方面促進成骨分化,另一方面還可以促進成骨及其前體細胞分泌VEGF,VEGF反過來作用于VECs,促進內(nèi)皮細胞的分裂、增殖、分化及血管形成。兩者相互促進,起到級聯(lián)放大的作用,共同促進血管生成。
總之,BMSCs與VEGF 165-HUVEC共移植入大鼠背部缺血皮瓣后,在體內(nèi)能持續(xù)高表達VEGF蛋白,大鼠背部缺血皮瓣的存活率及皮瓣局部的MVD明顯增加,具有提高缺血皮瓣存活的能力。

